计算并填空:(在标准状况下15gCO与CO2的混合气体,体积为11.2L,则:
(1)混合气体的平均摩尔质量是___________________ g/mol
(2)CO的体积分数是___________________
(3)CO2与CO的质量比是____________________________
(4)混合气体中所含碳原子的质量是___________________ g
(1)混合气体的平均摩尔质量是
(2)CO的体积分数是
(3)CO2与CO的质量比是
(4)混合气体中所含碳原子的质量是
更新时间:2018-11-07 21:11:03
|
相似题推荐
【推荐1】已知丁烷在催化剂、加热、加压的条件下会以如下两种方式发生裂解:
①C4H10 CH4+C3H6
CH4+C3H6
②C4H10 C2H4+C2H6
C2H4+C2H6
现有1 mol丁烷,其中有36%以方式①裂解,有24%以方式②裂解,还有40%没有裂解,则最终所得混合气体的平均摩尔质量是______________________ 。
①C4H10
 CH4+C3H6
CH4+C3H6②C4H10
 C2H4+C2H6
C2H4+C2H6现有1 mol丁烷,其中有36%以方式①裂解,有24%以方式②裂解,还有40%没有裂解,则最终所得混合气体的平均摩尔质量是
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】某元素及其气态氢化物化学式为H2R,其高价氧化物中氧的质量分数是60%,且该元素的质子数和中子数相等,写出元素R的相对原子质量__________ 和元素符号___________ 。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】(1)2molO3和3molO2的质量之比_______ ,分子数之比______ ,同温同压下密度之比________ ,含氧原子数之比______ ,体积之比______ 。
(2)O3与Cl2具有相似的性质,均可用于自来水的消毒。已知二者在消毒时均被还原为最低价态,则相同状况下10LO3与______ LCl2的消毒能力相当。
(3)气体化合物A分子式可表示为OxFy,已知同温同压下10mLA受热分解生成15mLO2和10mLF2,则A的化学式为_________ 。
(2)O3与Cl2具有相似的性质,均可用于自来水的消毒。已知二者在消毒时均被还原为最低价态,则相同状况下10LO3与
(3)气体化合物A分子式可表示为OxFy,已知同温同压下10mLA受热分解生成15mLO2和10mLF2,则A的化学式为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐1】按要求计算、整理化简并填空:
(1)若20g密度为ρg•cm﹣3的硝酸钙溶液里含1gCa2+,则NO3-的物质的量浓度是____ 。
(2)现有mg某气体,它由双原子分子构成,它的摩尔质量为Mg/mol。若阿伏加 德罗常数的值用NA表示,则:
①该气体所含原子总数为___ 个。
②该气体在标准状况下的体积为____ L。
③该气体溶于1L水中(不考虑反应),形成的溶液密度为ρg/cm3,则该溶液的物质的量浓度为____ mol•L-1。
(1)若20g密度为ρg•cm﹣3的硝酸钙溶液里含1gCa2+,则NO3-的物质的量浓度是
(2)现有mg某气体,它由双原子分子构成,它的摩尔质量为Mg/mol。若阿伏加 德罗常数的值用NA表示,则:
①该气体所含原子总数为
②该气体在标准状况下的体积为
③该气体溶于1L水中(不考虑反应),形成的溶液密度为ρg/cm3,则该溶液的物质的量浓度为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】根据下列化学方程式回答问题: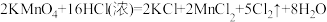
(1)反应中电子转移的数目是________ 。
(2)在该反应中,还原剂是_______ 。
(3)当有0.10mol电子发生转移时,生成氯气的体积为________ (标准状况下)。
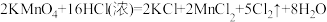
(1)反应中电子转移的数目是
(2)在该反应中,还原剂是
(3)当有0.10mol电子发生转移时,生成氯气的体积为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】氧化还原反应在生产生活中有广泛的应用,中国传统文化中有广泛记载。
(1)“熬胆矾铁釜,久之亦化为铜”涉及到的化学反应为:CuSO4+Fe=FeSO4+Cu,该反应中CuSO4的摩尔质量是___________ 。28 g铁粉完全反应,析出Cu单质的物质的量为___________ 。
(2)宋代《洗冤集录》中记载有“银针探毒”,其原理是:4Ag+2H2S+O2=2Ag2S+2H2O,在相同条件下体积相同的H2S和O2两种气体原子数之比为___________ ,质量比为___________ 。标准状况下22.4 mL O2中氧原子的物质的量n(O)=___________ mol,当发生上述反应时氧气完全反应,消耗的标准状况下H2S的体积是___________ mL。
(3)我国古代四大发明之一的黑火药是由硫磺粉、硝酸钾和木炭按一定比例混合而成的,爆炸时发生的反应为: ,在此反应中,被还原的元素为
,在此反应中,被还原的元素为___________ (填元素符号),氧化产物是___________ (填化学式),6.4gS参加反应时,产生气体的体积为___________ L(标况下),反应中被S氧化的C的物质的量为___________ mol。
(1)“熬胆矾铁釜,久之亦化为铜”涉及到的化学反应为:CuSO4+Fe=FeSO4+Cu,该反应中CuSO4的摩尔质量是
(2)宋代《洗冤集录》中记载有“银针探毒”,其原理是:4Ag+2H2S+O2=2Ag2S+2H2O,在相同条件下体积相同的H2S和O2两种气体原子数之比为
(3)我国古代四大发明之一的黑火药是由硫磺粉、硝酸钾和木炭按一定比例混合而成的,爆炸时发生的反应为:
 ,在此反应中,被还原的元素为
,在此反应中,被还原的元素为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】设NA表示阿伏加 德罗常数的值。回答下列问题:
(1)0.3molNH3分子中所含原子数与____ 个H2O分子中所含原子数相等。
(2)含0.4molAl3+的Al2(SO4)3中所含的 的物质的量是
的物质的量是_____
(3)一定条件下,16gA和20gB恰好完全反应生成0.04molC和31.76gD,则C的摩尔质量为____
(4)0.4molSiH4分子中所含原子数与____ gHCl分子中所含原子数相等。
(5)1.5molH2SO4的质量是____ ,其中含有____ molH,含有____ g氧元素。
(6)9.03×1023个氨分子含___ mol氨分子,_____ mol质子,___ 个电子。
(1)0.3molNH3分子中所含原子数与
(2)含0.4molAl3+的Al2(SO4)3中所含的
 的物质的量是
的物质的量是(3)一定条件下,16gA和20gB恰好完全反应生成0.04molC和31.76gD,则C的摩尔质量为
(4)0.4molSiH4分子中所含原子数与
(5)1.5molH2SO4的质量是
(6)9.03×1023个氨分子含
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】阿伏加 德罗常数的近似值为6.02×1023.按要求完成下列填空:
(1)1mol Cl2中约含有______ 个氯气分子,约含有______ 个氯原子,含有6.02×1023个氢原子的H2SO4的物质的量是______ ;
(2)标准状况下11.2L N2O4和______ mol NO所含有的原子数相等。
(3)某硫酸钠溶液中含有3.01×1023个Na+,则该溶液中SO42-的物质的量是______ 。
(4)2L 1mol/L MgCl2中镁离子的物质的量为______ ,Cl-的物质的量浓度为______ 。
(1)1mol Cl2中约含有
(2)标准状况下11.2L N2O4和
(3)某硫酸钠溶液中含有3.01×1023个Na+,则该溶液中SO42-的物质的量是
(4)2L 1mol/L MgCl2中镁离子的物质的量为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐1】填空。
(1)标准状况下,和2 mol NH3含有相同氢原子数的CH4的体积为_______ 。
(2)现有9 g H2O,若阿伏加德罗常数的值用NA表示,则该物质的物质的量为_______ ,所含质子数为_______ ,所含电子数为_______ 。
(3)12.4 g Na2R含0.4 mol Na+,则Na2R的摩尔质量为____ ,R的相对原子质量为_____ 。
(4)原子数相同的N2和SO2分子数之比为_______ ,质量之比为_______ 。
(5)在标准状况下,由CO和CO2组成的混合气体为6.72 L,质量为12 g,此混合物中CO和CO2物质的量之比是_______ ,混合气体的平均相对分子质量是_______ 。
(1)标准状况下,和2 mol NH3含有相同氢原子数的CH4的体积为
(2)现有9 g H2O,若阿伏加德罗常数的值用NA表示,则该物质的物质的量为
(3)12.4 g Na2R含0.4 mol Na+,则Na2R的摩尔质量为
(4)原子数相同的N2和SO2分子数之比为
(5)在标准状况下,由CO和CO2组成的混合气体为6.72 L,质量为12 g,此混合物中CO和CO2物质的量之比是
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】(1)相同条件下,0.6mol的氧气与0.4mol臭氧(O3)质量之比为___________ , 分子个数之比为___________ , 体积之比___________ ,氧原子个数之比为___________ 。
(2)0.5 mol CH4 的质量为___________ g,在标准状况下的体积为___________ L;含___________ 个碳原子。
(3)将标准状况下 22.4 L 的 HCl 溶于水配成 200 mL 的溶液,所得溶液的物质的量浓度为___________ mol/L;配制 300 mL 0.5 mol/L 氯化钠溶液,需要 1.5 mol/L 的氯化钠溶液的体积为___________ mL。
(4)1.204×1024 个水分子的物质的量为___________ mol。
(2)0.5 mol CH4 的质量为
(3)将标准状况下 22.4 L 的 HCl 溶于水配成 200 mL 的溶液,所得溶液的物质的量浓度为
(4)1.204×1024 个水分子的物质的量为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】物质的量是高中化学常用的物理量,请完成以下有关计算:
(1)在一定温度和压强下,0.4mol某气体的体积为9.8L,则该条件下的气体摩尔体积______ 。
(2)某气体氧化物的化学式为RO2,在标准状况下,1.28g该氧化物的体积为448mL,则R的相对原子质量为______ 。
(3)标准状况下,1.7gNH3与______ LH2S气体含有的氢原子数相同,
(4)标准状况下,NH3与CH4组成的混合气体的平均密度为0.75g/L该混合气体中NH3的体积分数为______ ,该混合气体对氢气的相对密度为______ 。
(1)在一定温度和压强下,0.4mol某气体的体积为9.8L,则该条件下的气体摩尔体积
(2)某气体氧化物的化学式为RO2,在标准状况下,1.28g该氧化物的体积为448mL,则R的相对原子质量为
(3)标准状况下,1.7gNH3与
(4)标准状况下,NH3与CH4组成的混合气体的平均密度为0.75g/L该混合气体中NH3的体积分数为
您最近一年使用:0次



