按要求计算、整理化简并填空:
(1)若20g密度为ρg•cm﹣3的硝酸钙溶液里含1gCa2+,则NO3-的物质的量浓度是____ 。
(2)现有mg某气体,它由双原子分子构成,它的摩尔质量为Mg/mol。若阿伏加 德罗常数的值用NA表示,则:
①该气体所含原子总数为___ 个。
②该气体在标准状况下的体积为____ L。
③该气体溶于1L水中(不考虑反应),形成的溶液密度为ρg/cm3,则该溶液的物质的量浓度为____ mol•L-1。
(1)若20g密度为ρg•cm﹣3的硝酸钙溶液里含1gCa2+,则NO3-的物质的量浓度是
(2)现有mg某气体,它由双原子分子构成,它的摩尔质量为Mg/mol。若阿伏加 德罗常数的值用NA表示,则:
①该气体所含原子总数为
②该气体在标准状况下的体积为
③该气体溶于1L水中(不考虑反应),形成的溶液密度为ρg/cm3,则该溶液的物质的量浓度为
更新时间:2019-10-19 16:43:22
|
相似题推荐
计算题
|
适中
(0.65)
名校
【推荐1】CO2的减排已经引起国际社会的广泛关注,近日我国科学家实现了CO2高选择性、高稳定性加氢合成甲醇(CH3OH)。回答下列问题:
(1)CO2的摩尔质量是______ g/mol。
(2)在标准状态下,5.6LCO2的物质的量是______ mol,质量是_______ g。
(3)22gCO2的体积是_______ L(标准状况)。
(4)相同质量的CO和CO2所含的氧原子个数比是_______ 。
(5)同温同压下,同体积的CO和CO2的物质的量之比为__________ 。
(1)CO2的摩尔质量是
(2)在标准状态下,5.6LCO2的物质的量是
(3)22gCO2的体积是
(4)相同质量的CO和CO2所含的氧原子个数比是
(5)同温同压下,同体积的CO和CO2的物质的量之比为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】在标准状况下氢气和一氧化碳的混合气体6.72L,质量为3.2g,求:H2的质量___________ 和CO的质量________ ;H2的体积______ 和CO的体积_________ 。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】现有14.4 g CO和CO2的混合气体,在标准状况下所占的体积约为8.96 L。回答下列问题:
(1)该混合气体中CO物质的量为________ ;CO2物质的量为_________ 。
(2)混合气体中碳原子的个数___________ 。(用NA表示阿伏加 德罗常数的值)
(3)将混合气体依次通过如图装置,最后收集在气球中。
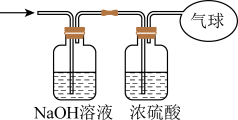
①气球中收集到的气体的摩尔质量_________ ;
②标况下气球中收集到的气体的体积为________________ ;
③气球中收集到的气体的电子总数为________ 。(用NA表示阿伏加 德罗常数的值)
(1)该混合气体中CO物质的量为
(2)混合气体中碳原子的个数
(3)将混合气体依次通过如图装置,最后收集在气球中。

①气球中收集到的气体的摩尔质量
②标况下气球中收集到的气体的体积为
③气球中收集到的气体的电子总数为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐1】回答下列问题:
Ⅰ.向500mLNaOH溶液中投入10.8 g Al,二者恰好完全反应后,则
(1)溶液中发生反应的离子方程式___________ 。
(2)原NaOH溶液的物质的量浓度为___________ 。
(3)生成标准状况下H2的体积为___________ 。
Ⅱ.向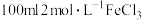 溶液中加入6 g铜粉,完全溶解后,再加入a g铁粉,充分反应后得到b g固体。
溶液中加入6 g铜粉,完全溶解后,再加入a g铁粉,充分反应后得到b g固体。
(1)写出加入6 g铜粉时,溶液中发生反应的离子方程式___________ 。
(2)若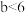 ,则最后得到的溶液中一定含有的金属阳离子是
,则最后得到的溶液中一定含有的金属阳离子是___________ 。
(3)若 ,则
,则
___________ 。
Ⅰ.向500mLNaOH溶液中投入10.8 g Al,二者恰好完全反应后,则
(1)溶液中发生反应的离子方程式
(2)原NaOH溶液的物质的量浓度为
(3)生成标准状况下H2的体积为
Ⅱ.向
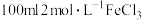 溶液中加入6 g铜粉,完全溶解后,再加入a g铁粉,充分反应后得到b g固体。
溶液中加入6 g铜粉,完全溶解后,再加入a g铁粉,充分反应后得到b g固体。(1)写出加入6 g铜粉时,溶液中发生反应的离子方程式
(2)若
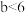 ,则最后得到的溶液中一定含有的金属阳离子是
,则最后得到的溶液中一定含有的金属阳离子是(3)若
 ,则
,则
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】向某AgNO3溶液中,逐滴加入密度为1.10g/mL的盐酸,恰好完全反应时,过滤所得沉淀的质量恰好与盐酸的质量相等。求盐酸的质量分数和物质的量浓度。(要求有简单计算过程)
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐3】完成下列问题
(1)8 g CH4在标准状况下所占的体积约为_______ L。
(2)20g重水(D2O)中所含中子数目为_______ 。
(3)10.8g R2O5中氧原子数目为3.01×1023 ,则元素R的相对原子质量为_______ 。
(4)向10.0mL1.00mol·L-1 Na2CO3溶液加水稀释至100mL溶液,此时溶液中Na+的物质的量浓度为_______ 。
(5)实验室常用邻苯二甲酸氢钾(KHC8H4O4)来标定氢氧化钠溶液的浓度,其操作过程为:准确称取4.080g邻苯二甲酸氢钾,加水配成溶液,向溶液中加入1~2滴指示剂,用氢氧化钠溶液滴定至终点,消耗氢氧化钠溶液19.60mL。该氢氧化钠溶液的物质的量浓度为_______ 。(已知:KHC8H4O4+NaOH=KNaC8H4O4+H2O)
(6)100g质量分数为46%的酒精(CH3CH2OH)溶液中氧原子的物质的量为_______ 。
(1)8 g CH4在标准状况下所占的体积约为
(2)20g重水(D2O)中所含中子数目为
(3)10.8g R2O5中氧原子数目为3.01×1023 ,则元素R的相对原子质量为
(4)向10.0mL1.00mol·L-1 Na2CO3溶液加水稀释至100mL溶液,此时溶液中Na+的物质的量浓度为
(5)实验室常用邻苯二甲酸氢钾(KHC8H4O4)来标定氢氧化钠溶液的浓度,其操作过程为:准确称取4.080g邻苯二甲酸氢钾,加水配成溶液,向溶液中加入1~2滴指示剂,用氢氧化钠溶液滴定至终点,消耗氢氧化钠溶液19.60mL。该氢氧化钠溶液的物质的量浓度为
(6)100g质量分数为46%的酒精(CH3CH2OH)溶液中氧原子的物质的量为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐1】(1)9g水与_______ g硫酸所含的分子数相等,它们所含氧原子数之比是_______ ,氢原子数之比是_______ ;
(2)已知8gA能与32gB恰好完全反应,生成22gC和一定量的D,现将16gA与70gB的混合物充分反应后,生成2molD和一定量的C,则D的摩尔质量是_______ g/mol;
(2)已知8gA能与32gB恰好完全反应,生成22gC和一定量的D,现将16gA与70gB的混合物充分反应后,生成2molD和一定量的C,则D的摩尔质量是
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】在下面的横线上填上适当的内容。
(1)6.02×1024个Na+约含有________ mol Na+,其质量为________ g。
(2)0.5mol CH4约含有________ 个CH4,其含有的电子数为________ mol。
(3)49 g H3PO4共含有________ mol原子。
(4)3.01×1024个 与
与________ mol  的质量相同。
的质量相同。
(5)15.6g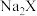 中含有0.4mol
中含有0.4mol ,则X的相对原子质量为
,则X的相对原子质量为__________ 。
(6)常温常压下,用等质量的 、
、 、
、 、
、 四种气体分别吹出四个气球,其中气体为
四种气体分别吹出四个气球,其中气体为 的是
的是________ (填序号)。
A. B.
B. C.
C. D.
D.
(1)6.02×1024个Na+约含有
(2)0.5mol CH4约含有
(3)49 g H3PO4共含有
(4)3.01×1024个
 与
与 的质量相同。
的质量相同。(5)15.6g
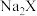 中含有0.4mol
中含有0.4mol ,则X的相对原子质量为
,则X的相对原子质量为(6)常温常压下,用等质量的
 、
、 、
、 、
、 四种气体分别吹出四个气球,其中气体为
四种气体分别吹出四个气球,其中气体为 的是
的是A.
 B.
B. C.
C. D.
D.
您最近一年使用:0次
【推荐3】玻璃仪器内壁残留的硫单质可用热KOH溶液洗涤除去,发生如下反应:
①3S+6KOH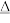 2K2S+K2SO3+3H2O
2K2S+K2SO3+3H2O
②(x-1)S+K2S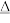 K2Sx(x=2~6之间)
K2Sx(x=2~6之间)
③S+K2SO3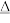 K2S2O3
K2S2O3
(1)以上于氧化还原反应的有_______ (填写序号)
(2)0.480 g硫单质与n mol热KOH溶液恰好完全反应,只生成K2S和K2SO3,则n=_______ 。
(3)2.560 g硫单质与0.06 mol热KOH溶液恰好完全反应,只生成K2Sx和K2S2O3,则x=_______ 。
臭氧层是地球生命的保护神,臭氧比氧气具有更强的氧化性,实验室可将氧气通过高压放电管来制取臭氧;3O2 2O3,回答下列问题:
2O3,回答下列问题:
(4)若在上述反应中有30%的氧气转化为臭氧,所得混合气的平均摩尔质量为_______ (保留一位小数);
(5)将8 L氧气通过放电管后,恢复到原状况,得到气体6.5 L,其中臭氧为_______ L;
(6)实验室将氧气和臭氧的混合气体0.896 L(标准状况)通入盛有20.0 g铜粉的反应器中,充分加热后(气态全部参与反应),粉末的质量变为21.6 g,则原混合气中臭氧的体积分数为_______ 。该混合气体对氢气的相对密度为_______ 。
①3S+6KOH
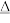 2K2S+K2SO3+3H2O
2K2S+K2SO3+3H2O②(x-1)S+K2S
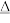 K2Sx(x=2~6之间)
K2Sx(x=2~6之间)③S+K2SO3
 K2S2O3
K2S2O3(1)以上于氧化还原反应的有
(2)0.480 g硫单质与n mol热KOH溶液恰好完全反应,只生成K2S和K2SO3,则n=
(3)2.560 g硫单质与0.06 mol热KOH溶液恰好完全反应,只生成K2Sx和K2S2O3,则x=
臭氧层是地球生命的保护神,臭氧比氧气具有更强的氧化性,实验室可将氧气通过高压放电管来制取臭氧;3O2
 2O3,回答下列问题:
2O3,回答下列问题:(4)若在上述反应中有30%的氧气转化为臭氧,所得混合气的平均摩尔质量为
(5)将8 L氧气通过放电管后,恢复到原状况,得到气体6.5 L,其中臭氧为
(6)实验室将氧气和臭氧的混合气体0.896 L(标准状况)通入盛有20.0 g铜粉的反应器中,充分加热后(气态全部参与反应),粉末的质量变为21.6 g,则原混合气中臭氧的体积分数为
您最近一年使用:0次



