CO2的减排已经引起国际社会的广泛关注,近日我国科学家实现了CO2高选择性、高稳定性加氢合成甲醇(CH3OH)。回答下列问题:
(1)CO2的摩尔质量是______ g/mol。
(2)在标准状态下,5.6LCO2的物质的量是______ mol,质量是_______ g。
(3)22gCO2的体积是_______ L(标准状况)。
(4)相同质量的CO和CO2所含的氧原子个数比是_______ 。
(5)同温同压下,同体积的CO和CO2的物质的量之比为__________ 。
(1)CO2的摩尔质量是
(2)在标准状态下,5.6LCO2的物质的量是
(3)22gCO2的体积是
(4)相同质量的CO和CO2所含的氧原子个数比是
(5)同温同压下,同体积的CO和CO2的物质的量之比为
更新时间:2020-12-05 20:10:46
|
相似题推荐
计算题
|
适中
(0.65)
【推荐1】
(1)5.4 g H2O的物质的量是________ ,含有__________________ 个水分子,含有________ mol H。
(2)11.7 g NaCl的物质的量是________ ,含有________ 个Na+,________________ 个Cl-,共含离子________ mol。
(3)6.02×1022个OH-的质量为________ ,含有质子的物质的量为________ ,含有电子的物质的量为________ ,这些OH-与________ mol NH3的质量相同,和________ g Na+含有的离子数相同。
(1)5.4 g H2O的物质的量是
(2)11.7 g NaCl的物质的量是
(3)6.02×1022个OH-的质量为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】白玉的化学式可用CaxMgySipO22(OH)2表示(也可用Ca、Mg、Si、H的氧化物表示)。取8.10g白玉粉末灼烧至恒重,固体减少了0.18g,则白玉的摩尔质量为_______ 。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】在50℃和1.01×105Pa时,相同质量的SO2和SO3的体积比是________ ,密度比是___________
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】(1)标准状况下,1.204×1023个氧气分子的体积是________ L;
(2)标准状况下,某气体的密度为1.25 g·L-1,则其摩尔质量为________ ;
(3)将4.6 g钠投入足量的水中,生成NaOH的质量为______ g,生成H2的体积在标准状况下为____________ 。
(4)400 mL某浓度的NaOH溶液恰好与11.2 L Cl2(标准状况)完全反应,生成NaClO的物质的量为________ ,原NaOH溶液物质的量浓度为_________________ 。
(5)在标准状况下,CO和CO2的混合气体共17.92 L,质量为28.8 g。则两种气体的物质的量之和为____________ mol,其中CO2为________ mol。
(2)标准状况下,某气体的密度为1.25 g·L-1,则其摩尔质量为
(3)将4.6 g钠投入足量的水中,生成NaOH的质量为
(4)400 mL某浓度的NaOH溶液恰好与11.2 L Cl2(标准状况)完全反应,生成NaClO的物质的量为
(5)在标准状况下,CO和CO2的混合气体共17.92 L,质量为28.8 g。则两种气体的物质的量之和为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】NH3和Cl2可快速反应:2NH3+3Cl2→N2+6HCl。有标况下100LNH3和Cl2混合气体,充分反应后的混合气体中N2占混合气体的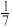 ,则N2的物质的量可能为
,则N2的物质的量可能为
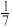 ,则N2的物质的量可能为
,则N2的物质的量可能为| A.0.263mol | B.0.483mol | C.0.526mol | D.0.663mol |
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】填空。
(1)9.5 g某二价金属氯化物中含有0.2 mol Cl-,此氯化物的摩尔质量为_______ ,该金属元素的相对原子质量为_______ 。
(2)a个X原子的总质量为b g,则X的相对原子质量为_______ 。
(3)将62 g Na2O溶于水并配成1L溶液,则该溶液的物质的量浓度为_______ 。
(4)0.2 g H2、8.8 g CO2组成的混合气体其密度是同样条件下H2的密度的_______ 倍。
(5)某气体在标准状况下的密度为1.25 g·L-1 ,则28 g该气体所含有的分子数为_______ 。
(1)9.5 g某二价金属氯化物中含有0.2 mol Cl-,此氯化物的摩尔质量为
(2)a个X原子的总质量为b g,则X的相对原子质量为
(3)将62 g Na2O溶于水并配成1L溶液,则该溶液的物质的量浓度为
(4)0.2 g H2、8.8 g CO2组成的混合气体其密度是同样条件下H2的密度的
(5)某气体在标准状况下的密度为1.25 g·L-1 ,则28 g该气体所含有的分子数为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐1】写出下列序号所代表的内容(假设温度为0℃,压强为101Kpa):
| 物质 | 分子数 | 质量 | 物质的量 | 摩尔质量 | 体积 |
| 氧气 | 3.01×1023 | 16g | ① | 32g/mol | ② |
| 水 | ③ | ④ | 2mol | ⑤ | 40cm3 |
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】Ⅰ.(1)标准状况下,1.92 g某气体的体积为672 mL,则此气体的相对分子质量为________ 。
(2)在25 ℃、101 kPa的条件下,同质量的CH4和A气体的体积之比是15∶8,则A的摩尔质量为______________ 。
(3)两个相同容积的密闭容器X、Y,在25 ℃下,X中充入a g A气体,Y中充入a g CH4气体,X与Y内的压强之比是4∶11,则A的摩尔质量为________ 。
Ⅱ.在标准状况下,将aLNH3完全溶于水得到VmL氨水,溶液的密度为ρ g·cm-3,计算该溶液的浓度(用以上字母表示)。
(1)该溶液的物质的量浓度________________
(2)该溶液的质量分数_________________________
Ⅲ.有两份溶液,其中所含溶质相同,设其摩尔质量为M g·mol-1。根据下表信息,回答有关问题:
(1)取等质量两份溶液混合,则所得混合液中溶质的质量分数w3=________ 。(用以上字母表示)
(2)若有w1>w2,取等体积的两份溶液混合,设所得混合液中溶质的质量分数为w4,若ρ1>ρ2,则w3___ w4;若ρ1<ρ2,w3______ w4(填“>”“<”或“=”)。
(2)在25 ℃、101 kPa的条件下,同质量的CH4和A气体的体积之比是15∶8,则A的摩尔质量为
(3)两个相同容积的密闭容器X、Y,在25 ℃下,X中充入a g A气体,Y中充入a g CH4气体,X与Y内的压强之比是4∶11,则A的摩尔质量为
Ⅱ.在标准状况下,将aLNH3完全溶于水得到VmL氨水,溶液的密度为ρ g·cm-3,计算该溶液的浓度(用以上字母表示)。
(1)该溶液的物质的量浓度
(2)该溶液的质量分数
Ⅲ.有两份溶液,其中所含溶质相同,设其摩尔质量为M g·mol-1。根据下表信息,回答有关问题:
| 溶质的质量分数 | 溶液的密度(g·cm-3) | |
| 第一份溶液 | w1 | ρ1 |
| 第二份溶液 | w2 | ρ2 |
(1)取等质量两份溶液混合,则所得混合液中溶质的质量分数w3=
(2)若有w1>w2,取等体积的两份溶液混合,设所得混合液中溶质的质量分数为w4,若ρ1>ρ2,则w3
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】(1)35Cl-离子结构示意图_______ 。
(2)16.4 g NaR含有Na+ 0.2 mol,则NaR的摩尔质量为____ ,则含R-的质量为5.9 g的NaR的物质的量为_______ 。
(3)标准状况下,3.2 g甲烷(CH4)所占的体积为___ L,它与标准状况下__ L硫化氢(H2S)含有相同数目的氢原子。
(4)在200 g浓度为18 mol·L-1、密度为ρ (g·cm-3)的浓硫酸中加入一定量的水稀释成9 mol·L-1的硫酸,则加入水的体积_____ 200 mL。(填“>”“<”、“=”)
(2)16.4 g NaR含有Na+ 0.2 mol,则NaR的摩尔质量为
(3)标准状况下,3.2 g甲烷(CH4)所占的体积为
(4)在200 g浓度为18 mol·L-1、密度为ρ (g·cm-3)的浓硫酸中加入一定量的水稀释成9 mol·L-1的硫酸,则加入水的体积
您最近一年使用:0次