现有14.4 g CO和CO2的混合气体,在标准状况下所占的体积约为8.96 L。回答下列问题:
(1)该混合气体中CO物质的量为________ ;CO2物质的量为_________ 。
(2)混合气体中碳原子的个数___________ 。(用NA表示阿伏加 德罗常数的值)
(3)将混合气体依次通过如图装置,最后收集在气球中。
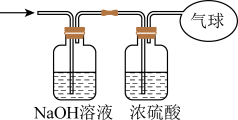
①气球中收集到的气体的摩尔质量_________ ;
②标况下气球中收集到的气体的体积为________________ ;
③气球中收集到的气体的电子总数为________ 。(用NA表示阿伏加 德罗常数的值)
(1)该混合气体中CO物质的量为
(2)混合气体中碳原子的个数
(3)将混合气体依次通过如图装置,最后收集在气球中。

①气球中收集到的气体的摩尔质量
②标况下气球中收集到的气体的体积为
③气球中收集到的气体的电子总数为
2019高一上·全国·专题练习 查看更多[1]
(已下线)2019年9月1日 《每日一题》 必修1 每周一测
更新时间:2019-08-23 15:42:16
|
相似题推荐
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】将2.1g镁铝合金的粉末放入过量的盐酸中,得到2.24LH2(标准状况下)。计算:
(1)反应得到H2的物质的量为_______ mol;
(2)该合金中镁的质量分数_______
(1)反应得到H2的物质的量为
(2)该合金中镁的质量分数
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】气体摩尔体积是指在一定温度和压强下,单位物质的量的气体所占的体积。22.4 L·mol-1是标准状况下的气体摩尔体积(Vm)。在不同的温度和压强下,气体摩尔体积的数值也会发生变化。例如,在273℃、101 kPa条件下,Vm约为44.8 L·mol-1。
(1)请判断101 kPa、50℃时的Vm比22.4 L·mol-1_____ (填“大”或“小”),理由是_______ 。
(2)标准状况下,CO气体的密度为_______ ,273℃、101 kPa时,67.2 L气体的物质的量为______ 。
(3)已知KClO3在MnO2催化、101 kPa、210℃时即可分解得到O2;现将73.5 g KClO3在MnO2催化、101 kPa条件下加热至273℃。若完全分解,则可以得到该状况下O2__________ L。
(1)请判断101 kPa、50℃时的Vm比22.4 L·mol-1
(2)标准状况下,CO气体的密度为
(3)已知KClO3在MnO2催化、101 kPa、210℃时即可分解得到O2;现将73.5 g KClO3在MnO2催化、101 kPa条件下加热至273℃。若完全分解,则可以得到该状况下O2
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐3】某气体的摩尔质量为Mg/mol,现有该气体mg, 用NA表示阿伏加 德罗常数,求下列量:
①该气体的物质的量为______________ mol;
②该气体在标准状况下的体积为_________________ L;
③该气体在标准状况下的密度为_________________ g/L;
④该气体一个分子的质量为_________________ g;
⑤该气体m g完全溶解于水(气体与水不反应),得到100mL溶液,所得溶液的物质的量浓度为___ mol/L。
①该气体的物质的量为
②该气体在标准状况下的体积为
③该气体在标准状况下的密度为
④该气体一个分子的质量为
⑤该气体m g完全溶解于水(气体与水不反应),得到100mL溶液,所得溶液的物质的量浓度为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】将30g MnO2的质量分数为76.6%的软锰矿石与足量的浓度为12 molL-1的浓盐酸完全反应(杂质不参加反应),试计算:
(1)参加反应的浓盐酸的体积的大小(结果保留3位小数)。____________
(2)在标准状况下,生成Cl2的体积的大小________ (结果保留1位小数,已知软锰矿石与浓盐酸反应的化学方程式为MnO2+4HCl(浓) =MnCl2+Cl2↑+2H2O)。
(1)参加反应的浓盐酸的体积的大小(结果保留3位小数)。
(2)在标准状况下,生成Cl2的体积的大小
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】已知实验室在加热条件下制取Cl2的化学方程式为:MnO2+4HCl(浓)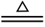 MnCl2+Cl2↑+2H2O。现将8.7 g MnO2投入到200 g质量分数为36.5%(过量)的浓盐酸中加热,充分反应后,求:
MnCl2+Cl2↑+2H2O。现将8.7 g MnO2投入到200 g质量分数为36.5%(过量)的浓盐酸中加热,充分反应后,求:
(1)标准状况下生成Cl2的体积为________ 。
(2)反应生成的MnCl2的物质的量为________ 。
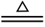 MnCl2+Cl2↑+2H2O。现将8.7 g MnO2投入到200 g质量分数为36.5%(过量)的浓盐酸中加热,充分反应后,求:
MnCl2+Cl2↑+2H2O。现将8.7 g MnO2投入到200 g质量分数为36.5%(过量)的浓盐酸中加热,充分反应后,求:(1)标准状况下生成Cl2的体积为
(2)反应生成的MnCl2的物质的量为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐3】(1)在标准状况下,5.6L A气体的质量是15g,则A的摩尔质量为___ 。
(2)一定量的液态化合物XY2,在一定量的O2中恰好完全燃烧,反应方程式为:XY2(液)+ 3O2(气)= XO2(气)+2YO2(气),冷却后,在标准状况下测得生成物的体积是672mL,密度是2.56g/L,则:
①反应前O2的体积是______ 。
②化合物XY2的摩尔质量是____ 。
③若XY2分子中X、Y两元素的质量之比为3:16,则X、Y两元素分别是_____ 和_____ 。(写元素符号)
(2)一定量的液态化合物XY2,在一定量的O2中恰好完全燃烧,反应方程式为:XY2(液)+ 3O2(气)= XO2(气)+2YO2(气),冷却后,在标准状况下测得生成物的体积是672mL,密度是2.56g/L,则:
①反应前O2的体积是
②化合物XY2的摩尔质量是
③若XY2分子中X、Y两元素的质量之比为3:16,则X、Y两元素分别是
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐1】物质的量是高中化学中常用的物理量,请完成以下内容。(注意:用NA表示阿伏加 德罗常数)
(1)3.01×1023个SO2分子中含有氧原子的个数为_____ 。
(2)常温常压下,92gNO2气体含有的原子数为______ 。
(3)200mLAl2(SO4)3溶液中含Al3+5.4g,则溶液中c( )=
)=_______ 。
(4)将2.86gNa2CO3·10H2O溶于水中,要使每100个水分子中溶有1个Na+,则需水的质量为____ g。向上述溶液中加入足量稀盐酸,反应产生的气体在标准状况下体积为___ mL。
(5)已知agA和bgB恰好完全反应生成0.2molC和dgD,则C的摩尔质量为_ 。(用a、b、d表示)
(1)3.01×1023个SO2分子中含有氧原子的个数为
(2)常温常压下,92gNO2气体含有的原子数为
(3)200mLAl2(SO4)3溶液中含Al3+5.4g,则溶液中c(
 )=
)=(4)将2.86gNa2CO3·10H2O溶于水中,要使每100个水分子中溶有1个Na+,则需水的质量为
(5)已知agA和bgB恰好完全反应生成0.2molC和dgD,则C的摩尔质量为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】按要求回答下列问题:
(1)在标准状况下,V L H2 中含有 N 个氢分子,则阿伏加 德罗常数为_____ mol-1
(2)8.5 g氢氧根离子含有的电子数目为________ 。
(3)已知8 g A能与32 g B恰好完全反应,生成22 g C和一定量的D;现将16 g A与70 g B混合,充分反应后,生成2 mol D和一定量的C,则D的相对分子质量为_________ 。
(4)标准状况下,8.96L的CH4和CO的混合气体,该混合气体对氢气的相对密度是9.5,则混合气体平均摩尔质量为____________ ,混合气体中CH4与CO的体积比为____ 。
(5)若在标准状况下,将VLHCl气体溶于1L水中,所得溶液密度为d g/mL,则此溶液的物质的量浓度为________ mol/L。(用带字母的表达式回答)
(1)在标准状况下,V L H2 中含有 N 个氢分子,则阿伏加 德罗常数为
(2)8.5 g氢氧根离子含有的电子数目为
(3)已知8 g A能与32 g B恰好完全反应,生成22 g C和一定量的D;现将16 g A与70 g B混合,充分反应后,生成2 mol D和一定量的C,则D的相对分子质量为
(4)标准状况下,8.96L的CH4和CO的混合气体,该混合气体对氢气的相对密度是9.5,则混合气体平均摩尔质量为
(5)若在标准状况下,将VLHCl气体溶于1L水中,所得溶液密度为d g/mL,则此溶液的物质的量浓度为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】(1)甲烷(CH4)的摩尔质量为____________ ;相对分子质量为__________ 。
(2)8 g CH4中约含有_______ 个分子,在标准状况下所占的体积约为________ L。
(3)所含物质的量相等的甲烷和氨气(NH3)的质量比为_________ 。
(2)8 g CH4中约含有
(3)所含物质的量相等的甲烷和氨气(NH3)的质量比为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】完成下列问题
(1)3.01×1023个氯气分子的物质的量是_______ ,质量为_______ ;
(2)1.5 mol Na2SO4·10H2O中所含的Na+的物质的量是_______ ,所含的SO 的物质的量是
的物质的量是_______ ,所含H2O的数目是_______ ;
(3)一定量的Na2CO3中,碳原子和氧原子的物质的量之比为_______ ;
(4)0.5 mol NaOH中含有电子的物质的量是_______ ,在_______ mol Na2CO3中所含Na+数目与上述0.5 mol NaOH所含Na+数目相等。
(5)12.4gNa2R含0.4molNa+,则Na2R的摩尔质量为_______ ,R的相对原子质量为_______ ,含R的质量为1.6g的Na2R,其物质的量为_______ ;
(6)标准状况下,1.92g某气体的体积为672mL,则此气体的相对分子质量为_______ ;
(7)在标准状况下,CO和CO2的混合气体共39.2L,质量为61g,则两种气体的物质的量之和为_______ mol,CO占总质量的_______ %(结果取整数)
(1)3.01×1023个氯气分子的物质的量是
(2)1.5 mol Na2SO4·10H2O中所含的Na+的物质的量是
 的物质的量是
的物质的量是(3)一定量的Na2CO3中,碳原子和氧原子的物质的量之比为
(4)0.5 mol NaOH中含有电子的物质的量是
(5)12.4gNa2R含0.4molNa+,则Na2R的摩尔质量为
(6)标准状况下,1.92g某气体的体积为672mL,则此气体的相对分子质量为
(7)在标准状况下,CO和CO2的混合气体共39.2L,质量为61g,则两种气体的物质的量之和为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐3】物质的量是沟通宏观和微观的桥梁,请回答下列问题。
(1)下列所给出的几组物质中:含有分子数最少的是__ ;标准状况下体积最小的是____ (填序号)。
①1gH2;②2.408×1023个CH4;③10.8gH2O; ④标准状况下6.72LCO2。
(2)标准状况下,44.8LHCl气体溶于水配制成500 mL的溶液,则溶液中Cl﹣的物质的量浓度为______ 。
(3)等质量的SO2和SO3所含的分子个数比为______ ,原子个数比为______ ,同温同压体积比为______ 。
(4)已知8.0gRO3中含有0.3mol O原子,则 RO3的摩尔质量是____ ,R元素是____ (填元素符号)。
(5)一定温度和压强下,20mL气体X2与10mL气体Y2恰好完全反应,生成20mL 气体Z,则Z 的化学式为_____ 。
(1)下列所给出的几组物质中:含有分子数最少的是
①1gH2;②2.408×1023个CH4;③10.8gH2O; ④标准状况下6.72LCO2。
(2)标准状况下,44.8LHCl气体溶于水配制成500 mL的溶液,则溶液中Cl﹣的物质的量浓度为
(3)等质量的SO2和SO3所含的分子个数比为
(4)已知8.0gRO3中含有0.3mol O原子,则 RO3的摩尔质量是
(5)一定温度和压强下,20mL气体X2与10mL气体Y2恰好完全反应,生成20mL 气体Z,则Z 的化学式为
您最近一年使用:0次



