完成下列问题。
(1)下列反应中,属于放热反应的是___________ (填字母,下同),属于吸热反应的是___________ 。
a.盐酸与烧碱溶液反应 b.Ba(OH)2·8H2O+2NH4Cl=BaCl2+10H2O+2NH3↑
c.氢气在氧气中燃烧生成水 d.高温煅烧石灰石使其分解
e.铝和盐酸反应 f.葡萄糖在人体内氧化分解
(2)为了研究化学反应A+B=C+D的能量变化情况,某同学设计了如图所示装置。当向盛有A的试管中滴加试剂B时,看到U形管中甲处液面下降乙处液面上升。
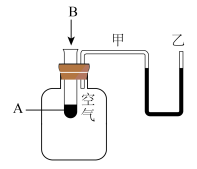
试回答下列问题:
①该反应为___________ 反应(填“放热”或“吸热”)。
②该反应的反应物化学键断裂吸收的能量________ (填“高”或“低”)于生成物化学键形成放出的能量。
(3) A、B、C、D四种金属按下表中装置进行实验。
根据实验现象回答下列问题:
①装置甲溶液中的阴离子移向________ (填“A”或“B”)极。
②装置乙中正极的电极反应式为________ 。
③四种金属活动性由强到弱的顺序是________ 。
(4)甲烷可直接应用于燃料电池,该电池采用KOH溶液为电解质,其工作原理如下图所示:
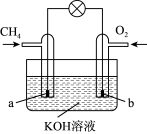
①外电路电子移动方向:___________ (填“a极到b极”或“b极到a极”)。
②a电极的电极方程式为___________ 。
(1)下列反应中,属于放热反应的是
a.盐酸与烧碱溶液反应 b.Ba(OH)2·8H2O+2NH4Cl=BaCl2+10H2O+2NH3↑
c.氢气在氧气中燃烧生成水 d.高温煅烧石灰石使其分解
e.铝和盐酸反应 f.葡萄糖在人体内氧化分解
(2)为了研究化学反应A+B=C+D的能量变化情况,某同学设计了如图所示装置。当向盛有A的试管中滴加试剂B时,看到U形管中甲处液面下降乙处液面上升。

试回答下列问题:
①该反应为
②该反应的反应物化学键断裂吸收的能量
(3) A、B、C、D四种金属按下表中装置进行实验。
| 装置 | 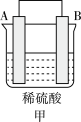 |  |  |
| 现象 | 金属A不断溶解 | C的质量增加 | A上有气体产生 |
①装置甲溶液中的阴离子移向
②装置乙中正极的电极反应式为
③四种金属活动性由强到弱的顺序是
(4)甲烷可直接应用于燃料电池,该电池采用KOH溶液为电解质,其工作原理如下图所示:

①外电路电子移动方向:
②a电极的电极方程式为
更新时间:2023-10-04 21:20:24
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】I.依据事实,写出下列反应的热化学方程式。
(1)在25℃、101kpa下,1g甲烷燃烧生成CO2和液态水时放热22.68kJ。则表示甲烷燃烧的热化学方程式为________ 。
(2)已知拆开1molH-H键,1molN-H键,1molN≡N键分别需要的能量是436kJ、391kJ、946kJ,则N2与H2反应生成NH3的热化学方程式为________ 。
II.某实验小组同学进行如图实验,以检验化学反应中的能量变化。请回答下列问题:
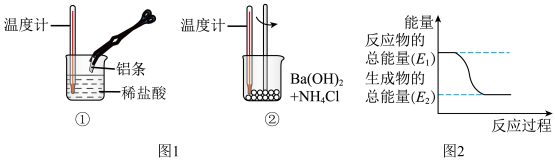
(3)实验中发现,反应后①中的温度升高;②中的温度降低,由此判断铝条与盐酸的反应是________ ,(选填“放热反应”或“吸热反应”,下同。)Ba(OH)2•8H2O与NH4Cl的反应是________ ,反应过程________ 。(填“①”或“②”)的能量变化可用图2表示。
(1)在25℃、101kpa下,1g甲烷燃烧生成CO2和液态水时放热22.68kJ。则表示甲烷燃烧的热化学方程式为
(2)已知拆开1molH-H键,1molN-H键,1molN≡N键分别需要的能量是436kJ、391kJ、946kJ,则N2与H2反应生成NH3的热化学方程式为
II.某实验小组同学进行如图实验,以检验化学反应中的能量变化。请回答下列问题:

(3)实验中发现,反应后①中的温度升高;②中的温度降低,由此判断铝条与盐酸的反应是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】I.(1)某种铵根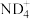 中的中子数是
中的中子数是_____ ,核外电子数是_____ 。
(2)下列装置能够组成原电池的是____ 。
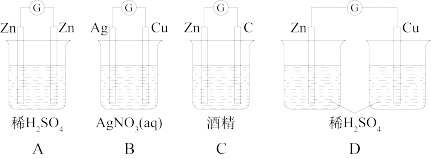
(3)已知拆开1molH—H键、1molI—I、1molH—I键分别需要吸收的能量为436kJ、151kJ、299kJ。则由氢气和碘反应生成1molHI需要____ (填“放出”或“吸收”)____ kJ的热量。
(4)用电子式表示CS2的形成过程:____ 。
Ⅱ.(1)下列物质:A.CO2 B.H2O2 C.He D.CuSO4•5H2O E.NH4Cl F.Na2O2 G.Al2O3
①既含有离子键又含有共价键的是____ ;(填序号,下同);
②既存在非极性共价键又存在极性共价键的是_______ 。
(2)下列变化:①碘的升华,②冰融化,③氯化钠溶于水,④氯化氢溶于水,⑤碳酸氢钠加热分解,化学键未被破坏的是____ ;仅共价键被破坏的是____ 。
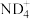 中的中子数是
中的中子数是(2)下列装置能够组成原电池的是

(3)已知拆开1molH—H键、1molI—I、1molH—I键分别需要吸收的能量为436kJ、151kJ、299kJ。则由氢气和碘反应生成1molHI需要
(4)用电子式表示CS2的形成过程:
Ⅱ.(1)下列物质:A.CO2 B.H2O2 C.He D.CuSO4•5H2O E.NH4Cl F.Na2O2 G.Al2O3
①既含有离子键又含有共价键的是
②既存在非极性共价键又存在极性共价键的是
(2)下列变化:①碘的升华,②冰融化,③氯化钠溶于水,④氯化氢溶于水,⑤碳酸氢钠加热分解,化学键未被破坏的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】(1)反应A(g)+B(g) 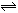 C(g)+D(g)过程中的能量变化如图所示,回答下列问题。
C(g)+D(g)过程中的能量变化如图所示,回答下列问题。
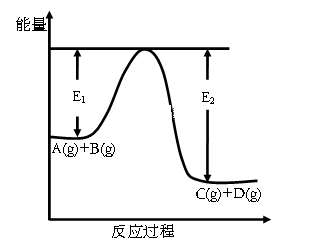
①该反应是____________ 反应(填“吸热”或“放热”);
②当反应达到平衡时,升高温度,A的转化率_____________ (填“增大”“减小”“不变”)。
③在反应体系中加入催化剂,反应速率增大,E1和E2的变化是:E1____________ ,E2_________________ (填“增大”“减小”“不变”)。
(2)101 kPa时,1 mol H2完全燃烧生成液态水,放出285.8 kJ的热量,表示H2燃烧热的化学方程式为__________________________________________________________ 。
(3)0.3 mol乙硼烷(分子式B2H6)在氧气中燃烧,生成固态三氧化二硼和液态水,放出649.5 kJ的热量,则其热化学方程式为______________________________________ 。
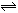 C(g)+D(g)过程中的能量变化如图所示,回答下列问题。
C(g)+D(g)过程中的能量变化如图所示,回答下列问题。
①该反应是
②当反应达到平衡时,升高温度,A的转化率
③在反应体系中加入催化剂,反应速率增大,E1和E2的变化是:E1
(2)101 kPa时,1 mol H2完全燃烧生成液态水,放出285.8 kJ的热量,表示H2燃烧热的化学方程式为
(3)0.3 mol乙硼烷(分子式B2H6)在氧气中燃烧,生成固态三氧化二硼和液态水,放出649.5 kJ的热量,则其热化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】氯铝电池是一种新型的燃料电池,电解质溶液是KOH溶液,试回答下列问题:
(1)通入氯气的电极是___________ 极(填“正”或“负”),电极反应式为:___________ 。
(2)加入铝的电极是___________ 极(填“正”或“负”),电极反应式为:___________ 。
(3)电子从___________ 极流向___________ 极(填“Al”或“Cl2”)。
(1)通入氯气的电极是
(2)加入铝的电极是
(3)电子从
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】某研究性学习小组的同学设计了一个原电池如图所示:
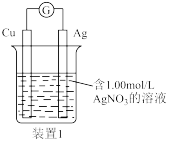
Ⅰ.根据上述原电池,请回答下列问题:
(1)Ag电极是_______ 极(填“正”或“负”),铜电极上发生的电极反应式是_______ 。
(2)溶液中的NO3-的移动方向为_______ (填“自右向左” 或“自左向右”)。
Ⅱ.研究性学习小组的同学们对该原电池中应出现的实验现象进行了预测,他们认为应该有这些现象:
①Cu电极要发生溶解;
②电流计中指针发生偏转;
③Ag电极上有固体物质析出;
④……
请回答下列问题:
(3)预测④的现象为_______ 。
(4)但同学们发现,除了以上预测的现象之外,在银电极附近出现了无色气泡,一段时间后银电极上方的空气中出现红棕色。该红棕色气体为_______ 。
(5)为了探究出现该现象的原因,同学们测定了电解质溶液的pH,发现溶液中的H+浓度为0.80mol/L,据此推断,原电池体系中应存在化学反应_______ (写出该反应的离子方程式)。
(6)同学们通过查阅资料了解到,常温下1.00mol/L的AgNO3溶液pH为5(即H+ 为10-5mol/L),说明装置1中硝酸银溶液已用硝酸进行了酸化。于是又设计了另一个原电池(装置2)以说明上述原电池中的确存在这一反应,如图所示,以下最宜 选用为该电池电解质溶液的是_______ (填标号)。
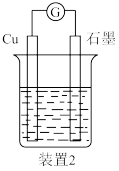
a.0.80mol/L HNO3
b.0.80mol/L HCl和1.00 mol/L NaNO3的混合液
c.0.40mol/L H2SO4和1.80mol/L NaNO3的混合溶液
d.0.80mol/L CH3COOH和1.00mol/L NaNO3的混合溶液
通过实验,发现该电池在一段时间后出现与(2)中相同的现象,说明原电池中的确存在该反应。
Ⅲ.为了进一步探究电解质溶液的浓度对电池反应速率的影响,同学们准备了两组装置,并分别在它们的银电极上安装了重力传感器,其中一组电解质溶液为500mL 1.00mol/L AgNO3溶液;另一组为500mL 0.50mol/L AgNO3溶液(两组硝酸银溶液均已净化,为单一组分),由传感器所得数据作图如图:
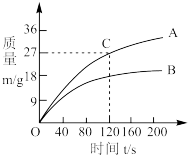
(7)其中代表电解质为0.50mol/L AgNO3溶液的一组的曲线是_______ (填“A”或“B”) 。
(8)对于A曲线,以硝酸银溶液浓度变化来表示120s内的反应速率υ=_______ (保留2位有效数字,忽略溶液的体积变化)。

Ⅰ.根据上述原电池,请回答下列问题:
(1)Ag电极是
(2)溶液中的NO3-的移动方向为
Ⅱ.研究性学习小组的同学们对该原电池中应出现的实验现象进行了预测,他们认为应该有这些现象:
①Cu电极要发生溶解;
②电流计中指针发生偏转;
③Ag电极上有固体物质析出;
④……
请回答下列问题:
(3)预测④的现象为
(4)但同学们发现,除了以上预测的现象之外,在银电极附近出现了无色气泡,一段时间后银电极上方的空气中出现红棕色。该红棕色气体为
(5)为了探究出现该现象的原因,同学们测定了电解质溶液的pH,发现溶液中的H+浓度为0.80mol/L,据此推断,原电池体系中应存在化学反应
(6)同学们通过查阅资料了解到,常温下1.00mol/L的AgNO3溶液pH为5(即H+ 为10-5mol/L),说明装置1中硝酸银溶液已用硝酸进行了酸化。于是又设计了另一个原电池(装置2)以说明上述原电池中的确存在这一反应,如图所示,以下

a.0.80mol/L HNO3
b.0.80mol/L HCl和1.00 mol/L NaNO3的混合液
c.0.40mol/L H2SO4和1.80mol/L NaNO3的混合溶液
d.0.80mol/L CH3COOH和1.00mol/L NaNO3的混合溶液
通过实验,发现该电池在一段时间后出现与(2)中相同的现象,说明原电池中的确存在该反应。
Ⅲ.为了进一步探究电解质溶液的浓度对电池反应速率的影响,同学们准备了两组装置,并分别在它们的银电极上安装了重力传感器,其中一组电解质溶液为500mL 1.00mol/L AgNO3溶液;另一组为500mL 0.50mol/L AgNO3溶液(两组硝酸银溶液均已净化,为单一组分),由传感器所得数据作图如图:

(7)其中代表电解质为0.50mol/L AgNO3溶液的一组的曲线是
(8)对于A曲线,以硝酸银溶液浓度变化来表示120s内的反应速率υ=
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】某研究小组设计的铜铁原电池如图所示。
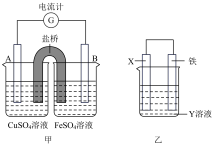
(1)若原电池装置为图甲:
①工作时,下列叙述正确的是________ (填字母)。
A.正极反应为Fe-2e-=Fe2+
B.电池反应为Fe+Cu2+=Fe2++Cu
C.在外电路中,电子从负极流向正极
D.盐桥中的K+移向FeSO4溶液
②A电极观察到的现象是________ 。
(2)若原电池装置为图乙:
①电极材料X可以是________ (填序号,下同)。
a.铁 b.铜 c.石墨
②Y溶液是________ 。
a.FeSO4溶液 b.CuSO4溶液 c.CuCl2溶液

(1)若原电池装置为图甲:
①工作时,下列叙述正确的是
A.正极反应为Fe-2e-=Fe2+
B.电池反应为Fe+Cu2+=Fe2++Cu
C.在外电路中,电子从负极流向正极
D.盐桥中的K+移向FeSO4溶液
②A电极观察到的现象是
(2)若原电池装置为图乙:
①电极材料X可以是
a.铁 b.铜 c.石墨
②Y溶液是
a.FeSO4溶液 b.CuSO4溶液 c.CuCl2溶液
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
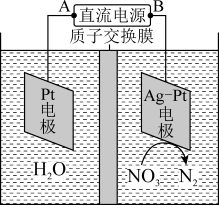
【推荐1】电化学降解NO3﹣的原理如图所示.
(1)电源A极为_____ (填“正极”或“负极”),阴极反应式为_____ 。
(2)若电解过程中转移了1mol电子,则膜左侧电解液的质量减少量为_____ g。
(1)电源A极为
(2)若电解过程中转移了1mol电子,则膜左侧电解液的质量减少量为

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】将质量相等的铁片和铜片用导线及电流计相连浸入500mL硫酸铜溶液中构成如图所示的装置(以下均假设反应过程中溶液体积不变),回答下列问题:

(1)该装置为_______ 池,其能量转化形式为_______ 。
(2)铜片作_______ (填“正”或“负”,下同)极,铁片作_______ 极,铁片上发生的反应为_______ 。
(3)若一段时间后,铁片与铜片的质量差为1.2 g,则导线中流过的电子的物质的量为_______ (不考虑其他形式的能量转化)。
(4)某同学利用家中废旧材料制作可使扬声器发出声音的电池,装置如图所示。下列说法正确的是_______ (填字母)。
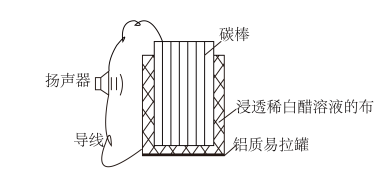
A.电流由铝制易拉罐经导线流向碳棒
B.在碳棒上有气体生成,该气体可能为氢气
C.铝质易拉罐逐渐被腐蚀,说明铝失去电子

(1)该装置为
(2)铜片作
(3)若一段时间后,铁片与铜片的质量差为1.2 g,则导线中流过的电子的物质的量为
(4)某同学利用家中废旧材料制作可使扬声器发出声音的电池,装置如图所示。下列说法正确的是

A.电流由铝制易拉罐经导线流向碳棒
B.在碳棒上有气体生成,该气体可能为氢气
C.铝质易拉罐逐渐被腐蚀,说明铝失去电子
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】I、
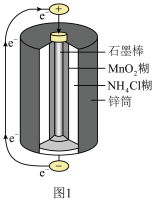
(1)锌锰干电池是最早使用的化学电池,其基本构造如图1所示:电路中每通过0.4mole-,负极质量减少___________________ g;工作时NH 在正极放电产生两种气体,其中一种气体分子是10eˉ的微粒,正极的电极反应式是
在正极放电产生两种气体,其中一种气体分子是10eˉ的微粒,正极的电极反应式是__________ 。
(2)比能量是指消耗单位质量的电极所释放的电量,用来衡量电池的优劣,则Li、Na、Al分别作为电极时比能量由大到小的顺序为__________ 。
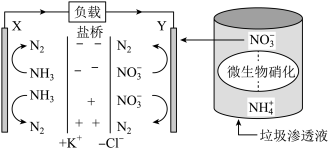
(3)某种利用垃圾渗透液实现发电装置示意图如下,当该装置工作时,Y极发生的电极反应式为____________ 。
II.锂一空气电池的理论能量密度高,是未来提高电动汽车续航里程的关键。
(4)锂一空气电池的反应原理可表示为: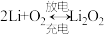 。其放电时的工作原理如图所示:
。其放电时的工作原理如图所示:
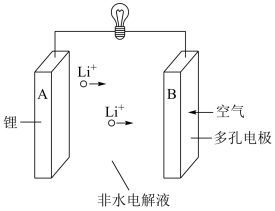
电池工作时,发生氧化反应的是___________ (填“A”或“B”)极。
(5)空气中的CO2、H2O影响电池放电。探究H2O对放电的影响:向非水电解液中加入少量水,放电后检测A、B电极上的固体物质。
A极:LiOH B极:Li2O2、LiOH
①A、B电极产生LiOH的化学方程式分别是__________ 、____________ 。
②H2O降低锂一空气电池放电、充电循环性能。
(6)探究CO2对放电的影响:使电池在三种不同气体(物质的量相等)中放电,测量外电路转移的电子与消耗O2的比值[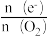 ]。
]。
①放电时,实验i中B极的电极反应式为_________________ 。
②下列分析正确的是_________________ 。
a.放电时,i、iii中通过外电路的电子数相等
b.ⅲ中B极所发生的电极反应的产物主要为Li2O2
c.ⅲ中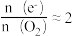 ,说明CO2未与Li2O2反应
,说明CO2未与Li2O2反应
(1)锌锰干电池是最早使用的化学电池,其基本构造如图1所示:电路中每通过0.4mole-,负极质量减少
 在正极放电产生两种气体,其中一种气体分子是10eˉ的微粒,正极的电极反应式是
在正极放电产生两种气体,其中一种气体分子是10eˉ的微粒,正极的电极反应式是
(2)比能量是指消耗单位质量的电极所释放的电量,用来衡量电池的优劣,则Li、Na、Al分别作为电极时比能量由大到小的顺序为
(3)某种利用垃圾渗透液实现发电装置示意图如下,当该装置工作时,Y极发生的电极反应式为

II.锂一空气电池的理论能量密度高,是未来提高电动汽车续航里程的关键。
(4)锂一空气电池的反应原理可表示为:
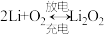 。其放电时的工作原理如图所示:
。其放电时的工作原理如图所示:
电池工作时,发生氧化反应的是
(5)空气中的CO2、H2O影响电池放电。探究H2O对放电的影响:向非水电解液中加入少量水,放电后检测A、B电极上的固体物质。
A极:LiOH B极:Li2O2、LiOH
①A、B电极产生LiOH的化学方程式分别是
②H2O降低锂一空气电池放电、充电循环性能。
(6)探究CO2对放电的影响:使电池在三种不同气体(物质的量相等)中放电,测量外电路转移的电子与消耗O2的比值[
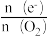 ]。
]。| 实验 | i | ii | iii |
| 气体 | O2 | CO2 | 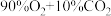 |
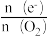 | ≈2 | 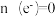 | ≈2 |
②下列分析正确的是
a.放电时,i、iii中通过外电路的电子数相等
b.ⅲ中B极所发生的电极反应的产物主要为Li2O2
c.ⅲ中
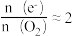 ,说明CO2未与Li2O2反应
,说明CO2未与Li2O2反应
您最近一年使用:0次



