硼氢化钠( )广泛用于化工生产,常温下能与水反应,易溶于异丙胺(沸点为33℃),工业上可用硼镁矿(主要成分为
)广泛用于化工生产,常温下能与水反应,易溶于异丙胺(沸点为33℃),工业上可用硼镁矿(主要成分为 ,含少量杂质
,含少量杂质 )制取
)制取
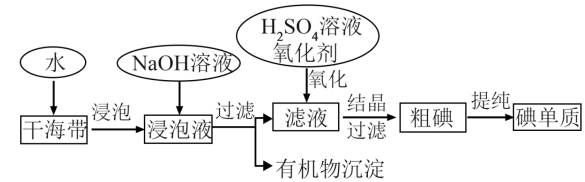
 其工艺流程如下:
其工艺流程如下:
 )广泛用于化工生产,常温下能与水反应,易溶于异丙胺(沸点为33℃),工业上可用硼镁矿(主要成分为
)广泛用于化工生产,常温下能与水反应,易溶于异丙胺(沸点为33℃),工业上可用硼镁矿(主要成分为 ,含少量杂质
,含少量杂质 )制取
)制取
 其工艺流程如下:
其工艺流程如下: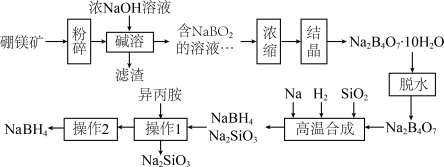
A.“碱溶”时产生的滤渣有 和 和 |
| B.“操作2”的名称为“蒸馏” |
| C.流程中可循环利用的物质有异丙胺 |
D.流程中理论上每生产 1g ,需加入还原剂的总质量约为1.92g ,需加入还原剂的总质量约为1.92g |
23-24高三上·重庆渝中·期中 查看更多[2]
更新时间:2023/11/16 10:07:34
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】下列反应的离子方程式正确的是
A.醋酸与氢氧化钠溶液反应: |
B.盐酸与铁屑反应: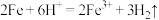 |
C.氯气溶于水: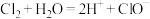 |
D.小苏打治疗胃酸过多: |
您最近一年使用:0次
【推荐2】向含Fe2+、I-、Br-的溶液中通入过量的氯气,溶液中四种粒子的物质的量变化如图所示,已知:b-a=5,线段Ⅳ表示一种含氧酸,且Ⅰ和Ⅳ表示的物质中含有相同的元素。下列说法正确的是


| A.线段Ⅰ表示Fe2+的变化情况 |
| B.根据图象可计算a=5 |
C.线段Ⅳ发生反应的离子方程式为I2+5Cl2+12OH-=2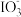 +10Cl-+6H2O +10Cl-+6H2O |
| D.原溶液中c(Fe2+):c(I-):c(Br-)=2:1:3 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】氮氧化物尾气可以用 溶液吸收,发生反应:
溶液吸收,发生反应: ;
; 。若用
。若用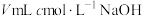 溶液恰好将尾气吸收完全,下列说法正确的是
溶液恰好将尾气吸收完全,下列说法正确的是
 溶液吸收,发生反应:
溶液吸收,发生反应: ;
; 。若用
。若用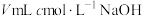 溶液恰好将尾气吸收完全,下列说法正确的是
溶液恰好将尾气吸收完全,下列说法正确的是A.氮氧化物尾气的体积一定为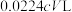 |
B.所得溶液中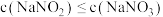 |
C.氮氧化物尾气中 可能大于 可能大于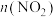 |
D.反应过程中转移电子的物质的量为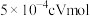 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】选择性催化还原技术是一种以NH3作为还原剂,将烟气中NOx分解成无害的N2和H2O的干法脱硝技术,反应原理为:
①6NO+4NH3 5N2+6H2O;
5N2+6H2O;
②6NO2+8NH3 7N2+12H2O;
7N2+12H2O;
③NO+NO2+2NH3=2N2+3H2O。
下列说法正确的是
①6NO+4NH3
 5N2+6H2O;
5N2+6H2O;②6NO2+8NH3
 7N2+12H2O;
7N2+12H2O;③NO+NO2+2NH3=2N2+3H2O。
下列说法正确的是
| A.NO2为酸性氧化物 |
| B.氮气性质不活泼,其原因是氮元素的非金属性较弱 |
| C.反应③中标准状况下每生成22.4LN2,转移电子数为1.5NA |
| D.NO→NO2→HNO3,以上各步变化均能通过一步完成 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】利用硼镁矿(主要成分为 ,含
,含 、
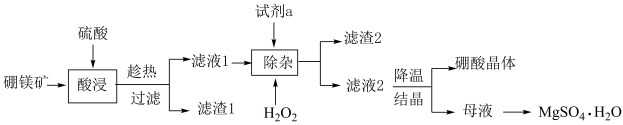
、 、铁和铝的氧化物等杂质)制备硼酸并回收硫酸镁工艺流程如图。下列叙述不正确的是
、铁和铝的氧化物等杂质)制备硼酸并回收硫酸镁工艺流程如图。下列叙述不正确的是
 ,含
,含 、
、 、铁和铝的氧化物等杂质)制备硼酸并回收硫酸镁工艺流程如图。下列叙述不正确的是
、铁和铝的氧化物等杂质)制备硼酸并回收硫酸镁工艺流程如图。下列叙述不正确的是
A.滤渣1的主要成分为 、 、 |
B.试剂a可选用 |
C.滤渣2仅含 |
D.母液经系列操作分离出晶体后,乙醇洗涤干燥可得 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】为除去括号内的杂质,所选用的试剂或者方法错误的是
| 选项 | 物质(括号内为杂质) | 除杂方法 |
| A | Fe(OH)3胶体(NaCl溶液) | 渗析 |
| B | CO2(H2O) | 通过浓硫酸 |
| C | Na2CO3固体(NaHCO3固体) | 加热至恒重 |
| D | NaCl溶液(Na2SO4) | 加适量Ba(OH)2溶液,过滤 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】常温下,下列物质久置于空气中易被氧化的是( )
| A.CH4 | B.浓硫酸 |
C.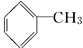 | D.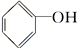 |
您最近一年使用:0次
单选题-单题
|
适中
(0.65)
【推荐2】约翰等化学家在锂电池研发中做出的突出贡献,获得2019年诺贝尔化学奖;锂电池是新能源汽车的动力电池之一,主要以磷酸亚铁锂 为原料。以下是在锂电池废料中回收锂和正极金属,流程如下,下列叙述正确的是
为原料。以下是在锂电池废料中回收锂和正极金属,流程如下,下列叙述正确的是
 为原料。以下是在锂电池废料中回收锂和正极金属,流程如下,下列叙述正确的是
为原料。以下是在锂电池废料中回收锂和正极金属,流程如下,下列叙述正确的是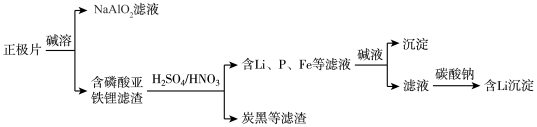
A.上述流程中可用 代替 代替 |
| B.废旧电池属于湿垃圾,可通过掩埋土壤中进行处理 |
C.从“正极片”中可回收的金属元素有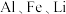 |
D.“沉淀”反应的金属离子为 |
您最近一年使用:0次

 =CaCO3↓+ H2O
=CaCO3↓+ H2O =BaSO4↓
=BaSO4↓ 中的O元素被还原
中的O元素被还原 共转移2mol电子
共转移2mol电子 为氧化产物
为氧化产物