我国化学家侯德榜发明了联合制碱法,对世界制碱工业做出了巨大贡献。联合制碱法的主要过程如图所示(部分物质已略去)。
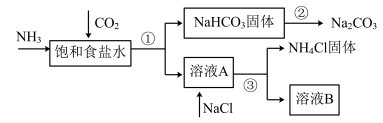
(1)①~③所涉及的操作方法中,包含过滤的是_______ ;(填序号)
(2)下列说法中,正确的是_______ (填字母)。
a.CO2可循环使用
b.副产物NH4Cl可用作肥料
c.溶液B中一定含有Na+、NH 、Cl﹣
、Cl﹣
(3)煅烧NaHCO3固体的化学方程式是_______ ;
(4)根据如图,写出①中发生反应的化学方程式:_______ 。

(1)①~③所涉及的操作方法中,包含过滤的是
(2)下列说法中,正确的是
a.CO2可循环使用
b.副产物NH4Cl可用作肥料
c.溶液B中一定含有Na+、NH
 、Cl﹣
、Cl﹣(3)煅烧NaHCO3固体的化学方程式是
(4)根据如图,写出①中发生反应的化学方程式:
更新时间:2023-10-05 10:29:34
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】我国化学家侯德榜发明了联合制碱法,对世界制碱工业做出了巨大贡献。联合制碱法的主要过程如下图所示(部分物质已略去)。
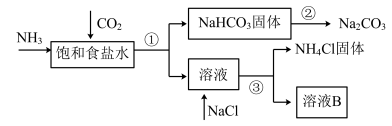
(1)根据上图,将化学方程式补充完整:________
NH3+CO2+___________+___________=NaHCO3↓+NH4Cl
(2)过程①对应的分离操作名称是___________ 。
(3)下列说法中,正确的是___________ (填字母)。
a.CO2可循环使用
b.副产物NH4Cl可用作肥料
c.溶液B中一定含有Na+、 、Cl-
、Cl-

(1)根据上图,将化学方程式补充完整:
NH3+CO2+___________+___________=NaHCO3↓+NH4Cl
(2)过程①对应的分离操作名称是
(3)下列说法中,正确的是
a.CO2可循环使用
b.副产物NH4Cl可用作肥料
c.溶液B中一定含有Na+、
 、Cl-
、Cl-
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】下列图示中,A为一种常见的单质,B、C、D、E是含A元素的常见化合物,它们的焰色反应均为黄色。
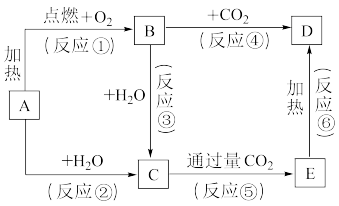
请填写下列空白:
(1)写出B的化学式:___________ 。
(2)以上反应中,属于氧化还原反应的有___________ (填写编号)
(3)写出A→C反应的离子方程式:___________ ,写出E→D的化学方程式:___________ 。

请填写下列空白:
(1)写出B的化学式:
(2)以上反应中,属于氧化还原反应的有
(3)写出A→C反应的离子方程式:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】I.现代工业常以氯化钠为原料制备纯碱,部分工艺流程如图:

已知NaHCO3在低温下溶解度较小。
反应:NaCl+CO2+NH3+H2O NaHCO3↓+NH4Cl,处理母液的两种方法:
NaHCO3↓+NH4Cl,处理母液的两种方法:
(1)向母液中加入石灰乳,可将其中_______ 循环利用。
(2)向母液中通入NH3,加入细小的食盐颗粒并降温,可得到NH4Cl晶体。试写出通入NH3后,溶解度较小的酸式碳酸盐转变为溶解度较大的碳酸盐的离子方程式:_______ 。
II.某化学小组模拟“侯氏制碱法”,以NaCl、NH3、CO2和水等为原料以及如图所示装置制取NaHCO3,然后再将NaHCO3制成Na2CO3。

(3)装置丙中冷水的作用是_______ 。
(4)由装置丙中产生的NaHCO3制取Na2CO3时,需要进行的实验操作有_______ 、洗涤、灼烧。NaHCO3转化为Na2CO3的化学方程式为_______ 。
(5)若取21.0gNaHCO3固体,加热了tmin后,剩余固体的质量为14.8g。如果把此剩余固体全部加入到200mL2mol•L-1的盐酸中,则充分反应后溶液中H+的物质的量浓度为_______ (设溶液体积变化忽略不计)。

已知NaHCO3在低温下溶解度较小。
反应:NaCl+CO2+NH3+H2O
 NaHCO3↓+NH4Cl,处理母液的两种方法:
NaHCO3↓+NH4Cl,处理母液的两种方法:(1)向母液中加入石灰乳,可将其中
(2)向母液中通入NH3,加入细小的食盐颗粒并降温,可得到NH4Cl晶体。试写出通入NH3后,溶解度较小的酸式碳酸盐转变为溶解度较大的碳酸盐的离子方程式:
II.某化学小组模拟“侯氏制碱法”,以NaCl、NH3、CO2和水等为原料以及如图所示装置制取NaHCO3,然后再将NaHCO3制成Na2CO3。

(3)装置丙中冷水的作用是
(4)由装置丙中产生的NaHCO3制取Na2CO3时,需要进行的实验操作有
(5)若取21.0gNaHCO3固体,加热了tmin后,剩余固体的质量为14.8g。如果把此剩余固体全部加入到200mL2mol•L-1的盐酸中,则充分反应后溶液中H+的物质的量浓度为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】按要求完成下列填空
I.某无色透明溶液中可能大量存在 中的几种。填写下列空白:
中的几种。填写下列空白:
(1)不做任何实验就可以肯定原溶液中不存在的离子是___________ 。
(2)取少量原溶液,加入过量稀盐酸,有白色沉淀生成;再加入过量的稀硝酸,沉淀不消失。说明原溶液中肯定存在的离子是___________ 。
(3)取(2)中的滤液,加入过量的氢氧化钠溶液,出现白色沉淀,说明原溶液中肯定有___________ ,有关的离子方程式为___________ 。
(4)原溶液可能大量共存的阴离子是___________ (填序号)。
① ②
② ③
③
Ⅱ.以不同类别物质间的转化为线索,认识钠及其化合物的性质。

(5)以上五种物质属于盐的是___________ (填化学式)。
(6)写出由 转化为
转化为 的化学方程式
的化学方程式___________ 。若反应中产生 氧气,则转移电子的数目为
氧气,则转移电子的数目为___________ 。
(7)写出由 转化为
转化为 的离子方程式
的离子方程式___________ 。
(8)除去 固体中的
固体中的 杂质的方法是
杂质的方法是___________ 。
I.某无色透明溶液中可能大量存在
 中的几种。填写下列空白:
中的几种。填写下列空白:(1)不做任何实验就可以肯定原溶液中不存在的离子是
(2)取少量原溶液,加入过量稀盐酸,有白色沉淀生成;再加入过量的稀硝酸,沉淀不消失。说明原溶液中肯定存在的离子是
(3)取(2)中的滤液,加入过量的氢氧化钠溶液,出现白色沉淀,说明原溶液中肯定有
(4)原溶液可能大量共存的阴离子是
①
 ②
② ③
③
Ⅱ.以不同类别物质间的转化为线索,认识钠及其化合物的性质。

(5)以上五种物质属于盐的是
(6)写出由
 转化为
转化为 的化学方程式
的化学方程式 氧气,则转移电子的数目为
氧气,则转移电子的数目为(7)写出由
 转化为
转化为 的离子方程式
的离子方程式(8)除去
 固体中的
固体中的 杂质的方法是
杂质的方法是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】某化学兴趣小组在实验室中利用侯氏制碱法制备 ,进一步处理得到产品
,进一步处理得到产品 和
和 ,制备流程如图:
,制备流程如图:

回答下列问题:
(1)上述流程中涉及到的下列物质①浓氨水② ③
③ ④
④ 溶液⑤
溶液⑤ ⑥
⑥ ,其中属于强电解质是的是
,其中属于强电解质是的是___________ (填标号)。
(2)写出饱和氨盐水和 反应的化学方程式
反应的化学方程式___________ 。
(3)“操作Ⅰ”的名称为___________ 。
(4)向母液中加入 粉末,存在
粉末,存在 (固体)
(固体) (溶液)
(溶液) (溶液)
(溶液) (固体)过程。为使
(固体)过程。为使 充分析出并分离,根据下图
充分析出并分离,根据下图 和
和 的溶解度曲线,需采用的操作为
的溶解度曲线,需采用的操作为___________ 、___________ 、过滤、洗涤、干燥。

(5)该工艺流程得到产品 ,请写出
,请写出 在生活生产中的一个用途
在生活生产中的一个用途___________ 。
(6)所得纯碱中可能含有少量 杂质,可以通过如下方法测定纯碱中
杂质,可以通过如下方法测定纯碱中 的质量分数:
的质量分数:
ⅰ.称取ag样品,溶于水中;
ⅱ.加入足量 溶液;
溶液;
ⅲ.过滤、洗涤、干燥、称量,所得沉淀质量为bg。
①证明所加 溶液已经足量的方法是
溶液已经足量的方法是___________ 。
②该纯碱中 的质量分数为
的质量分数为___________ (用含a、b的代数式表示)。
 ,进一步处理得到产品
,进一步处理得到产品 和
和 ,制备流程如图:
,制备流程如图:
回答下列问题:
(1)上述流程中涉及到的下列物质①浓氨水②
 ③
③ ④
④ 溶液⑤
溶液⑤ ⑥
⑥ ,其中属于强电解质是的是
,其中属于强电解质是的是(2)写出饱和氨盐水和
 反应的化学方程式
反应的化学方程式(3)“操作Ⅰ”的名称为
(4)向母液中加入
 粉末,存在
粉末,存在 (固体)
(固体) (溶液)
(溶液) (溶液)
(溶液) (固体)过程。为使
(固体)过程。为使 充分析出并分离,根据下图
充分析出并分离,根据下图 和
和 的溶解度曲线,需采用的操作为
的溶解度曲线,需采用的操作为
(5)该工艺流程得到产品
 ,请写出
,请写出 在生活生产中的一个用途
在生活生产中的一个用途(6)所得纯碱中可能含有少量
 杂质,可以通过如下方法测定纯碱中
杂质,可以通过如下方法测定纯碱中 的质量分数:
的质量分数:ⅰ.称取ag样品,溶于水中;
ⅱ.加入足量
 溶液;
溶液;ⅲ.过滤、洗涤、干燥、称量,所得沉淀质量为bg。
①证明所加
 溶液已经足量的方法是
溶液已经足量的方法是②该纯碱中
 的质量分数为
的质量分数为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】钠元素在自然界中以多种化合物的形式存在。
(1)Na2O2、Na2CO3、NaHCO3是重要的化工原料,具有多种用途。
①Na2O2可在呼吸面具和潜水艇中作为氧气的来源,请写出Na2O2与CO2反应的化学方程式_______ 。
②将一定量的Na2O2固体投入到含有下列离子的溶液中:Cl-、HCO 、CO
、CO 、Na+,反应完毕后,溶液中上述离子数目几乎不变的有
、Na+,反应完毕后,溶液中上述离子数目几乎不变的有_______ (填离子符号),上述离子中有一种离子数目明显减少,减少的原因是_______ (用离子方程式表示)。
③查阅资料知:Na2O2在一定条件下可以转化为NaNO2,亚硝酸钠外观酷似食盐且有咸味,是一种常用的发色剂和防腐剂。误食NaNO2会导致血红蛋白中的Fe2+转化为Fe3+而中毒,误食NaNO2后可服用维生素C解毒。下列分析错误的是_______ (填序号)。
A.NaNO2被还原 B.维生素C具有还原性
C.还原性:维生素C>Fe2+ D.NaNO2是还原剂
(2)我国化学家侯德榜发明了联合制碱法,对世界制碱工业做出了巨大贡献。联合制碱法的主要工艺流程如下图所示(部分物质已略去)。
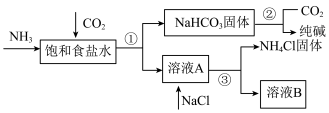
①实验室模拟“侯氏制碱法”,下列操作未涉及的是_______ (填字母)。
A.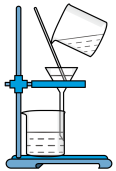 B.
B. C.
C. D.
D.
②下列联合制碱法流程说法正确的是_______ (填字母)。
a.CO2可以循环使用
b.副产物NH4Cl可用作肥料
c.溶液B中一定含有Na+、NH 、Cl-
、Cl-
③该工艺制得的纯碱中往往会含有杂质NaCl,为检验杂质的存在,简单的检验方案是:取少量试样溶于水后,_______ 。
④为了检验某含有NaHCO3杂质的Na2CO3样品的纯度,取5.00gNa2CO3样品充分加热,当固体质量不再变化时,再次称量固体质量为4.69g,写出加热时发生反应的化学方程式_______ ,该样品中Na2CO3的纯度是_______ 。
(1)Na2O2、Na2CO3、NaHCO3是重要的化工原料,具有多种用途。
①Na2O2可在呼吸面具和潜水艇中作为氧气的来源,请写出Na2O2与CO2反应的化学方程式
②将一定量的Na2O2固体投入到含有下列离子的溶液中:Cl-、HCO
 、CO
、CO 、Na+,反应完毕后,溶液中上述离子数目几乎不变的有
、Na+,反应完毕后,溶液中上述离子数目几乎不变的有③查阅资料知:Na2O2在一定条件下可以转化为NaNO2,亚硝酸钠外观酷似食盐且有咸味,是一种常用的发色剂和防腐剂。误食NaNO2会导致血红蛋白中的Fe2+转化为Fe3+而中毒,误食NaNO2后可服用维生素C解毒。下列分析错误的是
A.NaNO2被还原 B.维生素C具有还原性
C.还原性:维生素C>Fe2+ D.NaNO2是还原剂
(2)我国化学家侯德榜发明了联合制碱法,对世界制碱工业做出了巨大贡献。联合制碱法的主要工艺流程如下图所示(部分物质已略去)。

①实验室模拟“侯氏制碱法”,下列操作未涉及的是
A.
 B.
B. C.
C. D.
D.
②下列联合制碱法流程说法正确的是
a.CO2可以循环使用
b.副产物NH4Cl可用作肥料
c.溶液B中一定含有Na+、NH
 、Cl-
、Cl-③该工艺制得的纯碱中往往会含有杂质NaCl,为检验杂质的存在,简单的检验方案是:取少量试样溶于水后,
④为了检验某含有NaHCO3杂质的Na2CO3样品的纯度,取5.00gNa2CO3样品充分加热,当固体质量不再变化时,再次称量固体质量为4.69g,写出加热时发生反应的化学方程式
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】纯碱是重要的化工原料,在医药、冶金、化工、食品等领域被广泛使用。某实验小组的同学模拟侯德榜制碱法制取纯碱,流程如下:
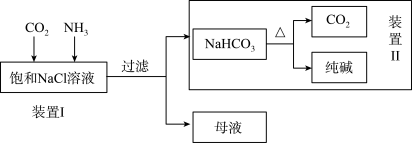
(1)工业生产纯碱的第一步是除去饱和食盐水的中SO42-、Ca2+离子,依次加入的试剂及其用量是______________ 、_______________ 、过滤、_______________ 。
(2)已知:几种盐的溶解度
①写出装置I中反应的化学方程式_____________________________________ 。
②写出装置Ⅱ中发生反应的化学方程式________________________________ 。
(3)该流程中可循环利用的物质是__________________ 。
(4)若制出的纯碱中只含有杂质NaCl。
①检验用该纯碱配制的溶液中含有Cl―的方法是_________________________ 。
②向m克纯碱样品中加入足量CaCl2溶液,沉淀经过滤、洗涤、干燥,称其质量为b g,则该纯碱的纯度(质量分数)为__________ (用m、b来表示)。

(1)工业生产纯碱的第一步是除去饱和食盐水的中SO42-、Ca2+离子,依次加入的试剂及其用量是
(2)已知:几种盐的溶解度
| NaCl | NH4HCO3 | NaHCO3 | NH4Cl | |
| 溶解度(20°C,100gH2O时) | 36.0 | 21.7 | 9.6 | 37.2 |
②写出装置Ⅱ中发生反应的化学方程式
(3)该流程中可循环利用的物质是
(4)若制出的纯碱中只含有杂质NaCl。
①检验用该纯碱配制的溶液中含有Cl―的方法是
②向m克纯碱样品中加入足量CaCl2溶液,沉淀经过滤、洗涤、干燥,称其质量为b g,则该纯碱的纯度(质量分数)为
您最近一年使用:0次





