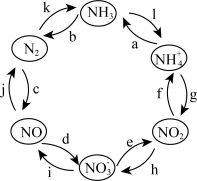
Ⅰ.氧化还原反应与离子反应在生产生活与科学实验中有重要作用,回答问题。过氧化氢俗名双氧水,医疗上利用它有杀菌消毒作用来清洗伤口。根据下列反应回答问题:
A. B.
B.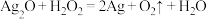
C. D.
D.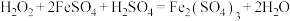
(1)上述反应中, 仅体现氧化性的反应是
仅体现氧化性的反应是___________ (填字母序号,下同), 既体现氧化性又体现还原性的反应是
既体现氧化性又体现还原性的反应是___________ , 、
、 、
、 的氧化性由强到弱的顺序是
的氧化性由强到弱的顺序是___________ 。
(2)某酸性溶液中发生的离子反应,反应物和生成物共六种微粒: 、
、 、
、 、
、 、
、 、
、 ,已知:氧化性
,已知:氧化性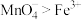 ,则反应的离子方程式为
,则反应的离子方程式为___________ 。
Ⅱ. 和浓盐酸在一定温度下反应会生成绿黄色的易爆物二氧化氯,其变化可表述为
和浓盐酸在一定温度下反应会生成绿黄色的易爆物二氧化氯,其变化可表述为 (浓)
(浓)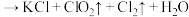 (未配平)
(未配平)
(3)氧化剂是___________ 氧化产物是___________
(4)产生1个 ,转移的电子的个数为
,转移的电子的个数为___________ 个
(5)某反应体系有反应物和生成物共五种物质: 、
、 、
、 (不溶于水)、
(不溶于水)、 、
、 ,已知该反应中
,已知该反应中 只发生如下过程
只发生如下过程 ,写出该反应的化学方程式:
,写出该反应的化学方程式:___________ 。
A.
 B.
B.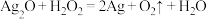
C.
 D.
D.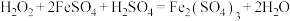
(1)上述反应中,
 仅体现氧化性的反应是
仅体现氧化性的反应是 既体现氧化性又体现还原性的反应是
既体现氧化性又体现还原性的反应是 、
、 、
、 的氧化性由强到弱的顺序是
的氧化性由强到弱的顺序是(2)某酸性溶液中发生的离子反应,反应物和生成物共六种微粒:
 、
、 、
、 、
、 、
、 、
、 ,已知:氧化性
,已知:氧化性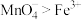 ,则反应的离子方程式为
,则反应的离子方程式为Ⅱ.
 和浓盐酸在一定温度下反应会生成绿黄色的易爆物二氧化氯,其变化可表述为
和浓盐酸在一定温度下反应会生成绿黄色的易爆物二氧化氯,其变化可表述为 (浓)
(浓)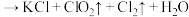 (未配平)
(未配平)(3)氧化剂是
(4)产生1个
 ,转移的电子的个数为
,转移的电子的个数为(5)某反应体系有反应物和生成物共五种物质:
 、
、 、
、 (不溶于水)、
(不溶于水)、 、
、 ,已知该反应中
,已知该反应中 只发生如下过程
只发生如下过程 ,写出该反应的化学方程式:
,写出该反应的化学方程式:
更新时间:2023-10-09 07:34:53
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】氧化还原反应在人类的生产、生活中有着重要的应用:
(1)我国古代四大发明之一的黑火药是由硫磺粉、硝酸钾和木炭按一定比例混合而成的,爆炸时发生的反应为: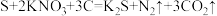 。该反应中,被还原的元素是
。该反应中,被还原的元素是___________ (元素符号),消耗的还原剂和氧化剂质量比为___________ 。
(2)在明代宋应星所著的《天工开物》中,有关火法炼锌的工艺记载:“每炉甘石十斤,装载入一泥罐内,……然后逐层用煤炭饼垫盛,其底铺薪,发火煅红,罐中炉甘石熔化成球。冷定毁罐取出。……即倭铅也。……以其似铅而性猛,故名之曰‘倭’云。”(注:炉甘石的主要成分是碳酸锌。)请完成上述火法炼锌反应的化学方程式:ZnCO3+___________ ___________
___________ ___________CO↑,
___________CO↑,___________ ,在该反应中,氧化剂是___________ ,CO是___________ (填“氧化产物”或“还原产物”)。
(3)维生素C又称“抗坏血酸”,在人体内有重要的功能,能帮助人体将食物中摄取的、不易吸收的Fe3+转变为易吸收的Fe2+,这说明维生素C具有___________ (填“氧化性”或“还原性”)。
(4)氮氧化物是造成酸雨的成分之一,治理汽车尾气的一种方法是在汽车的排气管上装一个催化转换装置,使NO和CO反应,生成无毒气体,写出该反应的化学方程式并用单线桥标出电子转移的方向和数目___________ 。
(1)我国古代四大发明之一的黑火药是由硫磺粉、硝酸钾和木炭按一定比例混合而成的,爆炸时发生的反应为:
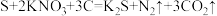 。该反应中,被还原的元素是
。该反应中,被还原的元素是(2)在明代宋应星所著的《天工开物》中,有关火法炼锌的工艺记载:“每炉甘石十斤,装载入一泥罐内,……然后逐层用煤炭饼垫盛,其底铺薪,发火煅红,罐中炉甘石熔化成球。冷定毁罐取出。……即倭铅也。……以其似铅而性猛,故名之曰‘倭’云。”(注:炉甘石的主要成分是碳酸锌。)请完成上述火法炼锌反应的化学方程式:ZnCO3+___________
 ___________
___________ ___________CO↑,
___________CO↑,(3)维生素C又称“抗坏血酸”,在人体内有重要的功能,能帮助人体将食物中摄取的、不易吸收的Fe3+转变为易吸收的Fe2+,这说明维生素C具有
(4)氮氧化物是造成酸雨的成分之一,治理汽车尾气的一种方法是在汽车的排气管上装一个催化转换装置,使NO和CO反应,生成无毒气体,写出该反应的化学方程式并用单线桥标出电子转移的方向和数目
您最近一年使用:0次
【推荐2】高铁酸盐是一种新型、高效、多功能绿色水处理剂,工业上可用湿法制备高铁酸钾: 。
。
(1) 中铁元素的化合价为
中铁元素的化合价为___________ ,在该反应中氧化剂与还原剂的物质的量之比为___________ ,氧化产物是___________ 。
(2)请用双线桥表示反应中电子转移情况:___________ 。
(3)根据化合价,推测 能和下列___________反应(填序号)。
能和下列___________反应(填序号)。
(4)在下列中,水既不作氧化剂又不作还原剂是___________(填序号)。
 。
。(1)
 中铁元素的化合价为
中铁元素的化合价为(2)请用双线桥表示反应中电子转移情况:
(3)根据化合价,推测
 能和下列___________反应(填序号)。
能和下列___________反应(填序号)。| A.KMnO4 | B.SO2 | C.H2S | D.O2 |
A.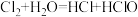 | B. |
C. | D. |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】Ⅰ.CO2、碳酸盐、有机物等均是自然界碳循环中的重要物质。回答下列问题:
(1)下列物质属于化合物但不属于电解质的是____ (填标号)。
(2)工业上制取金刚砂的反应为SiO2+3C SiC+2CO↑,则氧化剂与还原剂的物质的量之比为
SiC+2CO↑,则氧化剂与还原剂的物质的量之比为____ 。
(3)含KCN的废水可用氯氧化法处理,反应原理为KCN+2KOH+Cl2=KOCN+2KCl+H2O。该反应中被氧化的元素是____ (填元素符号)。
Ⅱ.N2O、NO和NO2等氮氧化物是空气污染物,含有氮氧化物的尾气需处理后才能排放。
(4)N2O是氨催化氧化的副产物,写出NH3与O2在加热和催化剂作用下生成N2O的化学方程式____ 。
(5)N2O的处理:用特殊催化剂使其分解为对大气友好的气体,则N2O分解的化学方程式为_____ 。
(6)NO和NO2的处理:已除去N2O的氮氧化物可用NaOH溶液吸收,主要反应为:NO+NO2+2NaOH=2NaNO2+H2O;2NO2+2NaOH=NaNO2+NaNO3+H2O。若V(NO)∶V(NO2)=5∶2的混合气体,通过足量NaOH溶液后,溶液中含有N元素的溶质为____ 。
(7)NO的处理:NO能将酸性的NaClO溶液的还原为Cl-,实验测得100mL1.2mol·L-1的NaClO溶液可以吸收标准状况下1.792LNO气体,则反应的离子方程式为____ 。
(1)下列物质属于化合物但不属于电解质的是
| A.石墨 | B.CO2 | C.NH3·H2O | D.CaCO3 |
 SiC+2CO↑,则氧化剂与还原剂的物质的量之比为
SiC+2CO↑,则氧化剂与还原剂的物质的量之比为(3)含KCN的废水可用氯氧化法处理,反应原理为KCN+2KOH+Cl2=KOCN+2KCl+H2O。该反应中被氧化的元素是
Ⅱ.N2O、NO和NO2等氮氧化物是空气污染物,含有氮氧化物的尾气需处理后才能排放。
(4)N2O是氨催化氧化的副产物,写出NH3与O2在加热和催化剂作用下生成N2O的化学方程式
(5)N2O的处理:用特殊催化剂使其分解为对大气友好的气体,则N2O分解的化学方程式为
(6)NO和NO2的处理:已除去N2O的氮氧化物可用NaOH溶液吸收,主要反应为:NO+NO2+2NaOH=2NaNO2+H2O;2NO2+2NaOH=NaNO2+NaNO3+H2O。若V(NO)∶V(NO2)=5∶2的混合气体,通过足量NaOH溶液后,溶液中含有N元素的溶质为
(7)NO的处理:NO能将酸性的NaClO溶液的还原为Cl-,实验测得100mL1.2mol·L-1的NaClO溶液可以吸收标准状况下1.792LNO气体,则反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】阅读下面科普信息,回答问题:
一个体重50 kg的健康人含铁2 g,这2 g铁在人体中以Fe2+和Fe3+的形式存在。亚铁离子易被吸收,给贫血者补充铁时,应给予含亚铁离子的亚铁盐,如硫酸亚铁。服用维生素C,可使食物中的铁离子还原成亚铁离子,有利于铁的吸收。
(1)以下为常见的铁元素的几种微粒,其中既有氧化性又有还原性的是____
A.Fe
B.Fe2+
C.Fe3+
(2)工业盐中毒后,可服用维生素C来缓解中毒状况,这说明维生素C具有________ 性。
(3)在Fe+4HNO3(稀)=Fe(NO3)3+NO↑+2H2O的反应中,HNO3表现了______ 性。
(4)钒性能优良,用途广泛,有金属“维生素”之称。将废钒催化剂(主要成分V2O5)与稀硫酸、亚硫酸钾溶液混合,充分反应后生成VO2+等离子,该反应的化学方程式是________ 。
(5)V2O5能与盐酸反应产生VO2+和一种黄绿色气体,该气体能与Na2SO3溶液反应被吸收,则 、Cl-、VO2+还原性由大到小的顺序是
、Cl-、VO2+还原性由大到小的顺序是________ 。
(6)在20.00 mL 0.1 mol.L-1 溶液中,加入0.195g锌粉,恰好完全反应,则还原产物可能是
溶液中,加入0.195g锌粉,恰好完全反应,则还原产物可能是 ________ 。
a.VO2+ b. c. V2+ d.V
c. V2+ d.V
一个体重50 kg的健康人含铁2 g,这2 g铁在人体中以Fe2+和Fe3+的形式存在。亚铁离子易被吸收,给贫血者补充铁时,应给予含亚铁离子的亚铁盐,如硫酸亚铁。服用维生素C,可使食物中的铁离子还原成亚铁离子,有利于铁的吸收。
(1)以下为常见的铁元素的几种微粒,其中既有氧化性又有还原性的是
A.Fe
B.Fe2+
C.Fe3+
(2)工业盐中毒后,可服用维生素C来缓解中毒状况,这说明维生素C具有
(3)在Fe+4HNO3(稀)=Fe(NO3)3+NO↑+2H2O的反应中,HNO3表现了
(4)钒性能优良,用途广泛,有金属“维生素”之称。将废钒催化剂(主要成分V2O5)与稀硫酸、亚硫酸钾溶液混合,充分反应后生成VO2+等离子,该反应的化学方程式是
(5)V2O5能与盐酸反应产生VO2+和一种黄绿色气体,该气体能与Na2SO3溶液反应被吸收,则
 、Cl-、VO2+还原性由大到小的顺序是
、Cl-、VO2+还原性由大到小的顺序是(6)在20.00 mL 0.1 mol.L-1
 溶液中,加入0.195g锌粉,恰好完全反应,则还原产物可能是
溶液中,加入0.195g锌粉,恰好完全反应,则还原产物可能是 a.VO2+ b.
 c. V2+ d.V
c. V2+ d.V
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】“溶解”后得到的酸性溶液中含有Zn2+、 ,另含有Fe2+、Cu2+等杂质。先加入
,另含有Fe2+、Cu2+等杂质。先加入_______ (填“Na2CO3”或“H2SO4”)调节溶液的pH至5.4,然后加入适量KMnO4,Fe2+转化为Fe(OH)3,同时KMnO4转化为MnO2,经检测溶液中Fe2+的浓度为0.009mol·L-1,则每升溶液中至少应加入_______ molKMnO4。
 ,另含有Fe2+、Cu2+等杂质。先加入
,另含有Fe2+、Cu2+等杂质。先加入
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】有以下反应方程式:
A.CuO+H2 Cu+H2O B.2KClO3
Cu+H2O B.2KClO3 2KCl + 3O2↑
2KCl + 3O2↑
C.Cl2+2NaOH==NaCl + NaClO+ H2O D.2FeBr2 + 3Cl2=2FeCl3+ 2Br2
E.MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O G.KClO3 +6HCl(浓)==KC1+ 3H2O + 3Cl2↑
MnCl2+Cl2↑+2H2O G.KClO3 +6HCl(浓)==KC1+ 3H2O + 3Cl2↑
H.HgS +O2=Hg + SO2
I.按要求将上述化学方程式序号填入相应空格内:
(1)一种单质使一种化合物中的一种元素被还原____________________
(2)同一种物质中,同种元素间发生氧化还原反应________________
(3)所有元素均参加氧化还原反应的是____________________________
(4)发生在不同物质间,只有部分元素被氧化或只有部分元素被还原的反应_______________
II.已知力程式G: KClO3+ 6HCI(浓)=KCl + 3H2O+ 3Cl2↑
(1)请用双线桥法标出电子转移的方向和数目_______________________
(2)标准状况下当有33.6L的氯气放出时,转移电子的数目是_________________________
(3)上述反应中氧化产物和还原产物的质量比为____________________________
A.CuO+H2
 Cu+H2O B.2KClO3
Cu+H2O B.2KClO3 2KCl + 3O2↑
2KCl + 3O2↑C.Cl2+2NaOH==NaCl + NaClO+ H2O D.2FeBr2 + 3Cl2=2FeCl3+ 2Br2
E.MnO2+4HCl(浓)
 MnCl2+Cl2↑+2H2O G.KClO3 +6HCl(浓)==KC1+ 3H2O + 3Cl2↑
MnCl2+Cl2↑+2H2O G.KClO3 +6HCl(浓)==KC1+ 3H2O + 3Cl2↑H.HgS +O2=Hg + SO2
I.按要求将上述化学方程式序号填入相应空格内:
(1)一种单质使一种化合物中的一种元素被还原
(2)同一种物质中,同种元素间发生氧化还原反应
(3)所有元素均参加氧化还原反应的是
(4)发生在不同物质间,只有部分元素被氧化或只有部分元素被还原的反应
II.已知力程式G: KClO3+ 6HCI(浓)=KCl + 3H2O+ 3Cl2↑
(1)请用双线桥法标出电子转移的方向和数目
(2)标准状况下当有33.6L的氯气放出时,转移电子的数目是
(3)上述反应中氧化产物和还原产物的质量比为
您最近一年使用:0次
【推荐1】完成下列反应的离子方程式
(1)酸性条件下KIO3溶液与KI溶液发生反应生成I2:_____________________________ ;
(2)钠与CuSO4溶液反应:_______________________________________________ ;
(3)磁性氧化铁溶于稀硝酸:_____________________________________________ ;
(4)向盛有H2O2溶液的试管中加入几滴酸化的FeCl2溶液,溶液变成棕黄色,发生反应的离子方程式为:_____________________________________ ;
(5)已知在酸性条件下NaClO2可发生反应生成NaCl并释放出ClO2,该反应的离子方程式为:_______________________________ 。
(1)酸性条件下KIO3溶液与KI溶液发生反应生成I2:
(2)钠与CuSO4溶液反应:
(3)磁性氧化铁溶于稀硝酸:
(4)向盛有H2O2溶液的试管中加入几滴酸化的FeCl2溶液,溶液变成棕黄色,发生反应的离子方程式为:
(5)已知在酸性条件下NaClO2可发生反应生成NaCl并释放出ClO2,该反应的离子方程式为:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】Ⅰ.已知制备Cl2的方法可以为:2KMnO4+16HCl(浓)═2MnCl2+2KCl+5Cl2↑+8H2O。
(1)用双线桥法表示该反应电子转移的方向和数目___________ 。
(2)反应中氧化剂是___________ ,氧化产物是___________ ,被氧化与未被氧化的的HCl质量之比为___________ ;
(3)HCl在上述反应中显示出来的性质是___________;
(4)若有112L(标准状况)Cl2生成,反应中转移电子的数目为___________ 。
Ⅱ.制取新型净水剂高铁酸钠( )原理为:
)原理为:
___________ ___________
___________ ___________ —___________
___________ —___________ ___________
___________ ___________(缺项处填
___________(缺项处填 、
、 或
或 )
)
(5)请配平该化学方程式___________ 。
Ⅲ.NaHCO3是生活中常见的物质,请回答下列问题:
(6)写出NaHCO3在水溶液中的电离方程式:___________ 。
(7)NaHCO3属于“酸”、“碱”、“盐”中的___________ 。
(8)写出NaHCO3溶液与NaOH溶液反应的离子方程式___________ 。
(9)Na2CO3固体中含有少量的NaHCO3杂质,除去杂质发生反应的化学方程式为___________ 。
(1)用双线桥法表示该反应电子转移的方向和数目
(2)反应中氧化剂是
(3)HCl在上述反应中显示出来的性质是___________;
| A.氧化性 | B.还原性 | C.酸性 | D.挥发性 |
Ⅱ.制取新型净水剂高铁酸钠(
 )原理为:
)原理为:___________
 ___________
___________ ___________ —___________
___________ —___________ ___________
___________ ___________(缺项处填
___________(缺项处填 、
、 或
或 )
)(5)请配平该化学方程式
Ⅲ.NaHCO3是生活中常见的物质,请回答下列问题:
(6)写出NaHCO3在水溶液中的电离方程式:
(7)NaHCO3属于“酸”、“碱”、“盐”中的
(8)写出NaHCO3溶液与NaOH溶液反应的离子方程式
(9)Na2CO3固体中含有少量的NaHCO3杂质,除去杂质发生反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】二氧化硒(SeO2)是一种氧化剂,其被还原后的单质硒可能成为环境污染物,通过与浓HNO3或浓H2SO4反应生成SeO2以回收Se。
已知: ① Se+2H2SO4(浓)=2SO2↑+SeO2+2H2O ② SO2+SeO2+ H2O Se + SO42-+ H+
Se + SO42-+ H+
(1)依据Se与浓H2SO4的反应,写出Se和浓HNO3(还原产物为NO2)反应的化学方程式:__________________ 。
(2)Se与浓HNO3的反应中,氧化剂是_______ , 反应中被还原的元素是_______ 。当有标准状况下33.6LNO2气体生成时,转移电子的物质的量是________ mol。
(3)依据反应①②, 判断SeO2、浓H2SO4、SO2的氧化性由强到弱的顺序是__________ 。
(4) 配平反应②, 并用双线桥法标出电子转移的方向和数目:_____________________ 。
已知: ① Se+2H2SO4(浓)=2SO2↑+SeO2+2H2O ② SO2+SeO2+ H2O
 Se + SO42-+ H+
Se + SO42-+ H+(1)依据Se与浓H2SO4的反应,写出Se和浓HNO3(还原产物为NO2)反应的化学方程式:
(2)Se与浓HNO3的反应中,氧化剂是
(3)依据反应①②, 判断SeO2、浓H2SO4、SO2的氧化性由强到弱的顺序是
(4) 配平反应②, 并用双线桥法标出电子转移的方向和数目:
您最近一年使用:0次
填空题
|
适中
(0.64)
名校
【推荐2】硝酸是一种具有强氧化性、腐蚀性的强酸,其还原产物因硝酸浓度的不同而有变化,从总体上说,硝酸浓度越高,平均每分子硝酸得到的电子数越少,浓硝酸的还原产物主要为NO2、稀确酸的还原产物为NO。实验室中,常用Cu与浓HNO3反应制取NO2,用Cu与稀HNO3反应制取NO。
(1)请写出实验室中用Cu与浓HNO3反应制取NO2的化学方程式:__________________________________ 。
(2)上述(1)反应中发生氧化反应的物质是___________ ,1 mol 氧化剂________ (填“得到"或"失去“)______ mol电子。
(3)48.0g Cu与适量的浓HNO3反应,铜全部作用后,共收集到22.4L气体(标准状况下),反应中消耗HNO3的物质的量是__________ (填字母代号)。
A.1.5mol B.2.0mol C.2.5mol D.3.0mol
(4)实际上硝酸不仅可被还原为NO2或NO,浓度更稀时硝酸还可以被还原为N2O、N2、NH4NO3等,请将下列3种物质:FeSO4、Fe(NO3)3和Fe2(SO4)3分别填入下面对应的横线上,并配平该反应的化学方程式。 HNO3+ → + + N2O↑+ H2O_____________________
(5)硝酸的还原产物NO、NO2、N2O等对环境均有副作用,为了可持续发展,当今社会提出的一个新概念--“绿色化学”,它要求从经济、环保和技术上设计可行的化学反应,则下列由单质铜制取硝酸铜的方法可行且符合“绿色化学”的是__________ (填字母代号)。
A.Cu Cu(NO3)2
Cu(NO3)2
B.Cu CuO
CuO  Cu(NO3)2
Cu(NO3)2
C.Cu CuO
CuO Cu(OH)2
Cu(OH)2  Cu(NO3)2
Cu(NO3)2
D.Cu CuSO4
CuSO4 Cu(NO3)2
Cu(NO3)2
(1)请写出实验室中用Cu与浓HNO3反应制取NO2的化学方程式:
(2)上述(1)反应中发生氧化反应的物质是
(3)48.0g Cu与适量的浓HNO3反应,铜全部作用后,共收集到22.4L气体(标准状况下),反应中消耗HNO3的物质的量是
A.1.5mol B.2.0mol C.2.5mol D.3.0mol
(4)实际上硝酸不仅可被还原为NO2或NO,浓度更稀时硝酸还可以被还原为N2O、N2、NH4NO3等,请将下列3种物质:FeSO4、Fe(NO3)3和Fe2(SO4)3分别填入下面对应的横线上,并配平该反应的化学方程式。 HNO3+ → + + N2O↑+ H2O
(5)硝酸的还原产物NO、NO2、N2O等对环境均有副作用,为了可持续发展,当今社会提出的一个新概念--“绿色化学”,它要求从经济、环保和技术上设计可行的化学反应,则下列由单质铜制取硝酸铜的方法可行且符合“绿色化学”的是
A.Cu
 Cu(NO3)2
Cu(NO3)2B.Cu
 CuO
CuO  Cu(NO3)2
Cu(NO3)2C.Cu
 CuO
CuO Cu(OH)2
Cu(OH)2  Cu(NO3)2
Cu(NO3)2D.Cu
 CuSO4
CuSO4 Cu(NO3)2
Cu(NO3)2
您最近一年使用:0次