实验室用下图所示装置进行氯气性质的探究并制备无水 FeCl3。查阅相关资料可知:无水 FeCl3在空气中易潮解,加热易升华。
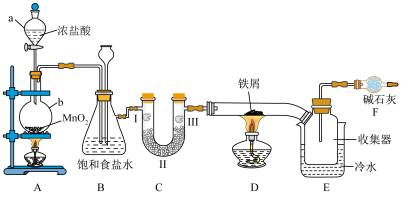
(1)仪器b的名称为___________ 。
(2)装置A中发生反应的化学方程式为___________ ;
若实验时使用的17.4gMnO2完全反应,产生的Cl2在标准状况下的体积为___________ 。
(3)装置B中饱和食盐水的作用是___________ ,装置B同时用作安全瓶(监测实验时装置C中是否发生堵塞);若装置C发生堵塞,则装置B中将观察到的现象是___________ 。
(4)装置C的作用是验证氯气是否具有漂白性,为此,实验时装置C 中 Ⅰ、 Ⅱ、Ⅲ处依次放入的物质是___________ (填"甲"、 "乙"、 "丙"、 "丁")。
(5)实验开始时,应先点燃___________ (填“A”或“D”)处酒精灯。
(6)装置F的作用___________ 。

(1)仪器b的名称为
(2)装置A中发生反应的化学方程式为
若实验时使用的17.4gMnO2完全反应,产生的Cl2在标准状况下的体积为
(3)装置B中饱和食盐水的作用是
(4)装置C的作用是验证氯气是否具有漂白性,为此,实验时装置C 中 Ⅰ、 Ⅱ、Ⅲ处依次放入的物质是
| I | II | III | |
| 甲 | 干燥的有色布条 | 碱石灰 | 湿润的有色布条 |
| 乙 | 湿润的有色布条 | 无水氯化钙 | 干燥的有色布条 |
| 丙 | 干燥的有色布条 | 无水氯化钙 | 湿润的有色布条 |
| 丁 | 湿润的有色布条 | 浓硫酸 | 干燥的有色布条 |
(5)实验开始时,应先点燃
(6)装置F的作用
更新时间:2023-11-27 15:52:58
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】次氯酸溶液是常用的消毒剂漂白剂。某学习小组根据需要欲制备浓度不小于0.8 mol·L-1的次氯酸溶液。
[查阅资料]
资料1:常温常压下,Cl2O为棕黄色气体,沸点为3.8℃,42℃以上会分解生成Cl2和O2,Cl2O易溶于水并与水立即发生化合反应生成HClO。
资料2:将氯气和空气(不参与反应)按体积比1∶3混合通入潮湿的碳酸钠中发生反应:2Cl2+2Na2CO3+H2O=Cl2O+2NaCl+2NaHCO3,用水吸收Cl2O(不含Cl2)制得次氯酸。
[装置及实验]用以下装置制备次氯酸溶液
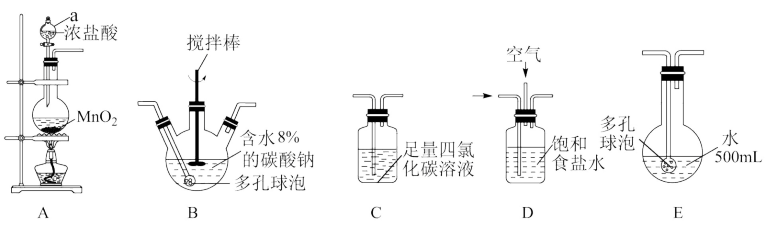
回答下列问题:
(1)仪器a名称___________ 。
(2)装置A中反应的化学方程式是___________ 。其中氧化剂与还原剂的物质的量之比为___________ 。
(3)各装置的连接顺序为A→___________→___________→___________→E。___________
(4)装置E中反应的化学方程式是___________ 。反应过程中,装置B需放在冷水中,其目的是___________ 。
(5)装置C的主要作用是___________ 。
(6)此方法相对于用氯气直接溶于水制备次氯酸溶液的优点是:___________ 。(答出一条即可)
[查阅资料]
资料1:常温常压下,Cl2O为棕黄色气体,沸点为3.8℃,42℃以上会分解生成Cl2和O2,Cl2O易溶于水并与水立即发生化合反应生成HClO。
资料2:将氯气和空气(不参与反应)按体积比1∶3混合通入潮湿的碳酸钠中发生反应:2Cl2+2Na2CO3+H2O=Cl2O+2NaCl+2NaHCO3,用水吸收Cl2O(不含Cl2)制得次氯酸。
[装置及实验]用以下装置制备次氯酸溶液

回答下列问题:
(1)仪器a名称
(2)装置A中反应的化学方程式是
(3)各装置的连接顺序为A→___________→___________→___________→E。
(4)装置E中反应的化学方程式是
(5)装置C的主要作用是
(6)此方法相对于用氯气直接溶于水制备次氯酸溶液的优点是:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】某小组利用高锰酸钾与8mol/L盐酸反应制氯气并进行氯气性质的探究,实验装置如图所示:
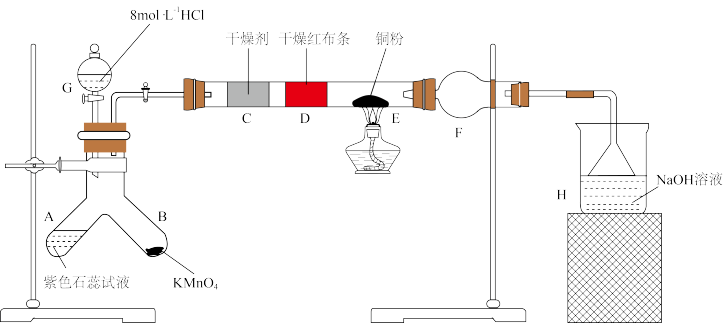
请回答下列问题:
(1)B中制取 的化学反应方程式为
的化学反应方程式为_______ 。
(2)根据相关实验现象就可以证明起漂白作用的不是氯气而是次氯酸,相关现象是_______ 。
(3)H处装置的作用是_______ 。
(4)实验室需要用12mol/L的浓盐酸来配制90mL6mol/L的盐酸,需该浓盐酸的体积为_______ mL。
为探究 对
对 溶解性的影响,进行如下实验。已知
溶解性的影响,进行如下实验。已知 在常温下溶解度为
在常温下溶解度为 。测定不同浓度
。测定不同浓度 溶液中的
溶液中的 溶解度,结果如下:
溶解度,结果如下:
(5)根据实验数据, 溶液浓度大于
溶液浓度大于_______  时,增加
时,增加 溶液浓度对
溶液浓度对 溶解度变化无明显影响。
溶解度变化无明显影响。
(6)为进一步探究食盐水中哪些微粒能降低 溶解度,取三支试管,分别加入一定浓度NaCl溶液、HCl溶液和
溶解度,取三支试管,分别加入一定浓度NaCl溶液、HCl溶液和 溶液,通入足量
溶液,通入足量 后,测定
后,测定 溶解度。
溶解度。
①a=_______ ,c=_______ 。
②对比实验1和实验2可以得到的结论是_______ 。
③设置实验3的目的是_______ 。
④实验结论:食盐水中能够降低 溶解度的微粒有
溶解度的微粒有_______ 。
(7)有同学认为H+会减弱 溶液降低
溶液降低 溶解度的效果。为验证该同学的猜想是否正确,可设计实验方案为
溶解度的效果。为验证该同学的猜想是否正确,可设计实验方案为_______ 。

请回答下列问题:
(1)B中制取
 的化学反应方程式为
的化学反应方程式为(2)根据相关实验现象就可以证明起漂白作用的不是氯气而是次氯酸,相关现象是
(3)H处装置的作用是
(4)实验室需要用12mol/L的浓盐酸来配制90mL6mol/L的盐酸,需该浓盐酸的体积为
为探究
 对
对 溶解性的影响,进行如下实验。已知
溶解性的影响,进行如下实验。已知 在常温下溶解度为
在常温下溶解度为 。测定不同浓度
。测定不同浓度 溶液中的
溶液中的 溶解度,结果如下:
溶解度,结果如下: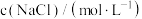 | 0.50 | 1.00 | 2.00 | 3.00 | 4.00 | 5.00 | 6.00 |
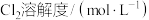 | 0.0658 | 0.0580 | 0.0490 | 0.0416 | 0.0385 | 0.0362 | 0.0362 |
 溶液浓度大于
溶液浓度大于 时,增加
时,增加 溶液浓度对
溶液浓度对 溶解度变化无明显影响。
溶解度变化无明显影响。(6)为进一步探究食盐水中哪些微粒能降低
 溶解度,取三支试管,分别加入一定浓度NaCl溶液、HCl溶液和
溶解度,取三支试管,分别加入一定浓度NaCl溶液、HCl溶液和 溶液,通入足量
溶液,通入足量 后,测定
后,测定 溶解度。
溶解度。| 实验编号 | 1 | 2 | 3 |
| 实验装置 | 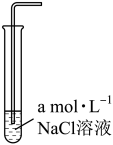 | 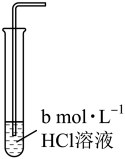 | 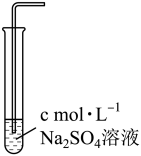 |
 溶解度/( 溶解度/( ) ) | 0.0490 | 0.0665 | 0.0800 |
②对比实验1和实验2可以得到的结论是
③设置实验3的目的是
④实验结论:食盐水中能够降低
 溶解度的微粒有
溶解度的微粒有(7)有同学认为H+会减弱
 溶液降低
溶液降低 溶解度的效果。为验证该同学的猜想是否正确,可设计实验方案为
溶解度的效果。为验证该同学的猜想是否正确,可设计实验方案为
您最近一年使用:0次
【推荐3】某校化学兴趣小组为验证 的性质,设计如图所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的红色纸条,b为湿润的红色纸条。
的性质,设计如图所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的红色纸条,b为湿润的红色纸条。
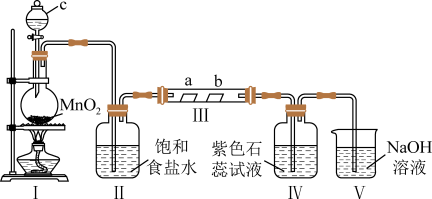
(1)装置Ⅰ中仪器c的名称是______ ,实验室用 和浓盐酸制备
和浓盐酸制备 的化学方程式为
的化学方程式为______ 。
(2)装置Ⅱ的作用是______ 。
(3)若实验中产生的 足量,装置Ⅳ中的实验现象
足量,装置Ⅳ中的实验现象______ 。
(4)写出装置Ⅴ中反应的离子方程式______ 。
(5)实验结束后,该组同学在装置Ⅲ中观察到b的红色褪去,但是并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为还需在图中装置Ⅱ与Ⅲ之间添加图中的______ 装置(填序号)。
①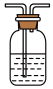
 溶液 ②
溶液 ②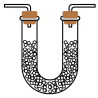 碱石灰
碱石灰
③
 溶液 ④
溶液 ④ 浓硫酸
浓硫酸
(6)可用 和
和 制备的漂粉精
制备的漂粉精
①漂粉精常用于游泳池的消毒,起消毒作用的是 。漂粉精在水中释放
。漂粉精在水中释放 的途径主要是:
的途径主要是:
______ (把反应补充完整)。
②池水的酸碱性对漂粉精的消毒效果影响明显。
a.若池水碱性过强,杀毒作用会______ (填“增强”或“减弱”)。
b.若池水酸性过强,会刺激眼睛和皮肤。有时加入 、
、 以降低酸性,起到降低酸性作用的离子分别是
以降低酸性,起到降低酸性作用的离子分别是______ (填离子符号)。
③漂白精中的 在碱性条件下能够制备新型净水剂——高铁酸钾
在碱性条件下能够制备新型净水剂——高铁酸钾 ,补全下面的离子方程式:
,补全下面的离子方程式:______ 。




 ______=
______=

 ______+
______+ ______
______
 的性质,设计如图所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的红色纸条,b为湿润的红色纸条。
的性质,设计如图所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的红色纸条,b为湿润的红色纸条。
(1)装置Ⅰ中仪器c的名称是
 和浓盐酸制备
和浓盐酸制备 的化学方程式为
的化学方程式为(2)装置Ⅱ的作用是
(3)若实验中产生的
 足量,装置Ⅳ中的实验现象
足量,装置Ⅳ中的实验现象(4)写出装置Ⅴ中反应的离子方程式
(5)实验结束后,该组同学在装置Ⅲ中观察到b的红色褪去,但是并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为还需在图中装置Ⅱ与Ⅲ之间添加图中的
①

 溶液 ②
溶液 ② 碱石灰
碱石灰③

 溶液 ④
溶液 ④ 浓硫酸
浓硫酸(6)可用
 和
和 制备的漂粉精
制备的漂粉精①漂粉精常用于游泳池的消毒,起消毒作用的是
 。漂粉精在水中释放
。漂粉精在水中释放 的途径主要是:
的途径主要是:
②池水的酸碱性对漂粉精的消毒效果影响明显。
a.若池水碱性过强,杀毒作用会
b.若池水酸性过强,会刺激眼睛和皮肤。有时加入
 、
、 以降低酸性,起到降低酸性作用的离子分别是
以降低酸性,起到降低酸性作用的离子分别是③漂白精中的
 在碱性条件下能够制备新型净水剂——高铁酸钾
在碱性条件下能够制备新型净水剂——高铁酸钾 ,补全下面的离子方程式:
,补全下面的离子方程式:



 ______=
______=

 ______+
______+ ______
______
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】为了探究Cl2、SO2同时通入H2O中发生的反应,某校化学兴趣小组同学设计了如图所示的实验装置。
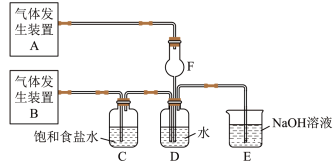
(1) SO2和Cl2通入H2O中发生反应的离子方程式是_______ 。装置E的作用:_______ 。
(2)为验证通入装置D中的气体是Cl2过量还是SO2过量,某小组同学准备了以下试剂:
①氯化铁溶液 ②氯化亚铁溶液 ③硫氰化钾溶液 ④苯酚溶液 ⑤品红溶液 ⑥酸性高锰酸钾溶液
a.若Cl2过量:取适量装置D中溶液滴入盛有___________ (选填一个序号,下同)的试管内,再加入___________ 试剂,实验现象是___________ 。
b.若SO2过量:取适量装置D中溶液滴入盛有___________ (选填一个序号)的试管内,实验现象是___________ ,再加热,实验现象是___________ 。
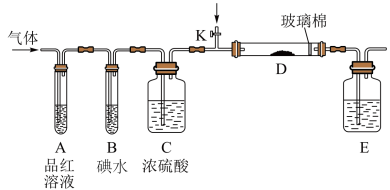
(3)另一小组设计如图所示的装置图(夹持和加热装置略去),分别探究SO2和Cl2的性质。若从左端分别通入SO2和Cl2,硬质玻璃管D中为湿润的pH试纸,观察到的现象是否相同?___________ (填“相同”或“不同”)。
(4)若由元素S和O组成-2价酸根离子X,X中S和O的质量比为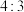 ;当Cl2与含X的溶液(1:1)完全反应后,有黄色沉淀产生,取上层清液加入氯化钡溶液,有白色沉淀产生。写出Cl2与含X的溶液反应的离子方程式:
;当Cl2与含X的溶液(1:1)完全反应后,有黄色沉淀产生,取上层清液加入氯化钡溶液,有白色沉淀产生。写出Cl2与含X的溶液反应的离子方程式:___________ 。

(1) SO2和Cl2通入H2O中发生反应的离子方程式是
(2)为验证通入装置D中的气体是Cl2过量还是SO2过量,某小组同学准备了以下试剂:
①氯化铁溶液 ②氯化亚铁溶液 ③硫氰化钾溶液 ④苯酚溶液 ⑤品红溶液 ⑥酸性高锰酸钾溶液
a.若Cl2过量:取适量装置D中溶液滴入盛有
b.若SO2过量:取适量装置D中溶液滴入盛有
(3)另一小组设计如图所示的装置图(夹持和加热装置略去),分别探究SO2和Cl2的性质。若从左端分别通入SO2和Cl2,硬质玻璃管D中为湿润的pH试纸,观察到的现象是否相同?

(4)若由元素S和O组成-2价酸根离子X,X中S和O的质量比为
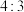 ;当Cl2与含X的溶液(1:1)完全反应后,有黄色沉淀产生,取上层清液加入氯化钡溶液,有白色沉淀产生。写出Cl2与含X的溶液反应的离子方程式:
;当Cl2与含X的溶液(1:1)完全反应后,有黄色沉淀产生,取上层清液加入氯化钡溶液,有白色沉淀产生。写出Cl2与含X的溶液反应的离子方程式:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】单晶硅是信息产业中重要的基础材料,通常用碳在高温还原二氧化硅制得粗硅(含铁、铝、硼、磷等杂质),粗硅与氯气反应生成四氯化硅(反应温度450~500℃),四氯化硅经提纯后用氢气还原可得高纯硅,以下是实验室制备四氯化硅的装置示意图。

相关信息如下:
a.四氯化硅遇水极易反应;
b.硼、铝、铁、磷在高温下均能与氯气直接反应生成相应的氯化物;
c.有关物质的物理常数见下表:
请回答下列问题:
(1)写出装置A中发生反应的离子方程式___________________________________ 。
(2)装置A上导管g的作用是______________________________ ;
(3)装置F中的试剂是___________ ,作用是_______________________________ 。
(4)装置E中的h瓶需要冷却的理由是_______________________________________ 。

相关信息如下:
a.四氯化硅遇水极易反应;
b.硼、铝、铁、磷在高温下均能与氯气直接反应生成相应的氯化物;
c.有关物质的物理常数见下表:
| 物质 | SiCl4 | BCl3 | AlCl3 | FeCl3 | PCl5 |
| 沸点/℃ | 57.7 | 12.8 | — | 315 | — |
| 熔点/℃ | −70.0 | −107.2 | — | — | — |
| 升华温度/℃ | — | — | 180 | 300 | 162 |
(1)写出装置A中发生反应的离子方程式
(2)装置A上导管g的作用是
(3)装置F中的试剂是
(4)装置E中的h瓶需要冷却的理由是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】锡箔纸常用于食品包装和食品加工。制作锡箔纸的主要金属元素锡( )位于周期表的第ⅣA族,它的常见价态有
)位于周期表的第ⅣA族,它的常见价态有 价,其单质沸点为
价,其单质沸点为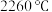 ,四氯化锡
,四氯化锡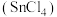 是无色液体,熔点
是无色液体,熔点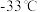 ,沸点
,沸点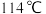 ,极易水解,在潮湿的空气中发烟。实验室中可用氯气与过量金属锡通过下图装置制备
,极易水解,在潮湿的空气中发烟。实验室中可用氯气与过量金属锡通过下图装置制备 (夹持装置已略去)。
(夹持装置已略去)。


(1)装置A中发生反应的化学方程式____________________ ;装置B的作用是__________ 。实验过程中应先点燃_______ 处酒精灯(填“甲”或“丁”)。
(2)装置甲中生成标况下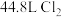 时,被氧化的
时,被氧化的 数目为
数目为_______ 。
(3)H中盛有氢氧化钠溶液,该实验装置的设计存在缺陷,你的改进措施的是:__________ 。
(4)用滴定法测定所用金属锡样品的纯度(杂质不参加反应)。
①将一定量锡粉完全溶于过量稀盐酸中,并用所得溶液去还原过量的 稀溶液。写出第二步反应的离子方程式:
稀溶液。写出第二步反应的离子方程式:____________________ 。
②取①所得溶液用 溶液滴定,发生反应的化学方程式为:
溶液滴定,发生反应的化学方程式为:____________________ 。
 )位于周期表的第ⅣA族,它的常见价态有
)位于周期表的第ⅣA族,它的常见价态有 价,其单质沸点为
价,其单质沸点为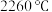 ,四氯化锡
,四氯化锡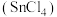 是无色液体,熔点
是无色液体,熔点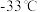 ,沸点
,沸点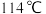 ,极易水解,在潮湿的空气中发烟。实验室中可用氯气与过量金属锡通过下图装置制备
,极易水解,在潮湿的空气中发烟。实验室中可用氯气与过量金属锡通过下图装置制备 (夹持装置已略去)。
(夹持装置已略去)。

(1)装置A中发生反应的化学方程式
(2)装置甲中生成标况下
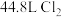 时,被氧化的
时,被氧化的 数目为
数目为(3)H中盛有氢氧化钠溶液,该实验装置的设计存在缺陷,你的改进措施的是:
(4)用滴定法测定所用金属锡样品的纯度(杂质不参加反应)。
①将一定量锡粉完全溶于过量稀盐酸中,并用所得溶液去还原过量的
 稀溶液。写出第二步反应的离子方程式:
稀溶液。写出第二步反应的离子方程式:②取①所得溶液用
 溶液滴定,发生反应的化学方程式为:
溶液滴定,发生反应的化学方程式为:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】某化学研究性学习小组拟用下列装置和药品制备无水氯化铁晶体,该物质极易水解,100℃左右时升华。请回答下列问题:
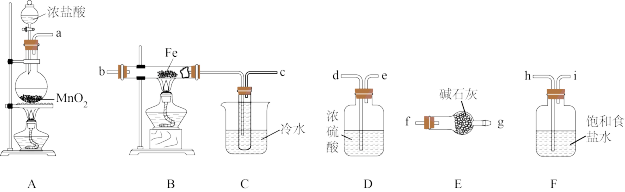
(1)不加热条件下检查A装置气密性的操作方法为_______ 。
(2)制备开始时A装置烧瓶中产生的现象为_______ 。发生反应的离子方程式为_______ 。
(3)按气流方向连接完整装置:a→_______ 。(填仪器接口字母编号)。
(4)装置F的作用是_______ 。B装置硬质玻璃管内导管口处棉花的作用是_______ 。若无E装置可能产生的后果是_______ 。
(5)本实验合理的操作步骤为_______ 。(按操作顺序选择序号)。
①添加药品
②连接仪器
③检查装置气密性
④点燃A处酒精灯
⑤点燃B处酒精灯
⑥使B中硬质玻璃管内充满黄绿色气体
(6)已知:亚铁离子与K3[Fe(SCN)6]溶液反应生成蓝色沉淀。设计实验证明装置 的硬质玻璃管中有少量的铁未能与Cl2发生反应。可选择的试剂有:KSCN溶液、酸性KMnO4溶液、K3[Fe(SCN)6]溶液、蒸馏水。其它仪器自选。
的硬质玻璃管中有少量的铁未能与Cl2发生反应。可选择的试剂有:KSCN溶液、酸性KMnO4溶液、K3[Fe(SCN)6]溶液、蒸馏水。其它仪器自选。_______ 。
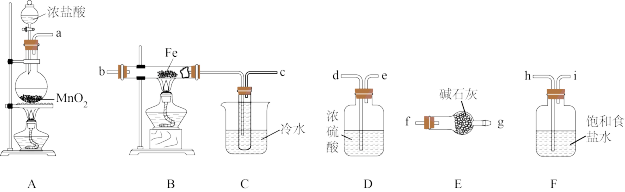
(1)不加热条件下检查A装置气密性的操作方法为
(2)制备开始时A装置烧瓶中产生的现象为
(3)按气流方向连接完整装置:a→
(4)装置F的作用是
(5)本实验合理的操作步骤为
①添加药品
②连接仪器
③检查装置气密性
④点燃A处酒精灯
⑤点燃B处酒精灯
⑥使B中硬质玻璃管内充满黄绿色气体
(6)已知:亚铁离子与K3[Fe(SCN)6]溶液反应生成蓝色沉淀。设计实验证明装置
 的硬质玻璃管中有少量的铁未能与Cl2发生反应。可选择的试剂有:KSCN溶液、酸性KMnO4溶液、K3[Fe(SCN)6]溶液、蒸馏水。其它仪器自选。
的硬质玻璃管中有少量的铁未能与Cl2发生反应。可选择的试剂有:KSCN溶液、酸性KMnO4溶液、K3[Fe(SCN)6]溶液、蒸馏水。其它仪器自选。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】氯气在生产生活中有较广泛应用。
(1)为了验证氯气的部分性质,某小组同学设计如图实验装置制取纯净、干燥的氯气后验证其性质,并进行尾气处理。
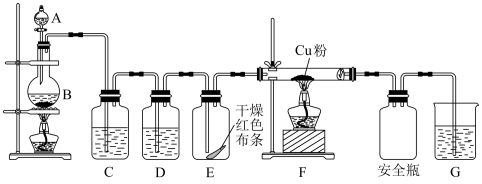
①装置C、G中盛装的试剂分别为___________ 、___________ 。
②实验中可以观察到装置E和装置F中的现象分别是___________ 、___________ 。
(2)1868年狄肯和洪特发明用地康法制氯气,反应原理图示如图(反应温度为450℃):

①反应II的化学方程式为___________ 。
②该方法制取氯气,主要消耗的原料是___________ ,每生成标准状况下33.6L氯气转移的电子数目是___________ 。
(3)家庭中常用消毒液(主要成分NaClO)与洁厕灵(主要成分盐酸)清洁卫生。两者同时使用容易产生氯气引起中毒,写出反应的离子方程式___________ 。
(1)为了验证氯气的部分性质,某小组同学设计如图实验装置制取纯净、干燥的氯气后验证其性质,并进行尾气处理。

①装置C、G中盛装的试剂分别为
②实验中可以观察到装置E和装置F中的现象分别是
(2)1868年狄肯和洪特发明用地康法制氯气,反应原理图示如图(反应温度为450℃):

①反应II的化学方程式为
②该方法制取氯气,主要消耗的原料是
(3)家庭中常用消毒液(主要成分NaClO)与洁厕灵(主要成分盐酸)清洁卫生。两者同时使用容易产生氯气引起中毒,写出反应的离子方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】高一3班某同学设计如图所示装置研究氯气能否与水发生反应。
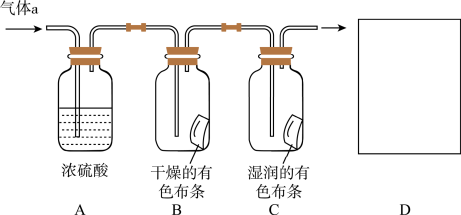
气体a的主要成分是含有少量空气和水蒸气的氯气。请回答下列问题:
(1)浓硫酸的作用是__________ 。
(2)与本实验研究结论相关的实验现象为________ 。
(3)从物质性质的方面来看,这样的实验设计存在缺陷。请用化学方程式表达图中D框克服事故隐患的措施:__________ 。

气体a的主要成分是含有少量空气和水蒸气的氯气。请回答下列问题:
(1)浓硫酸的作用是
(2)与本实验研究结论相关的实验现象为
(3)从物质性质的方面来看,这样的实验设计存在缺陷。请用化学方程式表达图中D框克服事故隐患的措施:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】实验室里除了用二氧化锰和浓盐酸加热制取氯气,也可以利用反应:2KMnO4+16HCl(浓)=2KCl+2MnC12+5Cl2↑+8H2O制取并收集纯净、干燥的氯气,部分装置如图所示:
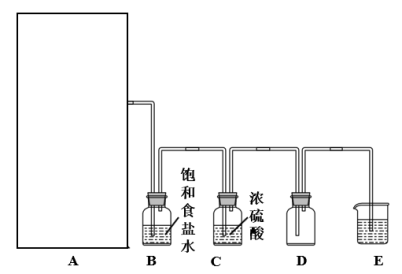
(1)若以KMnO4和浓盐酸为原料制取氯气,请根据反应原理从图中选择合适的制气装置___ (填代号)。
a.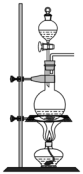 b.
b.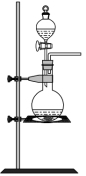 c.
c.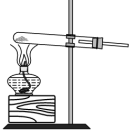
(2)装置B的作用___ 。
(3)E中的试剂选最好的是___ 。
A.NaOH溶液 B.NaCl溶液 C.Na2CO3溶液 D.水

(1)若以KMnO4和浓盐酸为原料制取氯气,请根据反应原理从图中选择合适的制气装置
a.
 b.
b. c.
c.
(2)装置B的作用
(3)E中的试剂选最好的是
A.NaOH溶液 B.NaCl溶液 C.Na2CO3溶液 D.水
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】2021 年10月16日神舟十三号载人飞船发射成功,肼是一种良好的火箭燃料,分子式N2H4,为无色油状液体,与水按任意比例互溶形成稳定的水合肼N2H4·H2O,沸点118°C,有强还原性。实验室先制备次氯酸钠,再与尿素[CO(NH2)2]反应制备水合肼,进一步脱水制得肼,实验装置如图所示(部分装置省略)。已知:CO(NH2)2+2NaOH+NaClO=Na2CO3+N2H4·H2O+NaCl

(1)装置C中制备NaClO的离子方程式为_______ 。反应过程中温度升高易产生副产物NaClO3,可采取的措施是_______ 。装置B中装有饱和食盐水,反应完后关闭K1,装置B的作用是_______ 。
(2)将装置C中制备的溶液转移到装置D的_______ 中,并缓缓滴入,原因是_______ 。
(3)装置D蒸馏获得水合肼粗品后,剩余溶液再进一步处理还可获得副产品NaCl和Na2CO3 ·10H2O,获得NaCl粗品的操作是_______ (NaCl和Na2CO3的溶解度曲线如图)。
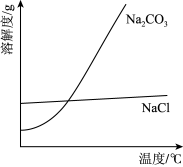
(4)称取5.0g水合肼样品,加水配成500mL溶液,从中取出10.00mL溶液于锥形瓶中,滴入几滴淀粉溶液,用0.20mol/L的I2溶液进行滴定,滴定终点的现象是_______ ,测得消耗I2溶液的体积为17.50mL,则样品中水合肼N2H4·H2O)的质量百分数为_______ (用百分数表示并保留3位有效数字)。(已知:N2H4·H2O +2I2=N2↑+4HI+H2O)
(5)脱水制得的液态肼,在加热条件下可与新制的Cu(OH)2制备纳米级Cu2O,并产生无污染气体,写出该反应的化学方程式:_______ 。

(1)装置C中制备NaClO的离子方程式为
(2)将装置C中制备的溶液转移到装置D的
(3)装置D蒸馏获得水合肼粗品后,剩余溶液再进一步处理还可获得副产品NaCl和Na2CO3 ·10H2O,获得NaCl粗品的操作是

(4)称取5.0g水合肼样品,加水配成500mL溶液,从中取出10.00mL溶液于锥形瓶中,滴入几滴淀粉溶液,用0.20mol/L的I2溶液进行滴定,滴定终点的现象是
(5)脱水制得的液态肼,在加热条件下可与新制的Cu(OH)2制备纳米级Cu2O,并产生无污染气体,写出该反应的化学方程式:
您最近一年使用:0次