完成下列问题
(1)检验NH 的实验方法
的实验方法___________ ;
(2)检验FeCl2、FeCl3混合溶液中的Fe2+的实验方法___________ ;
(3)解释生石灰和浓氨水反应能放出NH3的原因___________ ;
(4)SO2通入品红溶液中,一段时间后加热的现象及原因___________ 。
(1)检验NH
 的实验方法
的实验方法(2)检验FeCl2、FeCl3混合溶液中的Fe2+的实验方法
(3)解释生石灰和浓氨水反应能放出NH3的原因
(4)SO2通入品红溶液中,一段时间后加热的现象及原因
更新时间:2023-10-25 22:50:42
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】某小组同学设计了如图所示实验装置并开展研究(部分夹持装置已略去)。
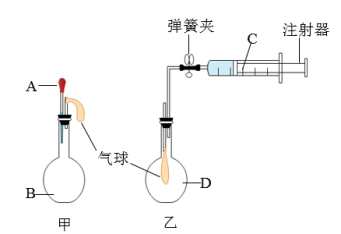
(1)当将A慢慢滴入甲瓶后,观察到甲瓶上的气球慢慢鼓起,则A和B分别可能是下列组合中的_______ (填标号)。
①稀硫酸和 溶液②浓硫酸和
溶液②浓硫酸和 溶液
溶液
③ 溶液和
溶液和 溶液④蒸馏水和
溶液④蒸馏水和 固体
固体
(2)打开弹簧夹将少量C慢慢推入乙瓶。
①若观察到乙瓶内的气球慢慢鼓起,且C为蒸馏水,则气体D可能为_______ (任填一种物质的化学式)。
②若C为 ,气体D为
,气体D为 ,则能观察到乙瓶中的现象是
,则能观察到乙瓶中的现象是_______ 。

(1)当将A慢慢滴入甲瓶后,观察到甲瓶上的气球慢慢鼓起,则A和B分别可能是下列组合中的
①稀硫酸和
 溶液②浓硫酸和
溶液②浓硫酸和 溶液
溶液③
 溶液和
溶液和 溶液④蒸馏水和
溶液④蒸馏水和 固体
固体(2)打开弹簧夹将少量C慢慢推入乙瓶。
①若观察到乙瓶内的气球慢慢鼓起,且C为蒸馏水,则气体D可能为
②若C为
 ,气体D为
,气体D为 ,则能观察到乙瓶中的现象是
,则能观察到乙瓶中的现象是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】某容积固定的密闭容器由可移动的活塞隔成A、B 两室,向B 室充入 1 molN2,A 室加入一定量的X 固体,加热,发生化学反应X 2Y↑+CO2↑+H2O↑,反应结束后活塞的位置如图所示。
2Y↑+CO2↑+H2O↑,反应结束后活塞的位置如图所示。

(1) A 室混合气体的物质的量为______________ ,生成的 CO2在标况下的体积为_____________ 。
(2)Y 是一种极易溶于水的有刺激性气味气体,实验室需要进行尾气处理,下列装置可用于作为Y 气体的尾气处理装置的是________________ 。

(3)实验测得反应后A 室混合气体的质量为 48g,则该混合气体的密度是同温同压条件下氢气密度的_______ 倍,X 的摩尔质量为____________ 。
(4)若在 A 室加入足量碱石灰(碱石灰可吸收 CO2和 H2O,忽略固体所占体积),保持温度不变,最终活塞停留的位置在___________ 刻度,此时容器内气体压强与加碱石灰前气体压强之比为_______________ 。
 2Y↑+CO2↑+H2O↑,反应结束后活塞的位置如图所示。
2Y↑+CO2↑+H2O↑,反应结束后活塞的位置如图所示。
(1) A 室混合气体的物质的量为
(2)Y 是一种极易溶于水的有刺激性气味气体,实验室需要进行尾气处理,下列装置可用于作为Y 气体的尾气处理装置的是

(3)实验测得反应后A 室混合气体的质量为 48g,则该混合气体的密度是同温同压条件下氢气密度的
(4)若在 A 室加入足量碱石灰(碱石灰可吸收 CO2和 H2O,忽略固体所占体积),保持温度不变,最终活塞停留的位置在
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】将SO2分别通入下列五种溶液中:

回答下列问题:
(1)试管①中的实验现象:KMnO4溶液____ ,证明SO2具有___ 性。
(2)试管②中的实验现象:溶液____ ,证明SO2具有____ 性。
(3)试管③中的实验现象:溶液____ ,证明SO2能中和NaOH,写出该反应的离子方程式:____ 。
(4)试管④中能产生____ 沉淀,该沉淀是____ 。
(5)试管⑤中能产生白色沉淀,该沉淀是____ 。

回答下列问题:
(1)试管①中的实验现象:KMnO4溶液
(2)试管②中的实验现象:溶液
(3)试管③中的实验现象:溶液
(4)试管④中能产生
(5)试管⑤中能产生白色沉淀,该沉淀是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】现有下列5种物质:① SO2、② NO2、③ HCl、④ HClO、⑤Al2O3。有颜色的气体是___________ ,遇氨气产生白烟的气体是___________ ,因见光而分解的是___________ ,能使品红溶液褪色且加热后又恢复红色的是___________ ,属于两性氧化物的是__________ 。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】在化学课上围绕浓硫酸的化学性质进行如下实验探究,将适量的蔗糖放入烧杯中,加几滴水,搅拌均匀,然后加入浓硫酸,生成黑色物质。请回答下列问题:
(1)这种黑色物质继续与浓硫酸作用会产生两种气体,其中一种气体有刺激性气味,是大气的污染物之一,反应的化学方程式为______ 。
(2)根据蔗糖与浓硫酸反应的实验现象,说明浓硫酸具有(填字母)_____ 。
(3)将(2)中产生的有刺激性气味的气体通入品红溶液中,可以看到品红溶液______ ,说明这种气体有_____ 性;将(2)中产生的有刺激性气味的气体通入氯水中,发生反应的化学方程式为_____ 。
(4)能否用澄清石灰水鉴别(2)中产生的两种气体(填“能”或“不能”)_____ ,若不能,请写出两种可以鉴别这两种气体的试剂:_____ 。
(1)这种黑色物质继续与浓硫酸作用会产生两种气体,其中一种气体有刺激性气味,是大气的污染物之一,反应的化学方程式为
(2)根据蔗糖与浓硫酸反应的实验现象,说明浓硫酸具有(填字母)
| A.酸性 | B.吸水性 | C.脱水性 | D.强氧化性 |
(4)能否用澄清石灰水鉴别(2)中产生的两种气体(填“能”或“不能”)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】非金属元素在化工生产中扮演着重要的角色。
(1)下列物质中,能吸收SO2的有_______ (填字母序号)。
a. 浓硫酸 b. 酸性KMnO4溶液 c. 生石灰
(2)久置在空气中的Na2SO3固体会部分变质,检验是否变质的方法是:取少量固体加水溶解,_______ (将实验操作和现象补充完整)。
(3)工业上利用氨的催化氧化制取NO,写出化学方程式_______ 。
(1)下列物质中,能吸收SO2的有
a. 浓硫酸 b. 酸性KMnO4溶液 c. 生石灰
(2)久置在空气中的Na2SO3固体会部分变质,检验是否变质的方法是:取少量固体加水溶解,
(3)工业上利用氨的催化氧化制取NO,写出化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】基础知识填空
(1)目前用途最广、使用量最大的合金是___________ 。
(2)重晶石的化学式为___________ 。
(3)除去 粉末中混有的少量
粉末中混有的少量 所涉及的反应的化学方程式为
所涉及的反应的化学方程式为___________ 。
(4)实验室中制备气体 的化学方程式为
的化学方程式为___________ ; 与氧气在红热的铂丝作用下的化学方程式为
与氧气在红热的铂丝作用下的化学方程式为___________ 。
(5)规范叙述-用实验方法证明某种白色晶体是
___________ 。
(6)将适量铁粉放入 溶液中,完全反应后,溶液中的
溶液中,完全反应后,溶液中的 和
和 浓度相等。则未反应的
浓度相等。则未反应的 和已反应的
和已反应的 的物质的量之比是
的物质的量之比是___________ 。
(1)目前用途最广、使用量最大的合金是
(2)重晶石的化学式为
(3)除去
 粉末中混有的少量
粉末中混有的少量 所涉及的反应的化学方程式为
所涉及的反应的化学方程式为(4)实验室中制备气体
 的化学方程式为
的化学方程式为 与氧气在红热的铂丝作用下的化学方程式为
与氧气在红热的铂丝作用下的化学方程式为(5)规范叙述-用实验方法证明某种白色晶体是

(6)将适量铁粉放入
 溶液中,完全反应后,溶液中的
溶液中,完全反应后,溶液中的 和
和 浓度相等。则未反应的
浓度相等。则未反应的 和已反应的
和已反应的 的物质的量之比是
的物质的量之比是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】中药常采用硫黄熏蒸法以达到防霉、防虫等目的。我国规定党参等中药 残留量不得超过
残留量不得超过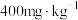 。某小组欲检测某药厂所售党参是否合格,查阅资料后得知:
。某小组欲检测某药厂所售党参是否合格,查阅资料后得知:
① 残留量是指残留硫的总量,以
残留量是指残留硫的总量,以 计;
计;
②中药中残留的 已大部分转化为
已大部分转化为 。
。
(1)将200g所售党参研碎,用 溶液充分浸泡,得无色浸泡液X,将X分成两等份。
溶液充分浸泡,得无色浸泡液X,将X分成两等份。
用 溶液浸泡的目的
溶液浸泡的目的______ (用化学方程式表示)。
(2)甲同学取一份X溶液采用如下方案测定党参中 残留量:
残留量:

判断 溶液已过量的操作为
溶液已过量的操作为______ ;
判断沉淀是否洗净所选用的试剂为______ ;党参中 残留量的表达式为
残留量的表达式为______ 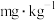 (用含m的式子表示)。
(用含m的式子表示)。
(3)乙同学取另一份X溶液采用如下方案进行测定(整个过程无气体放出),判断该党参______ (填“符合”或“不符合”)国家标准。

 残留量不得超过
残留量不得超过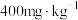 。某小组欲检测某药厂所售党参是否合格,查阅资料后得知:
。某小组欲检测某药厂所售党参是否合格,查阅资料后得知:①
 残留量是指残留硫的总量,以
残留量是指残留硫的总量,以 计;
计;②中药中残留的
 已大部分转化为
已大部分转化为 。
。(1)将200g所售党参研碎,用
 溶液充分浸泡,得无色浸泡液X,将X分成两等份。
溶液充分浸泡,得无色浸泡液X,将X分成两等份。用
 溶液浸泡的目的
溶液浸泡的目的(2)甲同学取一份X溶液采用如下方案测定党参中
 残留量:
残留量:
判断
 溶液已过量的操作为
溶液已过量的操作为判断沉淀是否洗净所选用的试剂为
 残留量的表达式为
残留量的表达式为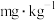 (用含m的式子表示)。
(用含m的式子表示)。(3)乙同学取另一份X溶液采用如下方案进行测定(整个过程无气体放出),判断该党参

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】有物质的量浓度均为0.1mo/L的下列溶液:
(1)①NH3·H2O ②FeCl2 ③NaHSO4 ④KOH ⑤Ba(OH)2 ⑥H2SO4,其pH由大到小的顺序排列的是(填序号)___ 。
(2)写出氯化亚铁溶液中,亚铁离子水解的离子方程式___ 。
(3)写出硫酸氢钠与氢氧化钡2:1反应的离子方程式___ 。
(4)将氢氧化钾与氯化亚铁溶液混合,现象___ 。依次发生的化学方程式____ 、___ 。
(5)氯化亚铁保存时为何加少量铁粉___ ,若保存硫酸铁溶液时应向溶液中加入____ 。
(6)如何利用氯水和硫氰化钾检验氯化亚铁溶液中的Fe2+,写出加入试剂的先后顺序和对应现象__ 。
(1)①NH3·H2O ②FeCl2 ③NaHSO4 ④KOH ⑤Ba(OH)2 ⑥H2SO4,其pH由大到小的顺序排列的是(填序号)
(2)写出氯化亚铁溶液中,亚铁离子水解的离子方程式
(3)写出硫酸氢钠与氢氧化钡2:1反应的离子方程式
(4)将氢氧化钾与氯化亚铁溶液混合,现象
(5)氯化亚铁保存时为何加少量铁粉
(6)如何利用氯水和硫氰化钾检验氯化亚铁溶液中的Fe2+,写出加入试剂的先后顺序和对应现象
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】以下为中学化学中常见的物质:①Cu; ②FeCl3溶液; ③CuCl2溶液;④CO2;⑤H2SO4;⑥酒精;⑦CaCO3;⑧FeSO4;⑨Ba(OH)2。
请根据要求回答下列有关问题:
(1)以上物质中属于电解质的是________ ;属于非电解质的是__________ 。(填序号)
(2)将②③⑧混合配制成浓度均为1mol•L﹣1的混合溶液100mL,加入一定量的铁粉,充分反应后,若铁粉无剩余,且有铜生成.则反应后的溶液中一定含有的阳离子是______ ,发生反应的离子方程式为_____________________________________________________ 。
(3)检验②溶液中阳离子的试剂是________________ ,证明其存在的现象是____________ 。
(4)向沸水中逐滴滴加1 mol·L-1 FeCl3溶液,至液体呈透明的红褐色,该分散系中粒子直径的范围是________ nm。
请根据要求回答下列有关问题:
(1)以上物质中属于电解质的是
(2)将②③⑧混合配制成浓度均为1mol•L﹣1的混合溶液100mL,加入一定量的铁粉,充分反应后,若铁粉无剩余,且有铜生成.则反应后的溶液中一定含有的阳离子是
(3)检验②溶液中阳离子的试剂是
(4)向沸水中逐滴滴加1 mol·L-1 FeCl3溶液,至液体呈透明的红褐色,该分散系中粒子直径的范围是
您最近一年使用:0次
【推荐3】某种催化剂为铁的氧化物。化学兴趣小组对该催化剂中铁元素的价态进行了探究。请回答下列实验方案中的有关问题:
(一)实验仪器与试剂
仪器:烧杯、试管、玻璃棒、药匙、滴管、酒精灯、试管夹;
试剂:3mol·L-1H2SO4、6mol·L-1HNO3、0.01mol·L-1KMnO4、NaOH稀溶液、20%KSCN溶液、蒸馏水。
(二)实验原理
Fe2+能使酸性KMnO4溶液紫色褪去;Fe3+溶液中滴加KSCN溶液变红色。
(1)一位同学将少许样品溶于稀硝酸中,取少许溶液滴加KSCN溶液后出现红色。由此得出为铁元素为+3价的结论。该结论是否合理___ ,并说明理由___ 。
(三)实验设计
(2)提出合理假设。
假设1:催化剂中铁元素全部为+3价;
假设2:催化剂中铁元素全部为+2价;
假设3:___ 。
(3)设计实验证明假设。请完成下表中的实验操作步骤,预期现象与结论。
(一)实验仪器与试剂
仪器:烧杯、试管、玻璃棒、药匙、滴管、酒精灯、试管夹;
试剂:3mol·L-1H2SO4、6mol·L-1HNO3、0.01mol·L-1KMnO4、NaOH稀溶液、20%KSCN溶液、蒸馏水。
(二)实验原理
Fe2+能使酸性KMnO4溶液紫色褪去;Fe3+溶液中滴加KSCN溶液变红色。
(1)一位同学将少许样品溶于稀硝酸中,取少许溶液滴加KSCN溶液后出现红色。由此得出为铁元素为+3价的结论。该结论是否合理
(三)实验设计
(2)提出合理假设。
假设1:催化剂中铁元素全部为+3价;
假设2:催化剂中铁元素全部为+2价;
假设3:
(3)设计实验证明假设。请完成下表中的实验操作步骤,预期现象与结论。
| 实验操作步骤 | 预期现象与结论 |
| 步骤1:用滴管取一定量3mol·L-1H2SO4于试管中,加热煮沸数分钟以出去溶于其中的氧气。 | 无明显现象 |
| 步骤2:用药匙取少量样品于试管中,用滴管加入除氧的3mol·L-1H2SO4,并加热,充分反应后得A溶液。 | 固体溶解,溶液颜色发生变化 |
| 步骤3:取少许A溶液于试管中滴加1~2滴20%KSCN溶液,振荡 | 若溶液不呈红色,则假设2成立;若溶液呈红色,则假设1或假设3成立 |
| 步骤4:另取少许A溶液于试管中, | 结合③,若 |
您最近一年使用:0次



