向两个锥形瓶中各加入0.048g镁条,塞紧橡胶塞,然后用注射器分别注入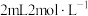 盐酸、
盐酸、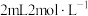 醋酸,测得锥形瓶内气体的压强随时间的变化如图所示,下列说法正确的是(不考虑盐酸和醋酸的挥发性)
醋酸,测得锥形瓶内气体的压强随时间的变化如图所示,下列说法正确的是(不考虑盐酸和醋酸的挥发性)
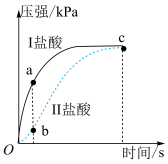
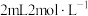 盐酸、
盐酸、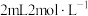 醋酸,测得锥形瓶内气体的压强随时间的变化如图所示,下列说法正确的是(不考虑盐酸和醋酸的挥发性)
醋酸,测得锥形瓶内气体的压强随时间的变化如图所示,下列说法正确的是(不考虑盐酸和醋酸的挥发性)
A.若将上述镁条换成等质量的镁粉,反应结束后,曲线Ⅱ生成 的物质的量不发生改变 的物质的量不发生改变 |
B.相同条件下,冰醋酸的导电能力比 醋酸强 醋酸强 |
C.由曲线Ⅰ和Ⅱ可知,盐酸比醋酸的反应速率快,是由于 的浓度比 的浓度比 大 大 |
D.镁与 醋酸反应的过程中,所得溶液的温度一直下降 醋酸反应的过程中,所得溶液的温度一直下降 |
23-24高二上·陕西西安·期中 查看更多[3]
陕西省西安市莲湖区2023-2024学年高二上学期期中联考化学试题广东省部分名校2023-2024学年高三上学期联合质量检测化学试题(已下线)寒假作业02 化学反应速率-【寒假分层作业】2024年高二化学寒假培优练(人教版2019)
更新时间:2023-12-02 15:17:03
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】下列说法正确的是
| A.可以用过滤的方法分离氯化铁溶液和氢氧化铁胶体 |
| B.氢氧化铁胶体无色、透明,能产生丁达尔效应 |
| C.Fe3+、SO2均既有氧化性又有还原性 |
| D.硫酸溶液的导电性不一定比醋酸溶液的导电性强 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】某研究性学习小组通过传感器测量一定温度下物质的电导率,各物质的电导率数据如表:
下列分析不正确 的是
| 编号 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ |
| 物质 | CaCO3(固体) | H2O | CaCO3 饱和溶液 | CaSO4 饱和溶液 | 0.001mol·L-1NaCl溶液 | 0.001mol·L-1AgNO3溶液 | AgCl 饱和溶液 |
| 电导率 | 0 | 7 | 37 | 389 | 1989 | 1138 | 13 |
| A.依据表中数据分析,CaCO3固体中不存在能自由移动的离子 |
| B.对比②和⑦,说明⑦中存在:AgCl=Ag++Cl- |
| C.对比③和④,可推出该温度下,Ksp(CaCO3)<Ksp(CaSO4) |
| D.⑤、⑥等体积混合后过滤,推测滤液的电导率等于13 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】下列事实一定能说明HF是弱酸的是
| A.用HF溶液做导电性实验,灯泡很暗 | B.1mol/L的HF水溶液能使紫色石蕊试液变红 |
| C.常温下0.1mol/L的HF溶液的pH为2.3 | D.HF与NaCl不能发生反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下表中产生H2的反应速率最大的是( )
| 编号 | 金属(粉末状) | 金属物质的量/mol | 酸及酸的浓度/(mol·L-1) | 酸的体积/mL | 反应温度/℃ |
| A | Al | 0.2 | H2SO4 18.4 | 20 | 30 |
| B | Mg | 0.2 | H2SO4 3 | 10 | 30 |
| C | Fe | 0.1 | HNO3 6 | 20 | 60 |
| D | Mg | 0.1 | H2SO4 3 | 10 | 60 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】少量铁块与100mL0.01mol·L-1的稀盐酸反应,反应速率太慢。为了加快此反应速率而不改变H2的产量,可以使用如下方法中的
①加H2O;②加NaOH固体;③将铁块换成等质量的铁粉;④加CH3COONa固体;⑤加NaCl溶液;⑥滴入几滴硫酸铜溶液;⑦升高温度(不考虑盐酸挥发);⑧改用10mL0.1mol·L-1盐酸
①加H2O;②加NaOH固体;③将铁块换成等质量的铁粉;④加CH3COONa固体;⑤加NaCl溶液;⑥滴入几滴硫酸铜溶液;⑦升高温度(不考虑盐酸挥发);⑧改用10mL0.1mol·L-1盐酸
| A.①⑥⑦ | B.③⑤⑧ | C.⑤⑦⑧ | D.③⑦⑧ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】部分弱酸的电离平衡常数如下表:
下列选项正确的是
| 弱酸 | HCOOH | HCN | H2CO3 |
| 电离平衡常数(25℃) | K1=1.77×10-4 | K1=4.9×10-10 | K1=4.3×10-7 K2=5.6×10-11 |
A.2CN- + H2O + CO2=2HCN + CO |
B.反应HCO +OH-⇌CO +OH-⇌CO +H2O的平衡常数K=5.6×103 +H2O的平衡常数K=5.6×103 |
C.0.1mol/LNa2CO3溶液中:c(H+)= c(OH-)+c(HCO )+2c(H2CO3) )+2c(H2CO3) |
| D.等体积等浓度的HCOONa和NaCN所含阴离子的数目相等 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列关于电解质溶液的叙述正确的是
| A.常温下,在NH4Cl溶液中离子浓度大小顺序为c(Cl—)>c(NH4+)>c(H+) > c(OH—) |
| B.将pH=4的醋酸溶液稀释后,溶液中所有离子的浓度均降低 |
| C.中和pH与体积均相同的盐酸和醋酸溶液,消耗NaOH的物质的量相同 |
| D.常温下,同浓度的Na2S与NaHS溶液相比,Na2S溶液的pH小 |
您最近一年使用:0次

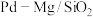 催化剂上
催化剂上 甲烷化反应机理如图所示,下列说法不正确的是
甲烷化反应机理如图所示,下列说法不正确的是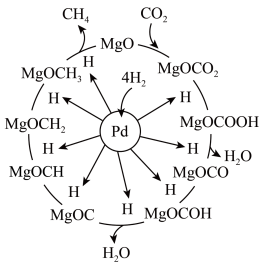
 和MgO
和MgO


