以黄铁矿的烧渣(主要成分为Fe2O3、FeO、SiO2等)为原料制取新型高效的无机高分子絮凝剂一聚合硫酸铁[Fe2(OH)n(SO4)3· ]工艺流程如下:
]工艺流程如下:
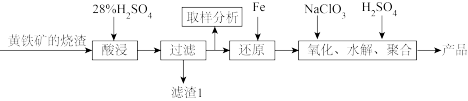
已知:为防止Fe3+水解,原料中的Fe3+必须先还原为Fe2+,下列有关说法错误的是
 ]工艺流程如下:
]工艺流程如下:
已知:为防止Fe3+水解,原料中的Fe3+必须先还原为Fe2+,下列有关说法错误的是
| A.“取样分析”可以用来确定下一步还原所需Fe的量和氧化所需NaClO3的量 |
| B.为促进水解反应和聚合生成产品,应在高温条件下进行 |
C.氧化反应的离子方程式为 +6H++6Fe2+=6Fe3++Cl-+3H2O +6H++6Fe2+=6Fe3++Cl-+3H2O |
| D.水解时溶液的pH偏小或偏大都会影响聚合硫酸铁的产率 |
更新时间:2023-12-06 21:11:14
|
相似题推荐
单选题
|
较难
(0.4)
解题方法
【推荐1】下列反应的离子方程式书写不正确的是( )
| A.酸性KI溶液在空气中变质:4I-+O2+4H+=2I2+2H2O |
| B.SO2通入过量的NaClO溶液:SO2+H2O+ClO-=SO42-+Cl-+2H+ |
| C.制印刷电路板常用溶液作为“腐蚀液”:2Fe3++Cu=2Fe2++Cu2+ |
| D.碳酸钠溶液与过量的醋酸反应:2 CH3COOH+CO32﹣=2CH3COO﹣+CO2↑+H2O |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐2】下列离子组中加(或通)入相应试剂后,判断和分析均正确的是
| 选项 | 离子组 | 加(或通)入试剂 | 判断和分析 |
| A | Na+、H+、Ba2+、Cl-、 | 足量CO2 | 能大量共存 |
| B | Na+、Mg2+、Cl-、 | 足量NaOH溶液 | 不能大量共存,只发生下列反应Mg2++ +OH-=MgCO3↓+H2O +OH-=MgCO3↓+H2O |
| C | Na+、K+、 、Cl- 、Cl- | 足量NaHCO3溶液 | 不能大量共存,因 和 和 之间会发生完全双水解生成CO2气体和Al(OH)3沉淀 之间会发生完全双水解生成CO2气体和Al(OH)3沉淀 |
| D | Na+、K+、ClO-、 | 少量SO2 | 不能大量共存,只发生下列氧化还原反应ClO-+H2O+SO2=Cl-+ +2H+ +2H+ |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐3】向10 mL a mol·L-1 NH4Al(SO4)2溶液中,滴加b mol·L-1 Ba(OH)2溶液10 mL,下列叙述不正确的是
| A.当2a=b时,溶液中生成的沉淀质量最大 |
| B.当a=2b时,发生的离子反应为:2NH4++ SO42-+ Ba2++2OH-= BaSO4↓+2NH3·H2O |
| C.当2b≤3a时,发生的离子反应为:3SO42-+2Al3++ 3Ba2++6OH-= 3BaSO4↓+2Al(OH)3↓ |
| D.当2a<b≤2.5a时,溶液中的n(AlO2-)为0.02(b-2a)mol |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐1】有FeO、Fe3O4的混合物若干克,在足量H2气流中加热充分反应,冷却后称得剩余固体全为铁单质,且比原混合物减轻了0.8g,将等质量的原混合物与硫酸反应,欲使之完全溶解,需0.5mol•L﹣1的硫酸的体积至少为
| A.0.1L | B.0.2L | C.0.4L | D.0.5L |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐2】已知:室温时,饱和 溶液的pH约为3.9;SnS沉淀完全时溶液的pH为1.6;FeS开始沉淀时溶液的pH为3.0,沉淀完全时的pH为5.5;
溶液的pH约为3.9;SnS沉淀完全时溶液的pH为1.6;FeS开始沉淀时溶液的pH为3.0,沉淀完全时的pH为5.5; 不溶于乙醇。根据以上信息设计以市售铁屑(含少量锡、氧化铁等杂质)为原料生产纯净绿矾的一种方法如图所示,下列说法错误的是
不溶于乙醇。根据以上信息设计以市售铁屑(含少量锡、氧化铁等杂质)为原料生产纯净绿矾的一种方法如图所示,下列说法错误的是

 溶液的pH约为3.9;SnS沉淀完全时溶液的pH为1.6;FeS开始沉淀时溶液的pH为3.0,沉淀完全时的pH为5.5;
溶液的pH约为3.9;SnS沉淀完全时溶液的pH为1.6;FeS开始沉淀时溶液的pH为3.0,沉淀完全时的pH为5.5; 不溶于乙醇。根据以上信息设计以市售铁屑(含少量锡、氧化铁等杂质)为原料生产纯净绿矾的一种方法如图所示,下列说法错误的是
不溶于乙醇。根据以上信息设计以市售铁屑(含少量锡、氧化铁等杂质)为原料生产纯净绿矾的一种方法如图所示,下列说法错误的是
| A.将浓硫酸稀释为25%稀硫酸,所需玻璃仪器有玻璃棒、烧杯、量筒、胶头滴管、容量瓶 |
B.操作Ⅱ中用硫酸酸化至pH=2的主要目的是抑制 的水解 的水解 |
C.操作Ⅱ中,通入 至饱和的目的是使 至饱和的目的是使 转化为SnS沉淀并防止 转化为SnS沉淀并防止 被氧化 被氧化 |
| D.操作Ⅳ中所得的晶体可用乙醇洗去晶体表面附着的水 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】下图为从海带中提取碘的工业生产过程,有关说法错误的是
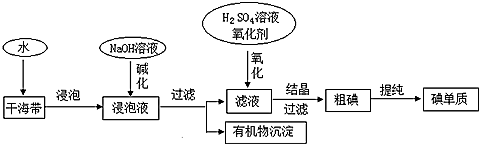

| A.因海水中蕴藏着极其丰富的碘元素,所以工业上也可以直接用海水来提取碘元素 |
| B.碱化操作时,加入NaOH溶液的原因是在碱性溶液中,可溶性有机质可形成沉淀 |
| C.在实验室进行氧化操作时,加入的氧化剂可以是新制氯水、双氧水等 |
| D.在实验室进行过滤操作时,需要用到玻璃仪器有玻璃棒、烧杯、漏斗 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】为除去某物质中所含的杂质,所选用的试剂或操作方法正确的是
| 序号 | 物质 | 杂质 | 除杂质应选用的试剂或操作方法 |
| ① | KNO3溶液 | KOH | 滴入HNO3同时测定pH至溶液呈酸性 |
| ② | FeSO4溶液 | CuSO4 | 加入过量铁粉并过滤 |
| ③ | CO2 | CO | 依次通过盛有NaOH溶液和浓硫酸的洗气瓶 |
| ④ | NaNO3 | CaCO3 | 加稀盐酸溶解、过滤、蒸发、结晶 |
| A.①② | B.②③④ | C.①②③ | D.①②③④ |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】当今环境保护越来越受重视,某化工集团为减少环境污染,提高资源的利用率、将钛厂、氯碱厂、甲醇厂进行联合生产。其主要生产工艺如下:(FeTiO3中Ti为+4价)
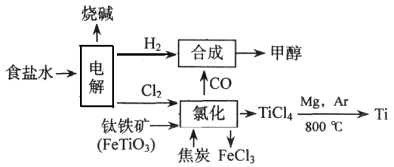
下列叙述正确的是

下列叙述正确的是
| A.该流程中只有“电解”、“氯化”涉及氧化还原反应 |
| B.“氯化”时每消耗36g焦炭,则转移7mol电子 |
| C.“合成”反应中氧化剂与还原剂的物质的量之比为1:1 |
| D.上述流程中“Mg,Ar"可用“Mg,CO2”代替 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】从铜阳极泥分铜渣碱浸液中制备 的工艺流程如图所示:
的工艺流程如图所示:

已知:①碱浸液中碲以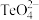 的形式存在。
的形式存在。
② 与氧化铝的性质具有一定的相似性。
与氧化铝的性质具有一定的相似性。
下列说法错误的是
 的工艺流程如图所示:
的工艺流程如图所示:
已知:①碱浸液中碲以
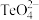 的形式存在。
的形式存在。②
 与氧化铝的性质具有一定的相似性。
与氧化铝的性质具有一定的相似性。下列说法错误的是
A.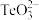 中Te元素的化合价为+4 中Te元素的化合价为+4 |
B.加入的 在反应中被氧化 在反应中被氧化 |
C.根据上述反应可以推知,还原性: |
| D.为防止产品产率降低,加入硫酸的量不宜过多 |
您最近一年使用:0次

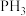 )是一种在空气中能自燃的剧毒气体,具有还原性,可作为电子工业原料。
)是一种在空气中能自燃的剧毒气体,具有还原性,可作为电子工业原料。
 转化为
转化为 的理论转化率为
的理论转化率为
 时转移电子数之比为3:4
时转移电子数之比为3:4 、
、 溶液反应消耗
溶液反应消耗

