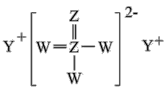元素R、X、T、Z、Q在元素周期表中的相对位置如下表所示, 其中R单质在暗处与H2剧烈化合并发生爆炸。则下列判断正确的是
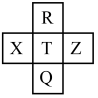

| A.非金属性:Z<T<X |
| B.R与Q的电子数相差26 |
| C.气态氢化物稳定性:R <T<Q |
| D.最高价氧化物的水化物的酸性:T>Q |
2013·广东·一模 查看更多[16]
(已下线)2013年全国普通高等学校招生统一考试理科综合能力测试化学(广东卷)(已下线)2013-2014学年广东省梅州市重点中学高一上学期质检化学试卷2013年普通高等学校招生全国统一考试化学(广东卷)(已下线)2013-2014天津市天津一中第二学期期中检测高一化学试卷(已下线)2013-2014广东省梅州市重点中学高一下学期期中化学试卷(已下线)2013-2014广东省广州六中高三5月第三次模拟理综化学试卷(已下线)2013-2014甘肃省肃南县第一中学高一下学期期末考试化学试卷(已下线)2013-2014广东省越秀区高一下学期学业水平测试调研化学试卷2015届广东省潮州金中等五校高三联考理综化学试卷2016-2017学年宁夏育才中学学益校区高一下学期第一次(3月)月考化学试卷2016-2017学年河北省辛集中学高一下学期第二次月考化学试卷鲁科版(2019)高一必修第二册 第1章 原子结构 元素周期律第3节 元素周期表的应用高一必修第一册(苏教2019)专题5 第一单元 元素周期律和元素周期表4湖南省常德市第一中学2021届高三第四次月水平检测试化学试题江西省抚州市资溪县第一中学2022-2023学年高二下学期5月期中考试化学试题山东省鄄城县第一中学2022-2023学年高一下学期3月月考化学试题
更新时间:2014-05-22 14:51:36
|
相似题推荐
多选题
|
适中
(0.65)
名校
【推荐1】下列实验操作、现象和结论均正确的是
| 选项 | 操作 | 现象 | 结论 |
| A | 向FeSO4溶液中滴入少量酸性KMnO4溶液 | KMnO4溶液紫色褪去 | Fe2+有氧化性 |
| B | 向Na2SiO3溶液中通入适量的CO2 | 产生白色胶状物质 | 酸性:H2CO3>H2SiO3 |
| C | 将新制氯水和NaBr溶液在试管中混合后,加入CCl4,振荡,静置 | 下层溶液呈橙红色 | 氧化性:Cl2>Br2 |
| D | 向Al2(SO4)3溶液中滴加过量氨水 | 溶液先浑浊后澄清 | Al3+与NH3·H2O不能大量共存 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐2】运用元素周期律分析下面的推断,其中错误 的是( )
| A.硼的氧化物的水化物可能具有两性 |
| B.砹(At)为有色固体,HAt不稳定,AgAt见光容易分解,但不溶于水也不溶于稀酸 |
| C.氢氧化铷(RbOH)易溶于水 |
| D.硒化氢(H2Se)是无色、有毒、比H2S稳定的气体 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐1】以下是部分短周期元素化合价与原子序数的关系图,下列说法正确的是
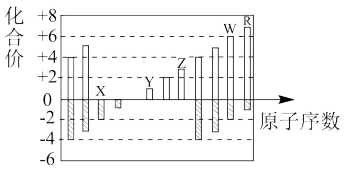

| A.原子半径:Z>Y>X |
| B.气态氢化物的稳定性:R>W |
| C.Y的最高价氧化物的水化物的碱性弱于Z的最高价氧化物的水化物的碱性 |
| D.Y、Z和W三者最高价氧化物对应的水化物两两之间能反应 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐2】运用元素周期律分析下面的推断,其中错误的是
| A.已知Ra是第7周期IIA族的元素,故Ra(OH)2的碱性比 Mg(OH)2的碱性弱 |
| B.已知As是第4周期ⅤA族的元素,故AsH3的稳定性比NH3的稳定性弱 |
| C.已知Cs的原子半径比Na的原子半径大,故Cs与水反应比Na与水反应更剧烈 |
| D.已知 Cl的原子半径比 S的原子半径小,故HClO3的酸性比 H2SO3的强 |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐3】科学探究与创新意识是中学生必备的学科素养,下列实验操作不能达到实验目的的是
| 选项 | 实验目的 | 实验操作 |
| A | 分离碘和氯化铵 | 将固体置于烧杯底部加热,烧杯上方用表面皿覆盖 |
| B | 证明氯水具有漂白性 | 分别向红布条和品红溶液中滴加氯水 |
| C | 证明钠的金属性比镁强 | 向氯化镁溶液中加入绿豆粒大小的一块钠 |
| D | 探究浓硫酸的脱水性 | 分别向白纸和蔗糖粉末上滴加浓硫酸 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列说法正确的是( )
| A.SiH4比CH4稳定 |
| B.铜的电子层数多于镁的电子层数,故铜的金属性强于镁 |
| C.Na和Cs属于第ⅠA族元素,Cs失电子能力比Na的强 |
| D.P和As属于第ⅤA族元素,H3PO4酸性比H3AsO4的强 |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
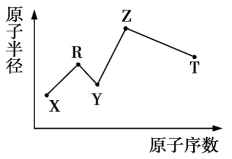
【推荐2】现有短周期主族元素X、Y、Z、R、T,R原子的最外层电子数是电子层数的2倍;Y与Z能形成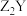 、
、 型离子化合物,Y与T同主族。五种元素的原子半径与原子序数之间的关系如图所示。下列推断正确的是( )
型离子化合物,Y与T同主族。五种元素的原子半径与原子序数之间的关系如图所示。下列推断正确的是( )
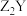 、
、 型离子化合物,Y与T同主族。五种元素的原子半径与原子序数之间的关系如图所示。下列推断正确的是( )
型离子化合物,Y与T同主族。五种元素的原子半径与原子序数之间的关系如图所示。下列推断正确的是( )
A.原子半径和离子半径: |
B.最简单氢化物的沸点: |
C.最高价氧化物对应水化物的酸性: |
| D.由X、Y、Z、R四种元素组成的常见化合物中含有离子键 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐1】X、Y、Z、M、Q五种短周期元素,原子序数依次增大。Y元素的最高正价为 价,Y元素与Z、M元素相邻,且与M元素同主族;化合物Z2X4的电子总数为18个;Q元素的原子最外层电子数比次外层少一个电子。下列说法
价,Y元素与Z、M元素相邻,且与M元素同主族;化合物Z2X4的电子总数为18个;Q元素的原子最外层电子数比次外层少一个电子。下列说法不正确 的是( )
 价,Y元素与Z、M元素相邻,且与M元素同主族;化合物Z2X4的电子总数为18个;Q元素的原子最外层电子数比次外层少一个电子。下列说法
价,Y元素与Z、M元素相邻,且与M元素同主族;化合物Z2X4的电子总数为18个;Q元素的原子最外层电子数比次外层少一个电子。下列说法| A.原子半径:Z<Y<M |
| B.最高价氧化物对应水化物的酸性:Z>Y>Q |
| C.X2Z—ZX2易溶于水,因为其分子极性与水分子相似 |
| D.X、Z和Q三种元素形成的化合物一定是共价化合物 |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐2】某元素X的核外电子数等于核内中子数.取该元素单质2.8克与氧气充分作用,可得到6克化合物XO2.该元素在周期表中的位置是( )
| A.第三周期 | B.第二周期 | C.第ⅣA族 | D.第ⅤA族 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐3】X、Y、Z、M、W为五种短周期元素,X、Y、Z是原子序数依次递增的同周期元素,最外层电子数之和为15;X与Z可形成XZ2分子;Y与M形成的气态化合物在标准状态下的密度为0.76g/L;W的质子数是X、Y、Z、M四种元素质子数之和的 。下列说法正确的是
。下列说法正确的是
 。下列说法正确的是
。下列说法正确的是| A.原子半径:W>X>Y>Z>M |
B. 、 、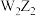 均为直线形的共价化合物 均为直线形的共价化合物 |
C.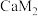 和 和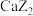 两种化合物中,阳离子与阴离子个数比均为1∶2 两种化合物中,阳离子与阴离子个数比均为1∶2 |
| D.由X、Y、Z、M四种元素共同形成的化合物中一定有共价键,可能有离子键 |
您最近一年使用:0次