过氧化物在生活和生产中用途广泛,过氧化钠和过氧化钙是常见的过氧化物。室温下,某同学进行CO2与Na2O2反应的探究实验,回答下列问题。
(1)用如图装置制备纯净干燥的CO2

B中的试剂是___________ ,C中试剂的作用是___________
(2)按照如图装置图进行实验(夹持装置略)。
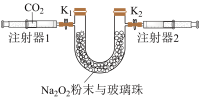
①先组装仪器,并检查好气密性,再用注射器1抽取100mL纯净的CO2,将其连接在K1处,注射器2的活塞推到底后连接在K2处,具支U形管中装入足量的Na2O2粉末与玻璃珠。
②打开止水夹K1、K2,向右推动注射器1的活塞,可观察到U形管中固体颜色逐渐由淡黄色变为白色,注射器2活塞外移。
③实验时,具支U形管中反应的化学方程式为___________
(3)实验结束后,当注射器1的活塞推到底时,测得注射器2中气体体积为70mL,则相同条件下反应消耗CO2的体积是___________
(4)已知:过氧化钙(CaO2)广泛应用于水产养殖、污水处理,是优良的供氧剂,化学性质与Na2O2类似。
实验探究:过氧化钙与水反应除生成氧气外,还生成什么物质?
①进行实验:取适量过氧化钙放入试管中,加适量水,向试管中滴加酚酞试液,溶液变成红色,说明生成了Ca(OH)2,写出该反应的化学方程式___________
②此供氧剂长期暴露在空气中,会变质生成CaCO3,为检验此供氧剂是变质,可向其中加入稀盐酸,若观察到有气泡生成,则判断此供氧剂已变质。你是否认同上述方案,理由是___________ 。
(1)用如图装置制备纯净干燥的CO2

B中的试剂是
(2)按照如图装置图进行实验(夹持装置略)。

①先组装仪器,并检查好气密性,再用注射器1抽取100mL纯净的CO2,将其连接在K1处,注射器2的活塞推到底后连接在K2处,具支U形管中装入足量的Na2O2粉末与玻璃珠。
②打开止水夹K1、K2,向右推动注射器1的活塞,可观察到U形管中固体颜色逐渐由淡黄色变为白色,注射器2活塞外移。
③实验时,具支U形管中反应的化学方程式为
(3)实验结束后,当注射器1的活塞推到底时,测得注射器2中气体体积为70mL,则相同条件下反应消耗CO2的体积是
(4)已知:过氧化钙(CaO2)广泛应用于水产养殖、污水处理,是优良的供氧剂,化学性质与Na2O2类似。
实验探究:过氧化钙与水反应除生成氧气外,还生成什么物质?
①进行实验:取适量过氧化钙放入试管中,加适量水,向试管中滴加酚酞试液,溶液变成红色,说明生成了Ca(OH)2,写出该反应的化学方程式
②此供氧剂长期暴露在空气中,会变质生成CaCO3,为检验此供氧剂是变质,可向其中加入稀盐酸,若观察到有气泡生成,则判断此供氧剂已变质。你是否认同上述方案,理由是
更新时间:2023-12-12 08:40:56
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】已知常温下D为生活中常见的无色无味的液体,F为淡黄色粉末(反应条件均已省略),请根据下列要求回答有关问题:

(1)写出②的化学方程式______ ,当生成5.6 L气体G(标准状况)时,此时反应转移的电子数目为(阿伏加德罗常数为NA)________ 。
(2)若A、C、E均含有氯元素,且A为单质,B为强碱溶液,写出该条件下反应①的离子方程式:______________ 。
(3)若A为固体单质,C、E是两种能使澄清石灰水变浑浊的气体,写出该条件下反应①的化学方程式:________ 。

(1)写出②的化学方程式
(2)若A、C、E均含有氯元素,且A为单质,B为强碱溶液,写出该条件下反应①的离子方程式:
(3)若A为固体单质,C、E是两种能使澄清石灰水变浑浊的气体,写出该条件下反应①的化学方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】X、Y、Z三种常见的短周期元素可以形成XY2、Z2Y、XY3、Z2Y2、Z2X等化合物,已知Y的离子和Z的离子有相同的电子层结构,X离子比Y离子多一个电子层。试回答:
(1)写出X、Y、Z三种元素的符号和名称:_____________ 、_______ 、_______ ;
(2)分析Z2Y2中含有的化学键类型:_______ ;
(3)写出Z2Y2与二氧化碳反应的方程式:_____________________ ;
(4)用电子式表示X和Z两元素形成化合物的过程:__________________ 。
(1)写出X、Y、Z三种元素的符号和名称:
(2)分析Z2Y2中含有的化学键类型:
(3)写出Z2Y2与二氧化碳反应的方程式:
(4)用电子式表示X和Z两元素形成化合物的过程:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】某工厂从含硫酸钡、氧化铜、氧化亚铁、氧化铝和少量氧化银的废渣中回收金属的工艺流程如图所示:

(1)滤渣①的化学式为__________ ,是__________ (填“强”、“弱”、“非”)电解质。
(2)加入过量铁粉,被还原的金属阳离子有__________ 。过氧化钠的电子式为__________ 。
(3)用滤渣②作粗铜电解精炼铜时,粗铜作__________ (填“阳”、“阴”)极,硫酸铜作电解质溶液,阳极泥中含有__________ (填物质名称)。
(4)滤液④的溶质是__________ 。B电解方程式为__________ 。
(5)写出滤渣③生成A的化学方程式__________ 。

(1)滤渣①的化学式为
(2)加入过量铁粉,被还原的金属阳离子有
(3)用滤渣②作粗铜电解精炼铜时,粗铜作
(4)滤液④的溶质是
(5)写出滤渣③生成A的化学方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】室温下.某同学进行CO2与Na2O2反应的探究实验(本实验所涉及气体体积均在相同状况下测定)。请回答下列问题:
(1)用下图装置制备纯净的CO2.

①丙装置的名称是_______ ,乙装置中盛装的试剂是_______ .
②若CO2中混有HCl,则HCl与Na2O2发生反应的化学方程式为_________ 。
(2)按下图所示装置进行实验(夹持装置略)。
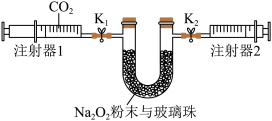
①先组装仪器.然后________ .再用注射器1抽取100 mL纯净的CO2,将其连接在K1处,注射器2的活塞推到底后连接在K2处,具支U形管中装入足量的Na2O2粉末与玻璃珠。
②打开止水夹K1、K2,向右推动注射器1的活塞。可观察到的现象是________ 。
③实验过程中.需缓慢推入CO2,其目的是__________ .为达到相同目的,还可进行的操作是__________________________ 。
(3)实验结束后,当注射器1的活塞推到底时,测得注射器2中气体的体积为65 mL。则CO2的转化率是_______________ .
(1)用下图装置制备纯净的CO2.

①丙装置的名称是
②若CO2中混有HCl,则HCl与Na2O2发生反应的化学方程式为
(2)按下图所示装置进行实验(夹持装置略)。

①先组装仪器.然后
②打开止水夹K1、K2,向右推动注射器1的活塞。可观察到的现象是
③实验过程中.需缓慢推入CO2,其目的是
(3)实验结束后,当注射器1的活塞推到底时,测得注射器2中气体的体积为65 mL。则CO2的转化率是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】某化学兴趣小组探究NO与Na2O2反应制备NaNO2。设计装置如图,请回答下列问题:

(1)组装好仪器后,必须进行的一项操作是______ 。
(2)装置A的产生的气体成分______ 。
(3)反应前,用N2将装置B、C、D中的空气排净,目的是______ ;反应后B中溶液变蓝的原因是______ (用一个化学方程式表示)。
(4)装置D中除生成NaNO2外,还有另一种杂质是______ ;若撤除装置C还能产生杂质是______ ;为了防止以上情况,可以把装置C改为______ (填试剂和仪器名称)。
(5)一定条件下,NH4+可以处理含NO2-的废水,生成无毒的气体。写出有关反应的离子方程式为______ 。
(6)已知装置E中试剂X为酸性高锰酸钾溶液,其作用是______ 。

(1)组装好仪器后,必须进行的一项操作是
(2)装置A的产生的气体成分
(3)反应前,用N2将装置B、C、D中的空气排净,目的是
(4)装置D中除生成NaNO2外,还有另一种杂质是
(5)一定条件下,NH4+可以处理含NO2-的废水,生成无毒的气体。写出有关反应的离子方程式为
(6)已知装置E中试剂X为酸性高锰酸钾溶液,其作用是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】下图是部分短周期元素的单质及其化合物(或其溶液)的转化关系(部分反应条件已省略),其中A、B是单质,A的焰色试验为黄色,C、D是化合物,其他物质已经给出化学式,依据转化关系回答下列问题(出现A、B、C、D请用元素符号表示):
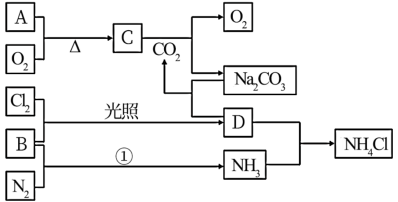
(1)元素A的原子结构示意图___________ ,元素B在周期表中的位置为___________ 。
(2)C物质的名称___________ ,D的电子式___________ 。
(3)离子半径A+___________ O2-(填“<”“>”或“=”),①的基本反应类型___________ 。
(4)D气体与氨气在空气中相遇发生反应,产生的现象是___________ ,所得产物NH4Cl的化学键类型是___________ 。
(5)化合物C可在呼吸面具中作为氧气的来源,用化学方程式描述其原因:___________ 。
(6)A单质可以通过电解熔融ACl制取,化学反应方程式___________ ,写出足量的D溶液与Na2CO3,溶液反应的离子方程式___________ 。

(1)元素A的原子结构示意图
(2)C物质的名称
(3)离子半径A+
(4)D气体与氨气在空气中相遇发生反应,产生的现象是
(5)化合物C可在呼吸面具中作为氧气的来源,用化学方程式描述其原因:
(6)A单质可以通过电解熔融ACl制取,化学反应方程式
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐1】某工厂酸性废液中含有Fe3+、Al3+、Fe2+、SO42-,以该废液为原料制备Fe2O3的工艺流程如下(部分操作和条件略):

已知:①NH4HCO3在热水中会分解。
②常温下,溶液中不同金属离子生成氢氧化物沉淀时的pH见下表:
回答下列问题:
(1)“还原”步骤中反应的离子方程式有Fe+2Fe3+=3Fe2+和_________ 。
(2)试剂X可选用_____ (任写一种,填化学式),“滤渣”的主要成分是______ 。
(3)加入碳酸氢铵后过滤,发现滤液仍然浑浊,可能的原因是______ ,用90°C热水洗涤FeCO3沉淀的目的是_____ 。
(4)若在实验室中灼烧FeCO3应在____ (填仪器名称)中进行,“灼烧氧化”发生的化学方程式为_____ 。
(5)若工业上灼烧氧化174.0吨FeCO3得到117.6吨产品,则该产品中Fe2O3的纯度为_____ (设产品中杂质只有FeO,保留一位小数)。

已知:①NH4HCO3在热水中会分解。
②常温下,溶液中不同金属离子生成氢氧化物沉淀时的pH见下表:
金属离子(0.lmol·L‑1) | Fe3+ | Fe2+ | Al3+ |
开始沉淀时的pH | 2.4 | 7.6 | 3.4 |
完全沉淀时的pH | 3.7 | 9.6 | 4.8 |
回答下列问题:
(1)“还原”步骤中反应的离子方程式有Fe+2Fe3+=3Fe2+和
(2)试剂X可选用
(3)加入碳酸氢铵后过滤,发现滤液仍然浑浊,可能的原因是
(4)若在实验室中灼烧FeCO3应在
(5)若工业上灼烧氧化174.0吨FeCO3得到117.6吨产品,则该产品中Fe2O3的纯度为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】我国科学家最近合成了高熵合金FeCoCrNiMn,其中锰的含量是合成的关键。以软锰矿(主要成分为 ,含少量FeO、
,含少量FeO、 、CoO、
、CoO、 等)和纤维素为原料制备高熵合金的简易工艺流程如下:
等)和纤维素为原料制备高熵合金的简易工艺流程如下:
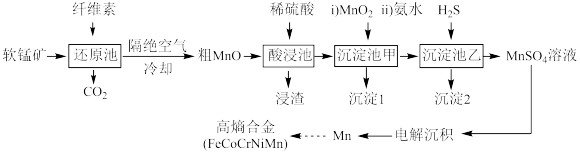
常温下,几种金属离子开始沉淀和完全沉淀的如下表。
请回答下列问题。
(1)沉淀1的主要成分是_______ (填化学式)。
(2)“还原池”中,软锰矿要粉碎且与纤维素混合均匀,其目的是_______ 。
(3)“沉淀池乙”中发生反应的离子方程式为_______ 。
(4)常温下, 的电离常数:
的电离常数: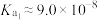 ,
,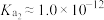 。从两个角度解释
。从两个角度解释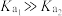 ,①
,①_______ ;②_______ 。
(5)如果用NaOH替代 ,其后果是
,其后果是_______ 。
(6)纤维素、软锰矿质量比与Mn浸出率的关系如图所示。
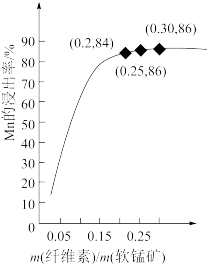
已知该生产工艺中纤维素来自生产加工副产品,价格低廉,则生产中选用的合成m(纤维素)/m(软锰矿)=_______ 。
 ,含少量FeO、
,含少量FeO、 、CoO、
、CoO、 等)和纤维素为原料制备高熵合金的简易工艺流程如下:
等)和纤维素为原料制备高熵合金的简易工艺流程如下:
常温下,几种金属离子开始沉淀和完全沉淀的如下表。
| 金属离子 |  |  |  |  |
| 开始沉淀的pH | 1.9 | 7.0 | 7.4 | 8.1 |
| 完全沉淀的pH | 3.2 | 9.0 | 9.4 | 10.1 |
(1)沉淀1的主要成分是
(2)“还原池”中,软锰矿要粉碎且与纤维素混合均匀,其目的是
(3)“沉淀池乙”中发生反应的离子方程式为
(4)常温下,
 的电离常数:
的电离常数: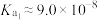 ,
,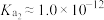 。从两个角度解释
。从两个角度解释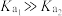 ,①
,①(5)如果用NaOH替代
 ,其后果是
,其后果是(6)纤维素、软锰矿质量比与Mn浸出率的关系如图所示。

已知该生产工艺中纤维素来自生产加工副产品,价格低廉,则生产中选用的合成m(纤维素)/m(软锰矿)=
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】二氯化二硫(S2Cl2)在工业上用于橡胶的硫化。为在实验室合成S2Cl2,某化学研究性学习小组查阅了有关资料,得到如下信息:
①将干燥纯净的氯气在110℃~140℃与硫反应,即可得S2Cl2粗品。
②有关物质的部分性质如下表:
设计实验装置图如下:
(1)仪器A的名称是______________ 。
B中反应的离子方程式为_________________________________ 。
(2) S2Cl2遇水会生成黄色单质、一种能使品红溶液褪色的气体化合物及酸雾,D中的试剂应是________ ,写出该反应的化学方程式__________________ 。
(3)装置H的作用是_______________ ,其中发生反应的化学方程式为 ______________________ 。
(4)S2Cl2粗品中可能混有的杂质是SCl2、Cl2、S,为了提高S2Cl2的纯度,关键的操作是控制好温度和_______ 。
①将干燥纯净的氯气在110℃~140℃与硫反应,即可得S2Cl2粗品。
②有关物质的部分性质如下表:
| 物质 | 熔点/℃ | 沸点/℃ | 化学性质 |
| S | 112.8 | 444.6 | 略 |
| S2Cl2 | -77 | 137 | 与过量氯气发生S2Cl2+Cl2 2SCl2;温度超300℃以上完全分解为硫和氯气 2SCl2;温度超300℃以上完全分解为硫和氯气 |
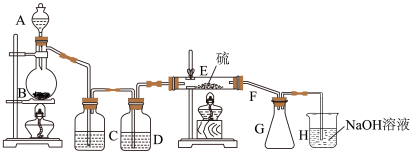
(1)仪器A的名称是
B中反应的离子方程式为
(2) S2Cl2遇水会生成黄色单质、一种能使品红溶液褪色的气体化合物及酸雾,D中的试剂应是
(3)装置H的作用是
(4)S2Cl2粗品中可能混有的杂质是SCl2、Cl2、S,为了提高S2Cl2的纯度,关键的操作是控制好温度和
您最近一年使用:0次



