填空
(1)已知: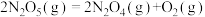
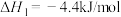

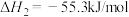
则反应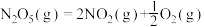

_______ kJ/mol。
(2)已知相关的化学键键能数据如下:
则

_______ kJ/mol。
(3)下图是 和
和 反应生成
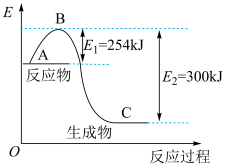
反应生成 过程中能量变化示意图,合成氨反应的热化学方程式为
过程中能量变化示意图,合成氨反应的热化学方程式为_______ 。
(4)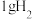 燃烧生成
燃烧生成 放热121 kJ,
放热121 kJ, 蒸发吸热44 kJ,
蒸发吸热44 kJ, 燃烧热的热化学方程式为
燃烧热的热化学方程式为_______ 。
(5)①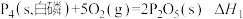
②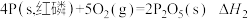
常温时红磷比白磷稳定,则
_______  (填“>”、“=”或“<”)
(填“>”、“=”或“<”)
(1)已知:
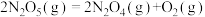
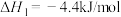

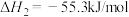
则反应
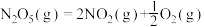

(2)已知相关的化学键键能数据如下:
| 化学键 | C—H | C=O | H—H | 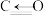 |
键能/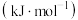 | 413 | 745 | 436 | 1075 |


(3)下图是
 和
和 反应生成
反应生成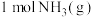 过程中能量变化示意图,合成氨反应的热化学方程式为
过程中能量变化示意图,合成氨反应的热化学方程式为
(4)
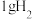 燃烧生成
燃烧生成 放热121 kJ,
放热121 kJ, 蒸发吸热44 kJ,
蒸发吸热44 kJ, 燃烧热的热化学方程式为
燃烧热的热化学方程式为(5)①
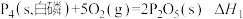
②
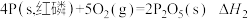
常温时红磷比白磷稳定,则

 (填“>”、“=”或“<”)
(填“>”、“=”或“<”)
更新时间:2024-01-12 17:21:55
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】已知下列热化学方程式:①H2(g)+1/2O2(g)=H2O(l)ΔH=-285kJ·mol-1,②H2(g)+1/2O2(g)=H2O(g)ΔH=-241.8kJ·mol-1,③C(s)+1/2O2(g)=CO(g)ΔH=-110.5kJ·mol-1,④C(s)+O2(g)=CO2(g)ΔH=-393.5kJ·mol-1,回答下列问题:
(1)H2燃烧热的热化学方程式为___________ ;C燃烧热的热化学方程式为___________ 。(选数字)
(2)燃烧1gH2生成液态水,放出的热量为_________________ 。
(3)液态水的稳定性_______ 气态水的稳定性(填“大于”、“小于”、“等于”)。。
(1)H2燃烧热的热化学方程式为
(2)燃烧1gH2生成液态水,放出的热量为
(3)液态水的稳定性
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】氮、磷、砷(As)、锑(Sb)、铋(Bi)、镆(Mc)为元素周期表中原子序数依次增大的同族元素。回答下列问题:
(1)砷在元素周期表中的位置_______ 。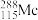 的中子数为
的中子数为_______ 。已知:P(s,白磷)=P(s,黑磷) 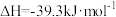 ;P(s,白磷)=P (s,红磷)
;P(s,白磷)=P (s,红磷)  ;由此推知,其中最稳定的磷单质是
;由此推知,其中最稳定的磷单质是_______ 。
(2)氮和磷氢化物性质的比较:热稳定性:NH3_______ PH3(填“>”或“<”)。沸点:N2H4_______ P2H4(填“>”或“<”),判断依据是_______ 。
(3)PH3和NH3与卤化氢的反应相似,产物的结构和性质也相似。下列对PH3与HI反应产物的推断正确的是___ (填序号)。
a.不能与NaOH反应 b.含离子键 c.含共价键
(4)SbCl3能发生较强烈的水解,生成难溶的SbOCl,写出该反应的化学方程式_____ 。
(5)下图是通过热化学循环在较低温度下由水或硫化氢分解制备氢气的反应系统原理。

通过计算,可知系统(I)和系统(II)制氢的热化学方程式分别为_____ 、_____ ,制得等量H2所需能量较少的是____ 。
(1)砷在元素周期表中的位置
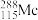 的中子数为
的中子数为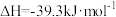 ;P(s,白磷)=P (s,红磷)
;P(s,白磷)=P (s,红磷)  ;由此推知,其中最稳定的磷单质是
;由此推知,其中最稳定的磷单质是(2)氮和磷氢化物性质的比较:热稳定性:NH3
(3)PH3和NH3与卤化氢的反应相似,产物的结构和性质也相似。下列对PH3与HI反应产物的推断正确的是
a.不能与NaOH反应 b.含离子键 c.含共价键
(4)SbCl3能发生较强烈的水解,生成难溶的SbOCl,写出该反应的化学方程式
(5)下图是通过热化学循环在较低温度下由水或硫化氢分解制备氢气的反应系统原理。

通过计算,可知系统(I)和系统(II)制氢的热化学方程式分别为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】汽车尾气中的主要污染物是NOx和CO,它们是现代化城市中的重要大气污染物。
(1)汽车发动机工作时会引发N2和O2反应生成NO,其能量变化如图1所示,则图1中三种分子最稳定的是_______ ,图1中对应反应的热化学方程式为_______ 。 △H。有关化学反应的能量变化过程如图2所示。
△H。有关化学反应的能量变化过程如图2所示。_______ ,该反应的△H=_______ ;
②在反应体系中加入Pt2O+作为该反应的催化剂,则△H_______ (填“增大”“减小”或“不变”)。
(3)利用NH3还原法可将NOx还原为N2进行脱除。已知:
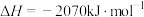 。若有15 g NO被还原,则释放的热量为
。若有15 g NO被还原,则释放的热量为_______ kJ。
(4)“绿水青山就是金山银山”,近年来,绿色发展、生态保护成为中国展示给世界的一张新“名片”。已知25℃和101 kPa下:
①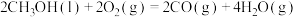 △H =-a kJ/mol
△H =-a kJ/mol
② △H =-b kJ/mol
△H =-b kJ/mol
③H2O(g)=H2O(l) △H =-c kJ/mol
则表示CH3OH(l)燃烧热的热化学方程式为_______ 。
(1)汽车发动机工作时会引发N2和O2反应生成NO,其能量变化如图1所示,则图1中三种分子最稳定的是

 △H。有关化学反应的能量变化过程如图2所示。
△H。有关化学反应的能量变化过程如图2所示。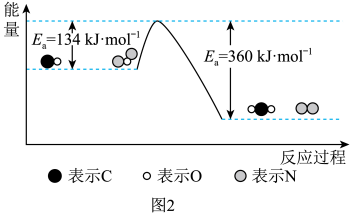
②在反应体系中加入Pt2O+作为该反应的催化剂,则△H
(3)利用NH3还原法可将NOx还原为N2进行脱除。已知:

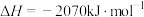 。若有15 g NO被还原,则释放的热量为
。若有15 g NO被还原,则释放的热量为(4)“绿水青山就是金山银山”,近年来,绿色发展、生态保护成为中国展示给世界的一张新“名片”。已知25℃和101 kPa下:
①
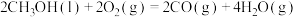 △H =-a kJ/mol
△H =-a kJ/mol②
 △H =-b kJ/mol
△H =-b kJ/mol ③H2O(g)=H2O(l) △H =-c kJ/mol
则表示CH3OH(l)燃烧热的热化学方程式为
您最近一年使用:0次
【推荐1】(1)101kPa下,1g氢气完全燃烧生成液态水放出142.9kJ热量,氢气的燃烧热△H =_______ ;氢气燃烧的热化学方程式为_______ 。
(2)某实验小组用0.50 mol/L NaOH溶液和0.50 mol/L硫酸溶液进行中和热的测定。
①倒入NaOH溶液的正确操作是________ (填选项字母,下同)。
A.沿玻璃棒缓慢倒入
B.一次性迅速倒入
C.分三次少量倒入
②使硫酸与NaOH溶液混合均匀的正确操作是_______ 。
A.用温度计小心搅拌
B.揭开硬纸片用玻璃棒搅拌
C.轻轻地振荡烧杯
D.用套在温度计上的环形玻璃搅拌棒轻轻地搅动
(3)工业合成氨反应为N2(g)+3H2(g)⇌2NH3(g),一定条件下,在2 L密闭容器中进行实验,测得有关数据如下表所示:
则0〜10 s内,用氢气的浓度变化表示的平均反应速率是_______ ,该反应的化学平衡常数是_________ 。根据混合气体各成分的物质性质,你认为工业上将氨气从混合气体中分离出来的措施是_______ ,从而达到反应气体循环利用的目的。
(2)某实验小组用0.50 mol/L NaOH溶液和0.50 mol/L硫酸溶液进行中和热的测定。
①倒入NaOH溶液的正确操作是
A.沿玻璃棒缓慢倒入
B.一次性迅速倒入
C.分三次少量倒入
②使硫酸与NaOH溶液混合均匀的正确操作是
A.用温度计小心搅拌
B.揭开硬纸片用玻璃棒搅拌
C.轻轻地振荡烧杯
D.用套在温度计上的环形玻璃搅拌棒轻轻地搅动
(3)工业合成氨反应为N2(g)+3H2(g)⇌2NH3(g),一定条件下,在2 L密闭容器中进行实验,测得有关数据如下表所示:
| 物质 | N2(g) | H2(g) | NH3(g) |
| 起始(mol) | 2 | 7 | 0 |
| 10 s(mol) | 1.6 | ||
| 平衡时(mol) | 2 |
则0〜10 s内,用氢气的浓度变化表示的平均反应速率是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】根据所学知识填写下列空白。
(1)已知拆开1mol H-H键,1mol N-H键,1mol N≡N键分别需要的能量是436kJ、391kJ、946kJ,则N2与H2反应生成1mol NH3的反应热ΔH =__________________ 。
(2)氢气的燃烧热为286kJ/mol。写出表示氢气燃烧热的热化学方程式____________________________________________ 。
(3)温度下纯水中的c(H+)=1×10-6.5mol/L。若温度不变,滴入稀硫酸使c(H+)=5×10-5mol/L,则由水电离出的c(H+)=__________ mol/L。
(4)已知在第(3)问条件下,盐酸的pH=a,氢氧化钡的pH=b。若酸碱按体积比1:10混合后溶液显中性,则a+b=_________ 。
(5)某二元酸(化学式用H2B表示)在水中的电离方程式是H2B=H++HB-,HB- H++B2-。
H++B2-。
已知0.1 mol/L NaHB溶液的pH=2,则0.1 mol/L H2B溶液中c(H+)小于0.11 mol/L的原因是____________________________________ 。
(1)已知拆开1mol H-H键,1mol N-H键,1mol N≡N键分别需要的能量是436kJ、391kJ、946kJ,则N2与H2反应生成1mol NH3的反应热ΔH =
(2)氢气的燃烧热为286kJ/mol。写出表示氢气燃烧热的热化学方程式
(3)温度下纯水中的c(H+)=1×10-6.5mol/L。若温度不变,滴入稀硫酸使c(H+)=5×10-5mol/L,则由水电离出的c(H+)=
(4)已知在第(3)问条件下,盐酸的pH=a,氢氧化钡的pH=b。若酸碱按体积比1:10混合后溶液显中性,则a+b=
(5)某二元酸(化学式用H2B表示)在水中的电离方程式是H2B=H++HB-,HB-
 H++B2-。
H++B2-。已知0.1 mol/L NaHB溶液的pH=2,则0.1 mol/L H2B溶液中c(H+)小于0.11 mol/L的原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】依据事实,写出下列反应的热化学方程式。
(1)在25℃、101kPa下,1g甲醇燃烧生成CO2和液态水时放热22.68kJ。则表示甲醇燃烧热的热化学方程式为_________________________________________ 。
(2)盖斯定律在生产和科学研究中有很重要的意义。有些反应的反应热虽然无法直接测得,但可通过间接的方法测定。现根据下列3个热化学方程式:
Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g) △H=- A kJ/mol
3Fe2O3(s)+ CO(g)=2Fe3O4(s)+ CO2(g) △H=- B kJ/mol
Fe3O4(s)+CO(g)=3FeO(s)+CO2(g) △H= + C kJ/mol
写出CO气体还原FeO固体得到Fe固体和CO2气体的热化学方程式:__________________
(1)在25℃、101kPa下,1g甲醇燃烧生成CO2和液态水时放热22.68kJ。则表示甲醇燃烧热的热化学方程式为
(2)盖斯定律在生产和科学研究中有很重要的意义。有些反应的反应热虽然无法直接测得,但可通过间接的方法测定。现根据下列3个热化学方程式:
Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g) △H=- A kJ/mol
3Fe2O3(s)+ CO(g)=2Fe3O4(s)+ CO2(g) △H=- B kJ/mol
Fe3O4(s)+CO(g)=3FeO(s)+CO2(g) △H= + C kJ/mol
写出CO气体还原FeO固体得到Fe固体和CO2气体的热化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】运用化学反应原理研究碳的氧化物的性质具有重要意义。
(1)CO2是一种重要的物质,但其过量排放,可能导致全球气温升高。下列措施不能够有效控制CO2所导致的温室效应的是___________ (填序号)
①大力发展低碳产业,提倡低碳生活,依法控制CO2的过量排放
②禁止滥砍滥伐,植树造林,恢复生态
③开发利用各种新型能源代替煤、石油、天然气等化石能源
④提倡使用脱硫煤、无铅汽油等清洁燃料
(2)常温下,碳酸在水中的电离常数Ka1=4.2×10-7,Ka2=5.6×10-11;次氯酸在水中的电离常数Ka=4.7×10-8.写出84消毒液露置在空气中发生反应的离子方程式___________ 。
(3)CO具有还原性,某同学设计图示装置(固定装置及胶管略去)验证CO气体能否与Na2O2反应。

已知:H2C2O4 CO2↑+CO↑+H2O,则实验选择的最简单的装置接口连接顺序为
CO2↑+CO↑+H2O,则实验选择的最简单的装置接口连接顺序为___________ ;若CO能够与Na2O2发生反应,则预测反应产物为___________ 。实验后用球形干燥管中的固体进行验证可选择的试剂是___________ 。
(4)已知C(s)+O2(g)=CO2(g) ΔH=-393.5kJ·mol-1;CO(g)+ O2(g)=CO2(g) ΔH=-283.0kJ·mol-1,写出CO2和C(s)反应的热化学方程式
O2(g)=CO2(g) ΔH=-283.0kJ·mol-1,写出CO2和C(s)反应的热化学方程式___________ 。以CO为燃料制作燃料电池,电池的正极通入O2和CO2,负极通入CO,电解质是熔融碳酸盐,放电时负极反应式为___________ 。若使用该电池电解饱和食盐水制取1molNaClO,则理论上需要氧气的体积为(标准状况下)___________ L。
(1)CO2是一种重要的物质,但其过量排放,可能导致全球气温升高。下列措施不能够有效控制CO2所导致的温室效应的是
①大力发展低碳产业,提倡低碳生活,依法控制CO2的过量排放
②禁止滥砍滥伐,植树造林,恢复生态
③开发利用各种新型能源代替煤、石油、天然气等化石能源
④提倡使用脱硫煤、无铅汽油等清洁燃料
(2)常温下,碳酸在水中的电离常数Ka1=4.2×10-7,Ka2=5.6×10-11;次氯酸在水中的电离常数Ka=4.7×10-8.写出84消毒液露置在空气中发生反应的离子方程式
(3)CO具有还原性,某同学设计图示装置(固定装置及胶管略去)验证CO气体能否与Na2O2反应。

已知:H2C2O4
 CO2↑+CO↑+H2O,则实验选择的最简单的装置接口连接顺序为
CO2↑+CO↑+H2O,则实验选择的最简单的装置接口连接顺序为(4)已知C(s)+O2(g)=CO2(g) ΔH=-393.5kJ·mol-1;CO(g)+
 O2(g)=CO2(g) ΔH=-283.0kJ·mol-1,写出CO2和C(s)反应的热化学方程式
O2(g)=CO2(g) ΔH=-283.0kJ·mol-1,写出CO2和C(s)反应的热化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】能源是国民经济发展的重要基础,我国目前使用的能源主要是化石燃料。
(1)在25℃、101kPa时,2gC2H2(g)完全燃烧生成液态水时放出的热量是100kJ,则C2H2燃烧的热化学方程式是_________________________ 。
(2)已知:C(石墨,s)+O2(g) = CO2(g) △H = —393.5kJ·mol—1,C(金刚石,s)+ O2(g) =CO2(g) △H =—395.0kJ·mol—1,则反应C(石墨,s) = C(金刚石,s) △H =______ kJ·mol—1。由此可知,石墨和金刚石相比更稳定的是 _______ (填“石墨”或“金刚石”)。
(3)已知H2(g)的燃烧热△H 1=—285.0kJ·mol—1,CO(g)的燃烧热△H 2=—283.0kJ·mol—1, CH3OH(l)的燃烧热△H3=—726.0kJ·mol—1。0.2mol由H2 和CO组成的混合气体在完全燃烧时放出56.8kJ的能量,则混合气体中H2 和CO的质量比为_________ 。工业上在催化剂的作用下,可用H2(g)和CO(g)合成CH3OH(l)。请写出由H2(g)和CO(g)合成CH3OH(l)的热化学方程式:_______________________ 。
(4)强酸和强碱的稀溶液的中和热可表示为 H+ (aq)+OH— (aq) = H2O(l) △H =—57.3kJ·mol—1。已知:CH3COOH(aq)+NaOH(aq) = CH3COONa(aq)+H2O(l) △H =—33.1kJ·mol—1。请写出醋酸溶液电离的热化学方程式:_______________ 。
(1)在25℃、101kPa时,2gC2H2(g)完全燃烧生成液态水时放出的热量是100kJ,则C2H2燃烧的热化学方程式是
(2)已知:C(石墨,s)+O2(g) = CO2(g) △H = —393.5kJ·mol—1,C(金刚石,s)+ O2(g) =CO2(g) △H =—395.0kJ·mol—1,则反应C(石墨,s) = C(金刚石,s) △H =
(3)已知H2(g)的燃烧热△H 1=—285.0kJ·mol—1,CO(g)的燃烧热△H 2=—283.0kJ·mol—1, CH3OH(l)的燃烧热△H3=—726.0kJ·mol—1。0.2mol由H2 和CO组成的混合气体在完全燃烧时放出56.8kJ的能量,则混合气体中H2 和CO的质量比为
(4)强酸和强碱的稀溶液的中和热可表示为 H+ (aq)+OH— (aq) = H2O(l) △H =—57.3kJ·mol—1。已知:CH3COOH(aq)+NaOH(aq) = CH3COONa(aq)+H2O(l) △H =—33.1kJ·mol—1。请写出醋酸溶液电离的热化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】作为目前发现的最薄、强度最大、导电导热性能最强的一种新型纳米材料,石墨烯被称为“黑金”,是“新材料之王”,科学家甚至预言石墨烯将“彻底改变21世纪”。极有可能掀起一场席卷全球的颠覆性新技术新产业革命。石墨烯一层层叠起来就是石墨,厚1毫米的石墨大约包含300万层石墨烯。英国曼彻斯特大学的两位科学家安德烈·盖姆(AnD.re Geim)和克斯特亚·诺沃消洛夫(Konstantin Novoselov)从高定向热解石墨中剥离出石墨片,然后将薄片的两面粘在一种特殊的胶带上,撕开胶带,就能把石墨片一分为二。不断地这样操作,于是薄片越来越薄,最后,他们得到了仅由一层碳原子构成的薄片,这就是石墨烯(如图)。

石墨 石墨稀
(1))石墨、金刚石、C60等互称为___________________ ;
(2)已知25℃,101KPa下,石墨、金刚石燃烧的热化学方程式分别为
C(石墨) + O2(g) = CO2(g);△H=-393.51kJ.mol-1
C(金刚石) + O2(g) = CO2(g);△H=-395.41kJ.mol-1
C(金刚石)=C(石墨);△H =________ kJ/mol
(3)石墨和金刚石相比,更稳定的是:________________ ;
(4)请用化学知识解释科学家为什么可以用特殊的胶带将石墨不断地粘撕得到石墨烯:_______________ 。
(5)12g石墨烯中含有___________ NA个如图所示的六元环。

石墨 石墨稀
(1))石墨、金刚石、C60等互称为
(2)已知25℃,101KPa下,石墨、金刚石燃烧的热化学方程式分别为
C(石墨) + O2(g) = CO2(g);△H=-393.51kJ.mol-1
C(金刚石) + O2(g) = CO2(g);△H=-395.41kJ.mol-1
C(金刚石)=C(石墨);△H =
(3)石墨和金刚石相比,更稳定的是:
(4)请用化学知识解释科学家为什么可以用特殊的胶带将石墨不断地粘撕得到石墨烯:
(5)12g石墨烯中含有
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】根据氢气分子的形成过程示意图,回答问题。
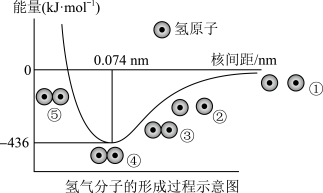
(1)H—H键的键长为______ ,①~⑤中,体系能量由高到低的顺序是________ 。
(2)下列说法中正确的是_________ 。
A 氢气分子中含有一个π键 B 由①到④,电子在核间出现的概率增加
C 由④到⑤,必须消耗外界的能量 D 氢气分子中含有一个极性共价键
(3)已知几种常见化学键的键能如下表所示。
请回答下列问题:
①比较Si—Si键与Si—C键的键能大小可知(填“>”“<”或“=”):X____ 176 kJ·mol−1。
②H2被喻为21世纪人类最理想的燃料,而更有科学家提出硅是“21世纪的能源”“未来的石油”的观点。试计算:每千克H2燃烧(生成水蒸气)放出的热量约为____ ;每摩尔硅完全燃烧放出的热量约为___ 。

(1)H—H键的键长为
(2)下列说法中正确的是
A 氢气分子中含有一个π键 B 由①到④,电子在核间出现的概率增加
C 由④到⑤,必须消耗外界的能量 D 氢气分子中含有一个极性共价键
(3)已知几种常见化学键的键能如下表所示。
| 化学键 | Si—O | H—O | O=O | Si—Si | Si—C |
| 键能/kJ·mol−1 | 460 | 467 | 498 | 176 | X |
①比较Si—Si键与Si—C键的键能大小可知(填“>”“<”或“=”):X
②H2被喻为21世纪人类最理想的燃料,而更有科学家提出硅是“21世纪的能源”“未来的石油”的观点。试计算:每千克H2燃烧(生成水蒸气)放出的热量约为
您最近一年使用:0次
【推荐2】宇宙中所有的一切都是能量的变化,研究化学反应中的能量变化意义重大。
(1)奥运会火炬常用的燃料为丙烷、丁烷等。已知:丙烷的燃烧热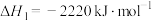 ,正丁烷的燃烧热
,正丁烷的燃烧热 ;异丁烷的燃烧热
;异丁烷的燃烧热 。下列有关说法正确的是
。下列有关说法正确的是_______ (填字母)。
A.奥运火炬燃烧时的能量转化形式主要是由化学能转化为热能、光能
B.燃烧等质量的正丁烷、异丁烷放热更多的是异丁烷
C.正丁烷比异丁烷稳定
(2)根据丙烷的燃烧热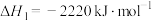 ,
,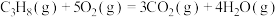

 ,则a
,则a___________ 2220(填“<”或“>”或“=”)。
(3)用 催化还原氮氧化物可以消除氮氧化物的污染。已知:
催化还原氮氧化物可以消除氮氧化物的污染。已知:
①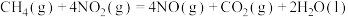
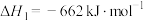
②
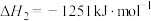
则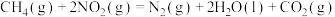

___________ 。
(4)已知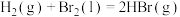
 ,其他相关数据如下表:
,其他相关数据如下表:
则表中a=___________ ;根据键能大小可判断,上述三种物质中最稳定的是___________ 。
(5)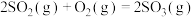 反应过程的能量变化如图所示。
反应过程的能量变化如图所示。

已知:1mol (g)氧化为1mol
(g)氧化为1mol  (g)的
(g)的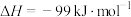 。请回答下列问题:
。请回答下列问题:
①图中
___________ 。
②根据上述计算的焓变值,阐述热化学方程式: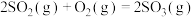
 代表的含义
代表的含义___________ 。
(1)奥运会火炬常用的燃料为丙烷、丁烷等。已知:丙烷的燃烧热
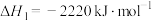 ,正丁烷的燃烧热
,正丁烷的燃烧热 ;异丁烷的燃烧热
;异丁烷的燃烧热 。下列有关说法正确的是
。下列有关说法正确的是A.奥运火炬燃烧时的能量转化形式主要是由化学能转化为热能、光能
B.燃烧等质量的正丁烷、异丁烷放热更多的是异丁烷
C.正丁烷比异丁烷稳定
(2)根据丙烷的燃烧热
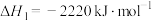 ,
,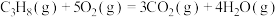

 ,则a
,则a(3)用
 催化还原氮氧化物可以消除氮氧化物的污染。已知:
催化还原氮氧化物可以消除氮氧化物的污染。已知:①
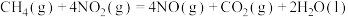
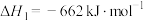
②

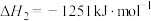
则
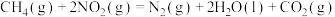

(4)已知
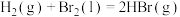
 ,其他相关数据如下表:
,其他相关数据如下表:| 物质 |  (g) (g) |  (l) (l) | HBr(g) |
| 1mol分子中的化学键断裂时需要吸收的能量(kJ) | 436 | 230 | a |
(5)
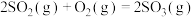 反应过程的能量变化如图所示。
反应过程的能量变化如图所示。
已知:1mol
 (g)氧化为1mol
(g)氧化为1mol  (g)的
(g)的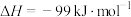 。请回答下列问题:
。请回答下列问题:①图中

②根据上述计算的焓变值,阐述热化学方程式:
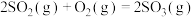
 代表的含义
代表的含义
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】氨广泛用于生产化肥、制冷剂等方面。回答下列问题:
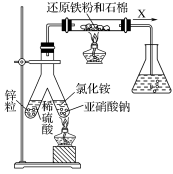
(1)实验室可用上图所示装置合成氨。
①亚硝酸钠与氯化铵反应的离子方程式为NO2-+NH4+ N2↑+2H2O。
N2↑+2H2O。
②锥形瓶中盛有一定量水并滴有几滴酚酞试剂。反应一段时间后,锥形瓶中溶液变红,则气体X的成分为N2、水蒸气、________ 和________ (填化学式)。
(2)最近斯坦福大学研究人员发明了一种SUNCAT的锂循环系统,可持续合成氨,其原理如图所示。
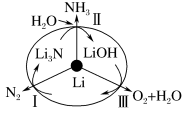
①图中反应Ⅱ属于________ (填“氧化还原反应”或“非氧化还原反应”)。
②反应Ⅲ中能量转化的方式是________ (填“电能转变为化学能”或“化学能转变为电能”)。
(3)液氨可用作制冷剂,液氨汽化时________ (填“释放”或“吸收”)能量;液氨泄漏遇明火会发生爆炸。已知部分化学键的键能数据如下表所示:
则反应4NH3(g)+3O2(g)=2N2(g)+6H2O(g)的反应热ΔH=________ 。

(1)实验室可用上图所示装置合成氨。
①亚硝酸钠与氯化铵反应的离子方程式为NO2-+NH4+
 N2↑+2H2O。
N2↑+2H2O。②锥形瓶中盛有一定量水并滴有几滴酚酞试剂。反应一段时间后,锥形瓶中溶液变红,则气体X的成分为N2、水蒸气、
(2)最近斯坦福大学研究人员发明了一种SUNCAT的锂循环系统,可持续合成氨,其原理如图所示。

①图中反应Ⅱ属于
②反应Ⅲ中能量转化的方式是
(3)液氨可用作制冷剂,液氨汽化时
| 共价键 | N-H | O=O | N≡N | O-H |
| 键能/kJ·mol-1 | 391 | 498 | 946 | 463 |
则反应4NH3(g)+3O2(g)=2N2(g)+6H2O(g)的反应热ΔH=
您最近一年使用:0次



