粗盐提纯实验的科学探究。
I.粗盐中含有较多的杂质,化学兴趣小组同学按照课本“活动与探究”的要求做粗盐提纯实验。
(1)“活动与探究”中,操作步骤有:①计算产率、②过滤、③溶解、④蒸发,正确的操作顺序为___________ (填序号)。
(2)仪器B的名称是___________ ,在实验中三个步骤中都须使用的一种仪器是___________ (填序号)。

Ⅱ.化学兴趣小组同学欲除去固体氯化钠中混有的氯化钙。设计实验方案如下,请参与实验并回答问题。
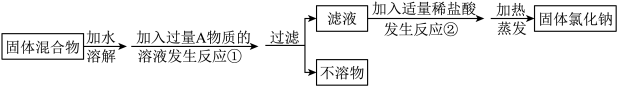
(3)写出A物质的化学式:___________ 。
(4)写出反应②的化学方程式:___________ 。
(5)反应①中加入过量A物质的目的是___________ ;反应②中如果加入盐酸也过量,则对所得到的氯化钠纯度___________ (填“有”或“没有”)影响。
(6)分离后所得氯化钠的质量与分离前原混合物中氯化钠的质量相比较,结果___________ (填增大、不变或减少)。
I.粗盐中含有较多的杂质,化学兴趣小组同学按照课本“活动与探究”的要求做粗盐提纯实验。
(1)“活动与探究”中,操作步骤有:①计算产率、②过滤、③溶解、④蒸发,正确的操作顺序为
(2)仪器B的名称是

Ⅱ.化学兴趣小组同学欲除去固体氯化钠中混有的氯化钙。设计实验方案如下,请参与实验并回答问题。

(3)写出A物质的化学式:
(4)写出反应②的化学方程式:
(5)反应①中加入过量A物质的目的是
(6)分离后所得氯化钠的质量与分离前原混合物中氯化钠的质量相比较,结果
更新时间:2024-01-11 07:57:11
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
【推荐1】Ⅰ.探究 和
和 的性质,实验步骤及记录如下(室温20℃):
的性质,实验步骤及记录如下(室温20℃):
①分别向盛有0.5gNa2CO3固体、0.5gNaHCO3固体的烧杯中加入10mL水(20℃),搅拌,测量温度为T1;
②静置恒温后测量温度为T2=20℃
③继续分别加入10mL密度约为1.1g/mL20%的盐酸(20℃),搅拌,测量温度T3。T3(Na2CO3)=23.7℃,T3(NaHCO3)=20.8℃
溶解度表;
(1)步骤①中Na2CO3、NaHCO3固体能否全部溶解___________ (填“能”或“否”)。
(2)T1(Na2CO3)___________ 20℃,T1(NaHCO3)___________ 20℃(填“>”或“<”)。
(3)甲同学分析③有关数据得出:Na2CO3和NaHCO3与盐酸反应都是放热反应。乙同学认为应该增加一个实验,并补做如下实验:向盛有10mL水(20℃)的烧杯中加入10mL___________ 搅拌,测量温度为22℃。
(4)结合上述探究,下列说法正确的是___________ (填序号)。
a.NaHCO3与盐酸的反应是吸热反应
b.不能用稀盐酸鉴别Na2CO3和NaHCO3固体
c.Na2CO3、NaHCO3固体与稀盐酸反应的能量变化与物质溶解等因素有关
Ⅱ.可用量气法测量Na2CO3和NaHCO3混合物中Na2CO3的质量分数,实验装置如图:

(5)装置中导管甲的作用是:___________ 。
(6)碱式滴定管作为量气管使用。待体系恢复到室温,测量气体体积时应注意:a:___________ ;b:___________ 。
 和
和 的性质,实验步骤及记录如下(室温20℃):
的性质,实验步骤及记录如下(室温20℃):①分别向盛有0.5gNa2CO3固体、0.5gNaHCO3固体的烧杯中加入10mL水(20℃),搅拌,测量温度为T1;
②静置恒温后测量温度为T2=20℃
③继续分别加入10mL密度约为1.1g/mL20%的盐酸(20℃),搅拌,测量温度T3。T3(Na2CO3)=23.7℃,T3(NaHCO3)=20.8℃
溶解度表;
| 温度 | 10℃ | 20℃ | 30℃ | 40℃ |
| 溶解度Na2CO3 | 12.5g | 21.5g | 39.7g | 40.0g |
| 溶解度NaHCO3 | 8.1g | 9.6g | 11.1g | 12.7g |
(2)T1(Na2CO3)
(3)甲同学分析③有关数据得出:Na2CO3和NaHCO3与盐酸反应都是放热反应。乙同学认为应该增加一个实验,并补做如下实验:向盛有10mL水(20℃)的烧杯中加入10mL
(4)结合上述探究,下列说法正确的是
a.NaHCO3与盐酸的反应是吸热反应
b.不能用稀盐酸鉴别Na2CO3和NaHCO3固体
c.Na2CO3、NaHCO3固体与稀盐酸反应的能量变化与物质溶解等因素有关
Ⅱ.可用量气法测量Na2CO3和NaHCO3混合物中Na2CO3的质量分数,实验装置如图:

(5)装置中导管甲的作用是:
(6)碱式滴定管作为量气管使用。待体系恢复到室温,测量气体体积时应注意:a:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】下图中表示A~E五种物质的转化关系。
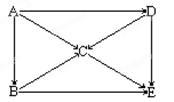
若将它们灼烧,火焰都呈黄色;A能跟水起剧烈反应,D常用作潜水艇里的氧气来源,E是生活中被称为纯碱的盐(物质间的反应均为一步反应)。试推断A~E各物质(写化学式):A______ B______ C______ D______ E______

若将它们灼烧,火焰都呈黄色;A能跟水起剧烈反应,D常用作潜水艇里的氧气来源,E是生活中被称为纯碱的盐(物质间的反应均为一步反应)。试推断A~E各物质(写化学式):A
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】Ⅰ、物质的量是高中化学常用的物理量,请完成以下有关计算:
(1)在标准状况下,6.72LCO的物质的量为___________ ,质量为___________ 。
(2)在标准状况下,23gC2H5OH的物质的量为___________ ,氢原子数目为___________ 。
Ⅱ、Na2CO3和NaHCO3都是重要的化工原料,在生产和生活中有着广泛的应用。
(3)Na2CO3俗称___________ ,往Na2CO3溶液中滴加酚酞,溶液呈___________ 色。
(4)胃液中含有盐酸,胃酸过多的人常有胃疼烧心的感觉,易吐酸水,服用适量的NaHCO3能治疗胃酸过多,请写出其反应的离子方程式:___________ 。
(5)除去Na2CO3粉末中混有的少量NaHCO3的方法是___________ ,化学方程式为___________ 。
(1)在标准状况下,6.72LCO的物质的量为
(2)在标准状况下,23gC2H5OH的物质的量为
Ⅱ、Na2CO3和NaHCO3都是重要的化工原料,在生产和生活中有着广泛的应用。
(3)Na2CO3俗称
(4)胃液中含有盐酸,胃酸过多的人常有胃疼烧心的感觉,易吐酸水,服用适量的NaHCO3能治疗胃酸过多,请写出其反应的离子方程式:
(5)除去Na2CO3粉末中混有的少量NaHCO3的方法是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】掌握仪器的名称、组装及使用方法是中学化学实验的基础,根据下图实验装置回答问题

(1)写出下列仪器的名称:①___________ ,②____________ ,④____________ 。
(2)仪器①~④中,使用时必须检查是否漏水的是_____________ (填序号)。
(3)若利用装置Ⅰ分离酒精和水的混合物,还缺少的仪器__________ ,将仪器补充完整后进行的实验操作的名称为____________ ;②的进水口是___________ (填“f”或“g”)。
(4)现需配制250 mL、0.2 mol·L-1NaCl溶液,装置Ⅱ是某同学转移溶液的示意图,指出图中的错误之处:①_____________________ ;②_______________________ 。

(1)写出下列仪器的名称:①
(2)仪器①~④中,使用时必须检查是否漏水的是
(3)若利用装置Ⅰ分离酒精和水的混合物,还缺少的仪器
(4)现需配制250 mL、0.2 mol·L-1NaCl溶液,装置Ⅱ是某同学转移溶液的示意图,指出图中的错误之处:①
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】海洋植物如海带、海藻中含有丰富的碘元素,碘元素以碘离子的形式存在。实验室里从海藻中提取碘的流程如图:

某化学兴趣小组将上述流程②③设计成如图所示:
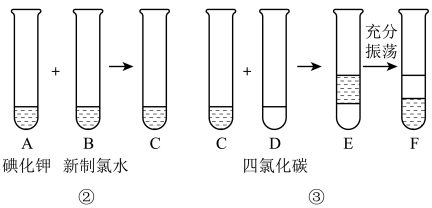
已知②中发生反应的化学方程式为Cl2+2KI=2KCl+I2
回答下列问题:
(1)写出提取过程①③中实验操作名称:①____ ,③____ 。
(2)四氯化碳是____ 色、密度比水____ 的液体。Y中下层液体的颜色为___ 色,上层液体中溶质的主要成分为_____ 。
(3)从碘的四氯化碳溶液中得到碘需进行的操作是______ 。
(4)在操作①过程中,使用到的实验仪器有____ (多选)。
A.试管 B.烧杯 C.玻璃棒 D.蒸发皿 E.漏斗 F.铁架台 G.分液漏斗

某化学兴趣小组将上述流程②③设计成如图所示:

已知②中发生反应的化学方程式为Cl2+2KI=2KCl+I2
回答下列问题:
(1)写出提取过程①③中实验操作名称:①
(2)四氯化碳是
(3)从碘的四氯化碳溶液中得到碘需进行的操作是
(4)在操作①过程中,使用到的实验仪器有
A.试管 B.烧杯 C.玻璃棒 D.蒸发皿 E.漏斗 F.铁架台 G.分液漏斗
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】实验室从含碘废液(除H2O外,含有CCl4、I2、KI等)中回收碘,其实验过程如下:

已知含KI等离子化合物易溶于水,不溶于非极性溶剂(如CCl4)中。
(1)若该含碘废液中CCl4足量(能充分萃取),经充分振荡、静置后,观察到分层现象,上层液体的成分是______________ ,呈_____ 色,下层液体的成分是_______________ ,呈_____ 色。
(2)操作X的名称为____________ 。
(3)流程中的氧化过程发生的反应是Cl2+2KI=2KCl+I2,该反应属于______ 反应(基本类型)。

已知含KI等离子化合物易溶于水,不溶于非极性溶剂(如CCl4)中。
(1)若该含碘废液中CCl4足量(能充分萃取),经充分振荡、静置后,观察到分层现象,上层液体的成分是
(2)操作X的名称为
(3)流程中的氧化过程发生的反应是Cl2+2KI=2KCl+I2,该反应属于
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐1】学习小组在实验室中设计利用铬钒废水(主要成分为Na3VO4、Na2CrO4)制备新型光催化剂钒酸铁和颜料Cr2O3的流程如下。

已知:(NH4)2S2O8具有强氧化性,不稳定易分解。
回答下列问题:
(1)上述实验操作中无需用到的仪器或装置为_______
(2)证明滤渣FeVO4洗涤干净的方法是_______ 。
(3)写出滤液A中CrO 与Na2S2O3溶液反应的离子方程式
与Na2S2O3溶液反应的离子方程式_______ 。
(4)抽滤时常用到下列装置:

①与普通过滤相比,抽滤的优点为。_______
②抽滤完毕后,应先断开_______ 之间的橡皮管。
(5)为检测滤液B中Cr3+的浓度,学习小组取10.00mL浓缩1000倍的滤液B,酸化后加入过量(NH4)2S2O8溶液充分反应后再充分微热,冷却至室温,加入足量淀粉KI溶液,用0.010mol·L-lNa2S2O3溶液滴定(I2+2S2O →S4O
→S4O +2I-)至终点,消耗Na2S2O3溶液30.00mL。
+2I-)至终点,消耗Na2S2O3溶液30.00mL。
①微热目的是_______
②滴定终点现象是_______
③滤液B中c(Cr3+)=_______

已知:(NH4)2S2O8具有强氧化性,不稳定易分解。
回答下列问题:
(1)上述实验操作中无需用到的仪器或装置为_______
A. | B. | C. | D. |
(3)写出滤液A中CrO
 与Na2S2O3溶液反应的离子方程式
与Na2S2O3溶液反应的离子方程式(4)抽滤时常用到下列装置:

①与普通过滤相比,抽滤的优点为。
②抽滤完毕后,应先断开
(5)为检测滤液B中Cr3+的浓度,学习小组取10.00mL浓缩1000倍的滤液B,酸化后加入过量(NH4)2S2O8溶液充分反应后再充分微热,冷却至室温,加入足量淀粉KI溶液,用0.010mol·L-lNa2S2O3溶液滴定(I2+2S2O
 →S4O
→S4O +2I-)至终点,消耗Na2S2O3溶液30.00mL。
+2I-)至终点,消耗Na2S2O3溶液30.00mL。①微热目的是
②滴定终点现象是
③滤液B中c(Cr3+)=
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】某化学小组采用类似制乙酸乙酯的装置(如图),以环己醇制备环己烯

已知:
I.制备粗品
将12.5mL环己醇加入试管A中,再加入1mL浓硫酸,摇匀后放入碎瓷片,缓慢加热至反应完全,在试管C内得到环己烯粗品。
(1)A中碎瓷片的作用是___________ ,导管B除了导气外还具有的作用是___________ 。
(2)给A加热采用水浴加热的优点是______ ,试管C置于冰水浴中的目的是________ 。
II.制备精品
(3)环己烯粗品中含有环己醇和少量酸性杂质等。加入饱和食盐水,振荡、静置、分层,环己烯在___________ 层(填上或下),分液后用__________ (填入编号)洗涤。
a. 溶液 b.稀
溶液 b.稀 c.
c. 溶液
溶液
(4)再将环己烯按图装置蒸馏,冷却水从_________ (“f”或者“g”)口进入。

(5)收集产品时,控制的温度应在_______ 左右,实验制得的环己烯精品质量低于理论产量,可能的原因是________ 。
a.蒸馏时从70℃开始收集产品
b.环己醇实际用量多了
c.制备粗品时环己醇随产品一起蒸出
(6)以下区分环己烯精品和粗品的方法,合理的是___________ 。
a.用酸性高锰酸钾溶液 b.用金属钠 c.测定沸点

已知:

密度( ) ) | 熔点(℃) | 沸点(℃) | 溶解性 | |
| 环己醇 | 0.96 | 25 | 161 | 能溶于水 |
| 环己烯 | 0.81 | -103 | 83 | 难溶于水 |
将12.5mL环己醇加入试管A中,再加入1mL浓硫酸,摇匀后放入碎瓷片,缓慢加热至反应完全,在试管C内得到环己烯粗品。
(1)A中碎瓷片的作用是
(2)给A加热采用水浴加热的优点是
II.制备精品
(3)环己烯粗品中含有环己醇和少量酸性杂质等。加入饱和食盐水,振荡、静置、分层,环己烯在
a.
 溶液 b.稀
溶液 b.稀 c.
c. 溶液
溶液(4)再将环己烯按图装置蒸馏,冷却水从

(5)收集产品时,控制的温度应在
a.蒸馏时从70℃开始收集产品
b.环己醇实际用量多了
c.制备粗品时环己醇随产品一起蒸出
(6)以下区分环己烯精品和粗品的方法,合理的是
a.用酸性高锰酸钾溶液 b.用金属钠 c.测定沸点
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】高纯硫酸锰作为合成镍钴锰三元正极材料的原料,工业上可由天然二氧化锰粉与硫化锰矿(还含Fe、Al、Mg、Zn、Ni、Si等元素)制备,工艺如下图所示。回答下列问题:

相关金属离子[c0(Mn+)=0.1 mol·L-1]形成氢氧化物沉淀的pH范围如下:
提示:SiO2或不溶性硅酸盐均不溶于H2SO4溶液。
(1)“滤渣1”含有S和________ 。
(2)“氧化”中添加适量的MnO2的作用是_________ 。
(3)“调pH”除铁和铝,溶液的pH范围应调节为_______ ~6之间。
(4)“除杂1”的目的是除去Zn2+和Ni2+,“滤渣3”的主要成分是________ 。
(5)“除杂2”的目的是生成MgF2沉淀除去Mg2+。若溶液酸度过高,Mg2+沉淀不完全,原因是______ 。
(6)写出“沉锰”的离子方程式:_________ 。
(7)层状镍钴锰三元材料可作为锂离子电池正极材料,其化学式为LiNixCoyMnzO2,其中Ni、Co、Mn的化合价分别为+2、+3、+4。当x=y= 时,z=
时,z=________ 。

相关金属离子[c0(Mn+)=0.1 mol·L-1]形成氢氧化物沉淀的pH范围如下:
| 金属离子 | Mn2+ | Fe2+ | Fe3+ | Al3+ | Mg2+ | Zn2+ | Ni2+ |
| 开始沉淀的pH | 8.1 | 6.3 | 1.5 | 3.4 | 8.9 | 6.2 | 6.9 |
| 沉淀完全的pH | 10.1 | 8.3 | 2.8 | 4.7 | 10.9 | 8.2 | 8.9 |
(1)“滤渣1”含有S和
(2)“氧化”中添加适量的MnO2的作用是
(3)“调pH”除铁和铝,溶液的pH范围应调节为
(4)“除杂1”的目的是除去Zn2+和Ni2+,“滤渣3”的主要成分是
(5)“除杂2”的目的是生成MgF2沉淀除去Mg2+。若溶液酸度过高,Mg2+沉淀不完全,原因是
(6)写出“沉锰”的离子方程式:
(7)层状镍钴锰三元材料可作为锂离子电池正极材料,其化学式为LiNixCoyMnzO2,其中Ni、Co、Mn的化合价分别为+2、+3、+4。当x=y=
 时,z=
时,z=
您最近一年使用:0次



