已知: 是有刺激性气味、黄绿色、有毒、易液化、溶于水的气体。实验室制取氯气的离子方程式为:
是有刺激性气味、黄绿色、有毒、易液化、溶于水的气体。实验室制取氯气的离子方程式为: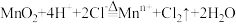 ,回答下列问题:
,回答下列问题:
(1)从方程式两边电荷守恒角度判断,方程式中
___________ 。
(2)该反应的还原剂是___________ ,实验室检验该离子的试剂是硝酸酸化的硝酸银溶液。
(3)该反应的还原产物是___________ 。
(4)若该反应消耗 ,产生标准状况下的
,产生标准状况下的
___________ L。
(5)实验室制取 时要用
时要用 溶液吸收多余的氯气。反应的化学方程式为:
溶液吸收多余的氯气。反应的化学方程式为: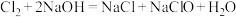 (已知:电离方程式
(已知:电离方程式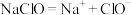 ),该反应的离子方程式为
),该反应的离子方程式为___________ 。
 是有刺激性气味、黄绿色、有毒、易液化、溶于水的气体。实验室制取氯气的离子方程式为:
是有刺激性气味、黄绿色、有毒、易液化、溶于水的气体。实验室制取氯气的离子方程式为: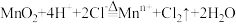 ,回答下列问题:
,回答下列问题:(1)从方程式两边电荷守恒角度判断,方程式中

(2)该反应的还原剂是
(3)该反应的还原产物是
(4)若该反应消耗
 ,产生标准状况下的
,产生标准状况下的
(5)实验室制取
 时要用
时要用 溶液吸收多余的氯气。反应的化学方程式为:
溶液吸收多余的氯气。反应的化学方程式为: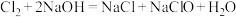 (已知:电离方程式
(已知:电离方程式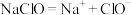 ),该反应的离子方程式为
),该反应的离子方程式为
23-24高一上·北京怀柔·期中 查看更多[2]
更新时间:2024-01-04 15:35:04
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】Ⅰ.用一种试剂除去下列各物质中的杂质(括号内为杂质),并写出离子方程式。
(1) 溶液
溶液 ,试剂:
,试剂:___________ ,离子方程式:___________ 。
(2) 溶液(BaCl2),试剂:
溶液(BaCl2),试剂:___________ ,离子方程式:___________ 。
Ⅱ.造纸术是我国古代四大发明之一,在《天工开物》中记载了比较完善的造纸方法,造纸工业亦是国民经济十大支柱制造业之一,但造纸过程会消耗大量的资源并产生大量的污水,因此资源的回收利用以及污水的处理非常重要。
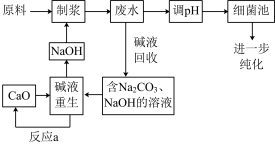
某造纸厂制浆及废水处理流程如下:
其中“制浆”是将木材、竹子等原料与烧碱共煮,制得纸浆,烧碱在制浆过程中转化为 。制浆废水中大部分碱性物质被回收利用,剩余的有机物在细菌池被微生物分解除去。
。制浆废水中大部分碱性物质被回收利用,剩余的有机物在细菌池被微生物分解除去。
(3)“碱液重生”过程分为以下两步反应,请补充反应ⅱ的离子方程式:
ⅰ.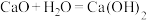 (石灰乳)
(石灰乳)
ⅱ.___________ 。
(4)反应a的化学方程式为___________ 。
(5)为防止细菌失活,需要先调 至中性,以下物质中,可以实现该目的的有___________
至中性,以下物质中,可以实现该目的的有___________
(6)上述过程中,循环使用的物质有___________ (写化学式)。
(1)
 溶液
溶液 ,试剂:
,试剂:(2)
 溶液(BaCl2),试剂:
溶液(BaCl2),试剂:Ⅱ.造纸术是我国古代四大发明之一,在《天工开物》中记载了比较完善的造纸方法,造纸工业亦是国民经济十大支柱制造业之一,但造纸过程会消耗大量的资源并产生大量的污水,因此资源的回收利用以及污水的处理非常重要。
某造纸厂制浆及废水处理流程如下:
其中“制浆”是将木材、竹子等原料与烧碱共煮,制得纸浆,烧碱在制浆过程中转化为
 。制浆废水中大部分碱性物质被回收利用,剩余的有机物在细菌池被微生物分解除去。
。制浆废水中大部分碱性物质被回收利用,剩余的有机物在细菌池被微生物分解除去。
(3)“碱液重生”过程分为以下两步反应,请补充反应ⅱ的离子方程式:
ⅰ.
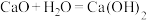 (石灰乳)
(石灰乳) ⅱ.
(4)反应a的化学方程式为
(5)为防止细菌失活,需要先调
 至中性,以下物质中,可以实现该目的的有___________
至中性,以下物质中,可以实现该目的的有___________A. | B. | C. | D. |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】回答下列问题:
(1)在一个小试管里放入一小粒碘晶体,加入约5 mL蒸馏水,振荡;然后在此碘水溶液中加入约1 mL四氯化碳,振荡试管;再向试管里加入1 mL浓碘化钾水溶液,振荡试管,此时现象为___________ ,原因是___________ (写出相应的离子方程式)。
(2)向盛有少量氯化钠溶液的试管中滴入少量硝酸银溶液,生成白色的氯化银沉淀,继续向试管里加入氨水,沉淀溶解了,试写出沉淀溶解的化学方程式_____
(3)向盛有氯化铁溶液的试管中滴加1滴KSCN溶液,写出相应的离子方程式_____
(4)向硫酸铜水溶液中逐滴加入足量氨水,发现先生成蓝色沉淀,然后沉淀溶解,写出沉淀溶解的离子方程式为___________ 。向硫酸铜溶液中加入过量的NaOH溶液可生成 ,不考虑空间构型,
,不考虑空间构型, 的结构可用示意图表示为
的结构可用示意图表示为_____
(1)在一个小试管里放入一小粒碘晶体,加入约5 mL蒸馏水,振荡;然后在此碘水溶液中加入约1 mL四氯化碳,振荡试管;再向试管里加入1 mL浓碘化钾水溶液,振荡试管,此时现象为
(2)向盛有少量氯化钠溶液的试管中滴入少量硝酸银溶液,生成白色的氯化银沉淀,继续向试管里加入氨水,沉淀溶解了,试写出沉淀溶解的化学方程式
(3)向盛有氯化铁溶液的试管中滴加1滴KSCN溶液,写出相应的离子方程式
(4)向硫酸铜水溶液中逐滴加入足量氨水,发现先生成蓝色沉淀,然后沉淀溶解,写出沉淀溶解的离子方程式为
 ,不考虑空间构型,
,不考虑空间构型, 的结构可用示意图表示为
的结构可用示意图表示为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】学习常见物质时,会从“价”和“类”两个方面进行学习。如图表示铁元素的常见化合价与含铁物质类别的关系。
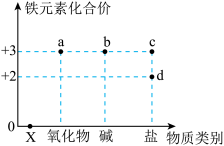
(1)X的物质类别是_______ 。
(2)铁和硫单质反应生成的含铁化合物属于如图中的_______ (填序号)。若不引入杂质,将FeCl3溶液转化FeCl2溶液的离子方程式为:_______ 。
(3)某同学弄清了氨的喷泉实验原理后,探究X与浓硝酸反应生成的气体能否用来做喷泉实验:标准状况下,用一充满该气体的烧瓶来做喷泉实验,实验结果水只能充到烧瓶体积的_______ 处,所得溶液的浓度为_______ mol·L-1。
(4)某同学欲用物质a制取物质b,设计了如图实验步骤:

物质a与稀盐酸反应的离子方程式为_______ 。如果向盛有溶液甲的烧杯中滴加NaOH溶液至过量,下面图象能正确表示烧杯中溶液质量变化的是_______ (填序号)。

(5)c点对应的阳离子用_______ 试剂检验(写出化学名称);现象是_______ ;写出对应的离子方程式_______ 。

(1)X的物质类别是
(2)铁和硫单质反应生成的含铁化合物属于如图中的
(3)某同学弄清了氨的喷泉实验原理后,探究X与浓硝酸反应生成的气体能否用来做喷泉实验:标准状况下,用一充满该气体的烧瓶来做喷泉实验,实验结果水只能充到烧瓶体积的
(4)某同学欲用物质a制取物质b,设计了如图实验步骤:

物质a与稀盐酸反应的离子方程式为

(5)c点对应的阳离子用
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】“价类”二维图是学习元素及其化合物的重要工具,如图所示是铁及其化合物的“价类”二维图。
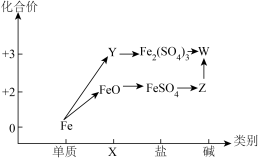
(1)X、Y分别代表_______ 、_______ ;Z在空气中转化为W的化学方程式为_______ 。
(2)某小组研究 性质,预测
性质,预测 能与
能与_______ 发生氧化还原反应(填序号)。
①NaOH溶液②氯水③稀盐酸④酸性 溶液⑤镁⑥碳酸钠
溶液⑤镁⑥碳酸钠
(3)铁盐溶液可用于金属刻蚀。如用 溶液刻蚀铜制电路板,
溶液刻蚀铜制电路板, 被
被_______ (填“还原”或“氧化”)为 ,该反应的离子方程式为
,该反应的离子方程式为_______ 。
(4)为检验食品中的铁元素,可将菠菜剪碎、研磨、溶解、_______ ,然后将少许滤液加入试管中,加入少量稀硝酸(稀硝酸具有氧化性),再滴加几滴KSCN溶液,振荡,若观察到_______ 现象,说明试验样品中含有铁元素。
(5)高铁酸钠是一种能杀菌、脱色、除臭的新型高效水处理剂。工业上可用 氧化
氧化 的方法制备
的方法制备 ,其原理为
,其原理为 ,用双线桥法表示该反应的电子转移方向和数目
,用双线桥法表示该反应的电子转移方向和数目_______ 。

(1)X、Y分别代表
(2)某小组研究
 性质,预测
性质,预测 能与
能与①NaOH溶液②氯水③稀盐酸④酸性
 溶液⑤镁⑥碳酸钠
溶液⑤镁⑥碳酸钠(3)铁盐溶液可用于金属刻蚀。如用
 溶液刻蚀铜制电路板,
溶液刻蚀铜制电路板, 被
被 ,该反应的离子方程式为
,该反应的离子方程式为(4)为检验食品中的铁元素,可将菠菜剪碎、研磨、溶解、
(5)高铁酸钠是一种能杀菌、脱色、除臭的新型高效水处理剂。工业上可用
 氧化
氧化 的方法制备
的方法制备 ,其原理为
,其原理为 ,用双线桥法表示该反应的电子转移方向和数目
,用双线桥法表示该反应的电子转移方向和数目
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】(1)(NH4)2SO4在强热条件下,可分解生成NH3、SO2、N2、H2O.
反应中氧化产物和还原产物的物质的量之比为_________________ 。
(2)将K2S跟HNO3反应,生成NO、S、KNO3、H2O,反应的化学方程式为__________________________________________ ;氧化产物是________ ; 若生成2molNO,反应中电子转移的总物质的量为________ mol。
反应中氧化产物和还原产物的物质的量之比为
(2)将K2S跟HNO3反应,生成NO、S、KNO3、H2O,反应的化学方程式为
您最近一年使用:0次
【推荐3】氧化还原反应是中学化学的重要内容。回答下列问题:
(1)野外,一般用铝热反应来焊接铁轨,其化学方程式为 ,该反应中氧化剂为
,该反应中氧化剂为_________ ;每生成1个 ,转移
,转移_________ 个电子。
(2)用双线桥法表示电子转移的方向和数目:_________ 。
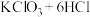 (浓)
(浓)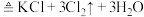
(3)高铁酸钠是一种新型的绿色消毒剂,主要用于饮用水处理,其中一种制备方法如下,配平该离子方程式:_________ 。
_________ _________
_________ _________
_________ _________
_________ _________
_________ _________
_________
(4)按如图所示操作,充分反应后。
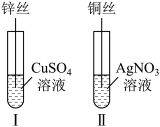
①试管Ⅰ中发生反应的化学方程式为_________ ;试管Ⅱ中铜丝上观察到的现象是_________ 。
(2)结合Ⅰ、Ⅱ实验现象可知 、
、 、
、 的氧化性由强到弱的顺序为
的氧化性由强到弱的顺序为_________ 。
(1)野外,一般用铝热反应来焊接铁轨,其化学方程式为
 ,该反应中氧化剂为
,该反应中氧化剂为 ,转移
,转移(2)用双线桥法表示电子转移的方向和数目:
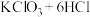 (浓)
(浓)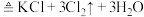
(3)高铁酸钠是一种新型的绿色消毒剂,主要用于饮用水处理,其中一种制备方法如下,配平该离子方程式:
_________
 _________
_________ _________
_________ _________
_________ _________
_________ _________
_________
(4)按如图所示操作,充分反应后。

①试管Ⅰ中发生反应的化学方程式为
(2)结合Ⅰ、Ⅱ实验现象可知
 、
、 、
、 的氧化性由强到弱的顺序为
的氧化性由强到弱的顺序为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】写出下来化学方程式:
(1)铝和氢氧化钠溶液反应______
(2)铁在高温下与水反应______
(3) 制取氢氧化铝______
(4) 实验室氨气的制备______
(5)实验室制备氯气______
(1)铝和氢氧化钠溶液反应
(2)铁在高温下与水反应
(3) 制取氢氧化铝
(4) 实验室氨气的制备
(5)实验室制备氯气
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】如图为氯及其化合物的“价—类”二维图。
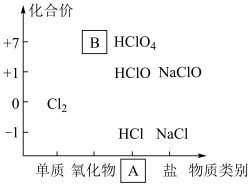
(1)缺失的类别 为
为___________ 、物质 为
为___________ (填化学式)。
(2) 在
在 中安静燃烧
中安静燃烧_______________________________ (化学方程式)。
(3) 溶于水
溶于水____________________________ (离子方程式)。
(4)工业制备漂白粉__________________________________ (化学方程式)。

(1)缺失的类别
 为
为 为
为(2)
 在
在 中安静燃烧
中安静燃烧(3)
 溶于水
溶于水(4)工业制备漂白粉
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】已知 Ca(OH)2 与 Cl2 反应的氧化产物与温度有关,在一定量的石灰乳中通入足量的氯气,二者恰好完全反应。生成 Cl-、ClO-、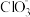 三种含氯元素的离子,其中 ClO- 、
三种含氯元素的离子,其中 ClO- 、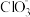 两种离子的物质的量(n)与反应时间
两种离子的物质的量(n)与反应时间
(t)的曲线如图所示。
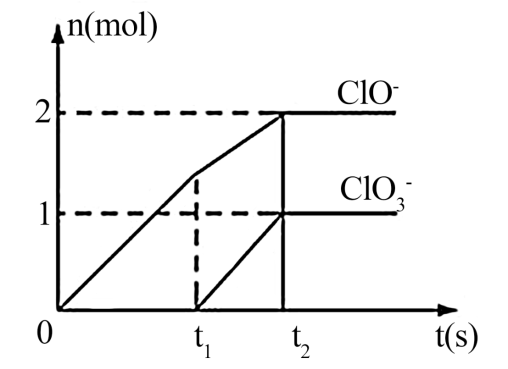
(1)t1 时,开始有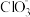 生成的原因是
生成的原因是_____ 。
(2)t2 时,Ca(OH)2 与 Cl2 发生反应的总的化学方程式为___________ 。
(3)该石灰乳中含有 Ca(OH)2 的物质的量是________ mol。
(4)若反应物的量不变,在某温度下恰好完全反应时,氧化产物比值为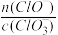 a ,则 n(Cl-)=
a ,则 n(Cl-)=_____ mol
(用含 a 的代数式来表示)。
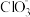 三种含氯元素的离子,其中 ClO- 、
三种含氯元素的离子,其中 ClO- 、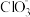 两种离子的物质的量(n)与反应时间
两种离子的物质的量(n)与反应时间(t)的曲线如图所示。

(1)t1 时,开始有
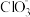 生成的原因是
生成的原因是(2)t2 时,Ca(OH)2 与 Cl2 发生反应的总的化学方程式为
(3)该石灰乳中含有 Ca(OH)2 的物质的量是
(4)若反应物的量不变,在某温度下恰好完全反应时,氧化产物比值为
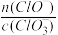 a ,则 n(Cl-)=
a ,则 n(Cl-)=(用含 a 的代数式来表示)。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】将含有少量 的氯气通入盛有潮湿消石灰的U形管中,可制得少量漂白粉(该反应为放热反应),据此回答下列问题:
的氯气通入盛有潮湿消石灰的U形管中,可制得少量漂白粉(该反应为放热反应),据此回答下列问题:
(1)写出生成漂白粉的化学方程式是_______ 。
(2)此实验所得 产率太低。经分析并查阅资料发现主要原因是在U形管中存在两个副反应。
产率太低。经分析并查阅资料发现主要原因是在U形管中存在两个副反应。
①温度较高时氯气与消石灰反应生成了 ,为避免此副反应的发生,可采取的措施是
,为避免此副反应的发生,可采取的措施是_______ ;如图为反应后溶液中 、
、 离子的物质的量(m)与反应时间(t)的关系曲线(不考虑氯气和水的反应)。
离子的物质的量(m)与反应时间(t)的关系曲线(不考虑氯气和水的反应)。

a.图中曲线Ⅰ表示_______ 离子的物质的量随反应时间变化的关系。
b.所用石灰乳中含有 的物质的量为
的物质的量为_______  。
。
c.另取一份含有等物质的量 的石灰乳,以较大的速率通入足量氯气,反应后测得产物中
的石灰乳,以较大的速率通入足量氯气,反应后测得产物中 的物质的量为
的物质的量为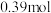 ,则产物中
,则产物中
_______ 。
②试判断另一个副反应是_______ (写出此反应的化学方程式);为避免此副反应发生,可以采取的改进措施是_______ 。
 的氯气通入盛有潮湿消石灰的U形管中,可制得少量漂白粉(该反应为放热反应),据此回答下列问题:
的氯气通入盛有潮湿消石灰的U形管中,可制得少量漂白粉(该反应为放热反应),据此回答下列问题:(1)写出生成漂白粉的化学方程式是
(2)此实验所得
 产率太低。经分析并查阅资料发现主要原因是在U形管中存在两个副反应。
产率太低。经分析并查阅资料发现主要原因是在U形管中存在两个副反应。①温度较高时氯气与消石灰反应生成了
 ,为避免此副反应的发生,可采取的措施是
,为避免此副反应的发生,可采取的措施是 、
、 离子的物质的量(m)与反应时间(t)的关系曲线(不考虑氯气和水的反应)。
离子的物质的量(m)与反应时间(t)的关系曲线(不考虑氯气和水的反应)。
a.图中曲线Ⅰ表示
b.所用石灰乳中含有
 的物质的量为
的物质的量为 。
。c.另取一份含有等物质的量
 的石灰乳,以较大的速率通入足量氯气,反应后测得产物中
的石灰乳,以较大的速率通入足量氯气,反应后测得产物中 的物质的量为
的物质的量为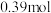 ,则产物中
,则产物中
②试判断另一个副反应是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】(1)某化学反应可用下式表示:A+B=C+D+H2O,若A、D均可用于消毒,且C是家家户户的厨房必备的物质之一,写出该反应的离子方程式:_________
(2)硝酸铅的稀溶液中,滴入几滴稀 生成白色
生成白色 沉淀,再滴入数滴饱和NaAc溶液,微热,并不断搅动,沉淀慢慢溶解,以上发生的都是复分解反应,写出反应过程的离子方程式①
沉淀,再滴入数滴饱和NaAc溶液,微热,并不断搅动,沉淀慢慢溶解,以上发生的都是复分解反应,写出反应过程的离子方程式①_______ ②________
(3)边微热边向铵明矾[NH4Al(SO4)2`12H2O]溶液中逐滴加入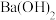 溶液至中性(提示:NH
溶液至中性(提示:NH 、Al3+恰好完全反应)
、Al3+恰好完全反应)
①此时发生反应的离子方程式为_________
②向以上所得中性溶液中继续滴加稀硫酸,相关反应的离子方程式是:____
(2)硝酸铅的稀溶液中,滴入几滴稀
 生成白色
生成白色 沉淀,再滴入数滴饱和NaAc溶液,微热,并不断搅动,沉淀慢慢溶解,以上发生的都是复分解反应,写出反应过程的离子方程式①
沉淀,再滴入数滴饱和NaAc溶液,微热,并不断搅动,沉淀慢慢溶解,以上发生的都是复分解反应,写出反应过程的离子方程式①(3)边微热边向铵明矾[NH4Al(SO4)2`12H2O]溶液中逐滴加入
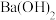 溶液至中性(提示:NH
溶液至中性(提示:NH 、Al3+恰好完全反应)
、Al3+恰好完全反应)①此时发生反应的离子方程式为
②向以上所得中性溶液中继续滴加稀硫酸,相关反应的离子方程式是:
您最近一年使用:0次

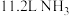 所含氢原子的物质的量为
所含氢原子的物质的量为 中含有
中含有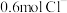 ,则该氯化物的摩尔质量为
,则该氯化物的摩尔质量为 ;
; 溶液中,
溶液中, 的物质的量浓度为
的物质的量浓度为 ;
;

