如图为氯及其化合物的“价—类”二维图。
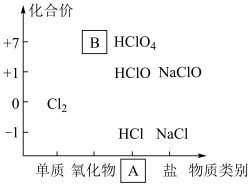
(1)缺失的类别 为
为___________ 、物质 为
为___________ (填化学式)。
(2) 在
在 中安静燃烧
中安静燃烧_______________________________ (化学方程式)。
(3) 溶于水
溶于水____________________________ (离子方程式)。
(4)工业制备漂白粉__________________________________ (化学方程式)。

(1)缺失的类别
 为
为 为
为(2)
 在
在 中安静燃烧
中安静燃烧(3)
 溶于水
溶于水(4)工业制备漂白粉
更新时间:2023-12-26 09:05:39
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】学习化学应该明确“从生活中来,到生活中去”道理。在生产生活中,我们会遇到各种各样的化学物质和化学反应。请按要求填空
(1)计算机芯片的主要成分是___ (填名称),节日的烟花是利用___ 。
(2)请你写出工业上用氯气和消石灰反应制取漂白粉的化学反应方程式:___ 。
(3)玉石的主要成分基本都属于硅酸盐,如某种翡翠的主要成分为NaAlSi2O6,将其表示为氧化物形式可写为___ 。
(4)沾有水的铁质器皿在加热时会发黑,该反应的化学方程式是___ 。
(5)补铁剂中的Fe2+易被氧化成Fe3+,服用时医生常建议同时服用维生素C,这是利用维生素C的___ 。
(1)计算机芯片的主要成分是
(2)请你写出工业上用氯气和消石灰反应制取漂白粉的化学反应方程式:
(3)玉石的主要成分基本都属于硅酸盐,如某种翡翠的主要成分为NaAlSi2O6,将其表示为氧化物形式可写为
(4)沾有水的铁质器皿在加热时会发黑,该反应的化学方程式是
(5)补铁剂中的Fe2+易被氧化成Fe3+,服用时医生常建议同时服用维生素C,这是利用维生素C的
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】(1)①写出漂白粉的有效成分的化学式_____ ;
②用系统命名法给有机物CH3CH(CH3)2命名________ 。
(2)①写出碳与浓硫酸反应的化学方程式______ ;
②写出乙醇与金属钠反应的方程式_______ 。
(3)H2O2和Fe3+都具有氧化性,氧化性强弱关系为H2O2____ Fe3+(填“>”“<”或“=”),用有关的离子反应方程式证明以上结论____ 。
②用系统命名法给有机物CH3CH(CH3)2命名
(2)①写出碳与浓硫酸反应的化学方程式
②写出乙醇与金属钠反应的方程式
(3)H2O2和Fe3+都具有氧化性,氧化性强弱关系为H2O2
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】(1)国际化学年的中国宣传口号是“化学——我们的生活,我们的未来”.学习化学应该明白“从生活中来,到生活中去”道理.请填空:
①若金属钠等活泼金属着火时,应该用______ 来灭火.
②经火焰灼烧,焰色反应为浅紫色(透过蓝色钴玻璃)的元素是_______ .
③胃舒平(含有氢氧化铝)可治疗胃酸过多,其反应的离子反应方程式为:_______________ .
④工业上将氯气通入石灰乳[Ca(OH)2]制取漂白粉,化学反应方程为__________________ 漂白粉的有效成分是(填化学式)_______________ 。漂白粉溶于水后,受空气中的CO2作用,即可漂白衣物,其原理用化学反应方程式表示为_______________________
(2)现有分别含有下列离子的溶液①Cu2+ ②Mg2+ ③Fe2+ ④Al3 + ⑤Fe3+,其中既能被氧化又能被还原的是_________ ;加入过量NaOH溶液,最后不生成沉淀的是_______ ;加入铁粉后溶液质量增加的是_______ ;加入铁粉后溶液质量减少的是_________ ;具有净水作用的是______________ ;露置在空气中溶液会变色的是_________ 。(均填序号 )
①若金属钠等活泼金属着火时,应该用
②经火焰灼烧,焰色反应为浅紫色(透过蓝色钴玻璃)的元素是
③胃舒平(含有氢氧化铝)可治疗胃酸过多,其反应的离子反应方程式为:
④工业上将氯气通入石灰乳[Ca(OH)2]制取漂白粉,化学反应方程为
(2)现有分别含有下列离子的溶液①Cu2+ ②Mg2+ ③Fe2+ ④Al3 + ⑤Fe3+,其中既能被氧化又能被还原的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】氯及其化合物在生产、生活中有着广泛的用途。
(1)①写出实验室中制取氯气的离子方程式:_______ 。
②已知KMnO4与浓盐酸反应的化学方程式:2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O,该反应也可以用来制取氯气,15.8gKMnO4能氧化_______ molHCl。
③实验室还可以利用反应KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O制取氯气。若制取标准状况下6.72L氯气,反应过程中转移电子的数目为_______ ;用双线桥表示该反应电子转移的方向和数目:_______ 。
(2)①浸泡衣物时加入“84”消毒液,在空气中放置一段时间漂白效果更好,原因为:_______ (用离子方程式表示,已知酸性:H2CO3>HClO> )。
)。
②某温度下,将氯气通入NaOH溶液中,反应得到NaCl、NaClO和NaClO3的混合溶液,经测定ClO-与 ;的物质的量之比为1:1,写出该反应的化学方程式:
;的物质的量之比为1:1,写出该反应的化学方程式:_______ 。
(3)世界卫生组织将ClO2定为A级高效安全灭菌消毒剂,它在食品保鲜、消毒等方面有广泛应用。消毒效率是用单位质量的消毒剂得电子数来表示的,ClO2作消毒剂时和氯气一样,还原产物均为Cl-,ClO2的消毒效率是氯气的_______ 倍(保留两位小数)。
(1)①写出实验室中制取氯气的离子方程式:
②已知KMnO4与浓盐酸反应的化学方程式:2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O,该反应也可以用来制取氯气,15.8gKMnO4能氧化
③实验室还可以利用反应KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O制取氯气。若制取标准状况下6.72L氯气,反应过程中转移电子的数目为
(2)①浸泡衣物时加入“84”消毒液,在空气中放置一段时间漂白效果更好,原因为:
 )。
)。②某温度下,将氯气通入NaOH溶液中,反应得到NaCl、NaClO和NaClO3的混合溶液,经测定ClO-与
 ;的物质的量之比为1:1,写出该反应的化学方程式:
;的物质的量之比为1:1,写出该反应的化学方程式:(3)世界卫生组织将ClO2定为A级高效安全灭菌消毒剂,它在食品保鲜、消毒等方面有广泛应用。消毒效率是用单位质量的消毒剂得电子数来表示的,ClO2作消毒剂时和氯气一样,还原产物均为Cl-,ClO2的消毒效率是氯气的
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】请回答:
(1)H2O2的电子式_____
(2)镁燃烧不能用CO2灭火,用化学方程式表示其理由________________ 。
(3)二氧化锰与浓盐酸制氯气的离子方程式______________
(1)H2O2的电子式
(2)镁燃烧不能用CO2灭火,用化学方程式表示其理由
(3)二氧化锰与浓盐酸制氯气的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】按要求填空:
(1)单质铝和氢氧化钾溶液反应的化学方程式:_____________________________ 。
(2)单质镁与二氧化碳反应的化学方程式:______________________________ 。
(3)工业制备粗硅的化学方程式:_________________________________________ 。
(4)氨的催化氧化反应:____________________________________________ 。
(5)实验室制氯气的离子方程式:__________________________________________ 。
(6)硫代硫酸钠与盐酸反应的离子方程式:_____________________________ 。
(1)单质铝和氢氧化钾溶液反应的化学方程式:
(2)单质镁与二氧化碳反应的化学方程式:
(3)工业制备粗硅的化学方程式:
(4)氨的催化氧化反应:
(5)实验室制氯气的离子方程式:
(6)硫代硫酸钠与盐酸反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】国际化学年的中国宣传口号是“化学-----我们的生活,我们的未来”。学习化学应该明白“从生活中来,到生活中去”道理。请填空:
(1)若金属钠等活泼金属着火时,应该用__________ 来灭火。金属钠应保存在__________ 中。
(2)胃舒平(含有氢氧化铝)治疗胃酸(盐酸)过多的离子反应方程式:_________________ 。
(3)“服用维生素C,可使食物中的Fe3+ 还原成Fe2+”这句话指出,维生素C在这一反应中作__ 剂,具有_______ 性;
(4)过氧化钠在太空及潜水艇中作为供氧剂的两个化学方程式是_________ 、___________ 。
(5)Fe与Cl2在一定条件下反应,所得产物的化学式是________ 。将该产物溶于水配成溶液,分装在两支试管中。请回答:
a.若向其中一支试管中滴加KSCN溶液,则溶液变成________ 色。
b.向另一支试管中滴加NaOH溶液,现象为________________ ,反应的离子方程式是__________ 。
(6)纯净的H2在Cl2中燃烧发出________ 色火焰。
(1)若金属钠等活泼金属着火时,应该用
(2)胃舒平(含有氢氧化铝)治疗胃酸(盐酸)过多的离子反应方程式:
(3)“服用维生素C,可使食物中的Fe3+ 还原成Fe2+”这句话指出,维生素C在这一反应中作
(4)过氧化钠在太空及潜水艇中作为供氧剂的两个化学方程式是
(5)Fe与Cl2在一定条件下反应,所得产物的化学式是
a.若向其中一支试管中滴加KSCN溶液,则溶液变成
b.向另一支试管中滴加NaOH溶液,现象为
(6)纯净的H2在Cl2中燃烧发出
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】下图是化学实验室浓盐酸试剂标签上的部分内容。

(1)写出工业上制HCl的化学方程式_______ ,在实验室中进行该反应,现象是_______
(2)该盐酸的物质的量浓度为_______ ,
(3)同学计划用该浓盐酸配制 的稀盐酸,现实验需要稀盐酸470 mL,可供选用的仪器有:
的稀盐酸,现实验需要稀盐酸470 mL,可供选用的仪器有:
A.胶头滴管;B.烧瓶;C.烧杯;D.药匙;E玻璃棒。
①配制稀盐酸时,选择的仪器有:_______ (填序号),还缺少的仪器有_______ 。
②经计算,配制 的稀盐酸需要用量筒量取上述浓盐酸的体积为
的稀盐酸需要用量筒量取上述浓盐酸的体积为_______ mL。
③测定所配制的稀盐酸,发现其浓度大于 ,引起误差的原因可能是
,引起误差的原因可能是_______ 。
A.量取浓盐酸时俯视刻度线
B.将量取的浓盐酸倒入烧杯后,洗涤量筒,洗涤液也注入容量瓶
C.转移溶液后,未洗涤烧杯和玻璃棒
D.定容时俯视容量瓶刻度线
E.定容摇匀后发现液面低于容量瓶的刻度线,再加水至刻度线
(4)现有该浓盐酸100g,需要加入一定量的水将其物质的量浓度稀释为原来的1/2,则加入水的体积是_______ 。
A.大于100 mL B.小于100 mL C.等于100 mL

(1)写出工业上制HCl的化学方程式
(2)该盐酸的物质的量浓度为
(3)同学计划用该浓盐酸配制
 的稀盐酸,现实验需要稀盐酸470 mL,可供选用的仪器有:
的稀盐酸,现实验需要稀盐酸470 mL,可供选用的仪器有:A.胶头滴管;B.烧瓶;C.烧杯;D.药匙;E玻璃棒。
①配制稀盐酸时,选择的仪器有:
②经计算,配制
 的稀盐酸需要用量筒量取上述浓盐酸的体积为
的稀盐酸需要用量筒量取上述浓盐酸的体积为③测定所配制的稀盐酸,发现其浓度大于
 ,引起误差的原因可能是
,引起误差的原因可能是A.量取浓盐酸时俯视刻度线
B.将量取的浓盐酸倒入烧杯后,洗涤量筒,洗涤液也注入容量瓶
C.转移溶液后,未洗涤烧杯和玻璃棒
D.定容时俯视容量瓶刻度线
E.定容摇匀后发现液面低于容量瓶的刻度线,再加水至刻度线
(4)现有该浓盐酸100g,需要加入一定量的水将其物质的量浓度稀释为原来的1/2,则加入水的体积是
A.大于100 mL B.小于100 mL C.等于100 mL
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】工业氯气通过电解饱和食盐水制得
(1)图(1)中,铁棒作_______ 极,电极反应式是_______ 。
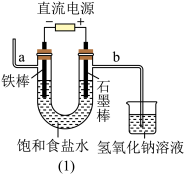
(2)检验导管b出来的气体可以用_______ ,反应的化学方程式是:_______ ;电解饱和食盐水的化学反应方程式为_______ 。
(3)图(1)方法制得的固体烧碱中可能混有少量NaCl,请写出检验是否混有NaCl的实验方法:_______ 。
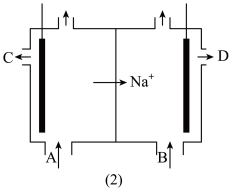
(4)下列关于图(2)的说法正确的是_______。
(5)工业上利用 与
与 反应制盐酸时使用过量的
反应制盐酸时使用过量的 ,理由是
,理由是_______ 。
A.氯气有毒 B.氯气可溶于水 C.氢气密度小
(1)图(1)中,铁棒作

(2)检验导管b出来的气体可以用
(3)图(1)方法制得的固体烧碱中可能混有少量NaCl,请写出检验是否混有NaCl的实验方法:
(4)下列关于图(2)的说法正确的是_______。

| A.A与C、B与D溶质相同 | B.A、B通入的均为浓溶液 |
| C.理论上NaCl利用率可达100% | D.图(2)是负离子交换膜法示意图 |
(5)工业上利用
 与
与 反应制盐酸时使用过量的
反应制盐酸时使用过量的 ,理由是
,理由是A.氯气有毒 B.氯气可溶于水 C.氢气密度小
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】含氧化合物具有广泛的应用,请回答下列问题。
(1) 中含有的电子数目为
中含有的电子数目为___________ 。
(2)将氯气持续通入紫色石蕊试液中,溶液颜色如图变化:

溶液中导致变色的微粒Ⅰ是___________ (填微粒符号,下同),Ⅱ是___________ ,Ⅲ是___________ 。
(3)氯气和氢氧化钠溶液反应可制备“84消毒液”,其化学方程式为___________ 。
(4)漂白粉漂白时,通入 可增加漂白效果,其化学方程式为
可增加漂白效果,其化学方程式为___________ 。
(5)用坩埚钳夹住一束铁丝,灼烧后立刻放入充满氯气的集气瓶中,反应的现象为___________ 。
(6) 是酸性氧化物,
是酸性氧化物, 和碱反应生成
和碱反应生成 的化学方程式为
的化学方程式为___________ 。
(1)
 中含有的电子数目为
中含有的电子数目为(2)将氯气持续通入紫色石蕊试液中,溶液颜色如图变化:

溶液中导致变色的微粒Ⅰ是
(3)氯气和氢氧化钠溶液反应可制备“84消毒液”,其化学方程式为
(4)漂白粉漂白时,通入
 可增加漂白效果,其化学方程式为
可增加漂白效果,其化学方程式为(5)用坩埚钳夹住一束铁丝,灼烧后立刻放入充满氯气的集气瓶中,反应的现象为
(6)
 是酸性氧化物,
是酸性氧化物, 和碱反应生成
和碱反应生成 的化学方程式为
的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】氯化铁(FeCl3)的用途广泛,实验室中可以用Fe与氯气(Cl2)反应制备。某同学将一定量的纯净的Cl2与Fe反应后得到固体混合物,然后将该固体混合物转移至锥形瓶中,并加入过量的稀盐酸和少量的植物油(反应过程中不振荡锥形瓶),充分反应后进行如下实验:

(1)试写出制备氯化铁过程中发生的化学反应方程式___________
(2)试剂A中的主要阴离子的名称为___________
(3)固体混合物加入盐酸时可能发生的反应的离子方程式为___________
(4)实验过程中加入少量植物油的作用是___________
(5)加入过量的 溶液时,溶液红色加深的原因是
溶液时,溶液红色加深的原因是___________
(6)溶液红色褪去的原因可能是过量的 溶液与试剂A中的阴离子发生反应生成SO
溶液与试剂A中的阴离子发生反应生成SO 与两种无污染的气体。根据氧化还原反应的基本规律判断两种气体的化学式为
与两种无污染的气体。根据氧化还原反应的基本规律判断两种气体的化学式为___________ ,试写出 与试剂A中的阴离子反应的离子方程式
与试剂A中的阴离子反应的离子方程式___________

(1)试写出制备氯化铁过程中发生的化学反应方程式
(2)试剂A中的主要阴离子的名称为
(3)固体混合物加入盐酸时可能发生的反应的离子方程式为
(4)实验过程中加入少量植物油的作用是
(5)加入过量的
 溶液时,溶液红色加深的原因是
溶液时,溶液红色加深的原因是(6)溶液红色褪去的原因可能是过量的
 溶液与试剂A中的阴离子发生反应生成SO
溶液与试剂A中的阴离子发生反应生成SO 与两种无污染的气体。根据氧化还原反应的基本规律判断两种气体的化学式为
与两种无污染的气体。根据氧化还原反应的基本规律判断两种气体的化学式为 与试剂A中的阴离子反应的离子方程式
与试剂A中的阴离子反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】判断下列正误:
(1)将氯水滴入Na2CO3溶液中有气泡产生______ 。
(2)铁丝在Cl2中燃烧,产生棕褐色的烟。______ 。
(3)钠在Cl2中燃烧,生成白色的雾。______ 。
(4)铜丝在Cl2中燃烧,生成棕黄色的烟。______ 。
(5)可将氯气与氢气混合光照制备氯化氢。______ 。
(6)实验室制氯气时,为了防止环境污染,多余氯气用氢氧化钙溶液吸收。______ 。
(7)向久置的氯水中滴入紫色石蕊试液,溶液将先变红后褪色。______ 。
(8)检验HCl气体中是否混有Cl2的方法是将气体通入硝酸银溶液。______ 。
(9)除去CO2中的HCl,可使气体通过饱和碳酸氢钠溶液。______ 。
(10))在含有NaOH的酚酞试液中加入新制氯水,红色褪去,说明氯水中含有HClO。______ 。
(1)将氯水滴入Na2CO3溶液中有气泡产生
(2)铁丝在Cl2中燃烧,产生棕褐色的烟。
(3)钠在Cl2中燃烧,生成白色的雾。
(4)铜丝在Cl2中燃烧,生成棕黄色的烟。
(5)可将氯气与氢气混合光照制备氯化氢。
(6)实验室制氯气时,为了防止环境污染,多余氯气用氢氧化钙溶液吸收。
(7)向久置的氯水中滴入紫色石蕊试液,溶液将先变红后褪色。
(8)检验HCl气体中是否混有Cl2的方法是将气体通入硝酸银溶液。
(9)除去CO2中的HCl,可使气体通过饱和碳酸氢钠溶液。
(10))在含有NaOH的酚酞试液中加入新制氯水,红色褪去,说明氯水中含有HClO。
您最近一年使用:0次



