Al在周期表中的位置是________ 。基态C原子核外最外层电子的轨道表示式是______ ,Zn是第30号元素,则基态Zn的价层电子排布式是________ 。
更新时间:2023-12-25 22:42:07
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】最近,德国科学家实现了铷原子气体超流体态与绝缘态的可逆转换,该成果将在量子计算机研究方面带来重大突破。已知铷是37号元素,质量数是85.根据材料完成下列问题:
(1)铷Rb37位于周期表的第___________ 周期,第___________ 族。
(2)关于铷的结构和性质判断正确的是________ 。
①与水反应比钠剧烈
②它的原子半径比钠小
③它的氧化物暴露在空气中易吸收CO2
④它的阳离子最外层电子数和镁相同
⑤它是还原剂
A.①③④ B.②③⑤ C.②④ D.①③⑤
(3)氢化铷与水反应可放出氢气,则下列叙述正确的是________ 。
A.氢化铷溶于水显酸性
B.氢化铷中氢离子被还原为氢气
C.氢化铷与水反应时,水是还原剂
D.氢化铷中氢离子最外层有两个电子
(4)现有铷和另一种碱金属形成的合金50 g,当它与足量水反应时,放出标准状况下的氢气22.4 L,这种碱金属可能是_________ 。
A.Li B.Na C.K D.Cs
(1)铷Rb37位于周期表的第
(2)关于铷的结构和性质判断正确的是
①与水反应比钠剧烈
②它的原子半径比钠小
③它的氧化物暴露在空气中易吸收CO2
④它的阳离子最外层电子数和镁相同
⑤它是还原剂
A.①③④ B.②③⑤ C.②④ D.①③⑤
(3)氢化铷与水反应可放出氢气,则下列叙述正确的是
A.氢化铷溶于水显酸性
B.氢化铷中氢离子被还原为氢气
C.氢化铷与水反应时,水是还原剂
D.氢化铷中氢离子最外层有两个电子
(4)现有铷和另一种碱金属形成的合金50 g,当它与足量水反应时,放出标准状况下的氢气22.4 L,这种碱金属可能是
A.Li B.Na C.K D.Cs
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】回答下列问题
Ⅰ.有下列物质:① 固体;②熔融的
固体;②熔融的 ;③NH4HCO3晶体;④稀硫酸;⑤
;③NH4HCO3晶体;④稀硫酸;⑤ 胶体;⑥铜;⑦液氨;⑧蔗糖晶体;⑨SO2;⑩冰醋酸
胶体;⑥铜;⑦液氨;⑧蔗糖晶体;⑨SO2;⑩冰醋酸
(1)上述状态下的物质可导电的是______ (填序号,下同),属于电解质的是_______ 。
(2)a个⑥原子的总质量为b g,则⑥的摩尔质量表示为_______ ,13.6g的②中阴阳离子总数为_______ 。
(3)在小烧杯中加入 蒸馏水,加热至沸腾后,向沸水中滴入几滴饱和
蒸馏水,加热至沸腾后,向沸水中滴入几滴饱和 溶液,
溶液,_______ ,即制得物质⑤ 胶体。
胶体。
(4)写出向①的水溶液中加入等物质的量的③的离子方程式:_______ 。
(5)向①溶液中通入少量⑨可产生白色沉淀,继续通入⑨可观察到白色沉淀消失,白色沉淀消失的原因为:_______ (离子方程式表示)
Ⅱ.元素周期表对学生学习化学有着重要的作用。其中过渡元素位于周期表中部,请补充以下元素的符号:
(6)原子序数21-25:_______ 、Ti、_______ 、Cr、Mn
元素周期表中同一纵列元素具有相似的化学性质,请补充以下元素的符号:
(7)第IVA族:C、Si、_______ 、_______ 、_______ 、Fl
Ⅰ.有下列物质:①
 固体;②熔融的
固体;②熔融的 ;③NH4HCO3晶体;④稀硫酸;⑤
;③NH4HCO3晶体;④稀硫酸;⑤ 胶体;⑥铜;⑦液氨;⑧蔗糖晶体;⑨SO2;⑩冰醋酸
胶体;⑥铜;⑦液氨;⑧蔗糖晶体;⑨SO2;⑩冰醋酸(1)上述状态下的物质可导电的是
(2)a个⑥原子的总质量为b g,则⑥的摩尔质量表示为
(3)在小烧杯中加入
 蒸馏水,加热至沸腾后,向沸水中滴入几滴饱和
蒸馏水,加热至沸腾后,向沸水中滴入几滴饱和 溶液,
溶液, 胶体。
胶体。(4)写出向①的水溶液中加入等物质的量的③的离子方程式:
(5)向①溶液中通入少量⑨可产生白色沉淀,继续通入⑨可观察到白色沉淀消失,白色沉淀消失的原因为:
Ⅱ.元素周期表对学生学习化学有着重要的作用。其中过渡元素位于周期表中部,请补充以下元素的符号:
(6)原子序数21-25:
元素周期表中同一纵列元素具有相似的化学性质,请补充以下元素的符号:
(7)第IVA族:C、Si、
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】下表列出了A-R9种元素在周期表中的位置:
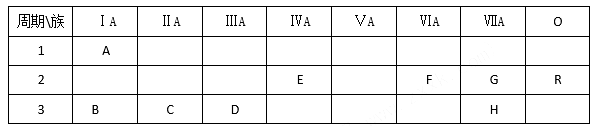
(1)这9种元素中B_______ ,D_______ ,E________ ,H________ 。
其中化学性质最不活泼的是_____________________ (以上均填元素符号)。
(2)B、C、D三种元素按原子半径由大到小的顺序排列为______________ (用元素符号表示).
(3)F元素简单氢化物的化学式是_____________ ,H元素跟B元素形成化合物的化学式是_______ ,高温灼烧该化合物时,火焰呈___________ 色。
(4)G元素和H元素两者核电荷数之差是___________ 。

(1)这9种元素中B
其中化学性质最不活泼的是
(2)B、C、D三种元素按原子半径由大到小的顺序排列为
(3)F元素简单氢化物的化学式是
(4)G元素和H元素两者核电荷数之差是
您最近一年使用:0次
【推荐1】铁(Fe)、钴(Co)、镍(Ni)是第四周期第VIII族的元素,称为铁系元素,相关化合物在生产生活中应用广泛。
(1)铁系元素能与CO形成 、
、 等金属羰基化合物。已知室温时
等金属羰基化合物。已知室温时 为浅黄色液体,沸点103℃,则
为浅黄色液体,沸点103℃,则 中含有的化学键类型包括___________(填字母)。
中含有的化学键类型包括___________(填字母)。
(2)镍能形成多种配合物,如 、
、 、
、 等,下列有关说法正确的是___________(填选项字母)。
等,下列有关说法正确的是___________(填选项字母)。
(3) 的一种配离子[
的一种配离子[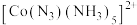 中,
中, 的配位数是
的配位数是___________ ,Fe、Co、Ni与Ca都位于第四周期且最外层电子数相同,但相应单质的熔点,Fe、Co、Ni明显高于Ca,其原因是___________ 。
(4)NiO晶胞与NaCl晶胞相似,如图所示:___________ 个;每个氧离子周围与它最近且相等距离的氧离子有___________ 个。NiO分子量为74.7,晶胞参数为apm, 代表阿伏加德罗常数的值。则NiO晶体的密度为
代表阿伏加德罗常数的值。则NiO晶体的密度为___________  (只列出计算式)。
(只列出计算式)。
(1)铁系元素能与CO形成
 、
、 等金属羰基化合物。已知室温时
等金属羰基化合物。已知室温时 为浅黄色液体,沸点103℃,则
为浅黄色液体,沸点103℃,则 中含有的化学键类型包括___________(填字母)。
中含有的化学键类型包括___________(填字母)。| A.极性共价键 | B.离子键 | C.配位键 | D.金属键 |
(2)镍能形成多种配合物,如
 、
、 、
、 等,下列有关说法正确的是___________(填选项字母)。
等,下列有关说法正确的是___________(填选项字母)。A. 中含有共价键和离子键 中含有共价键和离子键 |
B.CO与 互为等电子体,其中CO分子内σ键和π键的个数比为1:2 互为等电子体,其中CO分子内σ键和π键的个数比为1:2 |
C. 中N原子为 中N原子为 杂化,其空间构型为正四面体形 杂化,其空间构型为正四面体形 |
D. 在形成配合物时其配位数只能为4,Fe在形成配合物时其配位数只能为6 在形成配合物时其配位数只能为4,Fe在形成配合物时其配位数只能为6 |
(3)
 的一种配离子[
的一种配离子[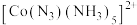 中,
中, 的配位数是
的配位数是(4)NiO晶胞与NaCl晶胞相似,如图所示:
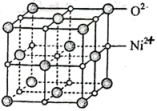
 代表阿伏加德罗常数的值。则NiO晶体的密度为
代表阿伏加德罗常数的值。则NiO晶体的密度为 (只列出计算式)。
(只列出计算式)。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】在一百多种化学元素中,非金属占了23种。80%的非金属元素在社会中占重要位置。如C、N、Si、Cl等。
(1)氯元素最外电子层上有___________ 种能量不同的电子,该元素的简单阴离子核外电子排布式是___________ 。
(2)由氮元素与硅元素组成的物质,可用于制造发动机的耐热部件,因为它属于___________ 晶体,请写出该化合物的化学式___________ 。
(3)下列事实能说明氯与氧两元素非金属性相对强弱的有___________ (选填编号)。
a.Cl原子最外层电子数比氧多 b.酸性:HCl>H2O
c.ClO2中氯元素为+4价,氧元素为-2价 d.沸点:H2O>HCl
(1)氯元素最外电子层上有
(2)由氮元素与硅元素组成的物质,可用于制造发动机的耐热部件,因为它属于
(3)下列事实能说明氯与氧两元素非金属性相对强弱的有
a.Cl原子最外层电子数比氧多 b.酸性:HCl>H2O
c.ClO2中氯元素为+4价,氧元素为-2价 d.沸点:H2O>HCl
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】推导下列元素,回答有关问题:
(1)具有1个4p电子的元素为________ (写元素名称,下同),简化电子排布式为________ 。
(2)N层只有1个电子的主族元素是________ ,其氯化物的焰色反应呈________ 色,其原子核外有________ 种不同运动状态的电子。
(3)3d能级全充满,4s能级只有1个电子的元素为________ ,原子序数为________ 。
(4)离子M2+的3d轨道中有5个电子,则M原子的最外层电子数和未成对电子数分别为_____ 和___ 。
(5)原子序数小于36的元素X和Y,在周期表中既处于同一周期又位于同一族,且Y的原子序数比X大2,则Y的基态原子的价电子排布式是____ ,X在参与化学反应时,1个原子失去的电子数为_____ 。
(1)具有1个4p电子的元素为
(2)N层只有1个电子的主族元素是
(3)3d能级全充满,4s能级只有1个电子的元素为
(4)离子M2+的3d轨道中有5个电子,则M原子的最外层电子数和未成对电子数分别为
(5)原子序数小于36的元素X和Y,在周期表中既处于同一周期又位于同一族,且Y的原子序数比X大2,则Y的基态原子的价电子排布式是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】CO2和CH4在一定条件下合成乙酸:CO2+CH4 CH3COOH。完成下列填空:
CH3COOH。完成下列填空:
(1)①写出碳原子最外电子层的轨道表示式______
②钛(Ti)是22号元素,它是______ (选填编号)
a.主族元素 b.副族元素 c.短周期元素 d.长周期元素
(2)CS2分子的电子式为______ ;其熔沸点比CO2高,原因是______ 常温下,向1L pH=10的 NaOH溶液中持续通入CO2。通入CO2的体积(V)与溶液中水电离产生的OH﹣离子浓度(c)的关系如图所示
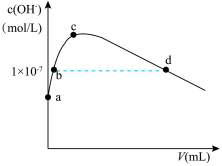
(3)c点溶液中离子浓度由大至小的关系是:______
(4)a点溶液中由水电离产生的c(H+)=______ ;b点溶液中c(H+)______ 1×10﹣7mol/L(填写“等于”、“大于”或“小于”)
(5)能使0.1mol/L乙酸溶液的电离程度以及pH都增大的是______ (选填序号)
a.加水稀释 b.加入少量乙酸钠固体 c.通氯化氢 d.加入少量苛性钠固体
 CH3COOH。完成下列填空:
CH3COOH。完成下列填空:(1)①写出碳原子最外电子层的轨道表示式
②钛(Ti)是22号元素,它是
a.主族元素 b.副族元素 c.短周期元素 d.长周期元素
(2)CS2分子的电子式为

(3)c点溶液中离子浓度由大至小的关系是:
(4)a点溶液中由水电离产生的c(H+)=
(5)能使0.1mol/L乙酸溶液的电离程度以及pH都增大的是
a.加水稀释 b.加入少量乙酸钠固体 c.通氯化氢 d.加入少量苛性钠固体
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】在1778年,法国马厚比无意中发现用硫酸钠、木炭和铁(后改用氧化铁)一起灼烧,再用水滗取可得到纯碱。这一发明使他建立起世界上第一座纯碱工厂。
2Fe2O3+3NazSO4+16C Na6Fe4S3+ 14CO↑+2CO2↑
Na6Fe4S3+ 14CO↑+2CO2↑
Na6Fe4S3+O2+2CO2 Na2Fe4S3+2Na2CO3
Na2Fe4S3+2Na2CO3
回答下列问题:
(1)基态铁原子的价层电子排布式为_______ ,其3d能级上有_______ 个运动状态不同的电子。
(2)基态 原子核外有
原子核外有_______ 对自旋方向相反的电子对。基态钠原子核外电子占据能量最高的能级符号是_______ 。
(3)在氧、硫、钠、碳、铁元素中,金属性最强的元素与非金属性最强的元素组成的化合物是_______ (填化学式)。C、O、F三种元素中,电负性由大到小的顺序为_______ 。
(4)某同学书写的基态碳原子轨道表示式为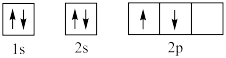 ,他违背了
,他违背了_______ 。
2Fe2O3+3NazSO4+16C
 Na6Fe4S3+ 14CO↑+2CO2↑
Na6Fe4S3+ 14CO↑+2CO2↑Na6Fe4S3+O2+2CO2
 Na2Fe4S3+2Na2CO3
Na2Fe4S3+2Na2CO3回答下列问题:
(1)基态铁原子的价层电子排布式为
(2)基态
 原子核外有
原子核外有(3)在氧、硫、钠、碳、铁元素中,金属性最强的元素与非金属性最强的元素组成的化合物是
(4)某同学书写的基态碳原子轨道表示式为
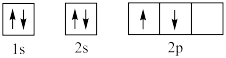 ,他违背了
,他违背了
您最近一年使用:0次
【推荐3】回答下列问题
(1)F元素的基态原子最外层电子排布式为nsnnpn+3,则n=___________ ;基态原子中能量最高的是___________ 电子,核外电子的轨道表示式为___________ 。
(2)硝酸和尿素( )的相对分子质量接近,但常温下硝酸为挥发性液体,尿素为固体,请解释原因:
)的相对分子质量接近,但常温下硝酸为挥发性液体,尿素为固体,请解释原因:___________ 。
(3)N、O、S的第一电离能(I1)由大到小的顺序为___________ ,原因是______________________ 。
(1)F元素的基态原子最外层电子排布式为nsnnpn+3,则n=
(2)硝酸和尿素(
 )的相对分子质量接近,但常温下硝酸为挥发性液体,尿素为固体,请解释原因:
)的相对分子质量接近,但常温下硝酸为挥发性液体,尿素为固体,请解释原因:(3)N、O、S的第一电离能(I1)由大到小的顺序为
您最近一年使用:0次



