某同学欲用购买的市售盐酸配制家庭中所需的洁厕灵(230mL ),可供选择的仪器如图所示。请回答下列问题:
),可供选择的仪器如图所示。请回答下列问题:
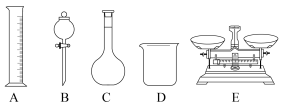
(1)如图所示的仪器中配制上述溶液肯定不需要的是___________ (填序号),配制过程中选用的玻璃仪器除了上述提供的还需要有___________ 。
(2)应量取浓盐酸的体积为___________ mL。
(3)如果取5mL该浓盐酸加水稀释至10mL。那么稀释后的盐酸的质量分数___________ 18.25%(填“大于”、“小于”或“等于”下同)。如果取5mL该浓盐酸加等质量的水稀释,那么稀释后盐酸的物质的量浓度___________ 原浓盐酸物质的量浓度的一半。
(4)装置C需标有以下5项中的___________ (填序号,下同);装置A的刻度表示应为下图中___________ 。
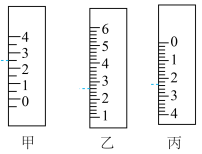
①温度②浓度③容量④压强⑤刻度线
(5)下列情况将使配制洁厕灵的物质的量浓度偏高的有___________ (填序号)。
A.容量瓶用蒸馏水洗净后,未等内壁干燥便用来配制
B.未等冷却,立即把溶液转移到容量瓶中
C.定容时,仰视刻度线
D.将洗涤量筒、烧杯、玻璃棒的洗涤液一并转移到容量瓶中
E.在稀释过程中有少量液体溅出烧杯外
 ),可供选择的仪器如图所示。请回答下列问题:
),可供选择的仪器如图所示。请回答下列问题:
盐酸 化学纯 CP 500mL 品名:盐酸 化学试:HCl 密度:1.18g/cm3 质量分数:36.5% |
(1)如图所示的仪器中配制上述溶液肯定不需要的是
(2)应量取浓盐酸的体积为
(3)如果取5mL该浓盐酸加水稀释至10mL。那么稀释后的盐酸的质量分数
(4)装置C需标有以下5项中的

①温度②浓度③容量④压强⑤刻度线
(5)下列情况将使配制洁厕灵的物质的量浓度偏高的有
A.容量瓶用蒸馏水洗净后,未等内壁干燥便用来配制
B.未等冷却,立即把溶液转移到容量瓶中
C.定容时,仰视刻度线
D.将洗涤量筒、烧杯、玻璃棒的洗涤液一并转移到容量瓶中
E.在稀释过程中有少量液体溅出烧杯外
更新时间:2024-01-01 10:08:58
|
相似题推荐
解答题-实验探究题
|
较难
(0.4)
名校
【推荐1】如图为实验室某浓盐酸试剂瓶标签上的部分数据,试根据标签.上的相关数据回答下列问题:.
(1)该浓盐酸中HCl的物质的量浓度为______ mol/L。
(2)取用任意体积的该盐酸时,下列物理量中不随所取体积的多少而变化的是______(填字母)。
(3)某学生欲用上述浓盐酸和蒸馏水配制480mL物质的量浓度为0.400mol/L的稀盐酸。
①该学生需要量取______ mL上述浓盐酸进行配制。
②在配制过程中,下列实验操作对所配制的稀盐酸的物质的量浓度有何影响?(填“偏大”“偏小”或“无影响”)
a.用量筒量取浓盐酸时俯视观察凹液面:______ ;
b.定容后经振荡、摇匀、静置,发现液面下降,再加适量的蒸馏水:______ 。
(4)①假设该同学成功配制了0.400mol/L的盐酸,他又用该盐酸中和含0.4g NaOH的NaOH溶液,则该同学需取______ mL盐酸。
②假设该同学用新配制的盐酸中和含0.4g NaOH的NaOH溶液,发现比①中所求体积偏小,则可能的原因是______ 。
A.浓盐酸挥发,浓度不足 B.配制溶液时,未洗涤烧杯
C.配制溶液时,俯视容量瓶刻度线 D.加水时超过刻度线,用胶头滴管吸出
| 盐酸 分子式:HCl 相对分子质量:36.5 密度:  HCl的质量分数:36.5% |
(2)取用任意体积的该盐酸时,下列物理量中不随所取体积的多少而变化的是______(填字母)。
| A.溶液中HCl的物质的量 | B.溶液的浓度 |
C.溶液中 的数目 的数目 | D.溶液的密度 |
①该学生需要量取
②在配制过程中,下列实验操作对所配制的稀盐酸的物质的量浓度有何影响?(填“偏大”“偏小”或“无影响”)
a.用量筒量取浓盐酸时俯视观察凹液面:
b.定容后经振荡、摇匀、静置,发现液面下降,再加适量的蒸馏水:
(4)①假设该同学成功配制了0.400mol/L的盐酸,他又用该盐酸中和含0.4g NaOH的NaOH溶液,则该同学需取
②假设该同学用新配制的盐酸中和含0.4g NaOH的NaOH溶液,发现比①中所求体积偏小,则可能的原因是
A.浓盐酸挥发,浓度不足 B.配制溶液时,未洗涤烧杯
C.配制溶液时,俯视容量瓶刻度线 D.加水时超过刻度线,用胶头滴管吸出
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
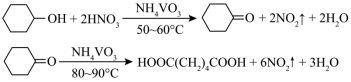
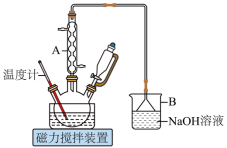
【推荐2】1,6己二酸是常用的化工原料,在高分子材料、医药、润滑剂的制造等方面都有重要作用。实验室利用图中的装置(夹持装置已省略),以环己醇和硝酸为反应物制备1,6己二酸。反应原理为:
实验步骤如下:
Ⅰ.向三颈烧瓶中加入0.03gNH4VO3固体和18mL浓HNO3(略过量),向恒压滴液漏斗中加入6mL环己醇
Ⅱ.将三颈烧瓶放入水浴中,电磁搅拌并加热至50℃。移去水浴,打开恒压滴液漏斗活塞滴加5~6滴环己醇,观察到三颈烧瓶中产生红棕色气体时,开始慢慢加入余下的环己醇。调节滴加环己醇的速度,使三颈烧瓶内温度维持在50~60℃之间,直至环己醇全部滴加完毕
Ⅲ.将三颈烧瓶放入80~90℃水浴中加热10min,至几乎无红棕色气体导出为止。然后迅速将三颈烧瓶中混合液倒入100mL烧杯中,冷却至室温后,有白色晶体析出,减压过滤,___________,干燥,得到粗产品
Ⅳ.1,6-己二酸粗产品的提纯
(1)将步骤Ⅲ补充完整:_______ 。步骤Ⅳ提纯方法的名称为_______ 。如图为1,6己二酸在水中的溶解度曲线,80℃时1,6-己二酸水溶液的密度为ρg·mL-1;该溶液的物质的量浓度为_______ 。
| 试剂 | 相对分子质量 | 密度/(g·mL-1) | 熔点/℃ | 沸点/℃ | 溶解性 |
| 环己醇 | 100 | 0.962 | 25.9 | 161.8 | 可溶于水、乙醇、乙醚 |
| 1,6-己二酸 | 146 | 1.360 | 152 | 330.5 | 微溶于冷水,易溶于乙醇 |
| NH4VO3 | 117 | 2.326 | 210(分解) | — | 微溶于冷水,易溶于热水 |
Ⅰ.向三颈烧瓶中加入0.03gNH4VO3固体和18mL浓HNO3(略过量),向恒压滴液漏斗中加入6mL环己醇
Ⅱ.将三颈烧瓶放入水浴中,电磁搅拌并加热至50℃。移去水浴,打开恒压滴液漏斗活塞滴加5~6滴环己醇,观察到三颈烧瓶中产生红棕色气体时,开始慢慢加入余下的环己醇。调节滴加环己醇的速度,使三颈烧瓶内温度维持在50~60℃之间,直至环己醇全部滴加完毕
Ⅲ.将三颈烧瓶放入80~90℃水浴中加热10min,至几乎无红棕色气体导出为止。然后迅速将三颈烧瓶中混合液倒入100mL烧杯中,冷却至室温后,有白色晶体析出,减压过滤,___________,干燥,得到粗产品
Ⅳ.1,6-己二酸粗产品的提纯
(1)将步骤Ⅲ补充完整:

| A.46.07% | B.57.08% | C.63.03% | D.74.61% |
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
解题方法
【推荐3】已知金属钠着火时不能使用干冰灭火器灭火。某课外小组进行如下实验(假设每步反应均完全进行):
I.从试剂瓶中取出金属钠块,吸干表面的煤油,去除表面氧化物,称重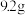 ;
;
II.将金属钠固体放在硬质玻璃管中,通入一段时间 后加热,金属钠燃烧,生成含有少量黑色颗粒的白色固体,称重
后加热,金属钠燃烧,生成含有少量黑色颗粒的白色固体,称重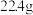 ;
;
III.将有黑色颗粒的白色固体加入足量密度为 的
的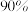
 溶液中并加热,产生无色气体;
溶液中并加热,产生无色气体;
IV.将无色气体依次通过盛有足量 溶液的A洗气瓶、足量
溶液的A洗气瓶、足量 溶液的B洗气瓶,均有白色沉淀生成。
溶液的B洗气瓶,均有白色沉淀生成。
回答下列问题:
(1)步骤I中吸干钠块表面的煤油的实验用品是___________ 。
(2)步骤II中生成的白色固体是 ,则少量黑色颗粒是
,则少量黑色颗粒是___________ (填化学式),反应的化学方程式为___________ 。
(3)步骤III中用到的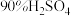 溶液的物质的量浓度为
溶液的物质的量浓度为___________  (结果保留一位小数)。
(结果保留一位小数)。
(4)步骤IV中A洗气瓶中发生反应的离子方程式为___________ ,B洗气瓶中生成白色沉淀的质量是___________ 。
I.从试剂瓶中取出金属钠块,吸干表面的煤油,去除表面氧化物,称重
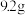 ;
;II.将金属钠固体放在硬质玻璃管中,通入一段时间
 后加热,金属钠燃烧,生成含有少量黑色颗粒的白色固体,称重
后加热,金属钠燃烧,生成含有少量黑色颗粒的白色固体,称重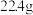 ;
;III.将有黑色颗粒的白色固体加入足量密度为
 的
的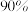
 溶液中并加热,产生无色气体;
溶液中并加热,产生无色气体;IV.将无色气体依次通过盛有足量
 溶液的A洗气瓶、足量
溶液的A洗气瓶、足量 溶液的B洗气瓶,均有白色沉淀生成。
溶液的B洗气瓶,均有白色沉淀生成。回答下列问题:
(1)步骤I中吸干钠块表面的煤油的实验用品是
(2)步骤II中生成的白色固体是
 ,则少量黑色颗粒是
,则少量黑色颗粒是(3)步骤III中用到的
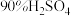 溶液的物质的量浓度为
溶液的物质的量浓度为 (结果保留一位小数)。
(结果保留一位小数)。(4)步骤IV中A洗气瓶中发生反应的离子方程式为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐1】实验室里要配制400mL0.2mol/L的硫酸钠溶液。实验步骤如下:
A.在天平上称出_______ g硫酸钠固体,把它放在烧杯里,用适量的蒸馏水溶解。
B.把得到的溶液冷却后小心地沿着__________ 注入_______________ 中。
C.用少量蒸馏水洗涤烧杯和玻璃棒2~3次,每次洗涤液也小心转入容量瓶中。
D.继续向容量瓶中加蒸馏水至液面距刻度l~2cm处,改用________ 小心滴加蒸馏水至溶液凹液面底部与刻度线水平相切。
E.将瓶塞塞紧,充分摇匀。
F.将配好的溶液倒入试剂瓶中,贴上标签,并洗涤容量瓶。
(1) 请填写上述空白处。
(2) 下列情况会使所配溶液浓度偏低的是___________ (填序号)。
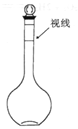
a.某同学定容时观察液面的情况如图所示
b.没有进行上述的操作步骤C
c.摇匀后发现液面低于刻度线
d.B操作时将少量液体洒到外面
e.容量瓶用前内壁沾有水珠
(3) 如果实验室用18mol/L的浓硫酸配制3. 6mol·L-1的稀硫酸250mL。计算所需浓硫酸的体积为___________ mL,在实验时应用_________ 量取浓硫酸。
A.在天平上称出
B.把得到的溶液冷却后小心地沿着
C.用少量蒸馏水洗涤烧杯和玻璃棒2~3次,每次洗涤液也小心转入容量瓶中。
D.继续向容量瓶中加蒸馏水至液面距刻度l~2cm处,改用
E.将瓶塞塞紧,充分摇匀。
F.将配好的溶液倒入试剂瓶中,贴上标签,并洗涤容量瓶。
(1) 请填写上述空白处。
(2) 下列情况会使所配溶液浓度偏低的是

a.某同学定容时观察液面的情况如图所示
b.没有进行上述的操作步骤C
c.摇匀后发现液面低于刻度线
d.B操作时将少量液体洒到外面
e.容量瓶用前内壁沾有水珠
(3) 如果实验室用18mol/L的浓硫酸配制3. 6mol·L-1的稀硫酸250mL。计算所需浓硫酸的体积为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐2】《必修1》中学习过:A过滤、B蒸发(结晶)、C蒸馏、D分液、E萃取、F配制一定物质的量浓度的溶液,根据所学的知识回答下列下列问题:
(1)选用适当的方法分离或提纯,应选用上述哪一种?(填序号)
①除去 NaCl 溶液中所含的少量 KNO3__________ ;
②从碘水中提取碘__________ ;
③用自来水制取蒸馏水__________ ;
④分离植物油和水__________ ;
(2)除过滤、蒸发(结晶)外还有_____ 实验用到了玻璃棒。需要加热的实验有蒸发(结晶)和__________ ;填序号)。
(3)图是硫酸试剂瓶标签上的内容。实验室用该硫酸配制240mL0.46mol/L的稀硫酸,则

a.需量取该硫酸的体积为__________ mL;
b.有以下仪器:①烧杯 ②100mL量筒 ③250mL容量瓶④500mL容量瓶 ⑤玻璃棒 ⑥托盘天平(带砝码)⑦10mL量筒⑧胶头滴管,配制过程中,必须使用的仪器是_____ (填代号);
(4)该同学实际配制得到的浓度为0.47mol/L,可能的原因是_______________
A.量取浓H2SO4时仰视刻度 B.容量瓶洗净后未经干燥处理
C.没有将洗涤液转入容量瓶 D.定容时仰视刻度
(1)选用适当的方法分离或提纯,应选用上述哪一种?(填序号)
①除去 NaCl 溶液中所含的少量 KNO3
②从碘水中提取碘
③用自来水制取蒸馏水
④分离植物油和水
(2)除过滤、蒸发(结晶)外还有
(3)图是硫酸试剂瓶标签上的内容。实验室用该硫酸配制240mL0.46mol/L的稀硫酸,则

a.需量取该硫酸的体积为
b.有以下仪器:①烧杯 ②100mL量筒 ③250mL容量瓶④500mL容量瓶 ⑤玻璃棒 ⑥托盘天平(带砝码)⑦10mL量筒⑧胶头滴管,配制过程中,必须使用的仪器是
(4)该同学实际配制得到的浓度为0.47mol/L,可能的原因是
A.量取浓H2SO4时仰视刻度 B.容量瓶洗净后未经干燥处理
C.没有将洗涤液转入容量瓶 D.定容时仰视刻度
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐3】食盐是日常生活的必需品,也是重要的化工原料。
(1)粗食盐常含有少量Ca2+、Mg2+、Fe3+、SO 等杂质离子,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
等杂质离子,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
步骤1:取一定量的粗盐,置于烧杯中,加入足量的水,配成粗盐水;
步骤2:向粗盐水中加入除杂试剂,然后进行过滤,滤去不溶物,再向滤液中加入盐酸调
节盐水的pH;
步骤3:将得到的溶液蒸发浓缩、冷却、结晶、过滤、烘干即得精盐;
请回答以下问题:
①上述实验中的过滤操作需要烧杯、____________ 、____________ 等玻璃仪器.
②步骤2中常用Na2CO3、NaOH、BaCl2作为除杂试剂,则加入除杂试剂的顺序为:
___________ 、__________ 、NaOH。
③步骤2中,判断加入BaCl2已过量的方法是_________________________________________________________________________ 。
(2)为检验精盐纯度,需配制100 mL 0.5mol/L(精盐)溶液,右图是该
同学转移溶液的示意图,图中的错误是
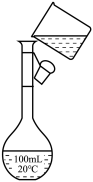
________________________________________________ 。
若在定容时仰视,则所配溶液的浓度_______ 0.5mol/L(填>或<)。
(3)电解饱和食盐水的装置如图所示,若收集的H2为2L,
则相同条件下收集的Cl2_____________ (填>、=或<)
2L,原因____
(4)某学习小组设计了如下图实验,将氯气依次通过下列装
置以验证氯气的性质:
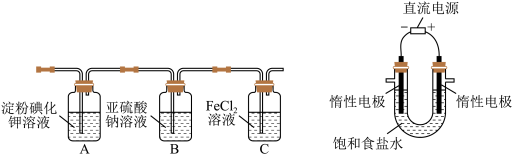
①通入氯气后,A中的现象是_________________________ ,整套实验装置存在的明显缺
陷是___________________________ 。
②C装置中发生反应的离子方程式为____________________________________ 。
③请你帮该小组同学设计一个实验,证明洗气瓶B中的Na2SO3已被氧化(简述实验步骤):________________________________________________________________________________________________________________________________________________________________
(1)粗食盐常含有少量Ca2+、Mg2+、Fe3+、SO
 等杂质离子,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
等杂质离子,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):步骤1:取一定量的粗盐,置于烧杯中,加入足量的水,配成粗盐水;
步骤2:向粗盐水中加入除杂试剂,然后进行过滤,滤去不溶物,再向滤液中加入盐酸调
节盐水的pH;
步骤3:将得到的溶液蒸发浓缩、冷却、结晶、过滤、烘干即得精盐;
请回答以下问题:
①上述实验中的过滤操作需要烧杯、
②步骤2中常用Na2CO3、NaOH、BaCl2作为除杂试剂,则加入除杂试剂的顺序为:
③步骤2中,判断加入BaCl2已过量的方法是
(2)为检验精盐纯度,需配制100 mL 0.5mol/L(精盐)溶液,右图是该
同学转移溶液的示意图,图中的错误是

若在定容时仰视,则所配溶液的浓度
(3)电解饱和食盐水的装置如图所示,若收集的H2为2L,
则相同条件下收集的Cl2
2L,原因
(4)某学习小组设计了如下图实验,将氯气依次通过下列装
置以验证氯气的性质:

①通入氯气后,A中的现象是
陷是
②C装置中发生反应的离子方程式为
③请你帮该小组同学设计一个实验,证明洗气瓶B中的Na2SO3已被氧化(简述实验步骤):
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐1】掌握仪器名称、组装及使用方法是中学化学实验的基础,下图为两套实验装置。
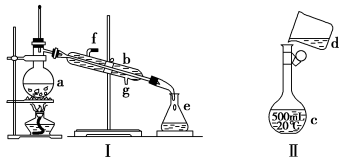
(1)写出下列仪器的名称:a.________ c.________ 。
(2)仪器a~e中,使用前必须检查是否漏水的有________ (填序号)。
(3)若利用装置Ⅰ分离四氯化碳和酒精的混合物,冷凝水的进水方向是________ (填序号)
(4)现需配制0.125 mol·L-1 NaOH溶液450 mL,装置Ⅱ是某同学转移溶液的示意图。
①图中的错误是__________________ 。除了图中给出的仪器和托盘天平外,为完成实验还需要的玻璃仪器有________ 。
②根据计算得知,需称量NaOH的质量为__________________________ g。
③下列操作使配制的NaOH溶液浓度偏低的有________ 。
A.将砝码放在左盘上,NaOH放在右盘上进行称量(使用游码)
B.选用的容量瓶内有少量蒸馏水
C.定容摇匀后,液面下降,又加水至刻度线
D.定容时俯视刻度线

(1)写出下列仪器的名称:a.
(2)仪器a~e中,使用前必须检查是否漏水的有
(3)若利用装置Ⅰ分离四氯化碳和酒精的混合物,冷凝水的进水方向是
(4)现需配制0.125 mol·L-1 NaOH溶液450 mL,装置Ⅱ是某同学转移溶液的示意图。
①图中的错误是
②根据计算得知,需称量NaOH的质量为
③下列操作使配制的NaOH溶液浓度偏低的有
A.将砝码放在左盘上,NaOH放在右盘上进行称量(使用游码)
B.选用的容量瓶内有少量蒸馏水
C.定容摇匀后,液面下降,又加水至刻度线
D.定容时俯视刻度线
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐2】某研究性学习小组欲测定室温下(25 ℃、101 kPa)的气体摩尔体积,请回答以下问题。该小组设计的简易实验装置如下图所示:

该实验的主要操作步骤如下:
步骤一:
(1)①配制100 mL 1.0 mol·L-1的盐酸,需要20%,密度为1.1g·cm-3的盐酸的体积为______ 。
②配制过程中所需要的玻璃仪器有__________________________________________ 。
③下列操作会导致物质的量浓度偏大的是_________________
A.转移溶液后未洗涤烧杯和玻璃棒就直接定容
B.在容量瓶中进行定容时仰视刻度线
C.在容量瓶中进行定容时俯视刻度线
D.定容后把容量瓶倒置摇匀,发现液面低于刻度线,又补足了所缺的水
步骤二: 用量筒量取出10.0 mL 1.0 mol·L-1的盐酸加入锥形瓶中;
步骤三: (2)称取a g已除去表面氧化膜的镁条,并系于铜丝末端,为使HCl全部参加反应,a的数值至少为________ ;
步骤四: 往广口瓶中装入足量水,按上图连接好装置,检查装置的气密性;
步骤五: (3)反应结束后待体系温度恢复至室温,读取量筒中水的体积为V mL。
①实验步骤五中应选用________ (填序号)的量筒。
A.100 mL B.200 mL C.500 mL
②读数时除恢复到室温,视线与液体凹液面的最低处相平外,还要注意_____________________ 。
③若忽略水蒸气的影响,在实验条件下测得气体摩尔体积的计算公式为Vm=________ ,若未除去镁条表面的氧化膜,则测量结果________ (填“偏大”“偏小”或“无影响”)。

该实验的主要操作步骤如下:
步骤一:
(1)①配制100 mL 1.0 mol·L-1的盐酸,需要20%,密度为1.1g·cm-3的盐酸的体积为
②配制过程中所需要的玻璃仪器有
③下列操作会导致物质的量浓度偏大的是
A.转移溶液后未洗涤烧杯和玻璃棒就直接定容
B.在容量瓶中进行定容时仰视刻度线
C.在容量瓶中进行定容时俯视刻度线
D.定容后把容量瓶倒置摇匀,发现液面低于刻度线,又补足了所缺的水
步骤二: 用量筒量取出10.0 mL 1.0 mol·L-1的盐酸加入锥形瓶中;
步骤三: (2)称取a g已除去表面氧化膜的镁条,并系于铜丝末端,为使HCl全部参加反应,a的数值至少为
步骤四: 往广口瓶中装入足量水,按上图连接好装置,检查装置的气密性;
步骤五: (3)反应结束后待体系温度恢复至室温,读取量筒中水的体积为V mL。
①实验步骤五中应选用
A.100 mL B.200 mL C.500 mL
②读数时除恢复到室温,视线与液体凹液面的最低处相平外,还要注意
③若忽略水蒸气的影响,在实验条件下测得气体摩尔体积的计算公式为Vm=
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐3】实验室欲配制1mol/L NaOH溶液240ml,请回答:
(1)需称取NaOH固体____________ g,用质量为23.1 g的烧杯放在托盘天平上称取所需NaOH固体时,请在附表中选取所需的砝码大小___________ (填字母),并在下图中选出能正确表示游码位置的选项____________ (填字母)。
附表砝码规格

(2)选用的主要玻璃仪器除烧杯、玻璃棒外还有_____________________________ 。
(3)下列操作的顺序是(用序号表示)_________________ 。
A、用30mL水洗涤烧杯2—3次,洗涤液均注入容量瓶,振荡
B、用天平准确称取所需的NaOH的质量,加入少量水,用玻璃棒慢慢搅动,使其充分溶解
C、将已冷却的NaOH溶液沿玻璃棒注入容量瓶中
D、将容量瓶盖紧,颠倒摇匀
E、改用胶头滴管加水,使溶液凹面恰好与刻度相切
F、继续往容量瓶内小心加水,直到液面接近刻度1—2cm处
(4)下列情况对所配制的NaOH溶液浓度有何影响?(用“偏大”“偏小”“无影响”填写)
①容量瓶用蒸馏洗涤后残留有少量的水________________
②将热的溶液直接移入了容量瓶________________
③定容时,仰视容量瓶的刻度线________________
④转移溶液时,玻璃棒的下端在容量瓶的刻度线以上________________
(1)需称取NaOH固体
附表砝码规格
| a | b | c | d | e | |
| 砝码大小/g | 100 | 50 | 20 | 10 | 5 |

(2)选用的主要玻璃仪器除烧杯、玻璃棒外还有
(3)下列操作的顺序是(用序号表示)
A、用30mL水洗涤烧杯2—3次,洗涤液均注入容量瓶,振荡
B、用天平准确称取所需的NaOH的质量,加入少量水,用玻璃棒慢慢搅动,使其充分溶解
C、将已冷却的NaOH溶液沿玻璃棒注入容量瓶中
D、将容量瓶盖紧,颠倒摇匀
E、改用胶头滴管加水,使溶液凹面恰好与刻度相切
F、继续往容量瓶内小心加水,直到液面接近刻度1—2cm处
(4)下列情况对所配制的NaOH溶液浓度有何影响?(用“偏大”“偏小”“无影响”填写)
①容量瓶用蒸馏洗涤后残留有少量的水
②将热的溶液直接移入了容量瓶
③定容时,仰视容量瓶的刻度线
④转移溶液时,玻璃棒的下端在容量瓶的刻度线以上
您最近一年使用:0次



