电解原理在化学工业中有广泛应用。
(1)用固态碳燃料电池电解饱和食盐水(M极室为食盐水,N极室为稀NaOH溶液)的装置如下图所示。
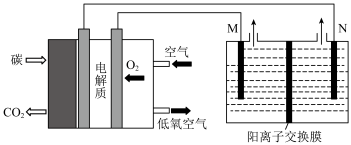
①电极M是___________ 极,N极区的产物为:___________ (用化学式表示);
②已知电解前M极区溶液的浓度为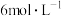 ,体积为200mL。当消耗标准状况下1.12L
,体积为200mL。当消耗标准状况下1.12L 时,M极区溶液的浓度变为
时,M极区溶液的浓度变为___________  。(电解前后溶液体积变化忽略不计)。
。(电解前后溶液体积变化忽略不计)。
(2)电化学理论在钢铁防腐、废水处理中有着重要应用价值。请按要求回答下列问题:
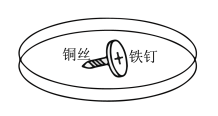
①下图为探究金属Fe是否腐蚀的示意图,在培养皿中加入一定量的琼脂与饱和NaCl溶液混合,滴入5~6滴酚酞溶液,混合均匀,将缠有铜丝的铁钉放入培养皿中。溶液变红的部位为___________ (填“左”或“右”端),结合化学用语解释变红的原因:___________ 。
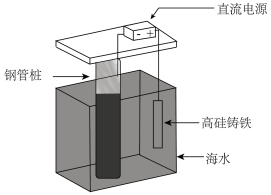
②支撑海港码头基础的钢管桩常采用如图所示的方法进行防腐,其中高硅铸铁为惰性辅助阳极。该保护方法叫作___________ (填“牺牲阳极法”或“外加电流法”)。下列有关表述正确的是___________ (填字母)。
a.钢管桩被迫成为阴极而受到保护,其表面的腐蚀电流接近于零
b.高硅铸铁的作用是作为损耗阳极材料和传递电流
c.通电后,调整外加电压,外电路中的电子被强制从钢管桩流向高硅铸铁
d.石墨能导电且化学性质不活泼,可用石墨代替高硅铸铁作辅助阳极
(1)用固态碳燃料电池电解饱和食盐水(M极室为食盐水,N极室为稀NaOH溶液)的装置如下图所示。

①电极M是
②已知电解前M极区溶液的浓度为
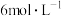 ,体积为200mL。当消耗标准状况下1.12L
,体积为200mL。当消耗标准状况下1.12L 时,M极区溶液的浓度变为
时,M极区溶液的浓度变为 。(电解前后溶液体积变化忽略不计)。
。(电解前后溶液体积变化忽略不计)。(2)电化学理论在钢铁防腐、废水处理中有着重要应用价值。请按要求回答下列问题:
①下图为探究金属Fe是否腐蚀的示意图,在培养皿中加入一定量的琼脂与饱和NaCl溶液混合,滴入5~6滴酚酞溶液,混合均匀,将缠有铜丝的铁钉放入培养皿中。溶液变红的部位为

②支撑海港码头基础的钢管桩常采用如图所示的方法进行防腐,其中高硅铸铁为惰性辅助阳极。该保护方法叫作

a.钢管桩被迫成为阴极而受到保护,其表面的腐蚀电流接近于零
b.高硅铸铁的作用是作为损耗阳极材料和传递电流
c.通电后,调整外加电压,外电路中的电子被强制从钢管桩流向高硅铸铁
d.石墨能导电且化学性质不活泼,可用石墨代替高硅铸铁作辅助阳极
更新时间:2024-01-02 14:50:26
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】铁、铝及其化合物在生产和生活中有着广泛的应用。
(1)某研究性学习小组设计了如图所示装置探究钢铁的腐蚀与防护。
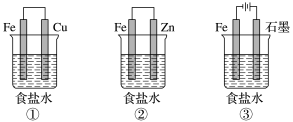
为防止金属Fe被腐蚀,可以采用上述____ (填装置序号)装置原理进行防护:装置③中总反应的离子方程式为_____ 。
(2)用甲烷或其他有机物、氧气为原料可设计成原电池,以CnH2nOn、O2为原料,硫酸溶液为电解质设计成燃料电池,则____ 极的电极反应式为CnH2nOn-4ne-+nH2O=nCO2+4nH+。
(3)图1是在金属锌板上贴上一张用某溶液浸湿的滤纸,图2是NaBH4/H2O2燃料电池。
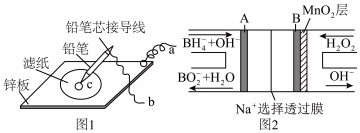
图2电池负极区的电极反应为____ ;若用硫酸钠和酚酞的混合溶液浸湿滤纸,用导线将a、b直接相连,则滤纸出现____ 色,c位置的电极反应式为____ ,若用淀粉-KI溶液浸湿滤纸,用导线将a、b与A、B电极相连,铅笔芯c点处出现蓝色,则b接的是____ (填“A”或“B”)电极。
(1)某研究性学习小组设计了如图所示装置探究钢铁的腐蚀与防护。

为防止金属Fe被腐蚀,可以采用上述
(2)用甲烷或其他有机物、氧气为原料可设计成原电池,以CnH2nOn、O2为原料,硫酸溶液为电解质设计成燃料电池,则
(3)图1是在金属锌板上贴上一张用某溶液浸湿的滤纸,图2是NaBH4/H2O2燃料电池。

图2电池负极区的电极反应为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】过渡元素镍(Ni)、钒(V)、钛(Ti)等在工业上具有广泛的用途,根据原子结构与周期表及元素的性质,向答下列问题:
(1)镍可形成多种配合物,其中[Ni(NH3)6]SO4所含元素电负性最大的为___ (填元素符号),配位体的电子式为___ ,阴离子的立体构型是___ 。
(2)基态23V原子的电子排布式为___ ,其氧化物V2O5难溶于水,可以由VOCl3(易溶于水)水解来制备,反应的化学方程式为___ 。
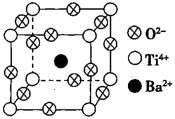
(3)钡钛矿晶体的晶胞结构如图所示,晶胞边长为acm。若该晶体的密度为ρg·cm-3,阿伏加德罗常数的值为NA,则a=___ cm(列出计算式,用ρ表示)。
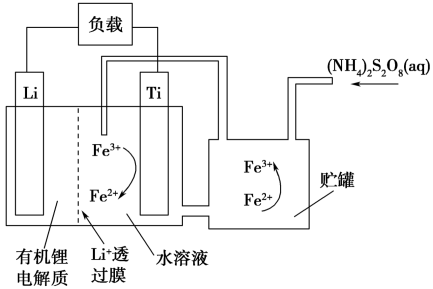
(4)钛可作为电池电极材料应用,在某种锂离子电池中,电池结构如图。写出钛电极上发生的电极反应式___ ,充电时,钛电极与电源___ 极相连。
(1)镍可形成多种配合物,其中[Ni(NH3)6]SO4所含元素电负性最大的为
(2)基态23V原子的电子排布式为
(3)钡钛矿晶体的晶胞结构如图所示,晶胞边长为acm。若该晶体的密度为ρg·cm-3,阿伏加德罗常数的值为NA,则a=

(4)钛可作为电池电极材料应用,在某种锂离子电池中,电池结构如图。写出钛电极上发生的电极反应式

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】碳氮及其化合物广泛存在于自然界中。
Ⅰ、(l)化学家Gethard Ertl证实了氢气与氮气在固体催化剂表面合成氨的过程,示意如图:
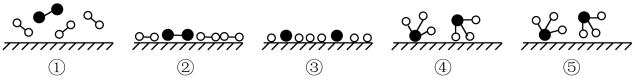
下列说法正确的是___________ (选填字母)。
A.①表示N2、H2分子中均是单键
B.②→③需要吸收能量
C.该过程表示了化学变化中包含旧化学键的断裂和新化学键的生成
(2)氨气分解反应的热化学方程式如下:2NH3(g)⇌N2(g)+3H2(g) △H。若:N≡N键、H-H键和N-H键的键能分别记作a、b和c(单位:kJ•mol﹣l),则上述反应的△H=___________ kJ•mol﹣1。
Ⅱ、(1)CO与H2在一定条件下可反应生成甲醇:CO(g)+2H2(g)=CH3OH(g)。以KOH溶液为电解质溶液,甲醇、空气构成的原电池(图2)作图3的电源,电极M与___________ (填“X”或“Y”)极相连,N极的电极反应式为___________ 。
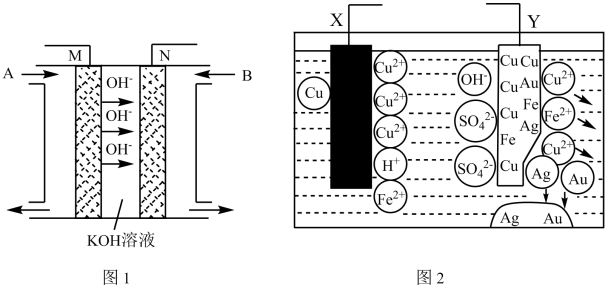
(2)若用图2燃料电池,以惰性电极电解100 mL 0.5 mol/L CuSO4溶液,阳极产生56 mL 标况下气体时,所得溶液的pH 为___________ (不考虑溶液体积变化),若要使电解质溶液恢复到电解前的状态,可加入___________ (填序号)。
A.CuO B.Cu(OH)2 C.CuCO3 D.Cu2(OH)2CO3
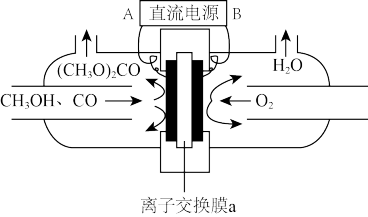
(3)以甲醇和CO为原料通过电化学合成碳酸二甲酯的工作原理如图所示。离子交换膜a为___________ (填“阳膜”或“阴膜”),阳极的电极反应式为___________ 。
Ⅰ、(l)化学家Gethard Ertl证实了氢气与氮气在固体催化剂表面合成氨的过程,示意如图:

下列说法正确的是
A.①表示N2、H2分子中均是单键
B.②→③需要吸收能量
C.该过程表示了化学变化中包含旧化学键的断裂和新化学键的生成
(2)氨气分解反应的热化学方程式如下:2NH3(g)⇌N2(g)+3H2(g) △H。若:N≡N键、H-H键和N-H键的键能分别记作a、b和c(单位:kJ•mol﹣l),则上述反应的△H=
Ⅱ、(1)CO与H2在一定条件下可反应生成甲醇:CO(g)+2H2(g)=CH3OH(g)。以KOH溶液为电解质溶液,甲醇、空气构成的原电池(图2)作图3的电源,电极M与

(2)若用图2燃料电池,以惰性电极电解100 mL 0.5 mol/L CuSO4溶液,阳极产生56 mL 标况下气体时,所得溶液的pH 为
A.CuO B.Cu(OH)2 C.CuCO3 D.Cu2(OH)2CO3
(3)以甲醇和CO为原料通过电化学合成碳酸二甲酯的工作原理如图所示。离子交换膜a为

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】氮化硅(Si3N4)是一种新型陶瓷材料,它可由石英与焦炭在高温的氮气流中,通过以下反应制得:
SiO2(s)+ C(s)+ N2(g) Si3N4(s)+ CO(g)
Si3N4(s)+ CO(g)
(1)配平反应中各物质的化学计量数______ ,已知生成1 mol氮化硅(Si3N4)放出1 591.2 kJ的热量,该反应每转移1 mol e-,放出______ kJ的热量。
(2)该反应的平衡常数表达式为K=____ 。升高温度,其平衡常数______ (选填“增大”“减小”或“不变”)。
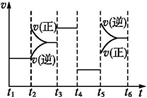
(3)该化学反应速率与反应时间的关系如上图所示,t2时引起v(正)突变、v(逆)渐变的原因是_________ ,t3引起变化的因素为_________ ,t5时引起v(逆)大变化、v(正)小变化的原因是_________ 。
(4)利用右图装置,可以模拟铁的电化学防护。
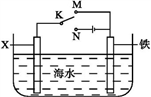
若X为碳棒,为减缓铁的腐蚀,开关K应置于___ 处。若X为锌,开关K置于M处,该电化学防护法称为____________ 。
SiO2(s)+ C(s)+ N2(g)
 Si3N4(s)+ CO(g)
Si3N4(s)+ CO(g)(1)配平反应中各物质的化学计量数
(2)该反应的平衡常数表达式为K=

(3)该化学反应速率与反应时间的关系如上图所示,t2时引起v(正)突变、v(逆)渐变的原因是
(4)利用右图装置,可以模拟铁的电化学防护。

若X为碳棒,为减缓铁的腐蚀,开关K应置于
您最近一年使用:0次
【推荐2】根据有关知识回答下列问题。
(Ⅰ)研究CO2的利用具有现实意义,比如将CO2与焦炭作用生成CO,CO可用于炼铁、设计燃料电池等。
(1)已知:Fe2O3(s)+3C(石墨)=2Fe(s)+3CO(g) ΔH 1 =+489 kJ/mol
C(石墨)+CO2(g)=2CO(g) ΔH 2 = +172 kJ/mol
写出Fe2O3和CO为原料冶炼铁的热化学方程式___________________________ 。
(2)利用CO燃烧反应可设计成CO/O2燃料电池(以H2SO4溶液为电解质溶液),写出该电池的正极反应式_____________________________________ 。
(Ⅱ)初中我们学过铜不能与稀硫酸反应。某学生利用上述CO/O2燃料电池设计了如图所示装置(框内部分未画出),实现了铜与稀硫酸的反应:Cu+H2SO4=H2↑+CuSO4(未注明反应条件)。回答下列问题。

(3)A是石墨棒,B是一种金属,该金属是________ (填名称)。
(4)B应接电源的________ 极(填“通入CO”或“通入O2”)。
(5)写出该装置中发生还原反应的电极反应式___________________________________ 。
(6)若C溶液为100mL饱和食盐水,A和B电极均为石墨棒,该学生连通电路,写出烧杯中反应的离子方程式_________________ ,当放出标况下112mL氢气时,该溶液的pH=_____________ (室温下)。
(Ⅲ)将(Ⅱ)中装置改造成下图装置,可以模拟铁的电化学防护。
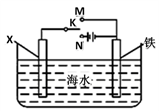
(7)若X为铜,为减缓铁的腐蚀,开关K应置于______ 处。
(8)若X为锌棒,开关K置于M处,该电化学防护法称为________________ 。
(Ⅰ)研究CO2的利用具有现实意义,比如将CO2与焦炭作用生成CO,CO可用于炼铁、设计燃料电池等。
(1)已知:Fe2O3(s)+3C(石墨)=2Fe(s)+3CO(g) ΔH 1 =+489 kJ/mol
C(石墨)+CO2(g)=2CO(g) ΔH 2 = +172 kJ/mol
写出Fe2O3和CO为原料冶炼铁的热化学方程式
(2)利用CO燃烧反应可设计成CO/O2燃料电池(以H2SO4溶液为电解质溶液),写出该电池的正极反应式
(Ⅱ)初中我们学过铜不能与稀硫酸反应。某学生利用上述CO/O2燃料电池设计了如图所示装置(框内部分未画出),实现了铜与稀硫酸的反应:Cu+H2SO4=H2↑+CuSO4(未注明反应条件)。回答下列问题。

(3)A是石墨棒,B是一种金属,该金属是
(4)B应接电源的
(5)写出该装置中发生还原反应的电极反应式
(6)若C溶液为100mL饱和食盐水,A和B电极均为石墨棒,该学生连通电路,写出烧杯中反应的离子方程式
(Ⅲ)将(Ⅱ)中装置改造成下图装置,可以模拟铁的电化学防护。

(7)若X为铜,为减缓铁的腐蚀,开关K应置于
(8)若X为锌棒,开关K置于M处,该电化学防护法称为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】学好化学有助于理解生活中某些现象的本质,从而提高生活质量。
(1)泡菜过酸时加入少量白酒,既可减少酸酸味又可增加香味,该过程生成有机物的类别是________ ,醋汤过酸时,加入少量的面碱(Na2CO3)可以减弱酸味,发生反应的离子方程式是________ 。
(2)在和面炸油条时,加入适量水、明矾和小苏打,可以使油条更蓬松酥脆,这是由于明矾和小苏打在溶液中发生双水解反应,该反应的离子方程式为_________ 。
(3)研究发现,长期使用铁锅炒菜,可有效减少缺铁性贫血病症的发生。炒完菜之后若不及时洗锅擦干,铁锅会发生_________ 腐蚀(选填“化学”或“电化学”),负极发生的电极反应式为________ 。
(4)现需要对农作物同时施用氮肥、磷肥、钾肥三种化肥,对给定的下列化肥①K2CO3②KCl ③Ca(H2PO4)2④(NH)2SO4 ⑤氨水,最适当的组合是_________ .。
a.①③④ b.③⑤ c.②③⑤ d.②③④
(1)泡菜过酸时加入少量白酒,既可减少酸酸味又可增加香味,该过程生成有机物的类别是
(2)在和面炸油条时,加入适量水、明矾和小苏打,可以使油条更蓬松酥脆,这是由于明矾和小苏打在溶液中发生双水解反应,该反应的离子方程式为
(3)研究发现,长期使用铁锅炒菜,可有效减少缺铁性贫血病症的发生。炒完菜之后若不及时洗锅擦干,铁锅会发生
(4)现需要对农作物同时施用氮肥、磷肥、钾肥三种化肥,对给定的下列化肥①K2CO3②KCl ③Ca(H2PO4)2④(NH)2SO4 ⑤氨水,最适当的组合是
a.①③④ b.③⑤ c.②③⑤ d.②③④
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】对金属制品进行抗腐蚀处理,可延长其使用寿命。
(1)以下为铝材表面处理的一种方法:

①碱洗的目的是洗去铝材表面的自然氧化膜,碱洗时候常有气泡冒出,原因是(用离子方程式表示)___________ 。为将碱洗槽液中的铝以沉淀形式回收,最好向槽液中加入下列试剂中的___________ 。
a.NH3 b.CO2 c.NaOH d.HNO3
②以铝材为阳极,在H2SO4溶液中电解,铝材表面形成氧化膜,阳极电极反应式为___________ 。
(2)镀铜可防止铁制品腐蚀,电镀时用铜而不用石墨做阳极的原因是___________ 。
(3)利用图装置,可以模拟铁的电化学防护。

若X为碳棒,为减缓铁的腐蚀,开关K应该置于___________ 处(填“M”或“N”);若X为锌,开关K置于M处,该电化学防护法称为___________ 。
(4)已知:H2O2是弱酸,在碱性条件下以HO2-存在。目前研究比较热门的Al-H2O2燃料电池,其原理如下图所示:

电池总反应如下:2Al+3HO2-=2AlO2-+OH-+H2O 。写出负极反应式为___________ ;写出正极反应式为___________ 。
(1)以下为铝材表面处理的一种方法:

①碱洗的目的是洗去铝材表面的自然氧化膜,碱洗时候常有气泡冒出,原因是(用离子方程式表示)
a.NH3 b.CO2 c.NaOH d.HNO3
②以铝材为阳极,在H2SO4溶液中电解,铝材表面形成氧化膜,阳极电极反应式为
(2)镀铜可防止铁制品腐蚀,电镀时用铜而不用石墨做阳极的原因是
(3)利用图装置,可以模拟铁的电化学防护。

若X为碳棒,为减缓铁的腐蚀,开关K应该置于
(4)已知:H2O2是弱酸,在碱性条件下以HO2-存在。目前研究比较热门的Al-H2O2燃料电池,其原理如下图所示:

电池总反应如下:2Al+3HO2-=2AlO2-+OH-+H2O 。写出负极反应式为
您最近一年使用:0次
【推荐2】含氮化合物的综合利用是当前重要的研究课题。
I.汽车尾气中的 和
和 在一定条件下可发生反应生成无毒的
在一定条件下可发生反应生成无毒的 和
和 。
。
已知:①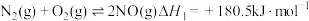
② 的燃烧热
的燃烧热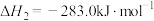
③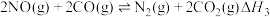 。
。
(1)
_______  ;
;
(2)该反应达到平衡后,为了同时提高反应速率和NO的平衡转化率,可采取的措施包括_______ (填字母序号)。
a.改用高效催化剂
b.恒温恒容条件下,按投料比增大反应物浓度
c.移去
d.升高温度
e.缩小反应容器的体积
 时,将等浓度
时,将等浓度 和NO充入刚性密闭容器中发生上述反应,每隔一定时间测得容器内NO的浓度如下表所示:
和NO充入刚性密闭容器中发生上述反应,每隔一定时间测得容器内NO的浓度如下表所示:
(3)下列可判断以上平衡体系达到平衡状态的包括_______ 。(填序号)
a.
b.混合气体的平均相对分子质量不变
c.容器内的总压强不变
d.
(4)若起始时体系的压强为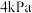 ,反应开始至
,反应开始至 ,体系的压强为
,体系的压强为_______  ,该反应的平衡常数
,该反应的平衡常数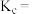
_______ (保留3位有效数字)。
(5)反应达到平衡后,若再向容器中加入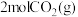 和
和 ,再次达到平衡时
,再次达到平衡时 的百分含量将
的百分含量将_______ (填“增大”“减小”或“不变”)。
Ⅱ.如图所示是一种以液态肼 为燃料,固态氧化物为电解质的新型燃料电池。已知:在工作温度达
为燃料,固态氧化物为电解质的新型燃料电池。已知:在工作温度达 时,
时, 可在该固体氧化物电解质中自由移动,反应生成物均为无毒无害的物质。
可在该固体氧化物电解质中自由移动,反应生成物均为无毒无害的物质。
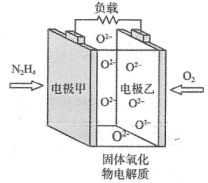
(6)电极甲上发生的电极反应方程式为_______ 。
(7)若想用外加电流的方法保护金属免受腐蚀,金属应该与该电池的_______ (填“电极甲”或“电极乙”)直接相连。
I.汽车尾气中的
 和
和 在一定条件下可发生反应生成无毒的
在一定条件下可发生反应生成无毒的 和
和 。
。已知:①
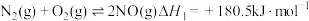
②
 的燃烧热
的燃烧热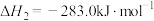
③
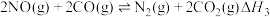 。
。(1)

 ;
;(2)该反应达到平衡后,为了同时提高反应速率和NO的平衡转化率,可采取的措施包括
a.改用高效催化剂
b.恒温恒容条件下,按投料比增大反应物浓度
c.移去

d.升高温度
e.缩小反应容器的体积
 时,将等浓度
时,将等浓度 和NO充入刚性密闭容器中发生上述反应,每隔一定时间测得容器内NO的浓度如下表所示:
和NO充入刚性密闭容器中发生上述反应,每隔一定时间测得容器内NO的浓度如下表所示:时间 | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
浓度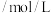 | 1.00 | 0.80 | 0.65 | 0.52 | 0.40 | 0.40 | 0.40 |
(3)下列可判断以上平衡体系达到平衡状态的包括
a.

b.混合气体的平均相对分子质量不变
c.容器内的总压强不变
d.

(4)若起始时体系的压强为
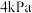 ,反应开始至
,反应开始至 ,体系的压强为
,体系的压强为 ,该反应的平衡常数
,该反应的平衡常数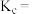
(5)反应达到平衡后,若再向容器中加入
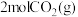 和
和 ,再次达到平衡时
,再次达到平衡时 的百分含量将
的百分含量将Ⅱ.如图所示是一种以液态肼
 为燃料,固态氧化物为电解质的新型燃料电池。已知:在工作温度达
为燃料,固态氧化物为电解质的新型燃料电池。已知:在工作温度达 时,
时, 可在该固体氧化物电解质中自由移动,反应生成物均为无毒无害的物质。
可在该固体氧化物电解质中自由移动,反应生成物均为无毒无害的物质。
(6)电极甲上发生的电极反应方程式为
(7)若想用外加电流的方法保护金属免受腐蚀,金属应该与该电池的
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】Ⅰ、已知下面在298K时的热化学方程式:2H2(g)+O2(g)=2H2O(l) ΔH=-571.6 kJ·mol-1,CH4(g)+2O2(g)=CO2(g)+2H2O (l) ΔH=-890.3 kJ·mol-1,C(s)+O2(g)=CO2(g) ΔH=-393.5kJ·mol-1。根据上面的热化学方程式完成下列问题:
(1)通过计算说明等质量的H2、C、CH4完全燃烧时放出热量最多的是___ 。
(2)根据以上反应,则C(s)+2H2(g)=CH4(g)的焓变ΔH=___ 。
(3)已知H2O(l)=H2O(g) ΔH=+44.0kJ·mol-1
试写出甲烷燃烧生成二氧化碳和水蒸气的热化学方程式:___ 。
Ⅱ、为了解金属腐蚀的原因和寻求防止金属腐蚀的方法具有重要意义。
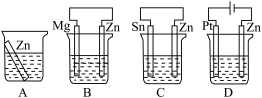
(1)分别放在以下装置(都盛有0.1mol·L-1的H2SO4溶液)中的四块相同的纯锌片,其中腐蚀最快的是___ 。
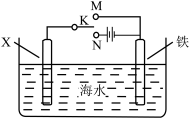
(2)利用如图装置,可以模拟铁的电化学防护。其中X为碳棒,为减缓铁的腐蚀,开关K应置于___ 处。若X为锌,开关K置于M处,该电化学防护法称为___ 。
(1)通过计算说明等质量的H2、C、CH4完全燃烧时放出热量最多的是
(2)根据以上反应,则C(s)+2H2(g)=CH4(g)的焓变ΔH=
(3)已知H2O(l)=H2O(g) ΔH=+44.0kJ·mol-1
试写出甲烷燃烧生成二氧化碳和水蒸气的热化学方程式:
Ⅱ、为了解金属腐蚀的原因和寻求防止金属腐蚀的方法具有重要意义。
(1)分别放在以下装置(都盛有0.1mol·L-1的H2SO4溶液)中的四块相同的纯锌片,其中腐蚀最快的是

(2)利用如图装置,可以模拟铁的电化学防护。其中X为碳棒,为减缓铁的腐蚀,开关K应置于

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】某兴趣小组的同学用下图所示装置研究有关电化学的问题(甲、乙、丙三池中溶质足量),当闭合该装置的电键K时,观察到电流计的指针发生了偏转。请回答下列问题:

(1)甲池为______ (填原电池、电解池或电镀池),通入甲醇电极的电极反应式为________ 。
(2)乙池中B电极为______ (填“正极”、“负极”、“阴极”或“阳极”),该池的总反应化学方程式为________ 。
(3)当乙池中B极质量增重5.4g时,甲池中理论上消耗O2的体积为______ mL(标准状况)。
(4)丙池中,C上的电极反应式为________________ 。如果起始时盛有1000 mL pH=5的硫酸铜溶液(25℃,CuSO4足量),一段时间后溶液的pH变为1。若要使溶液恢复到起始浓度(温度不变,忽略溶液体积的变化),可向溶液中加入_____ (填物质名称),其质量约为_______ g。
(5)若将丙池中两个电极改成等质量的Fe和Cu,实现在Fe上镀Cu,当甲中消耗1.6g甲醇时,丙中两个电极质量差为______ g。

(1)甲池为
(2)乙池中B电极为
(3)当乙池中B极质量增重5.4g时,甲池中理论上消耗O2的体积为
(4)丙池中,C上的电极反应式为
(5)若将丙池中两个电极改成等质量的Fe和Cu,实现在Fe上镀Cu,当甲中消耗1.6g甲醇时,丙中两个电极质量差为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】如图所示,通电5min后,电极5的质量增加2.16g,请回答下列问题:
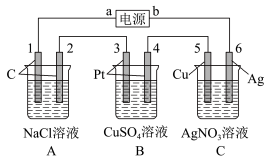
(1)电源a是________ 极,C槽是________ 池。A槽的阴、阳极电极反应:________ ;_______ 。C槽的阴、阳极电极反应:________ ;_______
(2)如果B槽中共收集到224 mL气体(标准状况)且溶液体积为200 mL(设电解过程中溶液体积不变),则通电前溶液中Cu2+的物质的量浓度为_______ 。
(3)室温下如果A槽溶液是200 mL足量的食盐水(电解过程中溶液体积不变),则通电后溶液中氢离子浓度c(H+)=_______ ;

(1)电源a是
(2)如果B槽中共收集到224 mL气体(标准状况)且溶液体积为200 mL(设电解过程中溶液体积不变),则通电前溶液中Cu2+的物质的量浓度为
(3)室温下如果A槽溶液是200 mL足量的食盐水(电解过程中溶液体积不变),则通电后溶液中氢离子浓度c(H+)=
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】Ⅰ.当今社会的主题之一:发展经济,节能减排。而燃料电池因其无污染,且原料来源广可再生被人们青睐,广泛应用于生产、生活、科学研究中,现有如下图所示装置,所有电极均为Pt,请按要求回答下列问题:

(1)写出a极的电极反应_______ 。
(2)当b极消耗标准状况下的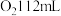 时,若乙中硫酸铜溶液的体积是200mL,假若电解前后溶液体积保持不变,此时乙池中的
时,若乙中硫酸铜溶液的体积是200mL,假若电解前后溶液体积保持不变,此时乙池中的
_______ 。
(3)若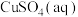 足够,电解一段时间后,要恢复到原来的状态,则可加入_______。(填序号)
足够,电解一段时间后,要恢复到原来的状态,则可加入_______。(填序号)
(4)现用丙装置电解硫酸钾溶液制取氢气、氧气、硫酸和氢氧化钾,其中M、N为离子交换膜,只允许某些离子通过,M为_______ 离子交换膜(填“阴”或“阳”)。
Ⅱ.下图为青铜器在潮湿环境中发生的电化学腐蚀的示意图。
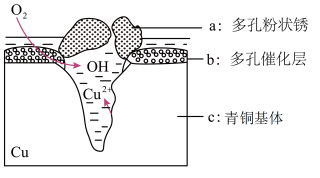
(5)环境中的 扩散到孔口,并与正极反应产物和负极反应产物作用生成多孔铜锈
扩散到孔口,并与正极反应产物和负极反应产物作用生成多孔铜锈 ,其离子方程式为
,其离子方程式为_______ 。
(6)若生成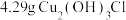 ,则理论上耗氧体积为
,则理论上耗氧体积为_______ L(标准状况)。

(1)写出a极的电极反应
(2)当b极消耗标准状况下的
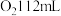 时,若乙中硫酸铜溶液的体积是200mL,假若电解前后溶液体积保持不变,此时乙池中的
时,若乙中硫酸铜溶液的体积是200mL,假若电解前后溶液体积保持不变,此时乙池中的
(3)若
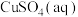 足够,电解一段时间后,要恢复到原来的状态,则可加入_______。(填序号)
足够,电解一段时间后,要恢复到原来的状态,则可加入_______。(填序号)A. | B. | C. | D. |
Ⅱ.下图为青铜器在潮湿环境中发生的电化学腐蚀的示意图。

(5)环境中的
 扩散到孔口,并与正极反应产物和负极反应产物作用生成多孔铜锈
扩散到孔口,并与正极反应产物和负极反应产物作用生成多孔铜锈 ,其离子方程式为
,其离子方程式为(6)若生成
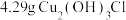 ,则理论上耗氧体积为
,则理论上耗氧体积为
您最近一年使用:0次



