过渡元素镍(Ni)、钒(V)、钛(Ti)等在工业上具有广泛的用途,根据原子结构与周期表及元素的性质,向答下列问题:
(1)镍可形成多种配合物,其中[Ni(NH3)6]SO4所含元素电负性最大的为___ (填元素符号),配位体的电子式为___ ,阴离子的立体构型是___ 。
(2)基态23V原子的电子排布式为___ ,其氧化物V2O5难溶于水,可以由VOCl3(易溶于水)水解来制备,反应的化学方程式为___ 。
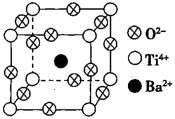
(3)钡钛矿晶体的晶胞结构如图所示,晶胞边长为acm。若该晶体的密度为ρg·cm-3,阿伏加德罗常数的值为NA,则a=___ cm(列出计算式,用ρ表示)。
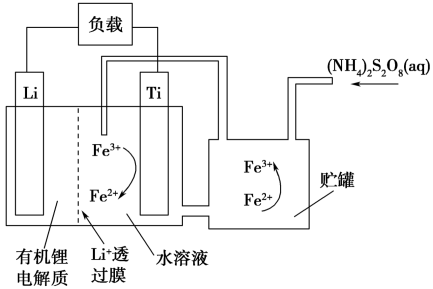
(4)钛可作为电池电极材料应用,在某种锂离子电池中,电池结构如图。写出钛电极上发生的电极反应式___ ,充电时,钛电极与电源___ 极相连。
(1)镍可形成多种配合物,其中[Ni(NH3)6]SO4所含元素电负性最大的为
(2)基态23V原子的电子排布式为
(3)钡钛矿晶体的晶胞结构如图所示,晶胞边长为acm。若该晶体的密度为ρg·cm-3,阿伏加德罗常数的值为NA,则a=

(4)钛可作为电池电极材料应用,在某种锂离子电池中,电池结构如图。写出钛电极上发生的电极反应式

更新时间:2021-05-14 08:42:43
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
【推荐1】分析如图所示装置,完成下列各题。
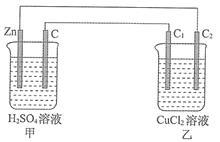
(1)一段时间后,可能发现的现象是:甲池,Zn棒逐渐溶解,石墨棒上有____________ 产生。与Zn棒相连的石墨棒质量____________ (填“增大”“减小”或“不变”)。
(2)甲池Zn极为____________ 极,电极反应式:____________________________________ 。
乙池中C1为____________ 极,电极反应式:____________________________________ 。乙池总反应式:____________________________________ 。

(1)一段时间后,可能发现的现象是:甲池,Zn棒逐渐溶解,石墨棒上有
(2)甲池Zn极为
乙池中C1为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】Ⅰ.回答下列问题
(1)用0.1000mol/L的NaOH溶液滴定20.00mL醋酸溶液,4次滴定所消耗NaOH溶液的体积如下:
①醋酸溶液中 的物质的量浓度为
的物质的量浓度为_______ mol/L。
②滴定过程中以酚酞做指示剂,下列说法正确的是_______ (填序号)。
a.滴定前,需用醋酸溶液润洗锥形瓶
b.滴定终点时,溶液由粉红色恰好变为无色
c.滴定时,溶液中[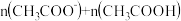 ]始终保持不变
]始终保持不变
③设计实验方案证明醋酸的 大于碳酸的
大于碳酸的 ,将实验操作及现象补充完整:向盛有2mL1mol/L醋酸溶液的试管中滴加
,将实验操作及现象补充完整:向盛有2mL1mol/L醋酸溶液的试管中滴加_______ 。
(2)25℃时,将pH=13的 溶液与pH=2的HCl溶液混合,所得混合溶液pH=7,则
溶液与pH=2的HCl溶液混合,所得混合溶液pH=7,则 溶液与HCl溶液的体积比为
溶液与HCl溶液的体积比为_______ 。
(3)25℃时,pH均为a的 和NaOH溶液中,水电离产生的
和NaOH溶液中,水电离产生的 之比为
之比为_______ 。
(4)向饱和 溶液中滴加饱和
溶液中滴加饱和 溶液,可观察到有白色沉淀和无色气泡产生。结合化学用语,从平衡移动角度解释其原因
溶液,可观察到有白色沉淀和无色气泡产生。结合化学用语,从平衡移动角度解释其原因_______ 。
(5)某工厂废水中含 的
的 ,为使废水能达标排放,作如下处理:
,为使废水能达标排放,作如下处理: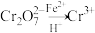 、
、 、
、 。若处理后的废水中残留的
。若处理后的废水中残留的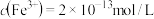 ,则残留的
,则残留的
_______ mol/L。(已知: ,
, )
)
Ⅱ.用甲醇( )燃料电池(装置甲)作为电源,以Ni、Fe作电极,电解浓KOH溶液制备
)燃料电池(装置甲)作为电源,以Ni、Fe作电极,电解浓KOH溶液制备 (装置乙),示意图如下:
(装置乙),示意图如下:
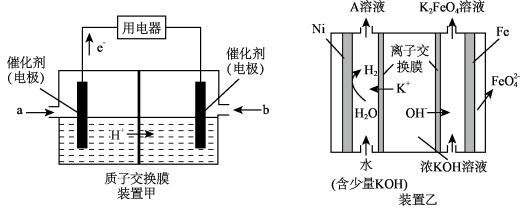
(6)装置甲中,b是_______ (填“甲醇”或“氧气”),负极的电极反应式为_______ 。
(7)装置乙中,Ni电极作_______ 极(填“阴”或“阳”),Fe电极上的电极反应式为_______ 。
(1)用0.1000mol/L的NaOH溶液滴定20.00mL醋酸溶液,4次滴定所消耗NaOH溶液的体积如下:
| 实验次数 | 1 | 2 | 3 | 4 |
| 所消耗NaOH溶液的体积/mL | 20.05 | 20.00 | 18.40 | 19.95 |
①醋酸溶液中
 的物质的量浓度为
的物质的量浓度为②滴定过程中以酚酞做指示剂,下列说法正确的是
a.滴定前,需用醋酸溶液润洗锥形瓶
b.滴定终点时,溶液由粉红色恰好变为无色
c.滴定时,溶液中[
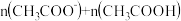 ]始终保持不变
]始终保持不变③设计实验方案证明醋酸的
 大于碳酸的
大于碳酸的 ,将实验操作及现象补充完整:向盛有2mL1mol/L醋酸溶液的试管中滴加
,将实验操作及现象补充完整:向盛有2mL1mol/L醋酸溶液的试管中滴加(2)25℃时,将pH=13的
 溶液与pH=2的HCl溶液混合,所得混合溶液pH=7,则
溶液与pH=2的HCl溶液混合,所得混合溶液pH=7,则 溶液与HCl溶液的体积比为
溶液与HCl溶液的体积比为(3)25℃时,pH均为a的
 和NaOH溶液中,水电离产生的
和NaOH溶液中,水电离产生的 之比为
之比为(4)向饱和
 溶液中滴加饱和
溶液中滴加饱和 溶液,可观察到有白色沉淀和无色气泡产生。结合化学用语,从平衡移动角度解释其原因
溶液,可观察到有白色沉淀和无色气泡产生。结合化学用语,从平衡移动角度解释其原因(5)某工厂废水中含
 的
的 ,为使废水能达标排放,作如下处理:
,为使废水能达标排放,作如下处理: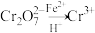 、
、 、
、 。若处理后的废水中残留的
。若处理后的废水中残留的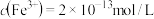 ,则残留的
,则残留的
 ,
, )
)Ⅱ.用甲醇(
 )燃料电池(装置甲)作为电源,以Ni、Fe作电极,电解浓KOH溶液制备
)燃料电池(装置甲)作为电源,以Ni、Fe作电极,电解浓KOH溶液制备 (装置乙),示意图如下:
(装置乙),示意图如下:
(6)装置甲中,b是
(7)装置乙中,Ni电极作
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】如图所示,某同学设计了一个燃料电池并探究氯碱工业原理的相关问题,其中乙装置中X为离子交换膜。请按要求回答相关问题:
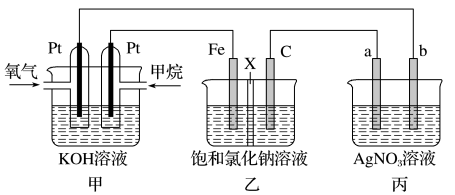
(1)甲烷燃料电池负极发生__________ 反应(“氧化”或“还原”)电极反应式是:______ 。
(2)乙中X是_________ 交换膜,向乙中加入几滴酚酞溶液,工作一段时间后铁电极附近溶液变红,请用化学用语解释相关原因______
(3)若在标准状况下,有4.48 L氧气参加反应,则乙装置中C电极上生成的气体的物质的量为__________ 。
(4)欲用丙装置给铜镀银,b应是____________ (填化学式)。
(5)化学在环境保护中起十分重要的作用,电化学降解法可用于治理水中硝酸盐污染,电化学降解NO 的原理如图所示。
的原理如图所示。
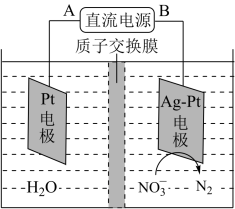
Ag-Pt电极上的电极反应式为_________ 。

(1)甲烷燃料电池负极发生
(2)乙中X是
(3)若在标准状况下,有4.48 L氧气参加反应,则乙装置中C电极上生成的气体的物质的量为
(4)欲用丙装置给铜镀银,b应是
(5)化学在环境保护中起十分重要的作用,电化学降解法可用于治理水中硝酸盐污染,电化学降解NO
 的原理如图所示。
的原理如图所示。
Ag-Pt电极上的电极反应式为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】2021年诺贝尔化学奖授予B.List与D.MacMillan两位科学家在“不对称有机催化”方面做出的杰出贡献。被誉为“第三类催化剂”的有机催化剂的特点是有一个由碳原子组成的稳定架构,搭配氧、氮、硫、磷等元素。化合物Ⅰ与Ⅱ均是重要的有机催化剂。
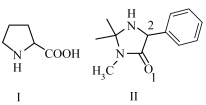
(1)基态H、C、N、O原子中,单电子数最多的是_______ (填元素符号,下同),电负性最大的是_______ 。
(2)化合物Ⅰ中碳原子采用的杂化方式为_______ ,化合物Ⅰ水溶性特别好,可能原因是________ 。
(3)关于化合物Ⅱ,以下说法正确的是_______ 。
A.在Ⅱ中所有C原子均形成极性共价键与非极性共价键
B.在Ⅱ中含有的五元环结构是正方形
C.1号O原子可与2号H原子产生分子内氢键,降低Ⅱ的沸点
D.Ⅱ属于极性分子
E.C-C键长小于C-N键
(4)科学家最早接触的“第一类催化剂”是过渡金属,比如铁、锰、镍等氧化物。
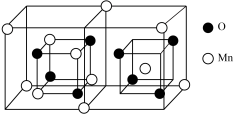
①已知锰的氧化物有多种,且科研工作者常使用MnxOy来表示各种锰氧化物。以下为某种锰的氧化物样品的晶胞结构,其化学式为_______ 。
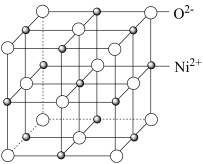
②纯粹的NiO晶体具有NaCl型晶胞结构,若将顶点O2-平移至棱心,则体心Ni2+的位置为_______ (填“体心”“棱心”“面心”“顶点”)。已知晶胞参数为a=425.43pm,晶胞密度ρ=6.47g•cm-3,则阿伏伽德罗常数NA=_______ (列出计算式)。

(1)基态H、C、N、O原子中,单电子数最多的是
(2)化合物Ⅰ中碳原子采用的杂化方式为
(3)关于化合物Ⅱ,以下说法正确的是
A.在Ⅱ中所有C原子均形成极性共价键与非极性共价键
B.在Ⅱ中含有的五元环结构是正方形
C.1号O原子可与2号H原子产生分子内氢键,降低Ⅱ的沸点
D.Ⅱ属于极性分子
E.C-C键长小于C-N键
(4)科学家最早接触的“第一类催化剂”是过渡金属,比如铁、锰、镍等氧化物。
①已知锰的氧化物有多种,且科研工作者常使用MnxOy来表示各种锰氧化物。以下为某种锰的氧化物样品的晶胞结构,其化学式为

②纯粹的NiO晶体具有NaCl型晶胞结构,若将顶点O2-平移至棱心,则体心Ni2+的位置为

您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】图表法是常用的科学研究方法,表中列出了同周期的五种短周期元素的部分性质(“电负性”即元素对应原子吸引电子能力的标度):
请回答下列问题:
(1)写出E元素的离子结构示意图:_______ 。
(2)X的值可能为_______ (填字母)。
A.3.6 B.3.1 C.2.1 D.1.4
(3)分析表中数据,简述同周期元素(惰性气体除外)电负性大小与原子半径的关系:_______ 。
(4)A、B、C三种元素形成的氢化物中,其稳定性由强到弱的顺序是_______ (用化学式表示)。
(5)A、D最高价氧化物对应水化物相互反应的化学方程式为_______ 。
(6)D、E最高价氧化物对应水化物相互反应的离子方程式为_______
(7)B和氢气化合后生成物的电子式为_______
| 元素 编号 | A | B | C | D | E |
| 电负性 | 3.0 | 2.5 | X | 1.5 | 0.9 |
| 原子 半径/ nm | 0.099 | 0.102 | 0.110 | 0.143 | 0.186 |
| 主要 化合价 | -1,+7 | -2,+6 | -3,+5 | +3 | +1 |
(1)写出E元素的离子结构示意图:
(2)X的值可能为
A.3.6 B.3.1 C.2.1 D.1.4
(3)分析表中数据,简述同周期元素(惰性气体除外)电负性大小与原子半径的关系:
(4)A、B、C三种元素形成的氢化物中,其稳定性由强到弱的顺序是
(5)A、D最高价氧化物对应水化物相互反应的化学方程式为
(6)D、E最高价氧化物对应水化物相互反应的离子方程式为
(7)B和氢气化合后生成物的电子式为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】G、M、R、X、Y、W、Q、T为原子序数依次增大的前四周期元素。G的一种简单粒子是一个质子,M基态原子L层中p轨道电子数是s轨道电子数的2倍,R原子K层的电子数与M层的电子数的乘积等于其L层的电子数,X和M形成的一种化合物是引起酸雨的主要大气污染物,Y与X同周期且相邻,W是第一种过渡元素,Q位于第ⅠB族,T元素最高正价和最低负价的代数和为4。请回答下列问题:
(1)W的元素符号___________ ,Q在周期表的第___________ 列,T基态原子的简化电子排布式是___________ 。
(2)X与M形成的XM3分子的VSEPR模型是___________ ,GYM的电子式为___________ 。
(3)R与M可以形成多种复杂阴离子,如下图所示,若其中a对应的阴离子化学式为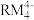 ,则c对应的阴离子的化学式为
,则c对应的阴离子的化学式为___________ (圆圈代表M原子,黑点代表R原子)。
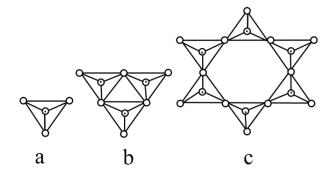
(4)R、T均能与氢元素形成气态氢化物,则它们形成的组成最简单的氢化物中,中心原子杂化类型___________ (填“相同”或“不相同”),若“R-H”中共用电子对偏向氢元素,氢气与T反应时单质T是氧化剂,则R与T的电负性相对大小为___________ (用元素符号作答)。
(5)已知高温下4QM→2Q2M+M2,从Q原子价层电子结构的角度分析,能生成Q2M的原因是___________ 。
(6)已知AlY3通常以二聚体(Al2Y6)形式存在,画出其二聚体的结构式___________ (标出配位键)
(1)W的元素符号
(2)X与M形成的XM3分子的VSEPR模型是
(3)R与M可以形成多种复杂阴离子,如下图所示,若其中a对应的阴离子化学式为
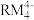 ,则c对应的阴离子的化学式为
,则c对应的阴离子的化学式为
(4)R、T均能与氢元素形成气态氢化物,则它们形成的组成最简单的氢化物中,中心原子杂化类型
(5)已知高温下4QM→2Q2M+M2,从Q原子价层电子结构的角度分析,能生成Q2M的原因是
(6)已知AlY3通常以二聚体(Al2Y6)形式存在,画出其二聚体的结构式
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】铁铜是人类最早大规模使用的金属,它们的化合物在科学研究和工业生产中具有许多用途。请回答以下问题:
(1)铁元素在周期表中的位置是____ ,铜的基态原子核外电子排布式为______ 。
(2)二茂铁[Fe(C5H5)2],橙色晶型固体,有类似樟脑的气味,抗磁性。熔点172.5~173℃,100℃以上升华,沸点249℃。据此判断二茂铁晶体类型为______________ 。
(3)蓝矾(CuSO4·5H2O)的结构如下图所示:
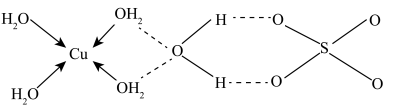
图中虚线表示_____________ ,SO42-的立体构型是__________ ,NO3-中N原子的杂化轨道类型是___________ ;O原子的价电子排布图为__________________ 。
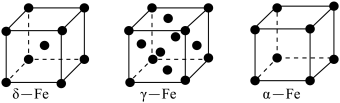
(4)铁有δ、γ、α三种同素异形体,下图是它们的晶体结构图,三种晶体中铁原子周围距离最近的铁原子个数之比为______ 。
(5)某种具有储氢功能的铜合金晶体具有立方最密堆积的结构,晶胞中Cu原子处于面心,Au原子处于顶点位置,氢原子可进入到由Cu原子与Au原子构成的四面体空隙中。若将Cu原子与Au原子等同看待,该晶体储氢后的晶胞结构与 CaF2的结构(晶胞结构如图)相似,该晶体储氢后的化学式为________ 。

(1)铁元素在周期表中的位置是
(2)二茂铁[Fe(C5H5)2],橙色晶型固体,有类似樟脑的气味,抗磁性。熔点172.5~173℃,100℃以上升华,沸点249℃。据此判断二茂铁晶体类型为
(3)蓝矾(CuSO4·5H2O)的结构如下图所示:

图中虚线表示
(4)铁有δ、γ、α三种同素异形体,下图是它们的晶体结构图,三种晶体中铁原子周围距离最近的铁原子个数之比为

(5)某种具有储氢功能的铜合金晶体具有立方最密堆积的结构,晶胞中Cu原子处于面心,Au原子处于顶点位置,氢原子可进入到由Cu原子与Au原子构成的四面体空隙中。若将Cu原子与Au原子等同看待,该晶体储氢后的晶胞结构与 CaF2的结构(晶胞结构如图)相似,该晶体储氢后的化学式为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】不锈钢以其优异的抗腐蚀性能越来越受到人们的青睐,它主要是由铁、铬、镍、铜、碳等元素所组成的合金。请完成以下有关物质结构的问题:
(1)写出Fe2+的最高能层的电子排布式:________________ 。
(2)[Cr(H2O)4Cl2] Cl·2H2O中Cr的配位数为________________ ;
已知CrO5中Cr为+6价,则CrO5的结构式为________ 。
(3)金属镍粉在CO气流中轻微加热,生成无色挥发性液体Ni(CO)n,推测Ni(CO)n的晶体类型为_______ ;已知该物质的中心原子价电子数与配体提供电子总数之和为18,则n=__________ ;与Ni(CO)n中配体互为等电子体的阴离子化学式为________________ 。
(4)金刚砂(SiC)结构与金刚石结构相似,若将金刚石晶体中一半的C原子换成Si原子且同种原子不成键,则得到金刚砂(SiC)结构。SiC是_________ 晶体,键角是_________ ;在SiC中,如果以一个硅原子为中心,则与硅原子次近的第二层有________ 个硅原子。
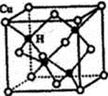
(5)铜是第四周期最重要的过渡元素之一,其单质及化合物具有广泛用途。CuH的晶体结构如下图所示,若CuH的密度为d g·cm-3,阿伏伽德罗常数的值为NA,则该晶胞的边长为______ cm(用含d和Na的式子表示)。
(1)写出Fe2+的最高能层的电子排布式:
(2)[Cr(H2O)4Cl2] Cl·2H2O中Cr的配位数为
已知CrO5中Cr为+6价,则CrO5的结构式为
(3)金属镍粉在CO气流中轻微加热,生成无色挥发性液体Ni(CO)n,推测Ni(CO)n的晶体类型为
(4)金刚砂(SiC)结构与金刚石结构相似,若将金刚石晶体中一半的C原子换成Si原子且同种原子不成键,则得到金刚砂(SiC)结构。SiC是
(5)铜是第四周期最重要的过渡元素之一,其单质及化合物具有广泛用途。CuH的晶体结构如下图所示,若CuH的密度为d g·cm-3,阿伏伽德罗常数的值为NA,则该晶胞的边长为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】钛是一种非常优越的金属,尤其是抵抗海水腐蚀的能力很强,被称为继铁、铝之后的第三金属。回答下列问题:
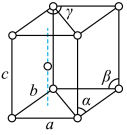
(1)基态钛原子的价电子排布式为_________________ 。金属钛晶胞如图所示,晶胞参数a=b=295.08pm,c=468.55pm,α=β=90°,γ=120°。金属钛为______ 堆积(填堆积方式),其中钛原子的配位数为__ 。
(2)现有Ti3+的配合物[TiCl(H2O)5]Cl2·H2O。该配合物的配体是_________ ,配位数是_______ 。
(3)C、N、O等元素可与钛形成二元化合物。C、N、O元素的电负性由大到小的顺序是__________ 。已知:中心原子相同时,配位原子的电负性越大,键角越小;配位原子相同时,中心原子的电负性越大,键角越大,则NF3、PF3、NH3的键角由大到小的顺序为_____________ ,乙二胺(H2N-CH2-CH2-NH2)和三甲胺[N(CH3)3]均属于胺,但乙二胺比三甲胺的沸点高的多,原因______________ 。
(4)钙钛矿晶体的结构如图所示。晶体的化学式为____________________ 。晶胞中的原子可用x、y、z组成的三数组来表达它在晶胞中的位置,称为原子坐标。已知原子坐标为A(0,0,0);B(0, ,0);则Ca离子的原子坐标为
,0);则Ca离子的原子坐标为__________________ 。
(1)基态钛原子的价电子排布式为

(2)现有Ti3+的配合物[TiCl(H2O)5]Cl2·H2O。该配合物的配体是
(3)C、N、O等元素可与钛形成二元化合物。C、N、O元素的电负性由大到小的顺序是
(4)钙钛矿晶体的结构如图所示。晶体的化学式为
 ,0);则Ca离子的原子坐标为
,0);则Ca离子的原子坐标为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】(I)多项选择题
下列说法中正确的是_______ 。
A.丙烯分子中有8个σ键,1个π键
B.在SiO2晶体中,1个Si原子和2个O原子形成2个共价键
C.NF3的沸点比NH3的沸点低得多,是因为NH3分子间有氢键,NF3只有范德华力
D.NCl3和BC13分子中,中心原子都采用sp3杂化
E.SO3与CO32-互为等电子体,SO3是极性分子
(II)人类在使用金属的历史进程中,经历了铜、铁、铝之后,第四种将被广泛应用的金属被科学家预测是钛(Ti),它被誉为“未来世纪的金属”。试回答下列问题:
(1)Ti元素在元素周期表中的位置是第________ 周期第________ 族;其基态原子的电子排布式为________ 。
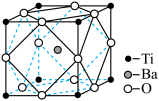
(2)在Ti的化合物中,可以呈现+2、+3、+4三种化合价,其中以+4价的Ti最为稳定。偏钛酸钡的热稳定性好,介电常数高,在小型变压器、话筒和扩音器中都有应用.偏钛酸钡晶体中晶胞的结构示意图如右图所示,它的化学式是___________ ,其中Ti4+的氧配位数为________ ,Ba2+的氧配位数为_________ ,
(3)常温下的TiCl4是有刺激性臭味的无色透明液体,熔点-23.2℃,沸点136.2℃,所以TiCl4是_______ 晶体。
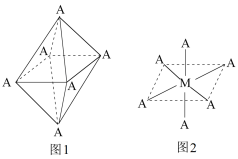
4)已知Ti3+可形成配位数为6的配合物,其空间构型为正八面体,如下图1所示,我们通常可以用下图2所示的方法来表示其空间构型(其中A表示配体,M表示中心原子)。配位化合物[Co(NH3)4Cl2]的空间构型也为八面体型,它有_______ 种同分异构体。
(Ⅲ)
(1)已知过氧化氢分子的空间结构如右图所示,分子中氧原子采取______ 杂化。
(2)R是1~36号元素中未成对电子数最多的原子。R3+在溶液中存在如下转化关系:
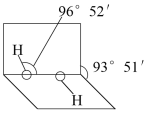
R3+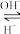 R(OH)3
R(OH)3 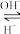 [R(OH)4]-
[R(OH)4]-
①基态R原子的价电子排布式为_______________________ ;
②[R(OH)4]-中存在的化学键是____________ 。
A.离子键 B.极性键 C.非极性键 D.配位键
下列说法中正确的是
A.丙烯分子中有8个σ键,1个π键
B.在SiO2晶体中,1个Si原子和2个O原子形成2个共价键
C.NF3的沸点比NH3的沸点低得多,是因为NH3分子间有氢键,NF3只有范德华力
D.NCl3和BC13分子中,中心原子都采用sp3杂化
E.SO3与CO32-互为等电子体,SO3是极性分子
(II)人类在使用金属的历史进程中,经历了铜、铁、铝之后,第四种将被广泛应用的金属被科学家预测是钛(Ti),它被誉为“未来世纪的金属”。试回答下列问题:
(1)Ti元素在元素周期表中的位置是第
(2)在Ti的化合物中,可以呈现+2、+3、+4三种化合价,其中以+4价的Ti最为稳定。偏钛酸钡的热稳定性好,介电常数高,在小型变压器、话筒和扩音器中都有应用.偏钛酸钡晶体中晶胞的结构示意图如右图所示,它的化学式是

(3)常温下的TiCl4是有刺激性臭味的无色透明液体,熔点-23.2℃,沸点136.2℃,所以TiCl4是
4)已知Ti3+可形成配位数为6的配合物,其空间构型为正八面体,如下图1所示,我们通常可以用下图2所示的方法来表示其空间构型(其中A表示配体,M表示中心原子)。配位化合物[Co(NH3)4Cl2]的空间构型也为八面体型,它有

(Ⅲ)
(1)已知过氧化氢分子的空间结构如右图所示,分子中氧原子采取
(2)R是1~36号元素中未成对电子数最多的原子。R3+在溶液中存在如下转化关系:

R3+
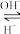 R(OH)3
R(OH)3 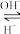 [R(OH)4]-
[R(OH)4]-①基态R原子的价电子排布式为
②[R(OH)4]-中存在的化学键是
A.离子键 B.极性键 C.非极性键 D.配位键
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】钴及其化合物在工业生产中具有广泛的用途,特别是作为工业生产的催化剂,钴及其化合物发挥了重要的作用。请回答下列问题:
(1)钴及其化合物广泛用作催化剂,说明钴元素在元素周期表中的位置为_______(填字母)。
(2)中国科学院院士、大连化学物理研究所研究员张涛及其团队开发出新型双原子催化剂(DACs),在丙烷脱氢性能上,该新型双原子催化剂优于单原子催化剂,其催化原理如图所示:_______ ,N原子为 杂化,未杂化的p轨道中容纳的电子数为
杂化,未杂化的p轨道中容纳的电子数为_______ 个;Zn或Co与N原子形成配位键时,提供孤电子对的原子是_______ (填元素符号);丙烷分解为丙烯的过程中,形成的化学键有_______ (填字母)。
A. 键 B.σ键 C.π键
键 B.σ键 C.π键
(3)CoO是石油化工中的一种催化剂,一种CoO的晶胞结构如图所示,该立方晶胞边长为a pm,设阿伏加德罗常数的值为 。
。 的分数坐标为
的分数坐标为_______ ;每个 周围与其距离最近且相等的
周围与其距离最近且相等的 共有
共有_______ 个;该CoO晶体的密度是_______ g⋅cm (用含a、
(用含a、 的代数式表示)。
的代数式表示)。
(1)钴及其化合物广泛用作催化剂,说明钴元素在元素周期表中的位置为_______(填字母)。
| A.主族元素 | B.金属与非金属分界线 |
| C.稀土元素 | D.过渡金属元素 |
(2)中国科学院院士、大连化学物理研究所研究员张涛及其团队开发出新型双原子催化剂(DACs),在丙烷脱氢性能上,该新型双原子催化剂优于单原子催化剂,其催化原理如图所示:

 杂化,未杂化的p轨道中容纳的电子数为
杂化,未杂化的p轨道中容纳的电子数为A.
 键 B.σ键 C.π键
键 B.σ键 C.π键(3)CoO是石油化工中的一种催化剂,一种CoO的晶胞结构如图所示,该立方晶胞边长为a pm,设阿伏加德罗常数的值为
 。
。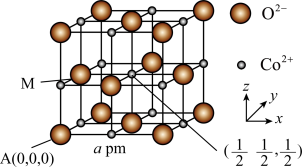
 的分数坐标为
的分数坐标为 周围与其距离最近且相等的
周围与其距离最近且相等的 共有
共有 (用含a、
(用含a、 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】形形色色的物质,构成了我们这个五彩缤纷的世界。世上万物,神奇莫测,常常超乎人们按“常理"的想象。学习物质结构和性质的知识,能使你想象的翅膀变得更加有力。
(1)基态Ga原子的核外电子排布式是[Ar]__ ,基态Ga原子核外电子占据最高能级的电子云轮廓图为___ 。
(2)HC≡CNa(乙炔钠)广泛用于有机合成,乙炔钠中C原子的杂化类型为__ 。乙炔钠中存在___ (填字母)。
A.金属键 B.σ键 C.π键 D.氢键 E.配位键 F.离子键 G.范德华力
(3)NaN3是汽车安全气囊中的主要化学成分,其阴离子的立体构型为___ 。写出和该阴离子互为等电子体的一种分子的结构式___ 。
(4)配体中配位原子提供孤电子对的能力与元素的电负性有关,SCN-的结构式可以表示为[S=C=N]-或[S-C≡N]-,SCN-与Fe3+、Au+和Hg2+等离子能形成配离子,N、C、S的电负性依次为3.0、2.5和2.5。SCN-中提供孤电子对的原子可能是___ 。
(5)某离子晶体的晶胞结构如图所示。
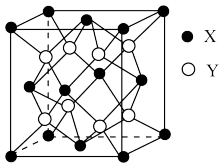
①晶体中在每个X周围与它最近且距离相等的X共有___ 个。
②设该晶体的摩尔质量为Mg·mol-1,晶胞的密度为ρg·cm-3,阿伏加 德罗常数为NA,则晶体中两个最近的X间的距离为___ cm。
(1)基态Ga原子的核外电子排布式是[Ar]
(2)HC≡CNa(乙炔钠)广泛用于有机合成,乙炔钠中C原子的杂化类型为
A.金属键 B.σ键 C.π键 D.氢键 E.配位键 F.离子键 G.范德华力
(3)NaN3是汽车安全气囊中的主要化学成分,其阴离子的立体构型为
(4)配体中配位原子提供孤电子对的能力与元素的电负性有关,SCN-的结构式可以表示为[S=C=N]-或[S-C≡N]-,SCN-与Fe3+、Au+和Hg2+等离子能形成配离子,N、C、S的电负性依次为3.0、2.5和2.5。SCN-中提供孤电子对的原子可能是
(5)某离子晶体的晶胞结构如图所示。

①晶体中在每个X周围与它最近且距离相等的X共有
②设该晶体的摩尔质量为Mg·mol-1,晶胞的密度为ρg·cm-3,阿伏加 德罗常数为NA,则晶体中两个最近的X间的距离为
您最近一年使用:0次



