现有含有少NaCl、 、
、 等杂质的
等杂质的 溶液,选择适当的试剂除去杂质,得到纯净的
溶液,选择适当的试剂除去杂质,得到纯净的 固体,实验流程如下图所示。
固体,实验流程如下图所示。

(1)沉淀A的主要成分是___________ (填化学式)。
(2)③加入过量的Y的目的是___________ 。
(3)溶液3中肯定含有的杂质是___________ ,为除去杂质可向溶液3中加入过量的___________ 。
 、
、 等杂质的
等杂质的 溶液,选择适当的试剂除去杂质,得到纯净的
溶液,选择适当的试剂除去杂质,得到纯净的 固体,实验流程如下图所示。
固体,实验流程如下图所示。 
(1)沉淀A的主要成分是
(2)③加入过量的Y的目的是
(3)溶液3中肯定含有的杂质是
更新时间:2024-01-02 18:19:25
|
相似题推荐
解答题-无机推断题
|
较难
(0.4)
【推荐1】某无色溶液中含有K+、Cl-、OH-、SO 、SO
、SO ,为检验溶液中所含的各种阴离子,限用的试剂有:盐酸、硝酸、硝酸银溶液、硝酸钡溶液和溴水。检验其中OH-的实验方法从略,检验其他阴离子的过程如下图所示。
,为检验溶液中所含的各种阴离子,限用的试剂有:盐酸、硝酸、硝酸银溶液、硝酸钡溶液和溴水。检验其中OH-的实验方法从略,检验其他阴离子的过程如下图所示。
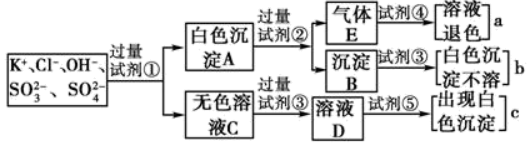
(1)图中试剂①~⑤溶质的化学式分别是:①___________ ,②___________ ,③___________ ,④___________ ,⑤___________ 。
(2)图中现象a、b、c表明检验出的离子分别是:a___________ ,b___________ ,c___________ 。
(3)白色沉淀A加试剂②反应的离子方程式是___________ 。
(4)白色沉淀A若加试剂③而不加试剂②,对实验的影响是___________ 。
(5)气体E通入试剂④发生反应的离子方程式是___________ 。
 、SO
、SO ,为检验溶液中所含的各种阴离子,限用的试剂有:盐酸、硝酸、硝酸银溶液、硝酸钡溶液和溴水。检验其中OH-的实验方法从略,检验其他阴离子的过程如下图所示。
,为检验溶液中所含的各种阴离子,限用的试剂有:盐酸、硝酸、硝酸银溶液、硝酸钡溶液和溴水。检验其中OH-的实验方法从略,检验其他阴离子的过程如下图所示。
(1)图中试剂①~⑤溶质的化学式分别是:①
(2)图中现象a、b、c表明检验出的离子分别是:a
(3)白色沉淀A加试剂②反应的离子方程式是
(4)白色沉淀A若加试剂③而不加试剂②,对实验的影响是
(5)气体E通入试剂④发生反应的离子方程式是
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐2】有A、B、C、D、E、F、G,7瓶不同物质的溶液,它们各是Na2CO3、Na2SO4、KCl、AgNO3、MgCl3、Ca(NO3)2和Ba (OH )2溶液中的一种。为了鉴别,各取少量溶液进行两两混合,实验结果如表所示。表中“↓”表示生成沉淀或微溶化合物,“-”表示观察不到明显变化。试回答下面问题。(已知AgOH微溶于水)
(1)A的化学式是____ ,G的化学式是_____ 。判断理由是_________________ 。
(2)写出其余几种物质的化学式。B:_____ ,C:_____ ,D:_____ ,E:_____ ,F:_____ 。
| A | B | C | D | E | F | G | |
| A | - | - | - | - | - | - | ↓ |
| B | - | - | - | - | ↓ | ↓ | ↓ |
| C | - | - | ― | ↓ | — | ↓ | ↓ |
| D | - | ↓ | - | ↓ | ↓ | ↓ | |
| E | - | ↓ | - | ↓ | - | ↓ | - |
| F | - | ↓ | ↓ | ↓ | ↓ | - | ↓ |
| G | ↓ | ↓ | ↓ | ↓ | - | ↓ | - |
(1)A的化学式是
(2)写出其余几种物质的化学式。B:
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐3】为了除去KCl溶液中少量的MgCl2、MgSO4,可选用Ba(OH)2、HCl和K2CO3三种试剂,按下图步骤操作:
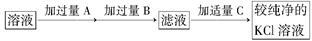
(1)写出三种试剂的化学式:A________ ,B________ ,C________ 。
(2)加过量A的原因是:__________________ ,
有关反应的化学方程式为:__________________ ,_________________ 。
(3)加过量B的原因是:__________________________ ,
有关反应的化学方程式为:_________________________ 。

(1)写出三种试剂的化学式:A
(2)加过量A的原因是:
有关反应的化学方程式为:
(3)加过量B的原因是:
有关反应的化学方程式为:
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐1】某研究性学习小组设计实验用30mL浓硫酸与10mL无水乙醇共热制备乙烯气体、并测定乙醇转化成乙烯的转化率。已知生成的乙烯气体中含有SO2、CO2、乙醇和乙醚等杂质。有关数据如下:
(1)制备乙烯
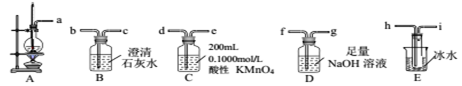
① 从A~E中选择必要的装置完成实验,并按气流方向连接的顺序为________ (填仪器接口的字母编号)。
② D装置中发生反应的离子方程式_____________ 实验后,检验D溶液中含有CO32-的实验方案为______________ 。
③ E装置的主要作用是__________________ 。
(2)测定乙烯
反应结束后,用移液管移取C中溶液20mL(不考虑溶液体积变化)于锥形瓶中,先加入约2mL稀硫酸酸化.再用0.1000mol/L的Na2C2O4溶液滴定未反应完的KMnO4。
已知:C2H4 CO2+H2O;C2O42-
CO2+H2O;C2O42-  CO2+H2O;MnO4-→Mn2+
CO2+H2O;MnO4-→Mn2+
④ 以下情况使得测定乙烯的量偏高的是( )
A.在用蒸馏水清洗碱式滴定管后,直接装Na2C2O4标准液
B.锥形瓶清洗干净后残有大量水珠
C.滴定前,滴定管内无气泡,滴定后有气泡
D.读数时,滴定前平视,滴定后俯视
⑤ 油定终点的现象为_______________ 。
⑥ 已知用去Na2C2O4溶液20.00mL,则乙醇转化成乙烯的转化率为___________ 。
| 熔点/℃ | 沸点/℃ | 溶解性 | 颜色状态 | 密度g/cm3 | |
| 乙醇 | -114.1 | 78.3 | 与水、有机溶剂互溶 | 无色液体 | 0.79 |
| 乙醚 | -116.2 | 34.5 | 不溶于水,易溶于有机溶剂 | 无色液体 | 0.7135 |

① 从A~E中选择必要的装置完成实验,并按气流方向连接的顺序为
② D装置中发生反应的离子方程式
③ E装置的主要作用是
(2)测定乙烯
反应结束后,用移液管移取C中溶液20mL(不考虑溶液体积变化)于锥形瓶中,先加入约2mL稀硫酸酸化.再用0.1000mol/L的Na2C2O4溶液滴定未反应完的KMnO4。
已知:C2H4
 CO2+H2O;C2O42-
CO2+H2O;C2O42-  CO2+H2O;MnO4-→Mn2+
CO2+H2O;MnO4-→Mn2+④ 以下情况使得测定乙烯的量偏高的是
A.在用蒸馏水清洗碱式滴定管后,直接装Na2C2O4标准液
B.锥形瓶清洗干净后残有大量水珠
C.滴定前,滴定管内无气泡,滴定后有气泡
D.读数时,滴定前平视,滴定后俯视
⑤ 油定终点的现象为
⑥ 已知用去Na2C2O4溶液20.00mL,则乙醇转化成乙烯的转化率为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐2】亚氯酸钠(NaClO2)是一种重要的消毒剂,主要用于水、砂糖、油脂的漂白与杀菌。以下是制取亚氯酸钠的工艺流程:
已知:①NaClO2的溶解度随着温度升高而增大,适当条件下可结晶析出。
②ClO2气体在中性和碱性溶液中不能稳定存在。
回答下列问题:
(1)用于电解的食盐水需先除去其中的Ca2+、Mg2+、SO42-等杂质。除杂操作时,往粗盐水中先加入过量的_________ (填化学式),至沉淀不再产生后。再加入过里的Na2CO3和NaOH,充分反应后将沉淀一并滤去。在无隔膜电解槽中用惰性电极电解一段时间生成NaClO3,阳极反应式为_______
(2)X酸是_________ 。写出二氧化氯发生器中生成ClO2的化学方程式_______ ,吸收塔内的温度不宜过高的原因为________
(3)亚氯酸钠在溶液中可生成ClO2、HClO2、ClO2-、Cl-等,其中HClO2和ClO2都具有漂白作用,但ClO2有毒,经测定,25℃时各组分含量随pH变化情况如图所示(Cl-没有画出)。则下列分析正确的是(_____ )
A.亚氯酸钠在碱性条件下较稳定
B.25℃时,HClO2的浓度随PH增大而增大
C.PH=6时,溶液中含氯微粒的浓度大小为:c(HClO2)>c(ClO2-)>c(ClO2)>c(Cl-)
D. 25℃时,该溶液在pH=4时比pH=2时更适合漂白
(4)akg 30%的双氧水理论上可最多制得___ kg NaClO2·3H2O

已知:①NaClO2的溶解度随着温度升高而增大,适当条件下可结晶析出。
②ClO2气体在中性和碱性溶液中不能稳定存在。
回答下列问题:
(1)用于电解的食盐水需先除去其中的Ca2+、Mg2+、SO42-等杂质。除杂操作时,往粗盐水中先加入过量的
(2)X酸是
(3)亚氯酸钠在溶液中可生成ClO2、HClO2、ClO2-、Cl-等,其中HClO2和ClO2都具有漂白作用,但ClO2有毒,经测定,25℃时各组分含量随pH变化情况如图所示(Cl-没有画出)。则下列分析正确的是(

A.亚氯酸钠在碱性条件下较稳定
B.25℃时,HClO2的浓度随PH增大而增大
C.PH=6时,溶液中含氯微粒的浓度大小为:c(HClO2)>c(ClO2-)>c(ClO2)>c(Cl-)
D. 25℃时,该溶液在pH=4时比pH=2时更适合漂白
(4)akg 30%的双氧水理论上可最多制得
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐3】已知某粗盐样品中含有Na2SO4、MgCl2、CaCl2等杂质.实验室提纯流程如下:

(1)用托盘天平称量粗盐时,若砝码和粗盐位置放颠倒,天平平衡时,读数为5.4g,实际称得粗盐的质量是__________ 。
A.5.4g B.4.6g C.6.0g D.5.0g
(2)第③步操作发生反应的化学方程式是__________________________
(3)第④步操作发生反应的化学方程式是_______________________
(4)第⑤步操作的目的是___________________________
(5)第⑥步操作a的名称是________ ,此步操作中,玻璃棒的末端要轻轻地斜靠在 _____________ 的一边。
(6)第⑦步操作中,向滤液中滴加足量盐酸的目的是_____________ ,此步操作中产生气泡的化学方程式是___________________ 。
(7)在第⑧步操作时,要用玻璃棒不断搅拌,目的是_______________________

(1)用托盘天平称量粗盐时,若砝码和粗盐位置放颠倒,天平平衡时,读数为5.4g,实际称得粗盐的质量是
A.5.4g B.4.6g C.6.0g D.5.0g
(2)第③步操作发生反应的化学方程式是
(3)第④步操作发生反应的化学方程式是
(4)第⑤步操作的目的是
(5)第⑥步操作a的名称是
(6)第⑦步操作中,向滤液中滴加足量盐酸的目的是
(7)在第⑧步操作时,要用玻璃棒不断搅拌,目的是
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐1】硼酸和硫酸镁是重要的化工原料。以硼铁混精矿[主要成分为MgBO2(OH)、UO2和Fe3O4,还有少量的Fe2O3、FeO、SiO2]为原料制备硼酸和硫酸镁的工艺流程如下:

已知:①UO22+在pH为4-5的溶液中生成UO2(OH)2沉淀;②Fe2+和Fe3+沉淀完全的pH分别为9.7、3.7。
(1)酸浸过程中MgBO2(OH)与硫酸反应的离子方程式为_____ 。
(2)酸浸过程中加入H2O2的目的是______ (写出两条),滤渣1的主要成分是___ (填化学式)。
(3)试剂1最好选择_____ (填化学式)。若调节溶液pH前,溶液中c(Mg2+)=0.2 mol/L,当溶液pH调至5时,UO2+沉淀完全,此时是否有Mg(OH)2沉淀生成____ 。{通过计算说明,Ksp[Mg(OH)2]=5.6×10-12}
(4)操作1的名称是_____ 。
(5)MgSO4·H2O加热脱水可以得无水MgSO4,那么MgCl2·6H2O晶体直接加热___ (填“能”或“不能”)得到无水MgCl2,理由是_______ 。
(6)已知:H2CO3的Ka1=4.4×10-7,Ka2=4.7×10-11;H3BO3的Ka=5.8×10-10。向碳酸钠溶液里逐滴加入硼酸溶液____ (填“有”或“无”)气泡产生,理由是____ 。

已知:①UO22+在pH为4-5的溶液中生成UO2(OH)2沉淀;②Fe2+和Fe3+沉淀完全的pH分别为9.7、3.7。
(1)酸浸过程中MgBO2(OH)与硫酸反应的离子方程式为
(2)酸浸过程中加入H2O2的目的是
(3)试剂1最好选择
(4)操作1的名称是
(5)MgSO4·H2O加热脱水可以得无水MgSO4,那么MgCl2·6H2O晶体直接加热
(6)已知:H2CO3的Ka1=4.4×10-7,Ka2=4.7×10-11;H3BO3的Ka=5.8×10-10。向碳酸钠溶液里逐滴加入硼酸溶液
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐2】某同学设计以下实验方案,从海带中提取I2。

(1)操作①的名称是______ 。
(2)向滤液中加入双氧水的作用是______ 。
(3)试剂a可以是______ (填序号)。
①四氯化碳 ②苯 ③酒精 ④乙酸
(4)I–和IO3-在酸性条件下生成I2的离子方程式是________________ 。
(5)上图中,含I2的溶液经3步转化为I2的悬浊液,其目的是____________ 。

(1)操作①的名称是
(2)向滤液中加入双氧水的作用是
(3)试剂a可以是
①四氯化碳 ②苯 ③酒精 ④乙酸
(4)I–和IO3-在酸性条件下生成I2的离子方程式是
(5)上图中,含I2的溶液经3步转化为I2的悬浊液,其目的是
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐3】废弃化学品循环再利用对节约资源和保护环境有重要意义。钴盐在新能源、催化、印染等领域应用广泛。利用电解工业产生的钴、镍废渣(含Fe、Cu等)制备CoCl2·6H2O,流程如下图所示:
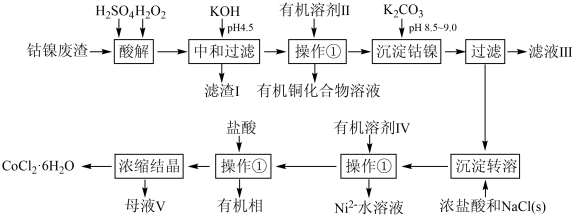
已知:通常认为溶液中离子浓度小于10-5mol·L-1为沉淀完全;室温下相关物质的Ksp见下表。
回答下列问题:
(1)滤渣Ⅰ的主要成分为Fe(OH)3,H2O2氧化Fe2+的离子方程式为___________ 。
(2)操作①是___________ ;滤液III对应的溶质是___________ (填化学式);浓盐酸溶解沉淀时,加入NaCl(s)的目的是___________ 。
(3)K2CO3与钴、镍离子反应的产物是氢氧化物沉淀,室温下,在pH8.5~9.0范围内Co2+___________ (填“能”或“不能”)沉淀完全,Co(OH)2易被氧化成Co(OH)3,Co(OH)3可氧化浓盐酸,其化学方程式为___________ 。
(4)浓缩结晶后的母液V可返回___________ 工序循环利用。
(5)利用硫化物分离钴镍离子,向浓度同为0.1mol·L-1的Ni2+和Co2+混合溶液中逐滴加入(NH4)2S溶液(忽略溶液体积变化),首先生成硫化物沉淀的离子为___________ ;当第二种离子生成硫化物沉淀时,第一种离子的浓度为___________ mol·L-1。

已知:通常认为溶液中离子浓度小于10-5mol·L-1为沉淀完全;室温下相关物质的Ksp见下表。
| 物质 | Co(OH)2 | NiS | CoS |
| Ksp | 1×10-14.2 | 1×10-18.5 | 1×10-20.4 |
(1)滤渣Ⅰ的主要成分为Fe(OH)3,H2O2氧化Fe2+的离子方程式为
(2)操作①是
(3)K2CO3与钴、镍离子反应的产物是氢氧化物沉淀,室温下,在pH8.5~9.0范围内Co2+
(4)浓缩结晶后的母液V可返回
(5)利用硫化物分离钴镍离子,向浓度同为0.1mol·L-1的Ni2+和Co2+混合溶液中逐滴加入(NH4)2S溶液(忽略溶液体积变化),首先生成硫化物沉淀的离子为
您最近一年使用:0次



