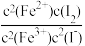氢能是清洁能源之一,工业制取氢气涉及的重要反应之一是:

已知:①
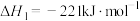
②
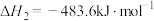
③
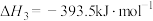
下列说法正确的是


已知:①

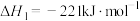
②

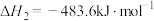
③

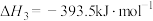
下列说法正确的是
A. 的燃烧热 的燃烧热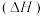 为 为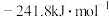 |
B. 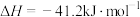 |
C.相比完全燃烧,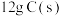 不完全燃烧生成 不完全燃烧生成 时损失的热量为 时损失的热量为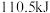 |
D. 的平衡常数表达式为 的平衡常数表达式为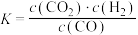 |
更新时间:2024-01-03 08:41:32
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】已知几种共价键的键能数据如下:
反应Ⅰ: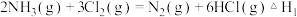
反应Ⅱ:
下列说法正确的是
| 共价键 |  |  |  |  |  |  |
键能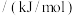 | 391 | 945 | 243 | 432 | 193 | 366 |
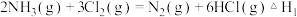
反应Ⅱ:

下列说法正确的是
A. |
B. |
C.稳定性: |
D.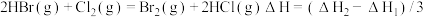 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列说法正确的是
A.甲烷的标准燃烧热为 ,则甲烷燃烧的热化学方程式可表示为 ,则甲烷燃烧的热化学方程式可表示为 |
B. 的燃烧热是 的燃烧热是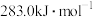 ,则 ,则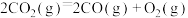 的反应热 的反应热 |
C. 和 和 反应的中和热 反应的中和热 ,则 ,则 和 和 反应的中和热 反应的中和热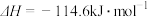 |
D.500℃、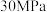 下,将 下,将 和 和 置于密闭的容器中充分反应生成 置于密闭的容器中充分反应生成 ,放热 ,放热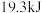 ,其热化学方程式为 ,其热化学方程式为 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】下列热化学方程式正确的是
| A.甲烷的标准燃烧热为890.3 kJ·mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH=-890.3 kJ·mol-1 |
B.500 ℃、30 MPa 下,将0.5 mol N2 和 1.5 mol H2 置于密闭容器中充分反应生成NH3(g),放热19.3 kJ,其热化学方程式为:N2(g)+3H2(g) 2NH3(g)ΔH=-38.6 kJ·mol-1 2NH3(g)ΔH=-38.6 kJ·mol-1 |
C.已知在120 ℃、101 kPa下,1 g H2燃烧生成水蒸气放出121 kJ热量,其热化学方程式为:H2(g)+ O2(g) O2(g) H2O(g) ΔH=-242 kJ/mol H2O(g) ΔH=-242 kJ/mol |
| D.CO(g)的燃烧热是283.0 kJ·mol-1,则2CO2(g)= 2CO(g)+O2(g)反应的ΔH=+283.0 kJ·mol-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】2021年10月16日,我国长征二号F运载火箭搭载神舟十三号载人飞船顺利升空,并取得圆满成功。航天飞行任务船成功发射,其动力燃料是偏二甲肼,这种燃料的优点是不需单独进行点火,火箭发射时只要将其和四氧化二氮在发动机燃烧室混合即可,核心反应为: 。对于该反应下列说法不正确的是
。对于该反应下列说法不正确的是
 。对于该反应下列说法不正确的是
。对于该反应下列说法不正确的是A.用E总表示键能之和,该反应 E总(反应物)-E总(生成物) E总(反应物)-E总(生成物) |
B.由该热化学反应方程式可知,偏二甲肼的燃烧热为 |
| C.偏二甲肼具有较强的还原性 |
D.该反应的 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】下列关于热化学反应的描述正确的是
| A.HCl和NaOH反应的中和热ΔH=-57.3kJ·mol-1,则1mol硫酸与足量氢氧化钙溶液反应放热114.6kJ |
| B.H2(g)的燃烧热ΔH=-285.8kJ·mol-1,则2H2O(l)=2H2(g)+O2(g)反应的ΔH=+571.6kJ·mo-1 |
C.101kPa时,2H2(g)+O2(g)=2H2O(g) ΔH=-QkJ·mol-1,则H2的燃烧热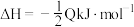 |
D.500℃、30MPa下,将0.5molN2和1.5molH2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为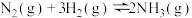  |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】在一定条件下, CO 和 CH 4 的燃烧热分别是 283 kJ/mol 和 890 kJ/mol 。现有 1 mol 由 CO 与 CH 4 组成的混合气体在上述条件下完全燃烧,生成 CO 2 气体和液态水,释放出 738.25 kJ 的热量,则混合气体中 CO 和 CH 4 的体积比为
| A.1 ∶ 3 | B.3 ∶ 1 | C.1 ∶ 2 | D.2 ∶ 1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】已知CH4(g)和CO(g)的燃烧热分别是890.3 kJ·mol-1和 283.0kJ·mol-1,则由CH4(g)不完全燃烧生成1 mol CO(g)和H2O(l)的ΔH为( )
| A.-607.3 kJ·mol-1 | B.+607.3 kJ·mol-1 | C.-324.3 kJ·mol-1 | D.+324.3 kJ·mol-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】已知在101kPa时,C(石墨)、H2和CO的燃烧热分别为393.5kJ/mol、285.8kJ/mol和282.8kJ/mol.现有H2和CO组成的混合气体112L(标况),经充分燃烧后,放出总热量为1420kJ,并生成液态水.下列热化学方程式或描述中正确的是( )
| A.2CO(g)+O2(g)═2CO2(g);△H=+282.8 kJ/mol |
| B.2H2(g)+O2(g)═2H2O(g);△H=-571.6 kJ/mol |
C.C(石墨,s)+ O2(g)═CO(g);△H=-110.7 kJ/mol O2(g)═CO(g);△H=-110.7 kJ/mol |
| D.燃烧前混合气体中H2的体积百分数为50% |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】对于反应4NH3(g)+5O2(g) 4NO(g)+6H2O(g),下列有关说法
4NO(g)+6H2O(g),下列有关说法不正确 的是
 4NO(g)+6H2O(g),下列有关说法
4NO(g)+6H2O(g),下列有关说法A.上述反应的平衡常数表达式K=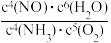 |
| B.适当提高NH3的浓度,可以加快反应速率,提高NH3的转化率 |
| C.1molN—H断裂同时有1molO—H断裂,说明达该条件下的平衡状态 |
| D.其它条件不变,加入高效的催化剂能提高单位体积内的活化分子百分数 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】硫酸是重要的化工原料。稀硫酸具有酸的通性;浓硫酸具有很强的氧化性,能氧化大多数金属单质和部分非金属单质。金属冶炼时产生的含SO2废气经回收处理、催化氧化、吸收后可制得硫酸。2SO2(g)+O2(g) 2SO3(g) ΔH=-196.6kJ·mol-1。工业制硫酸尾气中的SO2可用氨水吸收,吸收液经处理后释放出的SO2又可循环利用。对于反应2SO2(g)+O2(g)
2SO3(g) ΔH=-196.6kJ·mol-1。工业制硫酸尾气中的SO2可用氨水吸收,吸收液经处理后释放出的SO2又可循环利用。对于反应2SO2(g)+O2(g) 2SO3(g),下列说法正确的是
2SO3(g),下列说法正确的是
 2SO3(g) ΔH=-196.6kJ·mol-1。工业制硫酸尾气中的SO2可用氨水吸收,吸收液经处理后释放出的SO2又可循环利用。对于反应2SO2(g)+O2(g)
2SO3(g) ΔH=-196.6kJ·mol-1。工业制硫酸尾气中的SO2可用氨水吸收,吸收液经处理后释放出的SO2又可循环利用。对于反应2SO2(g)+O2(g) 2SO3(g),下列说法正确的是
2SO3(g),下列说法正确的是| A.反应的ΔS>0 |
B.反应的平衡常数可表示为K=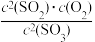 |
| C.增大体系的压强能提高SO2的反应速率和转化率 |
| D.使用催化剂能改变反应路径,提高反应的活化能 |
您最近一年使用:0次

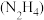 在足量氧气中完全燃烧生成水蒸气,放出642 kJ热量:
在足量氧气中完全燃烧生成水蒸气,放出642 kJ热量: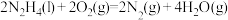

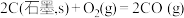
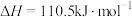

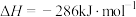 ,则
,则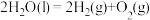
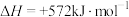
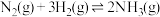
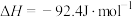 ,则在一定条件下向密闭容器中充入0.5mol
,则在一定条件下向密闭容器中充入0.5mol  和1.5mol
和1.5mol  充分反应放出46.2 kJ的热量
充分反应放出46.2 kJ的热量 2Fe2+(aq)+I2(aq),达到平衡,下列说法不正确的是
2Fe2+(aq)+I2(aq),达到平衡,下列说法不正确的是