完成下列有关物质的量的计算
(1) 个
个 含有原子的物质的量是
含有原子的物质的量是______ mol.
(2)标准状况下,34g 的体积是
的体积是______ L.
(3)含有相同氧原子数的 和
和 ,其分子的质量比为
,其分子的质量比为______ .
(4)标准状况下,aL HCl气体溶于水配制成bL溶液,其物质的量浓度为______ mol/L.
(5)3.6g碳在一定量的氧气中完全燃烧,反应后生成CO和 混合气体的平均摩尔质量是32g/mol,则生成的CO的质量是
混合气体的平均摩尔质量是32g/mol,则生成的CO的质量是______ g.
(1)
 个
个 含有原子的物质的量是
含有原子的物质的量是(2)标准状况下,34g
 的体积是
的体积是(3)含有相同氧原子数的
 和
和 ,其分子的质量比为
,其分子的质量比为(4)标准状况下,aL HCl气体溶于水配制成bL溶液,其物质的量浓度为
(5)3.6g碳在一定量的氧气中完全燃烧,反应后生成CO和
 混合气体的平均摩尔质量是32g/mol,则生成的CO的质量是
混合气体的平均摩尔质量是32g/mol,则生成的CO的质量是
更新时间:2024-01-03 22:16:06
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】回答下列问题
(1)水的摩尔质量是______ g/mol,1mol H2O的质量是_______ g,所含分子数是___________ ,所含原子数是___________ 。
(2)标准状况下,11.2 LO2的物质的量是___________ mol,质量是___________ g。
(3)100 mL 物质的量浓度为1mol/L NaCl溶液中含NaCl质量是___________ g。
(1)水的摩尔质量是
(2)标准状况下,11.2 LO2的物质的量是
(3)100 mL 物质的量浓度为1mol/L NaCl溶液中含NaCl质量是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】利用“化学计量在实验中的应用”的相关知识进行填空
(1)0.2 mol NH3气体中含的NH3分子数是_______ ,其中含氢原子数是_______ ,含有电子的物质的量是_______ 。
(2)1摩尔Ba(OH)2固体中含有的Ba2+的个数是_______ ,全部溶于水,电离产生的OH-的物质的量是_______ mol,通入二氧化碳气体,恰好完全反应,消耗的二氧化碳的物质的量是_______ 摩尔。
(3)H2SO4的摩尔质量是_______ ,49gH2SO4中含有_______ mol氧原子,含有氢的质量是_______ 。
能与_______ 摩尔NaOH恰好完全反应,生成水的质量是_______ 克。
(4)含有6.02×1023个氧原子的H3pO4的物质的量是_______
(5)与标准状况下VLCO2所含氧原子数目相同的水的质量是_______ (用分式表示)
(6)将4 g NaOH溶解在10 mL水中,再稀释成1 L,从中取出10 mL,这10 mL溶液的物质的量浓度为_______
(7)在一定的温度和压强下,1体积X2 (g)跟3体积Y2 (g)化合生成2体积化合物,则该化合物的化学式是_______
(1)0.2 mol NH3气体中含的NH3分子数是
(2)1摩尔Ba(OH)2固体中含有的Ba2+的个数是
(3)H2SO4的摩尔质量是
能与
(4)含有6.02×1023个氧原子的H3pO4的物质的量是
(5)与标准状况下VLCO2所含氧原子数目相同的水的质量是
(6)将4 g NaOH溶解在10 mL水中,再稀释成1 L,从中取出10 mL,这10 mL溶液的物质的量浓度为
(7)在一定的温度和压强下,1体积X2 (g)跟3体积Y2 (g)化合生成2体积化合物,则该化合物的化学式是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】现有14.4gCO和CO2的混合气体,在标准状况下其体积为8.96L。回答下列问题:
(1)该混合气体的平均摩尔质量为___ 。
(2)混合气体中碳原子的个数为___ (用NA表示阿伏加德罗常数的值)。
(3)将混合气体依次通过如图所示装置,最后收集在气球中。

①气球中收集到的气体的摩尔质量为___ 。
②气球中收集到的气体中,电子总数为___ (用NA表示阿伏加德罗常数的值)。
③标准状况下,气球中收集到的气体的体积为__ L。
(4)在标准状况下,1体积水溶解700体积氨气,所得溶液的密度是0.9g/cm3。则该氨水中溶质的质量分数为___ 。
(1)该混合气体的平均摩尔质量为
(2)混合气体中碳原子的个数为
(3)将混合气体依次通过如图所示装置,最后收集在气球中。

①气球中收集到的气体的摩尔质量为
②气球中收集到的气体中,电子总数为
③标准状况下,气球中收集到的气体的体积为
(4)在标准状况下,1体积水溶解700体积氨气,所得溶液的密度是0.9g/cm3。则该氨水中溶质的质量分数为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】(1)含有3.01×1023个H的H2O,其H2O物质的量是________ ;其H2O中含有电子的个数为______________ 。
(2)______ mol H2O中含有的氧原子数与1.5 mol CO2中含有的氧原子数相等。
(3)将等物质的量的NH3和CH4混合,混合气体中NH3与CH4的质量比为________ 。
(4)要使NH3与CH4含相同数目的H原子,则NH3和CH4的物质的量之比为__________ 。
(5)标准状况下,密度为0.75 g·L-1的NH3与CH4组成的混合气体中,NH3的体积分数为__________ ,(注:体积分数即为物质的量分数)
(6)已知a g A和b g B恰好完全反应生成0.4mol C和d g D,则C的摩尔质量为________
(7)同温、同压下等质量的SO2气体和CO2气体,体积之比___________ ,原子数目之比为___________ ,密度比为___________ ,氧元素的质量比为__________ 。
(8)某气态氧化物化学式为RO2,在标准状况下,1.28g该氧化物的体积为448mL,则该氧化物的摩尔质量为____________ ;R的相对原子质量为_____________ 。
(9)200mL、2.0mol/L的Al2(SO4)3溶液中含Al3+的物质的量为___________ ;从中取出10mL,将这10mL溶液用水稀释到50mL,所得溶液中溶质的物质的量浓度为______________ 。
(2)
(3)将等物质的量的NH3和CH4混合,混合气体中NH3与CH4的质量比为
(4)要使NH3与CH4含相同数目的H原子,则NH3和CH4的物质的量之比为
(5)标准状况下,密度为0.75 g·L-1的NH3与CH4组成的混合气体中,NH3的体积分数为
(6)已知a g A和b g B恰好完全反应生成0.4mol C和d g D,则C的摩尔质量为
(7)同温、同压下等质量的SO2气体和CO2气体,体积之比
(8)某气态氧化物化学式为RO2,在标准状况下,1.28g该氧化物的体积为448mL,则该氧化物的摩尔质量为
(9)200mL、2.0mol/L的Al2(SO4)3溶液中含Al3+的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】(1)3.6gH2O的物质的量是_______ mol,含有_________ 个H2O,含有_____ molH,含_____ mol电子。
(2)标准状况下,11.2L的H2R气体质量为17g,则H2R的摩尔质量是_________ ,相对分子质量为________ ;等物质的量的NH3与H2S质量比为___________ ,1.7g氨气与________ mol H2O含有的电子数相等。
(3)将1.06g Na2CO3溶于水配成500mL溶液,Na2CO3的浓度为______ mol/L,Na+浓度为______ mol/L,将该溶液加水稀释成1000 mL后,Na+浓度为____ mol/L。
(2)标准状况下,11.2L的H2R气体质量为17g,则H2R的摩尔质量是
(3)将1.06g Na2CO3溶于水配成500mL溶液,Na2CO3的浓度为
您最近一年使用:0次
【推荐1】氮、磷都是第ⅤA族元素,一些含氮、磷的化合物在生产生活中有重要应用。
(1)磷化铝、磷化锌、磷化钙是我国目前最常见的熏蒸杀虫剂,都能与水或酸反应产生有毒气体膦(PH3),写出磷化铝与水反应的化学方程式:_______ 。
(2)羟基磷灰石[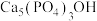 ]是一种重要的生物无机材料,也是我们牙齿表面的一层坚硬物质,可用磷酸和氢氧化钙悬浊液反应制得。已知3种钙盐的溶解度(以钙离子浓度的对数表示)随溶液pH的变化如图所示。
]是一种重要的生物无机材料,也是我们牙齿表面的一层坚硬物质,可用磷酸和氢氧化钙悬浊液反应制得。已知3种钙盐的溶解度(以钙离子浓度的对数表示)随溶液pH的变化如图所示。
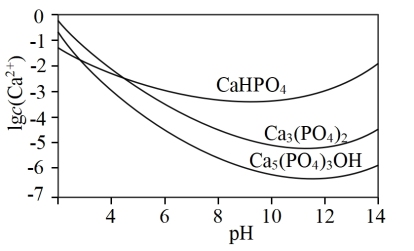
①图中所示3种钙盐,其中在人体中最稳定的存在形式是_______ (填化学式)。
②实验室制备羟基磷灰石时,应将_______ (填“磷酸”或“氢氧化钙悬浊液”,下同)滴加到_______ 中。
③进食后,口腔中残留的食物会在细菌和酶作用下产生有机酸,易造成龋齿,其原因是_______ 。
(3)氮的氧化物对大气污染比较严重,一定条件下可用NH3消除污染,则NO2与NH3的反应中,被氧化的氮原子和被还原的氮原子的物质的量之比为_______ 。
(4)标准状况下,由11.2LNH3制备得200mL硝酸溶液,向其中加入9.6g铜,充分反应后转移的电子数目为9.03×1022,则制备硝酸溶液过程中NH3的利用率为_______ ;最后得到的溶液中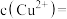
_______ (不考虑溶液体积的变化)。
(1)磷化铝、磷化锌、磷化钙是我国目前最常见的熏蒸杀虫剂,都能与水或酸反应产生有毒气体膦(PH3),写出磷化铝与水反应的化学方程式:
(2)羟基磷灰石[
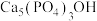 ]是一种重要的生物无机材料,也是我们牙齿表面的一层坚硬物质,可用磷酸和氢氧化钙悬浊液反应制得。已知3种钙盐的溶解度(以钙离子浓度的对数表示)随溶液pH的变化如图所示。
]是一种重要的生物无机材料,也是我们牙齿表面的一层坚硬物质,可用磷酸和氢氧化钙悬浊液反应制得。已知3种钙盐的溶解度(以钙离子浓度的对数表示)随溶液pH的变化如图所示。
①图中所示3种钙盐,其中在人体中最稳定的存在形式是
②实验室制备羟基磷灰石时,应将
③进食后,口腔中残留的食物会在细菌和酶作用下产生有机酸,易造成龋齿,其原因是
(3)氮的氧化物对大气污染比较严重,一定条件下可用NH3消除污染,则NO2与NH3的反应中,被氧化的氮原子和被还原的氮原子的物质的量之比为
(4)标准状况下,由11.2LNH3制备得200mL硝酸溶液,向其中加入9.6g铜,充分反应后转移的电子数目为9.03×1022,则制备硝酸溶液过程中NH3的利用率为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】将6.4g铜与一定量的质量分数为63%密度为1.24g/cm3浓硝酸反应,恰好反应完全。试计算:
(1)浓硝酸的物质的量浓度为:_______ mol/L,体现酸性的硝酸为:_______ mol;
(2)为防止污染空气,使气体和一定量氧气一起通入水中,如无气体放出,则氧气的体积为__ L?(写出计算过程)。
(1)浓硝酸的物质的量浓度为:
(2)为防止污染空气,使气体和一定量氧气一起通入水中,如无气体放出,则氧气的体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】工业上使用“氯碱工业”来制取氯气。制备的氯气为了方便运输,常采用_______ 的方式液化成液氯,从微观角度分析该过程中发生的变化是_______ 。氯碱厂用氯气生产包括氯化氢在内的副产品,写出生成氯化氢的化学方程式_______ ,生产过程中能看到_______ 色火焰。欲配制质量分数为36%的浓盐酸 ,需要标准状况下氯化氢气体
,需要标准状况下氯化氢气体_______ L(结果保留整数)。
 ,需要标准状况下氯化氢气体
,需要标准状况下氯化氢气体
您最近一年使用:0次



