我国化学家侯德榜发明了联合制碱法,对世界制碱工业做出了巨大贡献。联合制碱法的主要流程如下(部分物质已略去):
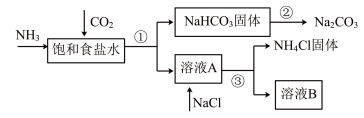
(1)①~③所涉及的操作方法中,包含过滤的是___________ (填序号)。
(2)根据上述流程图,将化学方程式补充完整:________
NH3+CO2+___________+___________=NaHCO3↓+NH4Cl
(3)煅烧NaHCO3固体的化学方程式是___________ 。
(4)下列联合制碱法流程说法正确的是___________ (填字母)。
a.CO2可以循环使用
b.副产物NH4Cl可用作肥料
c.溶液B中一定含有Na+、NH 、Cl-
、Cl-
d.①中NaHCO3析出是因为一定条件下NaHCO3的溶解度最小
(5)某纯碱样品中含杂质NaCl,取质量为ag的样品,加入足量的稀盐酸,充分反应后,加热、蒸干、灼烧,得到bg固体物质,则此样品中Na2CO3的质量分数为___________ 。(列出表达式即可)

(1)①~③所涉及的操作方法中,包含过滤的是
(2)根据上述流程图,将化学方程式补充完整:
NH3+CO2+___________+___________=NaHCO3↓+NH4Cl
(3)煅烧NaHCO3固体的化学方程式是
(4)下列联合制碱法流程说法正确的是
a.CO2可以循环使用
b.副产物NH4Cl可用作肥料
c.溶液B中一定含有Na+、NH
 、Cl-
、Cl-d.①中NaHCO3析出是因为一定条件下NaHCO3的溶解度最小
(5)某纯碱样品中含杂质NaCl,取质量为ag的样品,加入足量的稀盐酸,充分反应后,加热、蒸干、灼烧,得到bg固体物质,则此样品中Na2CO3的质量分数为
更新时间:2024-01-07 18:36:59
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】工业上用铝土矿(含氧化铝、氧化铁)制取铝的过程如下:
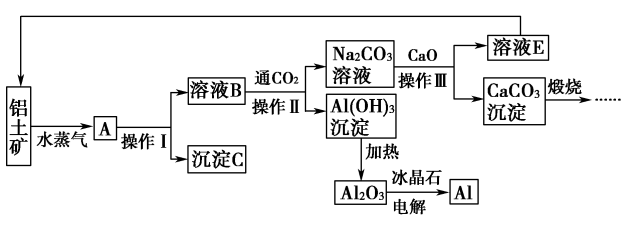
请回答下列问题:
(1)请说出沉淀C在工业上的一种用途:_____________________ 。
(2)生产过程中,除NaOH、H2O可以循环使用外,还可以循环使用的物质有_____ (填化学式)。
(3)操作Ⅰ、操作Ⅱ和操作Ⅲ都是________ (填操作名称)。实验室洗涤Al(OH)3沉淀的方法是__________________________________________ 。
(4)电解熔融的氧化铝,若得到标准状况下22.4 L O2,则同时生成铝的质量为________ g。
(5)写出Na2CO3溶液与CaO反应的离子方程式:_____________________ 。

请回答下列问题:
(1)请说出沉淀C在工业上的一种用途:
(2)生产过程中,除NaOH、H2O可以循环使用外,还可以循环使用的物质有
(3)操作Ⅰ、操作Ⅱ和操作Ⅲ都是
(4)电解熔融的氧化铝,若得到标准状况下22.4 L O2,则同时生成铝的质量为
(5)写出Na2CO3溶液与CaO反应的离子方程式:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】工业上,向500-600℃的铁屑中通入氯气生产无水氯化铁;向炽热铁屑中通入氯化氢生产无水氯化亚铁。现用如图所示的装置模拟上述过程进行实验。
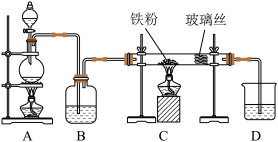
回答下列问题:
(1)制取无水氯化铁的实验中,A中反应的化学方程式为___________________ ,当生成1molCl2时,转移的电子数为______ ,玻璃丝的作用是___________ ,装置B中加入的试剂是_________ 。装置D中加入的试剂是___________________ 。
(2)制取无水氯化亚铁的实验中,尾气的成分是______ 。若仍用D的装置进行尾气处理,存在的问题是_____ 、_______ 。
(3)若操作不当,制得的FeCl2会含有少量FeCl3杂质,下列说法中正确的是_____
(4)现有一包FeCl2和FeCl3混合物,某化学兴趣小组为测定各成分的含量进行如下两个实验:
实验1:① 称取一定质量的样品,将样品溶解;② 向溶解后的溶液中加入足量的AgNO3溶液,产生沉淀;③ 将沉淀过滤、洗涤、干燥得到白色固体28.7g。
实验2:① 称取与实验1中相同质量的样品,溶解;② 加入足量的NaOH溶液,③ 将沉淀过滤、洗涤后,加热灼烧到质量不再减少,得到固体6.4g。则样品中FeCl3的物质的量为_______ 。

回答下列问题:
(1)制取无水氯化铁的实验中,A中反应的化学方程式为
(2)制取无水氯化亚铁的实验中,尾气的成分是
(3)若操作不当,制得的FeCl2会含有少量FeCl3杂质,下列说法中正确的是
| A.检验FeCl3常用的试剂是KSCN溶液 |
| B.可向固体混合物中加入适量Fe粉除去杂质 |
| C.可向固体混合物中通入适量Cl2除去杂质 |
| D.欲制得纯净的FeCl2,在实验操作中应先点燃A处的酒精灯,再点燃C处的酒精灯。 |
实验1:① 称取一定质量的样品,将样品溶解;② 向溶解后的溶液中加入足量的AgNO3溶液,产生沉淀;③ 将沉淀过滤、洗涤、干燥得到白色固体28.7g。
实验2:① 称取与实验1中相同质量的样品,溶解;② 加入足量的NaOH溶液,③ 将沉淀过滤、洗涤后,加热灼烧到质量不再减少,得到固体6.4g。则样品中FeCl3的物质的量为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】利用软锰矿(主要成分是MnO2)和黄铁矿(主要成分是FeS2)联合生产锰的化合物的工艺流程如图所示:

已知:ⅰ.酸浸后过滤所得溶液中的金属阳离子主要为 、
、 ,还含有少量的
,还含有少量的 和
和 。
。
ⅱ.CaF2难溶于水。
(1)酸浸时要将矿石粉碎的目的是______ 。
(2)酸浸时所用的稀酸X是______ ,两种矿石的主要成分在稀酸X中反应生成两种可溶性盐和一种淡黄色固体单质,酸浸时发生主要反应的离子方程式为____________________ 。
(3)除铁、铝时废渣2的主要成分为 和
和 ,则加入H2O2的目的是
,则加入H2O2的目的是______ ,加CaO的目的是______ ;净化后得到MnSO4溶液,废渣3的主要成分是______ 。
(4)由MnSO4溶液得到MnCO3、Mn3O4的过程如下:
①过程Ⅰ:制备MnCO3。MnCO3难溶于水,能溶于强酸,可用MnSO4溶液和NH4HCO3溶液混合得到MnCO3沉淀和一种气体,每制得1 mol MnCO3,至少消耗a mol/L的NH4HCO3溶液的体积为______ L。
②过程Ⅱ:制备Mn3O4,其流程如下图所示:

下图表示通入O2时溶液pH随时间的变化曲线,15~150 min内滤饼中一定参与反应的成分是______ (填化学式),判断的理由是____________________ (用方程式表示)。


已知:ⅰ.酸浸后过滤所得溶液中的金属阳离子主要为
 、
、 ,还含有少量的
,还含有少量的 和
和 。
。ⅱ.CaF2难溶于水。
(1)酸浸时要将矿石粉碎的目的是
(2)酸浸时所用的稀酸X是
(3)除铁、铝时废渣2的主要成分为
 和
和 ,则加入H2O2的目的是
,则加入H2O2的目的是(4)由MnSO4溶液得到MnCO3、Mn3O4的过程如下:
①过程Ⅰ:制备MnCO3。MnCO3难溶于水,能溶于强酸,可用MnSO4溶液和NH4HCO3溶液混合得到MnCO3沉淀和一种气体,每制得1 mol MnCO3,至少消耗a mol/L的NH4HCO3溶液的体积为
②过程Ⅱ:制备Mn3O4,其流程如下图所示:

下图表示通入O2时溶液pH随时间的变化曲线,15~150 min内滤饼中一定参与反应的成分是

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】现有一份Na2CO3和NaHCO3固体混合物,某化学兴趣小组设计如图所示实验装置(夹持仪器省略),测定固体混合物中NaHCO3的质量分数。实验步骤如下:

①组装好实验装置,并___________;
②加药品,称取mg样品放入硬质玻璃管中;称量装有碱石灰的U形管D的质量为m1g;。
③打开活塞K1、K2,关闭K3,缓缓鼓入空气数分钟;
④关闭活塞K1、K2,打开K3,点燃酒精灯加热至不再产生气体;
⑤打开活塞K1,缓缓鼓入空气数分钟后拆下装置,称量U形管D的质量为m2g。
请回答下列问题:
(1)补充实验步骤①的操作为___________ 。
(2)装置E中实验仪器的名称为___________ 。
(3)装置B中发生反应的化学方程式为___________ 。
(4)实验步骤⑤中“缓缓鼓入空气数分钟”的目的是___________ 。
(5)若缺少实验步骤③会导致测定结果___________ (填“偏大”“偏小”或“无影响”)。
(6)样品中NaHCO3的质量分数为___________ ×100%(用含m、m1、m2的式子表示)。

①组装好实验装置,并___________;
②加药品,称取mg样品放入硬质玻璃管中;称量装有碱石灰的U形管D的质量为m1g;。
③打开活塞K1、K2,关闭K3,缓缓鼓入空气数分钟;
④关闭活塞K1、K2,打开K3,点燃酒精灯加热至不再产生气体;
⑤打开活塞K1,缓缓鼓入空气数分钟后拆下装置,称量U形管D的质量为m2g。
请回答下列问题:
(1)补充实验步骤①的操作为
(2)装置E中实验仪器的名称为
(3)装置B中发生反应的化学方程式为
(4)实验步骤⑤中“缓缓鼓入空气数分钟”的目的是
(5)若缺少实验步骤③会导致测定结果
(6)样品中NaHCO3的质量分数为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】添加食品膨松剂能使面包、饼干等食品口感松软或脆酥。某兴趣小组选择某品牌膨松剂(其成分为: 与
与 ),设计实验方案测定
),设计实验方案测定 与
与 的物质的量之比。
的物质的量之比。

方案一:如图所示,向24.70g样品中滴加过量的NaOH溶液,加热至反应完全,再通入一段时间 。经测定,装置C中吸收
。经测定,装置C中吸收 的质量为m g。
的质量为m g。
方案二:称取等量的样品,加热至恒重,称其质量为10.6g。
(1)方案一中,仪器①的名称是__________ 。
(2)方案一中,通入 的目的是
的目的是__________ 。
(3)写出方案一中,任一离子反应方程式:__________ 。
(4)“误差”是指:物理量的测量值与客观存在的真实值之间总会存在着一定的差异。你认为方案一产生误差的可能原因有:__________ 。(写出一种即可)
(5)由方案二计算 与
与 的物质的量之比为
的物质的量之比为__________ (写出计算过程)。
 与
与 ),设计实验方案测定
),设计实验方案测定 与
与 的物质的量之比。
的物质的量之比。
方案一:如图所示,向24.70g样品中滴加过量的NaOH溶液,加热至反应完全,再通入一段时间
 。经测定,装置C中吸收
。经测定,装置C中吸收 的质量为m g。
的质量为m g。方案二:称取等量的样品,加热至恒重,称其质量为10.6g。
(1)方案一中,仪器①的名称是
(2)方案一中,通入
 的目的是
的目的是(3)写出方案一中,任一离子反应方程式:
(4)“误差”是指:物理量的测量值与客观存在的真实值之间总会存在着一定的差异。你认为方案一产生误差的可能原因有:
(5)由方案二计算
 与
与 的物质的量之比为
的物质的量之比为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】膨松剂反应时产生气体的量是检验膨松剂品质的一项重要指标。某校兴趣小组设计如图所示实验装置,通过测量某膨松剂加热反应产生气体的质量,确定其纯度。(已知该膨松剂中发挥作用的物质为 ,其他成分在加热条件下不产生气体)
,其他成分在加热条件下不产生气体)
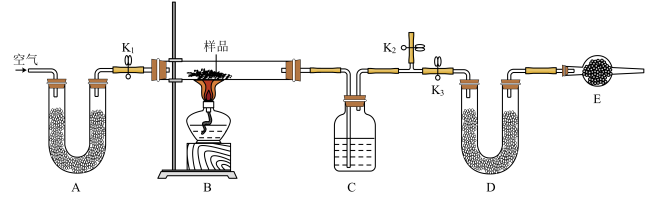
(1)实验步骤:
①组装实验装置,检验气密性。装置E的名称为___________ 。
②加药品。A、D和E中加入碱石灰,C中药品的作用为___________ ,硬质玻璃管B加入 样品。实验前称量装置D的质量为
样品。实验前称量装置D的质量为 。
。
③连接装置后,打开铁夹___________ ,关闭___________ (填“ ”、“
”、“ ”或“
”或“ ”),缓缓鼓入空气数分钟。
”),缓缓鼓入空气数分钟。
④关闭铁夹 、
、 ,打开
,打开 ,点燃酒精灯加热至不再产生气体。
,点燃酒精灯加热至不再产生气体。
⑤继续关闭铁夹 ,打开
,打开 和
和 ,缓缓鼓入空气数分钟,其目的是
,缓缓鼓入空气数分钟,其目的是___________ ,然后拆下装置,再次称量装置 的质量为
的质量为 。
。
(2)关于该实验方案,请回答下列问题。
①若加热反应前不鼓入空气,则会导致测量结果___________ (填“偏大”、“偏小”或“无影响”)
②若实验中没有 装置,则会导致测量结果
装置,则会导致测量结果___________ 。(填“偏大”、“偏小”或“无影响”)
③该膨松剂的纯度为___________ (用含 、
、 、
、 的代数式表示)。
的代数式表示)。
 ,其他成分在加热条件下不产生气体)
,其他成分在加热条件下不产生气体)
(1)实验步骤:
①组装实验装置,检验气密性。装置E的名称为
②加药品。A、D和E中加入碱石灰,C中药品的作用为
 样品。实验前称量装置D的质量为
样品。实验前称量装置D的质量为 。
。③连接装置后,打开铁夹
 ”、“
”、“ ”或“
”或“ ”),缓缓鼓入空气数分钟。
”),缓缓鼓入空气数分钟。④关闭铁夹
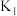 、
、 ,打开
,打开 ,点燃酒精灯加热至不再产生气体。
,点燃酒精灯加热至不再产生气体。⑤继续关闭铁夹
 ,打开
,打开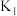 和
和 ,缓缓鼓入空气数分钟,其目的是
,缓缓鼓入空气数分钟,其目的是 的质量为
的质量为 。
。(2)关于该实验方案,请回答下列问题。
①若加热反应前不鼓入空气,则会导致测量结果
②若实验中没有
 装置,则会导致测量结果
装置,则会导致测量结果③该膨松剂的纯度为
 、
、 、
、 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】锶(Sr)和镁位于同主族,锶比镁更活泼,锶与氮气在加热条件下反应产生氮化锶,已知氮化锶遇水发生剧烈反应。某小组同学设计如下装置制备氮化锶(Sr3N2的相对分子质量为290.8)。
已知:碱性连苯三酚溶液能吸收O2。
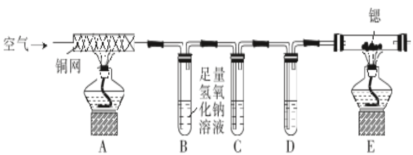
(1)装置B中发生反应的化学方程式为_______ 。装置D中盛装的试剂是_______ (填名称),装置C的作用为_______ 。
(2)该小组同学认为该实验存在明显不足,可能会导致产品变质,氮化锶遇水发生反应的化学方程式为_______ ,改进方案为_______ 。
(3)产品纯度的测定:称取0.5000g所得产品,加入干燥的三颈烧瓶中,加入蒸馏水,并通过足量水蒸气,将产生的氨全部蒸出,所蒸出的气体恰好被2mL 1.00mol/L HCl标准溶液完全吸收,则产品纯度为_______ 。
已知:碱性连苯三酚溶液能吸收O2。

(1)装置B中发生反应的化学方程式为
(2)该小组同学认为该实验存在明显不足,可能会导致产品变质,氮化锶遇水发生反应的化学方程式为
(3)产品纯度的测定:称取0.5000g所得产品,加入干燥的三颈烧瓶中,加入蒸馏水,并通过足量水蒸气,将产生的氨全部蒸出,所蒸出的气体恰好被2mL 1.00mol/L HCl标准溶液完全吸收,则产品纯度为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】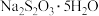 俗名“大苏打”,是无色透明晶体,不溶于乙醇,易溶于水,在
俗名“大苏打”,是无色透明晶体,不溶于乙醇,易溶于水,在 和
和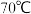 时的溶解度分别为
时的溶解度分别为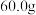 和212g。实验室常用
和212g。实验室常用 与
与 、
、 共热制备
共热制备 ,某兴趣小组拟用如下实验装置制备硫代硫酸钠。回答下列问题:
,某兴趣小组拟用如下实验装置制备硫代硫酸钠。回答下列问题:
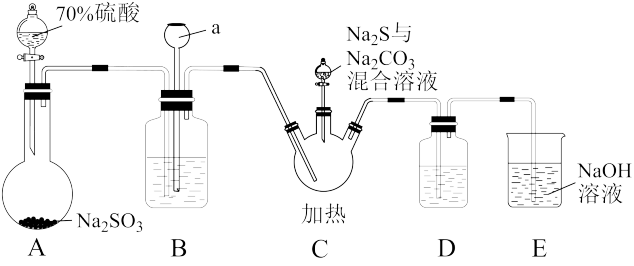
(1)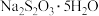 属于
属于_______  填“纯净物”或“混合物”
填“纯净物”或“混合物” ,仪器a的名称
,仪器a的名称_______ 。
(2)装置B中盛放的试剂是饱和 溶液,下列属于装置B作用的是_______。
溶液,下列属于装置B作用的是_______。
(3)在装置C中制备硫代硫酸钠时,有气体生成,写出该反应的化学方程式:_______ 。
(4) 装置用于检验C中
装置用于检验C中 的吸收效率进而调整
的吸收效率进而调整 的流速,则D中盛装的试剂可以为
的流速,则D中盛装的试剂可以为_______  填写一种即可
填写一种即可 。
。
(5)待反应结束后,从C中溶液获得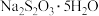 的方法是:
的方法是:_______ 、_______ 、过滤、洗涤、干燥。其中洗涤时应选用_______ 做洗涤剂。
(6)测定粗产品中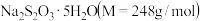 的含量。称取
的含量。称取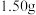 粗产品溶于水,用
粗产品溶于水,用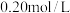 酸性
酸性 溶液进行滴定
溶液进行滴定 假设杂质不与酸性
假设杂质不与酸性 溶液反应
溶液反应 ,当溶液中
,当溶液中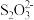 全部被氧化为
全部被氧化为 达到滴定终点时,消耗高锰酸钾溶液40.00mL。则滴定达到终点时的现象是
达到滴定终点时,消耗高锰酸钾溶液40.00mL。则滴定达到终点时的现象是_______ ;产品中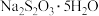 的质量分数为
的质量分数为_______  保留小数点后一位
保留小数点后一位 。
。
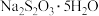 俗名“大苏打”,是无色透明晶体,不溶于乙醇,易溶于水,在
俗名“大苏打”,是无色透明晶体,不溶于乙醇,易溶于水,在 和
和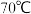 时的溶解度分别为
时的溶解度分别为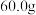 和212g。实验室常用
和212g。实验室常用 与
与 、
、 共热制备
共热制备 ,某兴趣小组拟用如下实验装置制备硫代硫酸钠。回答下列问题:
,某兴趣小组拟用如下实验装置制备硫代硫酸钠。回答下列问题:
(1)
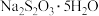 属于
属于 填“纯净物”或“混合物”
填“纯净物”或“混合物” ,仪器a的名称
,仪器a的名称(2)装置B中盛放的试剂是饱和
 溶液,下列属于装置B作用的是_______。
溶液,下列属于装置B作用的是_______。A.除去 中混有的 中混有的 | B.观察 的生成速率 的生成速率 |
| C.用于观察装置否堵塞 | D.用于除去A装置中挥发出的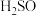 4 4 |
(4)
 装置用于检验C中
装置用于检验C中 的吸收效率进而调整
的吸收效率进而调整 的流速,则D中盛装的试剂可以为
的流速,则D中盛装的试剂可以为 填写一种即可
填写一种即可 。
。(5)待反应结束后,从C中溶液获得
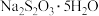 的方法是:
的方法是:(6)测定粗产品中
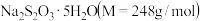 的含量。称取
的含量。称取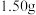 粗产品溶于水,用
粗产品溶于水,用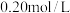 酸性
酸性 溶液进行滴定
溶液进行滴定 假设杂质不与酸性
假设杂质不与酸性 溶液反应
溶液反应 ,当溶液中
,当溶液中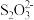 全部被氧化为
全部被氧化为 达到滴定终点时,消耗高锰酸钾溶液40.00mL。则滴定达到终点时的现象是
达到滴定终点时,消耗高锰酸钾溶液40.00mL。则滴定达到终点时的现象是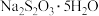 的质量分数为
的质量分数为 保留小数点后一位
保留小数点后一位 。
。
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】某磁性材料 广泛应用于磁记录、催化等领域。一种制备该材料的流程如下:
广泛应用于磁记录、催化等领域。一种制备该材料的流程如下:

已知反应原理为:①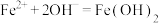
②
③
(1)用 溶液和
溶液和 溶液制备
溶液制备 反应的离子方程式为
反应的离子方程式为_______ 。
(2)当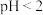 时,
时, 产率极低的原因是
产率极低的原因是_______ 。
(3)图1为回流时间与 产率的关系图,图2为回流
产率的关系图,图2为回流 所得产品的X射线衍射图。回流
所得产品的X射线衍射图。回流 所得产品
所得产品 中产生杂质可能的原因
中产生杂质可能的原因_______ 。

(4)一定条件下焙烧可制得 负载型催化剂。准确称取
负载型催化剂。准确称取 负载型催化剂样品,置于
负载型催化剂样品,置于 锥形瓶中,加入适量稀盐酸,加热溶解后,滴加稍过量的
锥形瓶中,加入适量稀盐酸,加热溶解后,滴加稍过量的 溶液(
溶液( 将
将 还原为
还原为 ),充分反应后,除去过量
),充分反应后,除去过量 。用
。用 溶液滴定至终点(滴定过程中
溶液滴定至终点(滴定过程中 与
与 反应生成
反应生成 和
和 ),消耗
),消耗 溶液
溶液 。计算该
。计算该 负载型催化剂的负载量
负载型催化剂的负载量_____ (写出计算过程)。 [负载量= ×100%]
×100%]
 广泛应用于磁记录、催化等领域。一种制备该材料的流程如下:
广泛应用于磁记录、催化等领域。一种制备该材料的流程如下:
已知反应原理为:①
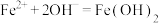
②

③

(1)用
 溶液和
溶液和 溶液制备
溶液制备 反应的离子方程式为
反应的离子方程式为(2)当
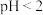 时,
时, 产率极低的原因是
产率极低的原因是(3)图1为回流时间与
 产率的关系图,图2为回流
产率的关系图,图2为回流 所得产品的X射线衍射图。回流
所得产品的X射线衍射图。回流 所得产品
所得产品 中产生杂质可能的原因
中产生杂质可能的原因
(4)一定条件下焙烧可制得
 负载型催化剂。准确称取
负载型催化剂。准确称取 负载型催化剂样品,置于
负载型催化剂样品,置于 锥形瓶中,加入适量稀盐酸,加热溶解后,滴加稍过量的
锥形瓶中,加入适量稀盐酸,加热溶解后,滴加稍过量的 溶液(
溶液( 将
将 还原为
还原为 ),充分反应后,除去过量
),充分反应后,除去过量 。用
。用 溶液滴定至终点(滴定过程中
溶液滴定至终点(滴定过程中 与
与 反应生成
反应生成 和
和 ),消耗
),消耗 溶液
溶液 。计算该
。计算该 负载型催化剂的负载量
负载型催化剂的负载量 ×100%]
×100%]
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】“侯氏制碱法”促进了我国纯碱工业的发展。某化学兴趣小组在实验室中模拟并改进侯氏制碱法用碳酸氢铵(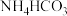 )和氯化钠为主要原料制备碳酸钠的实验流程如图。
)和氯化钠为主要原料制备碳酸钠的实验流程如图。

回答下列问题:
(1)“加热搅拌”中发生反应的化学方程式是___________ ,该反应属于___________ (填基本反应类型)。
(2)“300℃加热”需用到的仪器除酒精灯、坩埚、坩埚钳、泥三角、三角架外,还有___________ 。
(3)除去 溶液中混有的少量
溶液中混有的少量 的最佳方法是
的最佳方法是___________ ,化学方程式为___________ 。
(4)检验 中阳离子的实验方法是
中阳离子的实验方法是___________ 。
(5)现将 和
和 的固体均匀混合物等分成两份。第一份充分加热至恒重,固体质量减少6.2g;第二份与足量稀盐酸充分反应后,加热、蒸干、灼烧,得到固体23.4g。则混合物中
的固体均匀混合物等分成两份。第一份充分加热至恒重,固体质量减少6.2g;第二份与足量稀盐酸充分反应后,加热、蒸干、灼烧,得到固体23.4g。则混合物中 和
和 的物质的量之比为
的物质的量之比为___________ 。
(6)若将 和
和 的固体混合物溶于水,向溶液中加入盐酸,所加盐酸的体积与产生
的固体混合物溶于水,向溶液中加入盐酸,所加盐酸的体积与产生 的体积关系如图所示,则线段)
的体积关系如图所示,则线段)
___________ 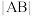 (填“>”“<”或“=”),OA段发生反应的离子方程式为
(填“>”“<”或“=”),OA段发生反应的离子方程式为___________ 。

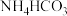 )和氯化钠为主要原料制备碳酸钠的实验流程如图。
)和氯化钠为主要原料制备碳酸钠的实验流程如图。
回答下列问题:
(1)“加热搅拌”中发生反应的化学方程式是
(2)“300℃加热”需用到的仪器除酒精灯、坩埚、坩埚钳、泥三角、三角架外,还有
(3)除去
 溶液中混有的少量
溶液中混有的少量 的最佳方法是
的最佳方法是(4)检验
 中阳离子的实验方法是
中阳离子的实验方法是(5)现将
 和
和 的固体均匀混合物等分成两份。第一份充分加热至恒重,固体质量减少6.2g;第二份与足量稀盐酸充分反应后,加热、蒸干、灼烧,得到固体23.4g。则混合物中
的固体均匀混合物等分成两份。第一份充分加热至恒重,固体质量减少6.2g;第二份与足量稀盐酸充分反应后,加热、蒸干、灼烧,得到固体23.4g。则混合物中 和
和 的物质的量之比为
的物质的量之比为(6)若将
 和
和 的固体混合物溶于水,向溶液中加入盐酸,所加盐酸的体积与产生
的固体混合物溶于水,向溶液中加入盐酸,所加盐酸的体积与产生 的体积关系如图所示,则线段)
的体积关系如图所示,则线段)
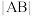 (填“>”“<”或“=”),OA段发生反应的离子方程式为
(填“>”“<”或“=”),OA段发生反应的离子方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
真题
名校
【推荐2】工业生产纯碱的工艺流程示意图如下:
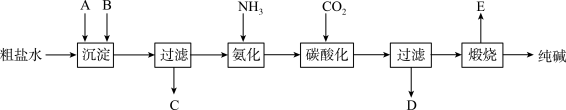
完成下列填空:
(1)粗盐水加入沉淀剂A、B除杂质(沉淀剂A来源于石灰窑厂),写出A、B的化学式。
A__________________________________ B__________________________________
(2)实验室提纯粗盐的实验操作依次为:
取样、______ 、沉淀、______ 、______ 、冷却结晶、______ 、烘干。
(3)工业生产纯碱工艺流程中,碳酸化时产生的现象是____________________________ 。
碳酸化时没有析出碳酸钠晶体,其原因是_______________________________________ 。
(4)碳酸化后过滤,滤液D最主要的成分是_____________________________ (填写化学式),检验这一成分的阴离子的具体方法是:________________________________________ 。
(5)氨碱法流程中氨是循环使用的,为此,滤液D加入石灰水产生氨。加石灰水后所发生的反应的离子方程式为:_________________________________________________________
滤液D加石灰水前先要加热,原因是_____________________________________________ 。
(6)产品纯碱中含有碳酸氢钠。如果用加热分解的方法测定纯碱中碳酸氢钠的质量分数,纯碱中碳酸氢钠的质量分数可表示为:
_____________________________________________________________________________
(注明你的表达式中所用的有关符号的含义)

完成下列填空:
(1)粗盐水加入沉淀剂A、B除杂质(沉淀剂A来源于石灰窑厂),写出A、B的化学式。
A
(2)实验室提纯粗盐的实验操作依次为:
取样、
(3)工业生产纯碱工艺流程中,碳酸化时产生的现象是
碳酸化时没有析出碳酸钠晶体,其原因是
(4)碳酸化后过滤,滤液D最主要的成分是
(5)氨碱法流程中氨是循环使用的,为此,滤液D加入石灰水产生氨。加石灰水后所发生的反应的离子方程式为:
滤液D加石灰水前先要加热,原因是
(6)产品纯碱中含有碳酸氢钠。如果用加热分解的方法测定纯碱中碳酸氢钠的质量分数,纯碱中碳酸氢钠的质量分数可表示为:
(注明你的表达式中所用的有关符号的含义)
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】我国化学家侯德榜改革国外的纯碱生产工艺,探索出了一种生产纯碱的方法,其生产流程可简要表示如下:
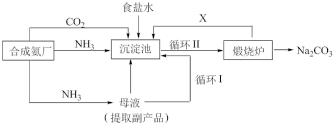
(1)上述生产纯碱的方法称为________ ,副产品的一种用途为_______ 。
(2)沉淀池中发生反应的化学方程式是__________________ 。
(3)写出上述流程中X物质的分子式为________ 。
(4)从沉淀池中取出沉淀的操作叫________________ 。
(5)为检验产品碳酸钠中是否含有氯化钠,可取少量试样溶于水后,再滴加________ 。
(6)向母液中通氨气,加入细小食盐颗粒,冷却析出副产品,通氨气的作用有________ 。
a.增大 的浓度,使NH4Cl更多地析出
的浓度,使NH4Cl更多地析出
b.使NaHCO3更多地析出
c.使NaHCO3转化为Na2CO3,提高析出NH4Cl的纯度

(1)上述生产纯碱的方法称为
(2)沉淀池中发生反应的化学方程式是
(3)写出上述流程中X物质的分子式为
(4)从沉淀池中取出沉淀的操作叫
(5)为检验产品碳酸钠中是否含有氯化钠,可取少量试样溶于水后,再滴加
(6)向母液中通氨气,加入细小食盐颗粒,冷却析出副产品,通氨气的作用有
a.增大
 的浓度,使NH4Cl更多地析出
的浓度,使NH4Cl更多地析出b.使NaHCO3更多地析出
c.使NaHCO3转化为Na2CO3,提高析出NH4Cl的纯度
您最近一年使用:0次



