工业上用铝土矿(含氧化铝、氧化铁)制取铝的过程如下:
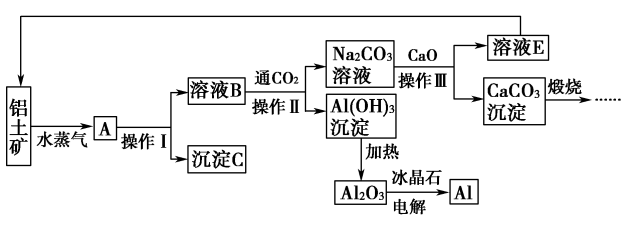
请回答下列问题:
(1)请说出沉淀C在工业上的一种用途:_____________________ 。
(2)生产过程中,除NaOH、H2O可以循环使用外,还可以循环使用的物质有_____ (填化学式)。
(3)操作Ⅰ、操作Ⅱ和操作Ⅲ都是________ (填操作名称)。实验室洗涤Al(OH)3沉淀的方法是__________________________________________ 。
(4)电解熔融的氧化铝,若得到标准状况下22.4 L O2,则同时生成铝的质量为________ g。
(5)写出Na2CO3溶液与CaO反应的离子方程式:_____________________ 。

请回答下列问题:
(1)请说出沉淀C在工业上的一种用途:
(2)生产过程中,除NaOH、H2O可以循环使用外,还可以循环使用的物质有
(3)操作Ⅰ、操作Ⅱ和操作Ⅲ都是
(4)电解熔融的氧化铝,若得到标准状况下22.4 L O2,则同时生成铝的质量为
(5)写出Na2CO3溶液与CaO反应的离子方程式:
更新时间:2018-09-06 11:01:23
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】工业上,处理低品位黄铜矿[二硫化亚铁铜(CuFeS2)含量较低]常采用生物堆浸法。堆浸所得的溶液可用于制备绿矾(FeSO4∙7H2O)和胆矾(CuSO4∙5H2O)。相关流程如下图。
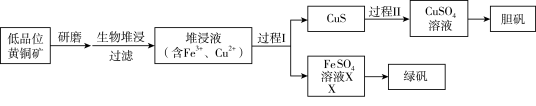
已知:①溶液中的c(H+)越大,pH越小,酸性越强。
②生物堆浸使用的氧化亚铁硫杆菌(T.f细菌)在pH1.0~6.0范围内可保持活性。
③溶液中pH很小时,金属通常以离子形式存在,随着pH增大,有些离子会形成氢氧化物沉淀(即使pH<7也可沉淀),不同离子形成沉淀时的pH如下表所示。
(1)生物堆浸过程的反应在T。f细菌的作用下进行,主要包括两个阶段,第一阶段是在T。f细菌作用下,将黄铜矿溶解,第二阶段为Fe2+继续被氧化转变成Fe3+。
①补全第一阶段反应的离子方程式(反应物已配平):_______ 。CuFeS2+4H++O2 =_______。
=_______。
②写出第二阶段反应的离子方程式:_______ 。
(2)结合已知推断:生物堆浸过程中,应控制溶液的pH在_______ 范围内。
(3)已知:CuS是一种难溶于水的黑色固体。过程II中,用H2O2和稀硫酸处理后,CuS完全溶解 ,用离子方程式表示H2O2的作用是_______ 。
(4)绿矾的纯度可通过其与KMnO4反应测定。取mg绿矾晶体,加适量稀硫酸溶解,与物质的量浓度为cmol/L的KMnO4溶液恰好反应时,消耗KMnO4溶液的体积为VmL。绿矾晶体质量分数的计算式为_______ 。(已知:FeSO4·7H2O摩尔质量为278g/mol)

已知:①溶液中的c(H+)越大,pH越小,酸性越强。
②生物堆浸使用的氧化亚铁硫杆菌(T.f细菌)在pH1.0~6.0范围内可保持活性。
③溶液中pH很小时,金属通常以离子形式存在,随着pH增大,有些离子会形成氢氧化物沉淀(即使pH<7也可沉淀),不同离子形成沉淀时的pH如下表所示。
| Fe3+ | Cu2+ | Fe2+ | |
| 开始沉淀时的pH | 1.5 | 4.2 | 6.3 |
| 完全沉淀时的pH | 2.8 | 6.7 | 8.3 |
①补全第一阶段反应的离子方程式(反应物已配平):
 =_______。
=_______。②写出第二阶段反应的离子方程式:
(2)结合已知推断:生物堆浸过程中,应控制溶液的pH在
(3)已知:CuS是一种难溶于水的黑色固体。过程II中,用H2O2和稀硫酸处理后,CuS
(4)绿矾的纯度可通过其与KMnO4反应测定。取mg绿矾晶体,加适量稀硫酸溶解,与物质的量浓度为cmol/L的KMnO4溶液恰好反应时,消耗KMnO4溶液的体积为VmL。绿矾晶体质量分数的计算式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】某同学利用如图装置(夹持仪器已略去)研究纯碱和小苏打的性质。

(1)该实验的目的是___________ 。
(2)观察到有白色沉淀生成的烧杯是___________ (填字母)。
(3)实验结论是___________ 。
(4)为进一步定量研究碳酸氢钠的性质,甲同学用天平准确称量8.4g碳酸氢钠,放入质量为37.4g的坩埚中加热,冷却称量,理论上坩埚及剩余固体的总质量为___________ g,但实际称得的质量比该数值要大,可能的原因是___________ 。

(1)该实验的目的是
(2)观察到有白色沉淀生成的烧杯是
(3)实验结论是
(4)为进一步定量研究碳酸氢钠的性质,甲同学用天平准确称量8.4g碳酸氢钠,放入质量为37.4g的坩埚中加热,冷却称量,理论上坩埚及剩余固体的总质量为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】为了测定某种碱金属的相对原子质量,设计装置如右图。该装置(包括水)的总质量为ag,将质量bg(不足量)碱金属放到水中,立即盖紧瓶塞,反应完全后再称量此装置的总质量为cg,则
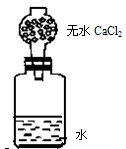
(1)计算该碱金属相对原子质量的数学表达式_________________
(2)无水CaCl2的作用是___________________________________ ,如果不用无水CaCl2,测出的相对原子质量比实际的相对原子质量__________ (填写偏大、偏小或相等)。

(1)计算该碱金属相对原子质量的数学表达式
(2)无水CaCl2的作用是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】某铜矿石的主要成分是Cu2O,还含有少量的A12O3、Fe2O3和SiO2。某工厂利用此矿石炼制粗铜的工艺流程如图所示(已知:Cu2O+2H+ =Cu+Cu2++H2O)。
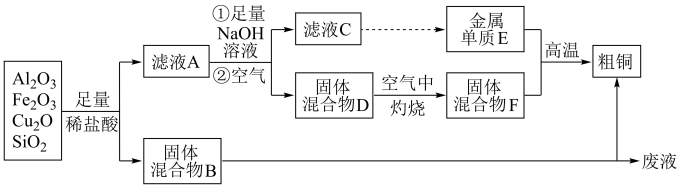
(1)加入足量稀盐酸前,需将铜矿石粉碎的目的是______ 。
(2)固体混合物B的成分是_____ 。(填化学式)
(3)NaOH溶液与固体混合物B反应的离子方程式为_______ 。
(4)为使固体混合物D在空气中灼烧完全分解,应______ 后称重,重复多次,直至连续两次测定的实验结果相同(或质量相差小于0.1g)时为止;灼烧时盛装固体混合物的实验仪器是______ 。
(5)金属E与固体混合物F中的某一物质反应可用于焊接钢轨,该反应的化学方程式为_______ ,在实验室中完成此实验还需要的试剂是______ 。(填字母)
a.KClO3 b.KCl c.Mg d.MnO2

(1)加入足量稀盐酸前,需将铜矿石粉碎的目的是
(2)固体混合物B的成分是
(3)NaOH溶液与固体混合物B反应的离子方程式为
(4)为使固体混合物D在空气中灼烧完全分解,应
(5)金属E与固体混合物F中的某一物质反应可用于焊接钢轨,该反应的化学方程式为
a.KClO3 b.KCl c.Mg d.MnO2
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】氧化锆(ZrO2)可用于生产压电陶瓷制品、日用陶瓷,还可用于生产钢及有色金属、光学玻璃等。以锆砂(主要成分为ZrSiO4,含少量Fe2O3、Al2O3、SiO2等杂质)为原料制备氧化锆的工艺流程如下图所示:
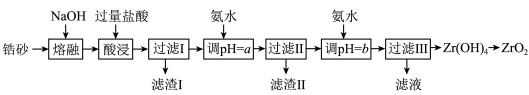
已知:①ZrO2与NaOH反应生成可溶性的Na2ZrO3,Na2ZrO3与盐酸反应生成ZrO2+。
②部分离子在溶液中开始沉淀和完全沉淀的pH如下表:
回答下列问题:
(1)ZrSiO4为硅酸盐,其用氧化物的形式进行表示,化学式为___________ 。
(2)锆砂中加入NaOH熔融,锆砂成分中不参加化学反应的物质是______________ (写化学式)。
(3)酸浸时除发生酸碱中和反应外,生成水的反应的离子方程式还有_____________ (任写一个),滤渣Ⅰ的成分是___________ (写化学式)。
(4)第一次加入氨水,调节pH=a时若用广泛pH试纸检验溶液的pH,则a值应该取_______ (写字母)。
A.3.2 B.5 C.5.2 D.6
(5)滤渣Ⅱ为混合物,写出其中阳离子溶于水无色的一种物质的电子式:______________ 。
(6)为了操作方便,调节pH=b时可不考虑b大小,直接加入过量氨水,这样操作的理论依据是_____________________ ,该操作发生反应的离子方程式为_____________________ 。

已知:①ZrO2与NaOH反应生成可溶性的Na2ZrO3,Na2ZrO3与盐酸反应生成ZrO2+。
②部分离子在溶液中开始沉淀和完全沉淀的pH如下表:
| 金属离子 | Fe3+ | Al3+ | ZrO2+ |
| 开始沉淀时pH | 1.9 | 3.3 | 6.2 |
| 沉淀完全时pH | 3.2 | 5.2 | 8.0 |
回答下列问题:
(1)ZrSiO4为硅酸盐,其用氧化物的形式进行表示,化学式为
(2)锆砂中加入NaOH熔融,锆砂成分中不参加化学反应的物质是
(3)酸浸时除发生酸碱中和反应外,生成水的反应的离子方程式还有
(4)第一次加入氨水,调节pH=a时若用广泛pH试纸检验溶液的pH,则a值应该取
A.3.2 B.5 C.5.2 D.6
(5)滤渣Ⅱ为混合物,写出其中阳离子溶于水无色的一种物质的电子式:
(6)为了操作方便,调节pH=b时可不考虑b大小,直接加入过量氨水,这样操作的理论依据是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】Ⅰ.以黄铁矿(主要成分 )为原料生产硫酸及尾气处理的一种流程如下图所示。回答下列问题:
)为原料生产硫酸及尾气处理的一种流程如下图所示。回答下列问题:
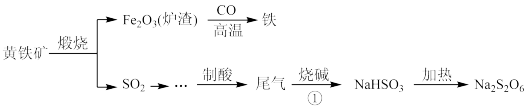
(1)黄铁矿中硫元素的化合价为___________ ,其煅烧的化学反应方程式为___________ 。
(2)焦亚硫酸钠( )是常用的食品抗氧化剂,常用于葡萄酒、果脯等食品中,其在空气中久置会与氧气反应生成
)是常用的食品抗氧化剂,常用于葡萄酒、果脯等食品中,其在空气中久置会与氧气反应生成 ,写出该反应的化学方程式
,写出该反应的化学方程式___________ 。
Ⅱ.聚合硫酸铝铁(PFAS)是一种新型高效水处理剂。以粉煤灰(主要成分为 、
、 、FeO等)为铝源,利用硫铁矿烧渣(主要成分为
、FeO等)为铝源,利用硫铁矿烧渣(主要成分为 、FeO、
、FeO、 等)为铁源,制备PFAS的工艺流程如下:
等)为铁源,制备PFAS的工艺流程如下:
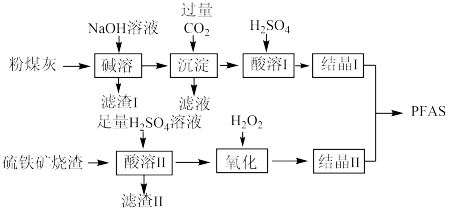
(3)“碱溶”时,粉煤灰发生反应的化学方程式为___________ 。
(4)“酸溶Ⅱ”时,将硫铁矿烧渣粉碎的目的是___________ ,所得滤渣Ⅱ的主要成分为___________ (填化学式)。
(5)“氧化”时应控制温度在50~57℃,其原因是___________ ;“氧化”时反应的离子方程式为___________ 。
 )为原料生产硫酸及尾气处理的一种流程如下图所示。回答下列问题:
)为原料生产硫酸及尾气处理的一种流程如下图所示。回答下列问题:
(1)黄铁矿中硫元素的化合价为
(2)焦亚硫酸钠(
 )是常用的食品抗氧化剂,常用于葡萄酒、果脯等食品中,其在空气中久置会与氧气反应生成
)是常用的食品抗氧化剂,常用于葡萄酒、果脯等食品中,其在空气中久置会与氧气反应生成 ,写出该反应的化学方程式
,写出该反应的化学方程式Ⅱ.聚合硫酸铝铁(PFAS)是一种新型高效水处理剂。以粉煤灰(主要成分为
 、
、 、FeO等)为铝源,利用硫铁矿烧渣(主要成分为
、FeO等)为铝源,利用硫铁矿烧渣(主要成分为 、FeO、
、FeO、 等)为铁源,制备PFAS的工艺流程如下:
等)为铁源,制备PFAS的工艺流程如下:
(3)“碱溶”时,粉煤灰发生反应的化学方程式为
(4)“酸溶Ⅱ”时,将硫铁矿烧渣粉碎的目的是
(5)“氧化”时应控制温度在50~57℃,其原因是
您最近一年使用:0次
【推荐1】某无机盐X除结晶水外,还含两种阳离子和一种阴离子,摩尔质量为392 g·mol-1,为探究其组成和性质,设计并完成了如图实验:

请回答:
(1)X的化学式为_______ 。
(2)红褐色沉淀A生成红色固体B的化学方程式为:_______ 。
(3)设计实验方案检验X溶液中金属阳离子的方法为_______ 。

请回答:
(1)X的化学式为
(2)红褐色沉淀A生成红色固体B的化学方程式为:
(3)设计实验方案检验X溶液中金属阳离子的方法为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】钨是我国丰产元素,是熔点最高的金属,广泛用于拉制灯泡的灯丝,在自然界主要以钨(+6价)酸盐的形式存在。有开采价值的钨矿石之一黑钨矿的主要成分是铁和锰的钨酸盐,化学式常写成FeWO4和MnWO4,钨酸(H2WO4)酸性很弱,难溶于水。碳和金属钨在高温下会反应生成碳化钨。黑钨矿传统冶炼工艺的第一阶段是碱熔法:
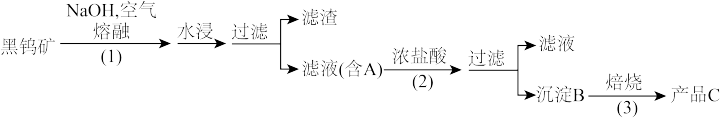
(1)黑钨矿浸入NaOH熔融液过程需通入大量空气,目的是为了使铁和锰转化为氧化物,其中一种红棕色的氧化物化学式为____ 。
(2)已知A的主要成分为Na2WO4,请写出Na2WO4与浓盐酸反应的离子方程式____ 。
(3)上述流程中B、C都是钨的化合物,则步骤(3)中B→C转化属于____ (填四种基本反应类型之一)。
(4)钨冶炼工艺的第二阶段则是用碳、氢气等还原剂把氧化钨(WO3)还原为金属钨。对钨的纯度要求不高时,可用碳作还原剂。写出用碳还原氧化钨制取金属钨的化学方程式:____ 。
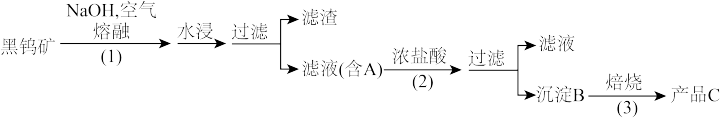
(1)黑钨矿浸入NaOH熔融液过程需通入大量空气,目的是为了使铁和锰转化为氧化物,其中一种红棕色的氧化物化学式为
(2)已知A的主要成分为Na2WO4,请写出Na2WO4与浓盐酸反应的离子方程式
(3)上述流程中B、C都是钨的化合物,则步骤(3)中B→C转化属于
(4)钨冶炼工艺的第二阶段则是用碳、氢气等还原剂把氧化钨(WO3)还原为金属钨。对钨的纯度要求不高时,可用碳作还原剂。写出用碳还原氧化钨制取金属钨的化学方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】下图各物质中,A、B、C是常见金属单质,甲、乙、丙是气体且乙是有特殊颜色的气体(图中有些反应的产物和反应的条件没有全部标出)。

请根据以上信息回答下列问题:
(1)写出:H的化学式_________ ,乙的两种重要用途________________________
(2)写出有关反应的离子方程式:
反应①__________________________________________
反应②____________________________________
(3)判断反应③已经发生的常用试剂是______________________
(4)胶态磁流体(液溶胶)在医学上有重要用途,C单质对应元素的某种纳米级氧化物是磁流体中的重要粒子,该磁流体的主要制备过程如下:(Ⅰ)将NH3通入F、G的混合溶液(F、G物质的量比为1:2)中会生成两种碱。(Ⅱ)这两种碱恰好反应就得到该氧化物。写出(Ⅱ)中反应的化学方程式为:_________________________ ,确定该磁流体己成功制取的方法_________________________________

请根据以上信息回答下列问题:
(1)写出:H的化学式
(2)写出有关反应的离子方程式:
反应①
反应②
(3)判断反应③已经发生的常用试剂是
(4)胶态磁流体(液溶胶)在医学上有重要用途,C单质对应元素的某种纳米级氧化物是磁流体中的重要粒子,该磁流体的主要制备过程如下:(Ⅰ)将NH3通入F、G的混合溶液(F、G物质的量比为1:2)中会生成两种碱。(Ⅱ)这两种碱恰好反应就得到该氧化物。写出(Ⅱ)中反应的化学方程式为:
您最近一年使用:0次
【推荐1】化工生产必须遵循科学原理。请根据下列工艺生产流程回答问题。
(1)某化学课外活动小组以海带为原料获得少量碘,其过程如下图所示:
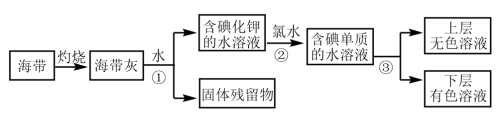
则:操作①的名称是_______ ,操作③使用的试剂(写化学式)_______ 。操作②中发生反应的离子方程式为_______ 。
(2)海水的综合利用可以制备金属钠和镁,其流程如下图所示:
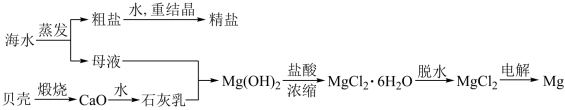
①上述流程中生成Mg(OH)2沉淀的离子方程式为_______ 。Mg(OH)2沉淀和盐酸反应的离子方程式为_______ 。
②实验室里将粗盐制成精盐的过程中,在溶解、过滤、蒸发三个步骤的操作中都要用到玻璃棒,分别说明这三种情况下使用玻璃棒的作用:
溶解时:_______ ;过滤时:_______ ;蒸发时:_______ 。
③工业上把电解饱和食盐水称为“氯碱工业”。请你写出电解饱和食盐水的化学方程式_________ 。
(1)某化学课外活动小组以海带为原料获得少量碘,其过程如下图所示:

则:操作①的名称是
(2)海水的综合利用可以制备金属钠和镁,其流程如下图所示:

①上述流程中生成Mg(OH)2沉淀的离子方程式为
②实验室里将粗盐制成精盐的过程中,在溶解、过滤、蒸发三个步骤的操作中都要用到玻璃棒,分别说明这三种情况下使用玻璃棒的作用:
溶解时:
③工业上把电解饱和食盐水称为“氯碱工业”。请你写出电解饱和食盐水的化学方程式
您最近一年使用:0次
【推荐2】废旧锂离子电池经处理得到的正极活性粉体中含有Li2O、NiO、Co2O3、MnO2、Fe、C、Al、Cu等。采用以下工艺流程可从废旧锂离子电池中分离回收钴、镍、锰,制备正极材料的前驱体(NiCO3·CoCO3·MnCO3)。
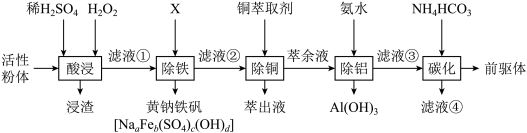
回答下列问题:
(1)“酸浸”温度为85℃,粉体中的钴(以Co2O3表示)还原浸出的化学方程式为_______ ;工业生产中通常不使用浓盐酸代替H2O2的原因是_______ 。
(2)“除铁”时需将溶液的pH调至3左右,加入的化合物X是_______ (填化学式)。
(3)“除铜”时获得萃余液的操作名称是_______ 。
(4)“除铝”时反应的离子方程式为_______ ;萃余液中Co2+的浓度为0.33 mol/L,通过计算说明,常温下除铝控制溶液pH为4.5,是否造成Co2+的损失?_______ (列出算式并给出结论)。已知:(Ksp[Co(OH)2=5.9×10-15)

回答下列问题:
(1)“酸浸”温度为85℃,粉体中的钴(以Co2O3表示)还原浸出的化学方程式为
(2)“除铁”时需将溶液的pH调至3左右,加入的化合物X是
(3)“除铜”时获得萃余液的操作名称是
(4)“除铝”时反应的离子方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】现有含NaCl、Na2SO4和NaNO3的混合物,选择适当的试剂除去溶液中的NaCl和Na2SO4,从而得到纯净的NaNO3溶液。相应的实验过程可用下图表示:
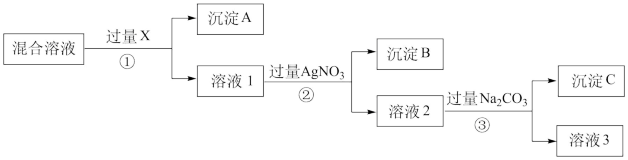
请回答下列问题:
(1)写出实验流程中下列物质的化学式:试剂X_____
(2)上述实验流程中加入过量的Na2CO3的目的是_______ 。
(3)按此实验方案得到的溶液3中肯定含有______ (填化学式)杂质,为了解决这个问题,可以向溶液3中加入适量的_______ ,之后若要获得固体NaNO3需进行的实验操作是______ (填操作名称).

请回答下列问题:
(1)写出实验流程中下列物质的化学式:试剂X
(2)上述实验流程中加入过量的Na2CO3的目的是
(3)按此实验方案得到的溶液3中肯定含有
您最近一年使用:0次



