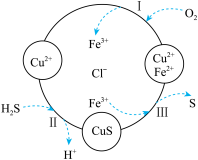
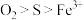下列有关氧化还原反应的说法正确的是
| A.由反应O3+2I-+H2O=O2+I2+2OH-可知,氧化性:I2>O2 |
| B.反应O3+2I-+H2O=O2+I2+2OH-中,生成1molI2时转移2 mol电子 |
| C.“银针验毒”的反应原理之一是:4Ag +2H2S +O2=2X +2H2O,Ag得到电子 |
| D.反应4Ag +2H2S +O2= 2X +2H2O中,X为AgS |
更新时间:2024/01/08 11:16:16
|
相似题推荐
【推荐1】已知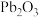 与
与 溶液发生反应Ⅰ:
溶液发生反应Ⅰ: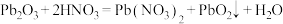 ,
, 与酸化的
与酸化的 溶液发生反应Ⅱ:
溶液发生反应Ⅱ: ,下列说法正确的是
,下列说法正确的是
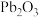 与
与 溶液发生反应Ⅰ:
溶液发生反应Ⅰ: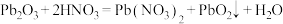 ,
, 与酸化的
与酸化的 溶液发生反应Ⅱ:
溶液发生反应Ⅱ: ,下列说法正确的是
,下列说法正确的是A.在反应Ⅰ中,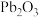 既是氧化剂,又是还原剂 既是氧化剂,又是还原剂 |
B.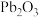 与盐酸反应: 与盐酸反应: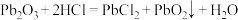 |
C.PbO与 溶液反应: 溶液反应: |
D.由反应Ⅰ、Ⅱ可知氧化性: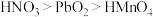 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】根据表中信息,判断下列叙述中正确的是
| 序号 | 氧化剂 | 还原剂 | 其他反应物 | 氧化产物 | 还原产物 |
| ① | Cl2(足量) | FeBr2 | / | Fe3+、Br2 | |
| ② | KClO3 | 浓盐酸 | / | Cl2 | |
| ③ | KMnO4 | H2O2 | H2SO4 | O2 | Mn2+ |
| A.氧化性强弱比较:KClO3>Fe3+>Cl2>Br2 |
| B.反应①中,发生反应2Cl2+2Fe2++2Br-=2Fe3++Br2+4Cl- |
| C.反应②中的Cl2既是氧化产物又是还原产物 |
D.③中反应的离子方程式为2MnO +3H2O2+6H+=2Mn2++4O2↑+6H2O +3H2O2+6H+=2Mn2++4O2↑+6H2O |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】将铜和镁的合金2.3g完全溶于浓硝酸,若反应中硝酸被还原只产生0.1moLNO2和0.0075molN2O4,在反应后的溶液中加入足量NaOH溶液,生成沉淀的质量约为
| A.3.52g | B.4.26g | C.4.13g | D.4.51g |
您最近一年使用:0次
【推荐2】NH4NO3在某温度下受热分解反应为4NH4NO3 3N2↑+2NO2↑+8H2O,下列说法中正确的是
3N2↑+2NO2↑+8H2O,下列说法中正确的是
 3N2↑+2NO2↑+8H2O,下列说法中正确的是
3N2↑+2NO2↑+8H2O,下列说法中正确的是| A.还原产物只有NO2 |
| B.该反应中还原产物和氧化产物的物质的量之比为3:2 |
| C.反应转移4mol电子时,生成22.4LN2 |
| D.0.4molNH4NO3完全分解转移的电子数目为2mol |
您最近一年使用:0次

 和
和 混合气体,通入
混合气体,通入 、
、 、
、 的混合溶液,转化关系如图所示。下列描述正确的是
的混合溶液,转化关系如图所示。下列描述正确的是