完成下列方程式
(1)在298K,101KPa条件下,1mol氢气在氧气中燃烧生成液态水放出285.8kJ热量,写出该反应的热化学方程式:___________ 。
(2)如图所示,写出①固体C和氧气生成CO2气体的热化学方程式:___________ 。
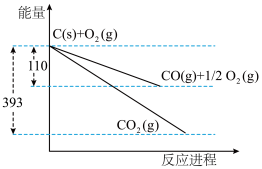
②固体C和CO2气体生成CO气体的热化学方程式:___________ 。
(3)电解质为H2SO4溶液的CH4和O2燃料电池负极电极反应式:___________ 。
(4)某碱性电池的电池反应为3Zn+2K2FeO4 Fe2O3+ZnO+2K2ZnO2,该电池充电时阳极的电极反应式:
Fe2O3+ZnO+2K2ZnO2,该电池充电时阳极的电极反应式:___________ 。
(1)在298K,101KPa条件下,1mol氢气在氧气中燃烧生成液态水放出285.8kJ热量,写出该反应的热化学方程式:
(2)如图所示,写出①固体C和氧气生成CO2气体的热化学方程式:

②固体C和CO2气体生成CO气体的热化学方程式:
(3)电解质为H2SO4溶液的CH4和O2燃料电池负极电极反应式:
(4)某碱性电池的电池反应为3Zn+2K2FeO4
 Fe2O3+ZnO+2K2ZnO2,该电池充电时阳极的电极反应式:
Fe2O3+ZnO+2K2ZnO2,该电池充电时阳极的电极反应式:
更新时间:2024-01-17 18:17:28
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】有一化合物X,其水溶液为浅绿色,可发生如下的转化关系(部分反应物、生成物已略)。其中B、D、E、F均为无色气体,M、L为常见的金属单质,C为难溶于水的红褐色固体。在混合液中加入BaCl2溶液可生成不溶于稀盐酸的白色沉淀,H和M反应可放出大量的热。请回答下列问题:

(1)B的电子式为____________ 。
(2)电解混合液时阳极反应式为_______________________ 。
(3)写出L长期放置在潮湿空气中的腐蚀原理:
负极:___________________________________ 。
正极:___________________________________ 。
总反应:______________________________________________________ 。
(4)已知a g E气体在D中完全燃烧生成稳定的化合物时,放出b kJ的热量,写出E气体燃烧热的热化学方程式为___________________________ 。

(1)B的电子式为
(2)电解混合液时阳极反应式为
(3)写出L长期放置在潮湿空气中的腐蚀原理:
负极:
正极:
总反应:
(4)已知a g E气体在D中完全燃烧生成稳定的化合物时,放出b kJ的热量,写出E气体燃烧热的热化学方程式为
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】化学在能源开发与利用中起着十分关键的作用。
(1)蕴藏在海底的“可燃冰”是高压下形成的外现象冰的甲烷水合物固体。甲烷气体燃烧和水汽化的热化学方程式分别为:
CH4(g)+ 2O2(g)═ CO2(g)+ 2H2O(g)△H=﹣802.3kJ•mol﹣1,
H2O(l)═ H2O(g)△H= +44kJ•mol﹣1;
则356g“可燃冰”(分子式为CH4•9H2O)释放的甲烷气体完全燃烧生成液态水,放出的热量为________ 。
(2)0.3mol的气态高能燃料乙硼烷(B2H6)在氧气中燃烧,生成固态三氧化二硼和液态水,放出649.5kJ热量,其热化学方程式为________ 。
(3)家用液化气中主要成分之一是丁烷(C4H10)。常温常压时,当1g丁烷完全燃烧并生成CO2和液态水时,放出热量50kJ。试写出该状态下表示丁烷燃烧热的热化学方程式________ 。
(4)联合国气候变化大会于2009年12月7~18日在哥本哈根召开。中国政府承诺到2020年,单位GDP二氧化碳排放比2005年下降40%~45%。
①有效“减碳”的手段之一是节能。下列制氢方法最节能的是________ (填字母序号)。
A.电解水制氢:2H2O 2H2↑+O2↑
2H2↑+O2↑
B.高温使水分解制氢:2H2O 2H2↑+O2↑
2H2↑+O2↑
C.太阳光催化分解水制氢:2H2O 2H2↑+O2↑
2H2↑+O2↑
D.天然气制氢:CH4+H2O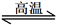 CO+3H2
CO+3H2
②用CO2和氢气合成CH3OCH3(甲醚)是解决能源危机的研究方向之一。
已知:CO(g)+2H2(g) CH3OH(g)△H=﹣90.7kJ•mol﹣1
CH3OH(g)△H=﹣90.7kJ•mol﹣1
2CH3OH(g) CH3OCH3(g)+H2O(g)△H=﹣23.5kJ•mol﹣1
CH3OCH3(g)+H2O(g)△H=﹣23.5kJ•mol﹣1
CO(g)+H2O(g) CO2(g)+H2(g)△H=﹣41.2kJ•mol﹣1
CO2(g)+H2(g)△H=﹣41.2kJ•mol﹣1
则CO2和氢气合成CH3OCH3(g)和水蒸气的热化学方程式为________ 。
(1)蕴藏在海底的“可燃冰”是高压下形成的外现象冰的甲烷水合物固体。甲烷气体燃烧和水汽化的热化学方程式分别为:
CH4(g)+ 2O2(g)═ CO2(g)+ 2H2O(g)△H=﹣802.3kJ•mol﹣1,
H2O(l)═ H2O(g)△H= +44kJ•mol﹣1;
则356g“可燃冰”(分子式为CH4•9H2O)释放的甲烷气体完全燃烧生成液态水,放出的热量为
(2)0.3mol的气态高能燃料乙硼烷(B2H6)在氧气中燃烧,生成固态三氧化二硼和液态水,放出649.5kJ热量,其热化学方程式为
(3)家用液化气中主要成分之一是丁烷(C4H10)。常温常压时,当1g丁烷完全燃烧并生成CO2和液态水时,放出热量50kJ。试写出该状态下表示丁烷燃烧热的热化学方程式
(4)联合国气候变化大会于2009年12月7~18日在哥本哈根召开。中国政府承诺到2020年,单位GDP二氧化碳排放比2005年下降40%~45%。
①有效“减碳”的手段之一是节能。下列制氢方法最节能的是
A.电解水制氢:2H2O
 2H2↑+O2↑
2H2↑+O2↑B.高温使水分解制氢:2H2O
 2H2↑+O2↑
2H2↑+O2↑C.太阳光催化分解水制氢:2H2O
 2H2↑+O2↑
2H2↑+O2↑D.天然气制氢:CH4+H2O
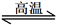 CO+3H2
CO+3H2②用CO2和氢气合成CH3OCH3(甲醚)是解决能源危机的研究方向之一。
已知:CO(g)+2H2(g)
 CH3OH(g)△H=﹣90.7kJ•mol﹣1
CH3OH(g)△H=﹣90.7kJ•mol﹣12CH3OH(g)
 CH3OCH3(g)+H2O(g)△H=﹣23.5kJ•mol﹣1
CH3OCH3(g)+H2O(g)△H=﹣23.5kJ•mol﹣1CO(g)+H2O(g)
 CO2(g)+H2(g)△H=﹣41.2kJ•mol﹣1
CO2(g)+H2(g)△H=﹣41.2kJ•mol﹣1则CO2和氢气合成CH3OCH3(g)和水蒸气的热化学方程式为
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】氮是重要的非金属元素,其化合物在生产、生活中广泛存在。
(1)键能是指在将1mol理想气体分子AB拆开为中性气态原子A和B所需的能量。已知下列化学键的键能如下表:
写出1mol气态肼(H2N—NH2)燃烧生成氮气和气态水的热化学方程式________ 。
(2)用焦炭还原NO的反应为:2NO(g)+C(s) N2(g)+CO2(g),向容积均为1L的甲、乙、丙三个恒容恒温(反应温度分别为400℃、400℃、T℃)容器中分别加入足量的焦炭和一定量的NO,测得各容器中n(NO)随反应时间t的变化情况如下表所示:
N2(g)+CO2(g),向容积均为1L的甲、乙、丙三个恒容恒温(反应温度分别为400℃、400℃、T℃)容器中分别加入足量的焦炭和一定量的NO,测得各容器中n(NO)随反应时间t的变化情况如下表所示:
① 该反应为________ (填“放热”或“吸热”)反应。
② 乙容器在50min时达到平衡状态,则NO的浓度是____________ ,0~50min内用NO的浓度变化表示的平均反应速率v(NO)=____________ 。
(3)用焦炭还原NO2的反应为:2NO2(g)+2C(s) N2(g)+2CO2(g),在恒温条件下,1molNO2和足量C发生该反应,测得平衡时NO2和CO2的物质的量浓度与平衡总压的关系如图所示:
N2(g)+2CO2(g),在恒温条件下,1molNO2和足量C发生该反应,测得平衡时NO2和CO2的物质的量浓度与平衡总压的关系如图所示:
① A、C两点的浓度平衡常数关系:Kc(A)______ Kc(C)(填“<”、“>”或“=”)。
② A、B、C三点中NO2的转化率最高的是______ (填“A”、“B”或“C”)点。
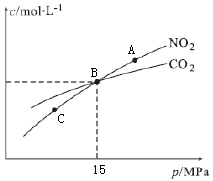
③ 计算B点时该反应的压强平衡常数Kp(B)=______ (Kp是用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(1)键能是指在将1mol理想气体分子AB拆开为中性气态原子A和B所需的能量。已知下列化学键的键能如下表:
| 化学键 | N≡N | O=O | N—N | N—H | O—H |
| 键能/ kJ·mol‾1 | 946 | 497 | 193 | 391 | 463 |
写出1mol气态肼(H2N—NH2)燃烧生成氮气和气态水的热化学方程式
(2)用焦炭还原NO的反应为:2NO(g)+C(s)
 N2(g)+CO2(g),向容积均为1L的甲、乙、丙三个恒容恒温(反应温度分别为400℃、400℃、T℃)容器中分别加入足量的焦炭和一定量的NO,测得各容器中n(NO)随反应时间t的变化情况如下表所示:
N2(g)+CO2(g),向容积均为1L的甲、乙、丙三个恒容恒温(反应温度分别为400℃、400℃、T℃)容器中分别加入足量的焦炭和一定量的NO,测得各容器中n(NO)随反应时间t的变化情况如下表所示:| t/min | 0 | 10 | 20 | 30 | 40 |
| n(NO)(甲容器)/mol | 2.00 | 1.50 | 1.10 | 0.80 | 0.80 |
| n(NO)(乙容器)/mol | 1.00 | 0.80 | 0.65 | 0.53 | 0.45 |
| n(NO)(丙容器)/mol | 2.00 | 1.45 | 1.00 | 1.00 | 1.00 |
① 该反应为
② 乙容器在50min时达到平衡状态,则NO的浓度是
(3)用焦炭还原NO2的反应为:2NO2(g)+2C(s)
 N2(g)+2CO2(g),在恒温条件下,1molNO2和足量C发生该反应,测得平衡时NO2和CO2的物质的量浓度与平衡总压的关系如图所示:
N2(g)+2CO2(g),在恒温条件下,1molNO2和足量C发生该反应,测得平衡时NO2和CO2的物质的量浓度与平衡总压的关系如图所示:① A、C两点的浓度平衡常数关系:Kc(A)
② A、B、C三点中NO2的转化率最高的是

③ 计算B点时该反应的压强平衡常数Kp(B)=
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】运用化学反应原理研究化学反应有重要的意义。一定条件下,甲烷与水蒸气发生反应: ,工业上可利用此反应生产合成氨原料气
,工业上可利用此反应生产合成氨原料气 。请回答下列问题:
。请回答下列问题:
(1)一定温度下,向2L恒容密闭容器中充入
 和
和
 发生上述反应,
发生上述反应, 的物质的量随时间的变化如图所示。
的物质的量随时间的变化如图所示。
______  ,平衡时
,平衡时 的转化率为
的转化率为_____ 。[转化率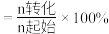 ]
]
(2)若要进一步提高该反应的化学反应速率,除了使用催化剂和升高温度外,还可以采取的措施有______ (任写一条)。
(3)下列能说明上述反应达到平衡状态的是_____ (填代号)。
①
②恒温恒容时,容器内的总压强不随时间而变化
③恒温恒容时,容器内混合气体的密度保持不变
④ 、
、 的浓度保持不变
的浓度保持不变
⑤ 、
、 的物质的量之比为1:3
的物质的量之比为1:3
⑥断开
 键的同时断开
键的同时断开
 键
键
(4)已知1g 气体完全燃烧,可放出10.1kJ的热,写出
气体完全燃烧,可放出10.1kJ的热,写出 完全燃烧的热化学方程式
完全燃烧的热化学方程式______ 。
 ,工业上可利用此反应生产合成氨原料气
,工业上可利用此反应生产合成氨原料气 。请回答下列问题:
。请回答下列问题:(1)一定温度下,向2L恒容密闭容器中充入

 和
和
 发生上述反应,
发生上述反应, 的物质的量随时间的变化如图所示。
的物质的量随时间的变化如图所示。

 ,平衡时
,平衡时 的转化率为
的转化率为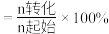 ]
](2)若要进一步提高该反应的化学反应速率,除了使用催化剂和升高温度外,还可以采取的措施有
(3)下列能说明上述反应达到平衡状态的是
①

②恒温恒容时,容器内的总压强不随时间而变化
③恒温恒容时,容器内混合气体的密度保持不变
④
 、
、 的浓度保持不变
的浓度保持不变⑤
 、
、 的物质的量之比为1:3
的物质的量之比为1:3⑥断开

 键的同时断开
键的同时断开
 键
键(4)已知1g
 气体完全燃烧,可放出10.1kJ的热,写出
气体完全燃烧,可放出10.1kJ的热,写出 完全燃烧的热化学方程式
完全燃烧的热化学方程式
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐2】合成氨技术的创立开辟了人工固氮的重要途径,解决了亿万人口生存问题。回答下列问题:
(1)科学家研究利用铁触媒催化合成氨的反应历程如图所示,其中吸附在催化剂表面的物种用“ad”标记。
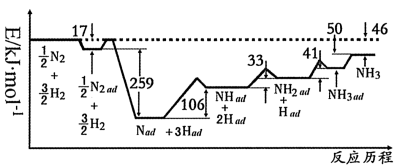
由图可知合成氨反应的热化学方程式为___ ,写出该历程中速率最慢一步的反应___ 。
(2)工业合成氨反应为:N2(g)+3H2(g) 2NH3(g),当进料体积比V(N2):V(H2)=1:3时,平衡气体中NH3的物质的量分数随温度和压强变化的关系如图所示:
2NH3(g),当进料体积比V(N2):V(H2)=1:3时,平衡气体中NH3的物质的量分数随温度和压强变化的关系如图所示:
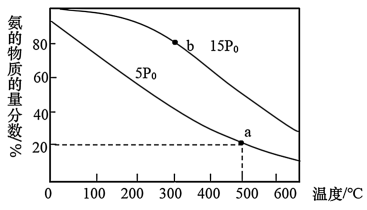
①该反应的平衡常数K(a)___ K(b)(填“<”或“=”或“>”)。
②500℃、压强为5P0时,Kp=___ [Kp为平衡分压代替平衡浓度计算求得的平衡常数(分压=总压×物质的量分数)]。
(3)科学家利用生物燃料电池原理研究室温下氨的合成并取得初步成果,电池工作时MV2+/MV+在电极与酶之间传递电子,示意图如图所示。

①A极是___ (填“正极”或“负极”),电极反应为___ 。
②电池工作时在固氮酶表面发生的反应为___ 。
(1)科学家研究利用铁触媒催化合成氨的反应历程如图所示,其中吸附在催化剂表面的物种用“ad”标记。

由图可知合成氨反应的热化学方程式为
(2)工业合成氨反应为:N2(g)+3H2(g)
 2NH3(g),当进料体积比V(N2):V(H2)=1:3时,平衡气体中NH3的物质的量分数随温度和压强变化的关系如图所示:
2NH3(g),当进料体积比V(N2):V(H2)=1:3时,平衡气体中NH3的物质的量分数随温度和压强变化的关系如图所示:
①该反应的平衡常数K(a)
②500℃、压强为5P0时,Kp=
(3)科学家利用生物燃料电池原理研究室温下氨的合成并取得初步成果,电池工作时MV2+/MV+在电极与酶之间传递电子,示意图如图所示。

①A极是
②电池工作时在固氮酶表面发生的反应为
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】碳是形成化合物种类最多的元素,其单质及化合物是人类生产生活的主要能源物质。请回答下列问题I:
(1)有机物M经过太阳光光照可转化成N,转化过程如下:
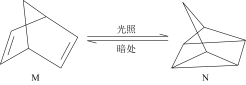 ΔH=+88.6 kJ·mol-1。
ΔH=+88.6 kJ·mol-1。
则M、N相比,较稳定的是_______ 。
(2)火箭和导弹表面的薄层是耐高温物质。将石墨、铝粉和二氧化钛按一定比例混合在高温下煅烧,所得物质可作耐高温材料,4Al(s)+3TiO2(s)+3C(s)=2Al2O3(s)+3TiC(s) ΔH=-1 176 kJ·mol-1,则反应过程中,每转移1 mol电子放出的热量为_______ kJ。
(3)CH4、H2、C都是优质的能源物质,它们燃烧的热化学方程式分别为
①CH4(g)+2O2(g) = CO2(g)+2H2O(l) ΔH=-890.3 kJ·mol-1;
②2H2(g)+O2(g) = 2H2O(l) ΔH=-571.6 kJ·mol-1;
③C(s)+O2(g) =CO2(g) ΔH=-393.5 kJ·mol-1。
CH4、H2组成的混合气体2mol,完全燃烧后放出热量1297.0kJ能量,该混合气体中CH4与H2的物质的量之比n(CH4):n(H2) =_______ ; C(s)与H2(g)不反应,所以C(s)+2H2(g)=CH4(g)的反应热无法直接测量,但通过上述反应可求出其反应热ΔH=_______ kJ·mol-1。
(4)饮用水中的NO 主要来自于NH
主要来自于NH 。已知在微生物的作用下,NH
。已知在微生物的作用下,NH 经过两步反应被氧化成NO
经过两步反应被氧化成NO 。两步反应的能量变化示意图如下:
。两步反应的能量变化示意图如下:
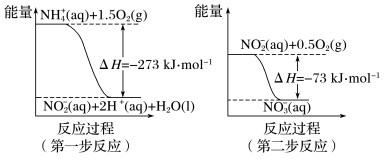
1 mol NH 全部被氧化成NO
全部被氧化成NO 的热化学方程式为
的热化学方程式为_______ 。
II.一种三室微生物燃料电池可用于污水净化、海水淡化,其工作原理如图所示

图中有机废水中有机物可用C6H10O5表示,回答下列问题。
(5)海水中的Na+由中间室移向_______ (选填“左”或“右”)室。
(6)该电池负极的电极反应方程式为_______ 。
(7)电路中每通过1 mol电子,产生标准状况下气体的体积为_______ L。
(1)有机物M经过太阳光光照可转化成N,转化过程如下:
 ΔH=+88.6 kJ·mol-1。
ΔH=+88.6 kJ·mol-1。则M、N相比,较稳定的是
(2)火箭和导弹表面的薄层是耐高温物质。将石墨、铝粉和二氧化钛按一定比例混合在高温下煅烧,所得物质可作耐高温材料,4Al(s)+3TiO2(s)+3C(s)=2Al2O3(s)+3TiC(s) ΔH=-1 176 kJ·mol-1,则反应过程中,每转移1 mol电子放出的热量为
(3)CH4、H2、C都是优质的能源物质,它们燃烧的热化学方程式分别为
①CH4(g)+2O2(g) = CO2(g)+2H2O(l) ΔH=-890.3 kJ·mol-1;
②2H2(g)+O2(g) = 2H2O(l) ΔH=-571.6 kJ·mol-1;
③C(s)+O2(g) =CO2(g) ΔH=-393.5 kJ·mol-1。
CH4、H2组成的混合气体2mol,完全燃烧后放出热量1297.0kJ能量,该混合气体中CH4与H2的物质的量之比n(CH4):n(H2) =
(4)饮用水中的NO
 主要来自于NH
主要来自于NH 。已知在微生物的作用下,NH
。已知在微生物的作用下,NH 经过两步反应被氧化成NO
经过两步反应被氧化成NO 。两步反应的能量变化示意图如下:
。两步反应的能量变化示意图如下:
1 mol NH
 全部被氧化成NO
全部被氧化成NO 的热化学方程式为
的热化学方程式为II.一种三室微生物燃料电池可用于污水净化、海水淡化,其工作原理如图所示

图中有机废水中有机物可用C6H10O5表示,回答下列问题。
(5)海水中的Na+由中间室移向
(6)该电池负极的电极反应方程式为
(7)电路中每通过1 mol电子,产生标准状况下气体的体积为
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】甲醛(HCHO)在化工、医药、农药等方面有广泛的应用.
(1)甲醇脱氢法可制备甲醛,反应方程式为CH3OH=HCHO+H2。
①发生反应时的过程如图所示,从热效应角度判断,可知该反应为___ 反应。
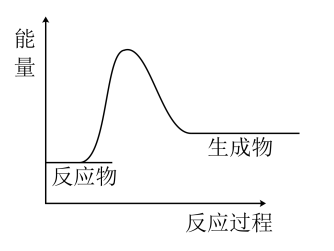
②下列方法中能减慢反应速率的是__ (填字母)
a.使用催化剂 b.升高温度 c.降低反应物浓度
(2)甲醛超标会危害人体健康,需对甲醛含量检测及处理。
①某甲醛气体探测仪利用燃料电池工作原理,其结构如图所示。电极a为__ (填“正”或“负”)极,在电极b上发生的反应类型为__ 反应(填“氧化”或“还原”)。
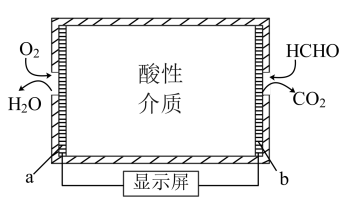
②探测仪工作时,电子从__ 极流出(填“a”或“b”),b电极反应式为__ 。
③如果在外电路中有1mol电子转移,则消耗标准状况下Q2的体积为__ L。
(1)甲醇脱氢法可制备甲醛,反应方程式为CH3OH=HCHO+H2。
①发生反应时的过程如图所示,从热效应角度判断,可知该反应为

②下列方法中能减慢反应速率的是
a.使用催化剂 b.升高温度 c.降低反应物浓度
(2)甲醛超标会危害人体健康,需对甲醛含量检测及处理。
①某甲醛气体探测仪利用燃料电池工作原理,其结构如图所示。电极a为

②探测仪工作时,电子从
③如果在外电路中有1mol电子转移,则消耗标准状况下Q2的体积为
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】某同学用如图装置电解硫酸钾溶液来获得氧气、氢气、硫酸和氢氧化钾。
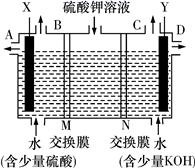
(1)Y极与电源的___________ (填“正”或“负”)极相连,氧气从___________ (填“A”“B”“C”或“D”)口导出。
(2)离子交换膜只允许一类离子通过,则N为___________ (填“阴离子”或“阳离子”,下同)交换膜,M为___________ 交换膜,图中少量硫酸和少量氢氧化钾的作用是___________ 。
(3)若将制得的氢气、氧气和氢氧化钾溶液组合为氢氧燃料电池(石墨为电极),则电池负极的电极反应式为___________ 。
(4)若使用铅蓄电池作电源完成上述电解(铅蓄电池的工作原理为:Pb+PbO2+2H2SO4=2PbSO4+2H2O),当制得5.6 L标准状况下的氢气时,理论上铅蓄电池消耗硫酸___________ mol,负极板质量增加___________ g。

(1)Y极与电源的
(2)离子交换膜只允许一类离子通过,则N为
(3)若将制得的氢气、氧气和氢氧化钾溶液组合为氢氧燃料电池(石墨为电极),则电池负极的电极反应式为
(4)若使用铅蓄电池作电源完成上述电解(铅蓄电池的工作原理为:Pb+PbO2+2H2SO4=2PbSO4+2H2O),当制得5.6 L标准状况下的氢气时,理论上铅蓄电池消耗硫酸
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】CO2的利用是国际社会普遍关注的问题。
(1)CO2的电子式是______ 。
(2)CO2在催化剂作用下可以直接转化为乙二醇和甲醇,但若反应温度过高,乙二醇会深度加氢生成乙醇。
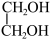 (g)+H2(g)
(g)+H2(g) C2H5OH(g)+H2(g)
C2H5OH(g)+H2(g)  H=-94.8kJ·mol-1
H=-94.8kJ·mol-1
获取乙二醇的反应历程可分为如下2步:
Ⅰ. (g)+CO2(g)
(g)+CO2(g)
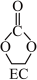 (g)
(g)  H=-60.3kJ·mol-1
H=-60.3kJ·mol-1
Ⅱ.EC加氢生成乙二醇与甲醇
 (g)+CO2(g)+3H2(g)
(g)+CO2(g)+3H2(g)
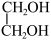 (g)+CH3OH(g)
(g)+CH3OH(g)  H=-131.9kJ·mol-1
H=-131.9kJ·mol-1
① 步骤Ⅱ的热化学方程式是______ 。
② 研究反应温度对EC加氢的影响(反应时间均为4小时),实验数据见下表:
由上表可知,温度越高,EC的转化率越高,原因是______ 。温度升高到220 ℃时,乙二醇的产率反而降低,原因是______ 。
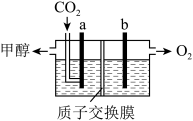
(3)用稀硫酸作电解质溶液,电解CO2可制取甲醇,装置如下图所示,电极a接电源的______ 极(填“正”或“负”),生成甲醇的电极反应式是______ 。
(4)CO2较稳定、能量低。为实现CO2的化学利用,下列研究方向合理的是______ (填序号)。
a.选择高能量的反应物和CO2反应获得低能量的生成物
b.利用电能、光能或热能活化CO2分子
c.选择高效的催化剂
(1)CO2的电子式是
(2)CO2在催化剂作用下可以直接转化为乙二醇和甲醇,但若反应温度过高,乙二醇会深度加氢生成乙醇。
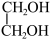 (g)+H2(g)
(g)+H2(g) C2H5OH(g)+H2(g)
C2H5OH(g)+H2(g)  H=-94.8kJ·mol-1
H=-94.8kJ·mol-1获取乙二醇的反应历程可分为如下2步:
Ⅰ.
 (g)+CO2(g)
(g)+CO2(g)
 (g)
(g)  H=-60.3kJ·mol-1
H=-60.3kJ·mol-1 Ⅱ.EC加氢生成乙二醇与甲醇
 (g)+CO2(g)+3H2(g)
(g)+CO2(g)+3H2(g)
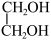 (g)+CH3OH(g)
(g)+CH3OH(g)  H=-131.9kJ·mol-1
H=-131.9kJ·mol-1① 步骤Ⅱ的热化学方程式是
② 研究反应温度对EC加氢的影响(反应时间均为4小时),实验数据见下表:
| 反应温度/ ℃ | EC转化率/ % | 产率/ % | |
| 乙二醇 | 甲醇 | ||
| 160 | 23.8 | 23.2 | 12.9 |
| 180 | 62.1 | 60.9 | 31.5 |
| 200 | 99.9 | 94.7 | 62.3 |
| 220 | 99.9 | 92.4 | 46.1 |
(3)用稀硫酸作电解质溶液,电解CO2可制取甲醇,装置如下图所示,电极a接电源的

(4)CO2较稳定、能量低。为实现CO2的化学利用,下列研究方向合理的是
a.选择高能量的反应物和CO2反应获得低能量的生成物
b.利用电能、光能或热能活化CO2分子
c.选择高效的催化剂
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】回答下列问题:
(1)已知:①Fe(s)+ O2(g)=FeO(s) ΔH1=-272.0kJ·mol-1;
O2(g)=FeO(s) ΔH1=-272.0kJ·mol-1;
②2Al(s)+ O2(g)=Al2O3(s) ΔH2=-1675.7kJ·mol-1。
O2(g)=Al2O3(s) ΔH2=-1675.7kJ·mol-1。
Al和FeO发生铝热反应的热化学方程式是____ 。
(2)N2O和CO是常见的环境污染气体。
对于反应N2O(g)+CO(g) CO2(g)+N2(g)来说,“Fe+”可作为此反应的催化剂。其总反应分两步进行:
CO2(g)+N2(g)来说,“Fe+”可作为此反应的催化剂。其总反应分两步进行:
第一步为Fe++N2O FeO++N2;则第二步为
FeO++N2;则第二步为___ (写方程式)。
已知第二步反应几乎不影响总反应达到平衡所用的时间,由此推知,第一步反应的活化能____ (填“大于”“小于”或“等于”)第二步反应的活化能。
(3)纳米级Cu2O由于具有优良的催化性能而受到关注,采用肼(N2H4)燃料电池为电源,用离子交换膜控制电解液中的c(OH-)制备纳米Cu2O,其装置如图甲、乙。
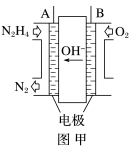
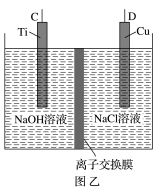
①上述装置中D电极应连接肼燃料电池的____ 极(填“A”或“B”),该电解池中离子交换膜为____ (填“阴”或“阳”)离子交换膜。
②该电解池的阳极反应式为____ ,肼燃料电池中A极发生的电极反应为____ 。
③当反应生成14.4gCu2O时,至少需要肼____ mol。
(1)已知:①Fe(s)+
 O2(g)=FeO(s) ΔH1=-272.0kJ·mol-1;
O2(g)=FeO(s) ΔH1=-272.0kJ·mol-1;②2Al(s)+
 O2(g)=Al2O3(s) ΔH2=-1675.7kJ·mol-1。
O2(g)=Al2O3(s) ΔH2=-1675.7kJ·mol-1。Al和FeO发生铝热反应的热化学方程式是
(2)N2O和CO是常见的环境污染气体。
对于反应N2O(g)+CO(g)
 CO2(g)+N2(g)来说,“Fe+”可作为此反应的催化剂。其总反应分两步进行:
CO2(g)+N2(g)来说,“Fe+”可作为此反应的催化剂。其总反应分两步进行:第一步为Fe++N2O
 FeO++N2;则第二步为
FeO++N2;则第二步为已知第二步反应几乎不影响总反应达到平衡所用的时间,由此推知,第一步反应的活化能
(3)纳米级Cu2O由于具有优良的催化性能而受到关注,采用肼(N2H4)燃料电池为电源,用离子交换膜控制电解液中的c(OH-)制备纳米Cu2O,其装置如图甲、乙。


①上述装置中D电极应连接肼燃料电池的
②该电解池的阳极反应式为
③当反应生成14.4gCu2O时,至少需要肼
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】金属锰在冶金工业中用来制造特种钢,常作为脱硫剂和去氧剂,其化合物广泛应用于电池、机械制造业等领域。
(1)以软锰矿(主要为MnO2)为原料通过热还原法得到金属锰涉及的两个反应:
①3MnO2(s)=Mn3O4(s)+ O2(g) △H1= akJ•mol-1
②3Mn3O4(s)+ 8Al(s) =4Al2O3(s) + 9Mn(s) △H2= bkJ•mol-1
已知Al的燃烧热为 △H3=ckJ•mol-1,则MnO2与Al发生铝热反应的热化学方程式为___________ 。
(2)科研人员将制得的锰粉碎后加入SnCl2溶液中使其浸出(假定杂质不反应,溶液 体积不变),发生反应Mn(s)+ Sn2+(aq) Mn2+(aq)+ Sn(s)(已知含Sn2+水溶液为米黄色)
Mn2+(aq)+ Sn(s)(已知含Sn2+水溶液为米黄色)
请回答下列问题:
①为加快反应速率可以采取的措施有__________ ;不考虑温度因素,一段时间后Mn的溶解速率加快,可能的原因是____________________ 。
②下列能说明反应已达平衡的有____________________ (填编号)。
A.溶液的颜色不发生变化 B.溶液中c(Mn2+)=c( Sn2+)
C.体系中固体的质量不变 D.Mn2+与Sn2+浓度的比值保持不变
③室温下,测得溶液中阳离子浓度c(R2+)随时间的变化情况如下图所示,则上述反应的平衡常数K=________________ ,Mn2+的产率为____________ 。

④若其他条件不变,10min后向容器中迅速加入蒸馏水至溶液体积变为原来的2倍,则 再次平衡时c(Mn2+) =____________ (不考虑离子水解的影响)。
(3)MnO2也可在MnSO4-H2SO4-H2O为体系的电解液中电解获得,其阳极反应式为_____________________ ,阳极附近溶液的pH____________ (选填“增大”、“减小”或“不变”)。
(1)以软锰矿(主要为MnO2)为原料通过热还原法得到金属锰涉及的两个反应:
①3MnO2(s)=Mn3O4(s)+ O2(g) △H1= akJ•mol-1
②3Mn3O4(s)+ 8Al(s) =4Al2O3(s) + 9Mn(s) △H2= bkJ•mol-1
已知Al的燃烧热为 △H3=ckJ•mol-1,则MnO2与Al发生铝热反应的热化学方程式为
(2)科研人员将制得的锰粉碎后加入SnCl2溶液中使其浸出(假定杂质不反应,溶液 体积不变),发生反应Mn(s)+ Sn2+(aq)
 Mn2+(aq)+ Sn(s)(已知含Sn2+水溶液为米黄色)
Mn2+(aq)+ Sn(s)(已知含Sn2+水溶液为米黄色)请回答下列问题:
①为加快反应速率可以采取的措施有
②下列能说明反应已达平衡的有
A.溶液的颜色不发生变化 B.溶液中c(Mn2+)=c( Sn2+)
C.体系中固体的质量不变 D.Mn2+与Sn2+浓度的比值保持不变
③室温下,测得溶液中阳离子浓度c(R2+)随时间的变化情况如下图所示,则上述反应的平衡常数K=

④若其他条件不变,10min后向容器中迅速加入蒸馏水至溶液体积变为原来的2倍,则 再次平衡时c(Mn2+) =
(3)MnO2也可在MnSO4-H2SO4-H2O为体系的电解液中电解获得,其阳极反应式为
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】污染物的有效去除和资源的充分利用是化学造福人类的重要研究课题。某研究小组利用软锰矿(主要成分为MnO2,另含有少量铁、铝、铜、镍等金属化合物)作脱硫剂,通过如下简化流程既脱除燃煤尾气中的SO2,又制得电池材料MnO2(反应条件已省略)。
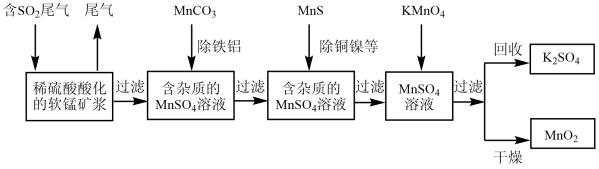
请回答下列问题:
(1)上述流程中多次涉及到过滤操作,实验室进行过滤操作时需要用到的硅酸盐仪器有玻璃棒、漏斗以及___ 。
(2)上述流程脱硫实现了___ (选填下列字母编号)。
A.废弃物的综合利用 B.白色污染的减少 C.酸雨的减少
(3)用MnCO3能除去溶液中的Al3+和Fe3+,其原理是调节溶液的pH,消耗溶液中的酸,促进Al3+和Fe3+水解生成氢氧化物沉淀,若25℃时,Ksp[Fe(OH)3]=8.0×10-38,lg2=0.3,要使溶液中的Fe3+完全沉淀,至少要把溶液pH调至___ 。
(4)已知Ksp(CuS)=8.4×10-45,Ksp(NiS)=1.4×10-24;在除铜镍的过程中,当Ni2+恰好完全沉淀(此时溶液中c(Ni2+)=1.0×10-5mol·L-1),溶液中c(Cu2+)=___ mol·L-1。
(5)已知:25℃、101kpa时,Mn(s)+O2(g)=MnO2(s) △H=-520kJ·mol-1
S(s)+O2(g)=SO2(g) △H=-297kJ·mol-1
Mn(s)+S(s)+2O2(g)=MnSO4(s) △H=-1065kJ·mol-1
SO2与MnO2反应生成无水MnSO4的热化学方程式是___ 。
(6)工业上采用电解K2MnO4水溶液的方法来生产KMnO4,其中隋性电极作阳极,铁作阴极,请写出阳极的电极反应式___ 。

请回答下列问题:
(1)上述流程中多次涉及到过滤操作,实验室进行过滤操作时需要用到的硅酸盐仪器有玻璃棒、漏斗以及
(2)上述流程脱硫实现了
A.废弃物的综合利用 B.白色污染的减少 C.酸雨的减少
(3)用MnCO3能除去溶液中的Al3+和Fe3+,其原理是调节溶液的pH,消耗溶液中的酸,促进Al3+和Fe3+水解生成氢氧化物沉淀,若25℃时,Ksp[Fe(OH)3]=8.0×10-38,lg2=0.3,要使溶液中的Fe3+完全沉淀,至少要把溶液pH调至
(4)已知Ksp(CuS)=8.4×10-45,Ksp(NiS)=1.4×10-24;在除铜镍的过程中,当Ni2+恰好完全沉淀(此时溶液中c(Ni2+)=1.0×10-5mol·L-1),溶液中c(Cu2+)=
(5)已知:25℃、101kpa时,Mn(s)+O2(g)=MnO2(s) △H=-520kJ·mol-1
S(s)+O2(g)=SO2(g) △H=-297kJ·mol-1
Mn(s)+S(s)+2O2(g)=MnSO4(s) △H=-1065kJ·mol-1
SO2与MnO2反应生成无水MnSO4的热化学方程式是
(6)工业上采用电解K2MnO4水溶液的方法来生产KMnO4,其中隋性电极作阳极,铁作阴极,请写出阳极的电极反应式
您最近半年使用:0次



