CO2的利用是国际社会普遍关注的问题。
(1)CO2的电子式是______ 。
(2)CO2在催化剂作用下可以直接转化为乙二醇和甲醇,但若反应温度过高,乙二醇会深度加氢生成乙醇。
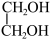 (g)+H2(g)
(g)+H2(g) C2H5OH(g)+H2(g)
C2H5OH(g)+H2(g)  H=-94.8kJ·mol-1
H=-94.8kJ·mol-1
获取乙二醇的反应历程可分为如下2步:
Ⅰ. (g)+CO2(g)
(g)+CO2(g)
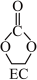 (g)
(g)  H=-60.3kJ·mol-1
H=-60.3kJ·mol-1
Ⅱ.EC加氢生成乙二醇与甲醇
 (g)+CO2(g)+3H2(g)
(g)+CO2(g)+3H2(g)
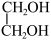 (g)+CH3OH(g)
(g)+CH3OH(g)  H=-131.9kJ·mol-1
H=-131.9kJ·mol-1
① 步骤Ⅱ的热化学方程式是______ 。
② 研究反应温度对EC加氢的影响(反应时间均为4小时),实验数据见下表:
由上表可知,温度越高,EC的转化率越高,原因是______ 。温度升高到220 ℃时,乙二醇的产率反而降低,原因是______ 。
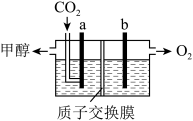
(3)用稀硫酸作电解质溶液,电解CO2可制取甲醇,装置如下图所示,电极a接电源的______ 极(填“正”或“负”),生成甲醇的电极反应式是______ 。
(4)CO2较稳定、能量低。为实现CO2的化学利用,下列研究方向合理的是______ (填序号)。
a.选择高能量的反应物和CO2反应获得低能量的生成物
b.利用电能、光能或热能活化CO2分子
c.选择高效的催化剂
(1)CO2的电子式是
(2)CO2在催化剂作用下可以直接转化为乙二醇和甲醇,但若反应温度过高,乙二醇会深度加氢生成乙醇。
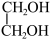 (g)+H2(g)
(g)+H2(g) C2H5OH(g)+H2(g)
C2H5OH(g)+H2(g)  H=-94.8kJ·mol-1
H=-94.8kJ·mol-1获取乙二醇的反应历程可分为如下2步:
Ⅰ.
 (g)+CO2(g)
(g)+CO2(g)
 (g)
(g)  H=-60.3kJ·mol-1
H=-60.3kJ·mol-1 Ⅱ.EC加氢生成乙二醇与甲醇
 (g)+CO2(g)+3H2(g)
(g)+CO2(g)+3H2(g)
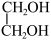 (g)+CH3OH(g)
(g)+CH3OH(g)  H=-131.9kJ·mol-1
H=-131.9kJ·mol-1① 步骤Ⅱ的热化学方程式是
② 研究反应温度对EC加氢的影响(反应时间均为4小时),实验数据见下表:
| 反应温度/ ℃ | EC转化率/ % | 产率/ % | |
| 乙二醇 | 甲醇 | ||
| 160 | 23.8 | 23.2 | 12.9 |
| 180 | 62.1 | 60.9 | 31.5 |
| 200 | 99.9 | 94.7 | 62.3 |
| 220 | 99.9 | 92.4 | 46.1 |
(3)用稀硫酸作电解质溶液,电解CO2可制取甲醇,装置如下图所示,电极a接电源的

(4)CO2较稳定、能量低。为实现CO2的化学利用,下列研究方向合理的是
a.选择高能量的反应物和CO2反应获得低能量的生成物
b.利用电能、光能或热能活化CO2分子
c.选择高效的催化剂
2018·北京西城·二模 查看更多[3]
更新时间:2018-05-17 08:43:07
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】镍是制取各种高强度合金、耐热材料的重要金属之一。以粗氧化镍(主要含NiO、CoO、Fe2O3等)为原料制备纯镍的流程示意图如下:
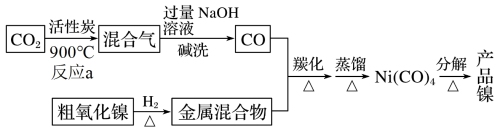
回答下列问题:
(1)已知:C(s)+O2(g)=CO2(g) △H1=+393.5kJ·mol-1
CO(g)+)+ O2(g)=CO2(g) △H2=-283.0kJ·mol-1
O2(g)=CO2(g) △H2=-283.0kJ·mol-1
反应a的化学方程式为___________ ,既有利于提高反应a的速率,又有利于提高原料CO2平衡转化率的措施是___________ 。
(2)用离子方程式表示碱洗过程发生的反应___________ 。
(3)镍的羰化反应为:Ni(s)+4CO(g) Ni(CO)4(g) △H。
Ni(CO)4(g) △H。
①一定温度下,将一定量的粗镍和CO加入到1L的恒容密闭容器中反应,3s后测得Ni(CO)4的物质的量为0.6mol,则0~3s内平均反应速率v(CO)=___________ mol·L-1·s-1。
②镍的羰化反应平衡常数表达式为K=___________ ,当温度升高时,K减小,则该反应的△H___________ 0(填“>”或“<”或“=”)
(4)羰化后的产物为Fe(CO)5、Co2(CO)8、Ni(CO)4,有关性质如下:
蒸馏提取Ni(CO)4应选择的适宜温度范围是___________ 。
(5)采用230℃分解Ni(CO)4(g)制取金属镍,所获金属镍中常常含有碳,原因是___________ (运用化学平衡移动原理解释)。

回答下列问题:
(1)已知:C(s)+O2(g)=CO2(g) △H1=+393.5kJ·mol-1
CO(g)+)+
 O2(g)=CO2(g) △H2=-283.0kJ·mol-1
O2(g)=CO2(g) △H2=-283.0kJ·mol-1反应a的化学方程式为
(2)用离子方程式表示碱洗过程发生的反应
(3)镍的羰化反应为:Ni(s)+4CO(g)
 Ni(CO)4(g) △H。
Ni(CO)4(g) △H。①一定温度下,将一定量的粗镍和CO加入到1L的恒容密闭容器中反应,3s后测得Ni(CO)4的物质的量为0.6mol,则0~3s内平均反应速率v(CO)=
②镍的羰化反应平衡常数表达式为K=
(4)羰化后的产物为Fe(CO)5、Co2(CO)8、Ni(CO)4,有关性质如下:
| 物质 | 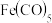 | 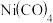 | 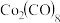 |
| 沸点/℃ | 106 | 43.2 | 52 |
| 熔点/℃ | -20 | -19.3 | 31 |
| 分解温度/℃ | >160 | 135 | —— |
蒸馏提取Ni(CO)4应选择的适宜温度范围是
(5)采用230℃分解Ni(CO)4(g)制取金属镍,所获金属镍中常常含有碳,原因是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】含NO烟气需要处理后才能排放。
(1)氢气催化还原含NO烟气。
主反应:2NO(g)+2H2(g) N2(g)+2H2O(g) ΔH1=akJ•mol-1
N2(g)+2H2O(g) ΔH1=akJ•mol-1
副反应:2NO(g)+H2(g) N2O(g)+H2O(g) ΔH2=bkJ•mol-1
N2O(g)+H2O(g) ΔH2=bkJ•mol-1
①2NO(g)+N2(g) 2N2O(g) ΔH=
2N2O(g) ΔH=_____ kJ•mol-1
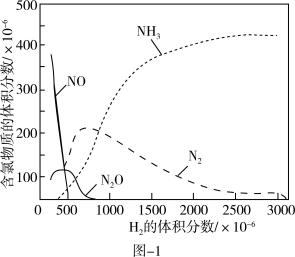
②某温度下H2的体积分数对H2还原NO反应的影响如图1所示。当H2的体积分数大于600×10-6时,N2的体积分数呈下降趋势,原因是_____ 。
(2)煤焦吸附还原含NO烟气。
将原煤经热解、冷却得到煤焦,NO的脱除主要含吸附和化学还原(ΔH<0)两个过程,煤焦表面存在的官能团有利于NO的吸附,其数量与煤焦中氢碳质量比的值密切相关。热解温度为500℃、900℃得到的煤焦分别用S—500、S—900表示,相关信息如表:
将NO浓度恒定的烟气以固定流速通过装有煤焦的反应器。不同温度下,测得NO的脱除率与温度的关系如图2所示。

①相同温度下,S—900对NO的脱除率比S—500的低,可能的原因是_____ 。
②350℃后,随着温度升高,NO的脱除率增大的原因是_____ 。
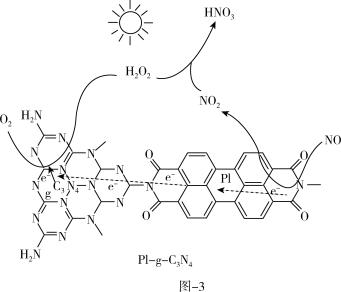
(3)P1—g—C3N4光催化氧化含NO烟气。
用P1—g—C3N4光催化氧化法脱除NO的过程如图3所示。在酸性水溶液中,光催化脱除原理和电化学反应原理类似,P1—g—C3N4光催化的P1和g—C3N4两端类似于两极,该反应过程可描述为_____ 。
(1)氢气催化还原含NO烟气。
主反应:2NO(g)+2H2(g)
 N2(g)+2H2O(g) ΔH1=akJ•mol-1
N2(g)+2H2O(g) ΔH1=akJ•mol-1副反应:2NO(g)+H2(g)
 N2O(g)+H2O(g) ΔH2=bkJ•mol-1
N2O(g)+H2O(g) ΔH2=bkJ•mol-1①2NO(g)+N2(g)
 2N2O(g) ΔH=
2N2O(g) ΔH=②某温度下H2的体积分数对H2还原NO反应的影响如图1所示。当H2的体积分数大于600×10-6时,N2的体积分数呈下降趋势,原因是

(2)煤焦吸附还原含NO烟气。
将原煤经热解、冷却得到煤焦,NO的脱除主要含吸附和化学还原(ΔH<0)两个过程,煤焦表面存在的官能团有利于NO的吸附,其数量与煤焦中氢碳质量比的值密切相关。热解温度为500℃、900℃得到的煤焦分别用S—500、S—900表示,相关信息如表:
| 煤焦 | 元素分析(%) | 比表面积(cm2∙g-1) | |
| C | H | ||
| S—500 | 80.79 | 2.76 | 105.69 |
| S—900 | 84.26 | 0.82 | 8.98 |

①相同温度下,S—900对NO的脱除率比S—500的低,可能的原因是
②350℃后,随着温度升高,NO的脱除率增大的原因是
(3)P1—g—C3N4光催化氧化含NO烟气。
用P1—g—C3N4光催化氧化法脱除NO的过程如图3所示。在酸性水溶液中,光催化脱除原理和电化学反应原理类似,P1—g—C3N4光催化的P1和g—C3N4两端类似于两极,该反应过程可描述为

您最近一年使用:0次
【推荐3】乙基叔丁基酸(以ETBE表示)是一种性能优良的高辛烷值汽油调和剂,用乙醇与异丁烯(以IB表示)在催化剂HZSM-5催化下合成ETBE,反应的化学方程式为:C2H5OH(g)+IB(g) ETBE(g) ΔH。回答下列问题:
ETBE(g) ΔH。回答下列问题:

(1)反应物被催化剂HZSM-5吸附的顺序与反应历程的关系如上图所示,该反应的ΔH=______ akJ·mol-1,下列选项正确的是______ (填序号)。
A.反应历程的最优途径是C1
B.HZSM-5没有参加化学反应
C.相同条件下,采用不同途径时,乙醇的平衡转化率C1>C2>C3
D.升高反应温度有利于提高平衡产率
(2)向刚性容器中按物质的量之比1:1充入乙醇和异丁烯,在温度为378K与388K时异丁烯的转化率随时间变化如图所示。

①图中A、M、B三点,化学反应速率由大到小的顺序为__________________ ,其中逆反应速率最大的点是_________ (用符号A、M、B填写)。
②388K时,容器内起始总压为P0Pa,用分压表示的该反应的平衡常数Kp=____________ Pa-1(用含有P0的式子表示)。
③瑞典化学家阿累尼乌斯的化学反应速率经验定律为:k=A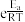 (其中,k为速率常数A、R为常数,Ea为活化能,T为绝对温度,e为自然对数底数,约为2.718)。由此判断下列说法中正确的是
(其中,k为速率常数A、R为常数,Ea为活化能,T为绝对温度,e为自然对数底数,约为2.718)。由此判断下列说法中正确的是_________ (填序号,k正、k逆为正、逆速率常数)。
A.其他条件不变,升高温度,k正增大,k逆变小
B.其他条件不变,使用催化剂,k正、k逆同倍数增大
C.其他条件不变,增大反应物浓度k正增大,k逆不变
D.其他条件不变,减小压强,k正、k逆都变小
已知反应速率 ,计算上图中M点
,计算上图中M点 =
=_________ (保留两位小数)
 ETBE(g) ΔH。回答下列问题:
ETBE(g) ΔH。回答下列问题:
(1)反应物被催化剂HZSM-5吸附的顺序与反应历程的关系如上图所示,该反应的ΔH=
A.反应历程的最优途径是C1
B.HZSM-5没有参加化学反应
C.相同条件下,采用不同途径时,乙醇的平衡转化率C1>C2>C3
D.升高反应温度有利于提高平衡产率
(2)向刚性容器中按物质的量之比1:1充入乙醇和异丁烯,在温度为378K与388K时异丁烯的转化率随时间变化如图所示。

①图中A、M、B三点,化学反应速率由大到小的顺序为
②388K时,容器内起始总压为P0Pa,用分压表示的该反应的平衡常数Kp=
③瑞典化学家阿累尼乌斯的化学反应速率经验定律为:k=A
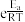 (其中,k为速率常数A、R为常数,Ea为活化能,T为绝对温度,e为自然对数底数,约为2.718)。由此判断下列说法中正确的是
(其中,k为速率常数A、R为常数,Ea为活化能,T为绝对温度,e为自然对数底数,约为2.718)。由此判断下列说法中正确的是A.其他条件不变,升高温度,k正增大,k逆变小
B.其他条件不变,使用催化剂,k正、k逆同倍数增大
C.其他条件不变,增大反应物浓度k正增大,k逆不变
D.其他条件不变,减小压强,k正、k逆都变小
已知反应速率
 ,计算上图中M点
,计算上图中M点 =
=
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐1】碳、氮及其化合物在工农业生产生活中有着重要作用。请回答下列问题:
(1)用CH4 催化还原NOx 可以消除氮氧化物的污染。例如:
CH4(g) + 4NO2(g) =4NO(g)+CO2(g) + 2H2O(g) ΔH1=-574 kJ·molˉ1
CH4(g) + 4NO(g) = 2N2(g)+CO2(g) + 2H2O(g) ΔH2
若2mol CH4 还原NO2 至N2,整个过程中放出的热量为1734 kJ,则ΔH2=______________ 。
(2)据报道,科学家在一定条件下利用Fe2O3与甲烷反应可制取“纳米级”的金属铁。其反应为:Fe2O3(s)+3CH4(g) 2Fe(s)+3CO(g)+6H2(g) ΔH>0
2Fe(s)+3CO(g)+6H2(g) ΔH>0
①若反应在5L的密闭容器中进行,1min后达到平衡,测得Fe2O3在反应中质量减少3.2g。则该段时间内CO的平均反应速率为____________________
②若该反应在恒温恒容容器中进行,能表明该反应达到平衡状态的是__________________ A.H2的逆反应速率
B.CH4的的体积分数
C.混合气体的平均相对分子质量
D.CO的体积分数
③该反应达到平衡时某物理量随温度变化如图所示,当温度由T1升高到T2时,平衡常数KA_______ KB(填“>”、“<”或“=”)。纵坐标可以表示的物理量有哪些___________________

A.CH4的转化率等于CO的产率
B.混合气体的密度不变
C.v(CO)与v(H2)的比值为1:2
D.固体的总质量不变
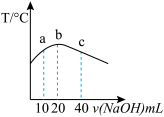
(3)若往20mL 0.0lmol·L-l的弱酸HNO2溶液中逐滴加入一定浓度的烧碱溶液,测得混合溶液的温度变化如图所示,下列有关说法正确的是_______________
①该烧碱溶液的浓度为0.02mol·L-1
②该烧碱溶液的浓度为0.01mol·L-1
③HNO2的电离平衡常数:b>a
④从b点到c点,混合溶液中一直存在:c(Na+)>c( )>c(OH
)>c(OH )>c(H+)
)>c(H+)
(1)用CH4 催化还原NOx 可以消除氮氧化物的污染。例如:
CH4(g) + 4NO2(g) =4NO(g)+CO2(g) + 2H2O(g) ΔH1=-574 kJ·molˉ1
CH4(g) + 4NO(g) = 2N2(g)+CO2(g) + 2H2O(g) ΔH2
若2mol CH4 还原NO2 至N2,整个过程中放出的热量为1734 kJ,则ΔH2=
(2)据报道,科学家在一定条件下利用Fe2O3与甲烷反应可制取“纳米级”的金属铁。其反应为:Fe2O3(s)+3CH4(g)
 2Fe(s)+3CO(g)+6H2(g) ΔH>0
2Fe(s)+3CO(g)+6H2(g) ΔH>0①若反应在5L的密闭容器中进行,1min后达到平衡,测得Fe2O3在反应中质量减少3.2g。则该段时间内CO的平均反应速率为
②若该反应在恒温恒容容器中进行,能表明该反应达到平衡状态的是
B.CH4的的体积分数
C.混合气体的平均相对分子质量
D.CO的体积分数
③该反应达到平衡时某物理量随温度变化如图所示,当温度由T1升高到T2时,平衡常数KA

A.CH4的转化率等于CO的产率
B.混合气体的密度不变
C.v(CO)与v(H2)的比值为1:2
D.固体的总质量不变
(3)若往20mL 0.0lmol·L-l的弱酸HNO2溶液中逐滴加入一定浓度的烧碱溶液,测得混合溶液的温度变化如图所示,下列有关说法正确的是

①该烧碱溶液的浓度为0.02mol·L-1
②该烧碱溶液的浓度为0.01mol·L-1
③HNO2的电离平衡常数:b>a
④从b点到c点,混合溶液中一直存在:c(Na+)>c(
 )>c(OH
)>c(OH )>c(H+)
)>c(H+)
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】Ⅰ.煤是一种重要的化工原料,人们将利用煤制取的水煤气、焦炭、二甲醚等广泛用于工农业生产中.已知: C(s)+H2O(g)═CO(g)+H2(g) △H=+131.3kJ•mol﹣1
CO2(g)+H2(g)═CO(g)+H2O(g)△H=+41.3kJ•mol﹣1
则炭与水蒸气反应生成二氧化碳和氢气的热化学方程式为___________________ 。该反应在____ (填“高温”、“低温”或“任何温度”)下有利于正向自发进行.
Ⅱ.二甲醚(CH3OCH3)被誉为“21世纪的清洁燃料”。 利用煤制取的CO和H2为原料生产二甲醚主要发生以下三个反应:① CO(g)+2H2(g) CH3OH(g) △H1
CH3OH(g) △H1
② 2CH3OH(g) CH3OCH3(g)+H2O(g)△H2=﹣24kJ•mol﹣1
CH3OCH3(g)+H2O(g)△H2=﹣24kJ•mol﹣1
③CO(g)+H2O(g) CO2(g)+H2(g)△H3=﹣41kJ•mol﹣1
CO2(g)+H2(g)△H3=﹣41kJ•mol﹣1
(1)已知反应①中的相关的化学键键能数据如下:
由上述数据计算△H1=______________ ;
(2)该工艺的总反应为3CO(g)+3H2(g) CH3OCH3(g)+CO2(g)△H,该反应
CH3OCH3(g)+CO2(g)△H,该反应
△H=____________ ,
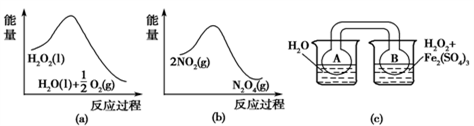
Ⅲ.在固定体积的密闭容器中,发生可逆反应:2NO2(g) N2O4(g)。已知Fe3+对H2O2的分解具有催化作用。利用下图(a)和(b)中的信息,按图(c)装置(连通的A、B瓶中已充有NO2气体)进行实验。可观察到B瓶中气体颜色比A瓶中的
N2O4(g)。已知Fe3+对H2O2的分解具有催化作用。利用下图(a)和(b)中的信息,按图(c)装置(连通的A、B瓶中已充有NO2气体)进行实验。可观察到B瓶中气体颜色比A瓶中的________ (填“深”或“浅”),其原因是____________________________
CO2(g)+H2(g)═CO(g)+H2O(g)△H=+41.3kJ•mol﹣1
则炭与水蒸气反应生成二氧化碳和氢气的热化学方程式为
Ⅱ.二甲醚(CH3OCH3)被誉为“21世纪的清洁燃料”。 利用煤制取的CO和H2为原料生产二甲醚主要发生以下三个反应:① CO(g)+2H2(g)
 CH3OH(g) △H1
CH3OH(g) △H1② 2CH3OH(g)
 CH3OCH3(g)+H2O(g)△H2=﹣24kJ•mol﹣1
CH3OCH3(g)+H2O(g)△H2=﹣24kJ•mol﹣1③CO(g)+H2O(g)
 CO2(g)+H2(g)△H3=﹣41kJ•mol﹣1
CO2(g)+H2(g)△H3=﹣41kJ•mol﹣1(1)已知反应①中的相关的化学键键能数据如下:
| 化学键 | H﹣H | C﹣O |  | H﹣O | C﹣H |
| E/(kJ·mol﹣1) | 436 | 343 | 1076 | 465 | 413 |
(2)该工艺的总反应为3CO(g)+3H2(g)
 CH3OCH3(g)+CO2(g)△H,该反应
CH3OCH3(g)+CO2(g)△H,该反应△H=
Ⅲ.在固定体积的密闭容器中,发生可逆反应:2NO2(g)
 N2O4(g)。已知Fe3+对H2O2的分解具有催化作用。利用下图(a)和(b)中的信息,按图(c)装置(连通的A、B瓶中已充有NO2气体)进行实验。可观察到B瓶中气体颜色比A瓶中的
N2O4(g)。已知Fe3+对H2O2的分解具有催化作用。利用下图(a)和(b)中的信息,按图(c)装置(连通的A、B瓶中已充有NO2气体)进行实验。可观察到B瓶中气体颜色比A瓶中的
您最近一年使用:0次
【推荐3】二甲醚是一种重要的清洁燃料,也可替代氟利昂作制冷剂等,对臭氧层无破坏作用。工业上可利用煤的气化产物(水煤气)合成二甲醚。请回答下列问题
(1)煤的气化的主要化学反应方程式为________________
(2)煤的气化过程中产生的有害气体H2S用Na2CO3溶液吸收,生成两种酸式盐,该反应的化学方程式为____________
(3)利用水煤气合成二甲醚的三步反应如下
①2H2(g)+CO(g)=CH3OH(g) △H=-90.8kJ.mo-1
②2CH3OH(g)= CH3OCH3(g)+ H2O(g) △H=-235kJ.mo-1
③CO(g)+H2O(g)=O2(g)+H2(g) △H=-413kJ.mo-1
总反应:3H2(g)+3CO(g)= CH3OCH3(g)+CO2(g)的△H=___________
一定条件下的密闭容器中,该总反应达到平衡,要提高CO的转化率,可以采取的措施是____ (填字母代号)
a. 高温高压 b.加入催化剂 c.减少CO2的浓度 d.增加Co的浓度 e.分离出二甲醚
(4)已知反应②2CH3OH(g)= CH3OCH3(g)+ H2O(g)某温度下的平衡常数为400.此温度下,在2L密闭容器中加入CH3OH,反应到某时刻测得各组分的浓度如下:
①加入的CH3OH的起始浓度为_________
②比较此时正、逆反应速率的大小:v正________ v逆(填少”、“<”或“=”)
③若加入CH3OH后,经10min反应达到平衡,此时CH3OH的转化率a(CH3OH)=_________ c(CH3OCH3)=____________
(1)煤的气化的主要化学反应方程式为
(2)煤的气化过程中产生的有害气体H2S用Na2CO3溶液吸收,生成两种酸式盐,该反应的化学方程式为
(3)利用水煤气合成二甲醚的三步反应如下
①2H2(g)+CO(g)=CH3OH(g) △H=-90.8kJ.mo-1
②2CH3OH(g)= CH3OCH3(g)+ H2O(g) △H=-235kJ.mo-1
③CO(g)+H2O(g)=O2(g)+H2(g) △H=-413kJ.mo-1
总反应:3H2(g)+3CO(g)= CH3OCH3(g)+CO2(g)的△H=
一定条件下的密闭容器中,该总反应达到平衡,要提高CO的转化率,可以采取的措施是

a. 高温高压 b.加入催化剂 c.减少CO2的浓度 d.增加Co的浓度 e.分离出二甲醚
(4)已知反应②2CH3OH(g)= CH3OCH3(g)+ H2O(g)某温度下的平衡常数为400.此温度下,在2L密闭容器中加入CH3OH,反应到某时刻测得各组分的浓度如下:
| 物质 | CH3OH | CH3OCH3 | H2O |
| 物质的量(mol) | 0.88 | 1.2 | 1.2 |
①加入的CH3OH的起始浓度为
②比较此时正、逆反应速率的大小:v正
③若加入CH3OH后,经10min反应达到平衡,此时CH3OH的转化率a(CH3OH)=
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】甲醇是一种可再生能源,具有广泛的开发和应用前景。工业上采用反应Ⅰ合成甲醇:CO(g)+2H2(g)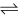 CH3OH(g)+Q。回答下列问题:
CH3OH(g)+Q。回答下列问题:
(1)反应Ⅰ的化学平衡常数表达式为_____ 。右表为该反应在不同温度下的化学平衡常数,由表中数据判断Q_____ 0(填“>”、“=”或“<”)。
(2)某温度下,将2mol CO和6mol H2充入2L的密闭容器中,1 min后达到平衡状态,测得 c(CO)=0.2mol/L,用H2表示这段时间内的平均化学反应速率为_____ 。参照右表,此时的反应温度为_____ ℃。
(3)为了提高CO的转化率,合成塔(恒容)中宜采取_____ 措施(填写编号)。
a.升高反应的温度
b.提高CO的浓度
c.采用更高效的催化剂
d.提高H2的浓度
(4)工业上也可以通过CO2与H2在一定条件下反应(反应Ⅱ)合成甲醇,写出反应Ⅱ的化学方程式:_____ 。两种反应中符合“原子经济”原则的是反应____________ (填“Ⅰ”或“Ⅱ”)。
(5)依据甲醇完全燃烧的原理,能将甲醇应用于燃料电池。反应的化学方程式:2CH3OH+3O2→2CO2+4H2O。此时,应将O2通入燃料电池的_____ 极(填“正”或“负”)。
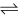 CH3OH(g)+Q。回答下列问题:
CH3OH(g)+Q。回答下列问题:(1)反应Ⅰ的化学平衡常数表达式为
| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
(2)某温度下,将2mol CO和6mol H2充入2L的密闭容器中,1 min后达到平衡状态,测得 c(CO)=0.2mol/L,用H2表示这段时间内的平均化学反应速率为
(3)为了提高CO的转化率,合成塔(恒容)中宜采取
a.升高反应的温度
b.提高CO的浓度
c.采用更高效的催化剂
d.提高H2的浓度
(4)工业上也可以通过CO2与H2在一定条件下反应(反应Ⅱ)合成甲醇,写出反应Ⅱ的化学方程式:
(5)依据甲醇完全燃烧的原理,能将甲醇应用于燃料电池。反应的化学方程式:2CH3OH+3O2→2CO2+4H2O。此时,应将O2通入燃料电池的
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】甲醇(CH3OH)是重要的溶剂和替代燃料,工业上用CO和H2在一定条件下制备CH3OH的反应为CO(g)+2H2(g) CH3OH(g) ΔH。
CH3OH(g) ΔH。
(1)在体积为1L的恒容密闭容器中,充入2molCO和4molH2,一定条件下发生上述反应,测得CO(g)和CH3OH(g)的浓度随时间变化如图所示。
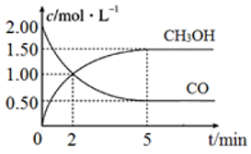
①从反应开始到2 min,用氢气表示的平均反应速率v(H2)=__________ 。
②下列说法正确的是______________ (填字母序号)。
A.达到平衡时,H2的转化率为75%
B.5min后容器中压强不再改变
C.达到平衡后,再充入氩气,反应速率增大
D.2min前v(正)>v(逆),2min后v(正)<v(逆)
(2)某温度下,在一恒压容器中分别充入1.2molCO和1molH2,达到平衡时容器体积为2L,且含有0.4molCH3OH(g),则该反应平衡常数的值为_______ ,此时向容器中再通入0.35molCO气体,则此平衡将______________ (填“向正反应方向”、“不”或“向逆反应方向”)移动。
(3)工业上另一种合成甲醇的方法是利用CO2和H2,已知:CH3OH、H2的燃烧热(ΔH)分别为-726.5kJ/mol、-285.8kJ/mol,则常温下CO2和H2反应生成CH3OH和H2O的热化学方程式是______________________ 。
(4)CH3OH(l)作为一种燃料还可用于燃料电池。在温度为650℃的熔融盐燃料电池中用甲醇、空气与CO2的混合气体作反应物,镍作电极,用Li2CO3和Na2CO3混合物作电解质。该电池的负极反应式为______________________ 。
 CH3OH(g) ΔH。
CH3OH(g) ΔH。(1)在体积为1L的恒容密闭容器中,充入2molCO和4molH2,一定条件下发生上述反应,测得CO(g)和CH3OH(g)的浓度随时间变化如图所示。

①从反应开始到2 min,用氢气表示的平均反应速率v(H2)=
②下列说法正确的是
A.达到平衡时,H2的转化率为75%
B.5min后容器中压强不再改变
C.达到平衡后,再充入氩气,反应速率增大
D.2min前v(正)>v(逆),2min后v(正)<v(逆)
(2)某温度下,在一恒压容器中分别充入1.2molCO和1molH2,达到平衡时容器体积为2L,且含有0.4molCH3OH(g),则该反应平衡常数的值为
(3)工业上另一种合成甲醇的方法是利用CO2和H2,已知:CH3OH、H2的燃烧热(ΔH)分别为-726.5kJ/mol、-285.8kJ/mol,则常温下CO2和H2反应生成CH3OH和H2O的热化学方程式是
(4)CH3OH(l)作为一种燃料还可用于燃料电池。在温度为650℃的熔融盐燃料电池中用甲醇、空气与CO2的混合气体作反应物,镍作电极,用Li2CO3和Na2CO3混合物作电解质。该电池的负极反应式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】氢气不仅是新能源,也是重要的化工原料。
(1)氢气可由甲烷制备: 。已知
。已知 时,
时,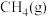 、
、 的燃烧热分别为
的燃烧热分别为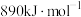 、
、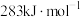 。写出氢气燃烧热的热化学方程式:
。写出氢气燃烧热的热化学方程式:_______ 。
(2)利用反应 合成清洁能源
合成清洁能源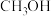 ,CO的平衡转化率与温度的关系如图所示:
,CO的平衡转化率与温度的关系如图所示:

①该可逆反应的正反应
_______ 0;压强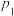
_______ 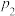 (均填“>”“<”或“=”)。
(均填“>”“<”或“=”)。
②若在恒温恒容条件下进行上述反应,能表示该可逆反应达到平衡状态的是_______ (填字母)。
a. 物质的量保持不变
物质的量保持不变
b.单位时间内消耗 的浓度和生成甲醇的浓度相等
的浓度和生成甲醇的浓度相等
c.混合气体的压强不再变化
d.混合气体的密度不再变化
③在 恒容密闭容器中充入
恒容密闭容器中充入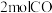 和
和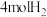 ,在
,在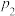 和
和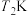 条件下经
条件下经 达到平衡状态C点,在该条件下,平衡常数
达到平衡状态C点,在该条件下,平衡常数 为
为_______ 。
(3)电池的比能量与消耗单位质量还原剂时转移的电子数成正比。理论上,H2、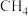 、
、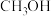 的酸性燃料电池的比能量由大到小排序为
的酸性燃料电池的比能量由大到小排序为_______ ,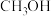 的酸性燃料电池的负极电极反应式为
的酸性燃料电池的负极电极反应式为_______ 。
(1)氢气可由甲烷制备:
 。已知
。已知 时,
时,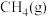 、
、 的燃烧热分别为
的燃烧热分别为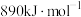 、
、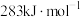 。写出氢气燃烧热的热化学方程式:
。写出氢气燃烧热的热化学方程式:(2)利用反应
 合成清洁能源
合成清洁能源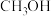 ,CO的平衡转化率与温度的关系如图所示:
,CO的平衡转化率与温度的关系如图所示:
①该可逆反应的正反应

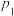
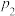 (均填“>”“<”或“=”)。
(均填“>”“<”或“=”)。②若在恒温恒容条件下进行上述反应,能表示该可逆反应达到平衡状态的是
a.
 物质的量保持不变
物质的量保持不变b.单位时间内消耗
 的浓度和生成甲醇的浓度相等
的浓度和生成甲醇的浓度相等c.混合气体的压强不再变化
d.混合气体的密度不再变化
③在
 恒容密闭容器中充入
恒容密闭容器中充入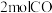 和
和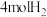 ,在
,在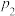 和
和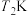 条件下经
条件下经 达到平衡状态C点,在该条件下,平衡常数
达到平衡状态C点,在该条件下,平衡常数 为
为(3)电池的比能量与消耗单位质量还原剂时转移的电子数成正比。理论上,H2、
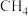 、
、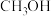 的酸性燃料电池的比能量由大到小排序为
的酸性燃料电池的比能量由大到小排序为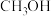 的酸性燃料电池的负极电极反应式为
的酸性燃料电池的负极电极反应式为
您最近一年使用:0次



