某兴趣小组设计如图实验装置制备次磷酸钠(NaH2PO2)。
已知:①白磷(P4)在空气中可自燃,与过量烧碱溶液混合,80~ 90℃生成NaH2PO2和PH3。
②PH3是一种有强还原性的有毒气体,空气中可自燃,可与NaClO溶液反应生成NaH2PO2。
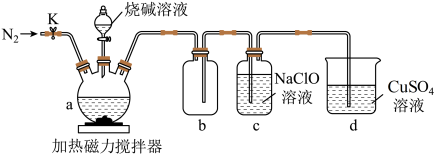
(1)仪器a的名称是___________ ,a 中发生反应的化学方程式是___________ 。
(2)仪器b组成的装置的作用是___________ ,检查装置气密性后,应先打开K通入N2一段时间,目的是___________ 。
(3)下列有关说法正确的是___________ 。
A.次磷酸(H3PO2)是三元酸
B.为加快反应速率,投料前应先在通风橱内将白磷碾成薄片状
C.d中所盛硫酸铜溶液,可用酸性高锰酸钾溶液代替
(4)①仪器c中充分反应后生成NaH2PO2和NaCl,经过一系列操作可获得固体NaH2PO2,相关物质的溶解度(S)如下:
从下列选项a-g中选择合理的仪器或操作,补全如下步骤。
取仪器c中溶液,用蒸发皿___________→___________(趁热过滤)→用烧杯(冷却结晶)→用漏斗(过滤得到NaH2PO2)→___________→干燥→NaH2PO2粗品。___________
选项:a.溶解 b.过滤 c.洗涤 d.普通三角漏斗 e.保温漏斗 f.蒸发浓缩至有大量晶体析出 g.蒸发浓缩至溶液表面出现晶膜
②写出c中发生反应的离子方程式___________ 。
(5)产品纯度的测定:
取产品mg配成250mL溶液,取25mL于锥形瓶中,然后用0.01 KMnO4标准溶液滴定至终点(还原产物是Mn2+,氧化产物是
KMnO4标准溶液滴定至终点(还原产物是Mn2+,氧化产物是 ),达到滴定终点时消耗VmL标准溶液,产品的纯度为
),达到滴定终点时消耗VmL标准溶液,产品的纯度为___________ 。
已知:①白磷(P4)在空气中可自燃,与过量烧碱溶液混合,80~ 90℃生成NaH2PO2和PH3。
②PH3是一种有强还原性的有毒气体,空气中可自燃,可与NaClO溶液反应生成NaH2PO2。

(1)仪器a的名称是
(2)仪器b组成的装置的作用是
(3)下列有关说法正确的是
A.次磷酸(H3PO2)是三元酸
B.为加快反应速率,投料前应先在通风橱内将白磷碾成薄片状
C.d中所盛硫酸铜溶液,可用酸性高锰酸钾溶液代替
(4)①仪器c中充分反应后生成NaH2PO2和NaCl,经过一系列操作可获得固体NaH2PO2,相关物质的溶解度(S)如下:
| S(25℃) | S(100℃) | |
| NaCl | 37 | 39 |
| NaH2PO2 | 100 | 667 |
取仪器c中溶液,用蒸发皿___________→___________(趁热过滤)→用烧杯(冷却结晶)→用漏斗(过滤得到NaH2PO2)→___________→干燥→NaH2PO2粗品。
选项:a.溶解 b.过滤 c.洗涤 d.普通三角漏斗 e.保温漏斗 f.蒸发浓缩至有大量晶体析出 g.蒸发浓缩至溶液表面出现晶膜
②写出c中发生反应的离子方程式
(5)产品纯度的测定:
取产品mg配成250mL溶液,取25mL于锥形瓶中,然后用0.01
 KMnO4标准溶液滴定至终点(还原产物是Mn2+,氧化产物是
KMnO4标准溶液滴定至终点(还原产物是Mn2+,氧化产物是 ),达到滴定终点时消耗VmL标准溶液,产品的纯度为
),达到滴定终点时消耗VmL标准溶液,产品的纯度为
更新时间:2024-01-18 09:37:29
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
【推荐1】下图为实验室制取氨气的实验装置。

(1)写出实验室制氨气的化学方程式:___________ ;
(2)该图中氨气的收集方式为___________ (填“向上排空气法”或“向下排空气法”);
(3)在收集氨时试管口棉花团的作用是___________ :
(4)要得到干燥的氨气可选用___________ (填“浓硫酸”或“碱石灰”)作干燥剂;
(5)欲收集氨气22.4L(标准状况下),则至少需要 固体
固体___________ g。

(1)写出实验室制氨气的化学方程式:
(2)该图中氨气的收集方式为
(3)在收集氨时试管口棉花团的作用是
(4)要得到干燥的氨气可选用
(5)欲收集氨气22.4L(标准状况下),则至少需要
 固体
固体
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】将一定质量的镁铝合金投入100mL一定浓度的盐酸中,合金完全溶解。向所得溶液中滴加浓度为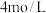 的NaOH溶液,生成沉淀的质量与加入的NaOH溶液体积的关系如图。请回答下列问题:
的NaOH溶液,生成沉淀的质量与加入的NaOH溶液体积的关系如图。请回答下列问题:

(1)合金完全溶解后,滴加NaOH溶液前,溶液中含有的阳离子是_______ ;
(2) 段反应的化学方程式为
段反应的化学方程式为_______ ;
(3)镁铝合金中Al的质量为_______ ;
(4)所用HC1的物质的量浓度为_______  。
。
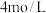 的NaOH溶液,生成沉淀的质量与加入的NaOH溶液体积的关系如图。请回答下列问题:
的NaOH溶液,生成沉淀的质量与加入的NaOH溶液体积的关系如图。请回答下列问题:
(1)合金完全溶解后,滴加NaOH溶液前,溶液中含有的阳离子是
(2)
 段反应的化学方程式为
段反应的化学方程式为(3)镁铝合金中Al的质量为
(4)所用HC1的物质的量浓度为
 。
。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】某化学小组利用下列装置,模拟呼吸面具中的有关反应原理测定样品中 的纯度。
的纯度。
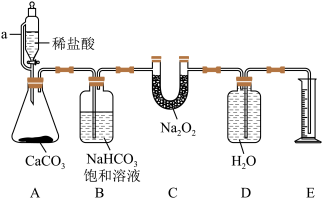
(1)装置A中a的作用是___________ ;装置A中发生反应的离子方程式是___________ 。
(2)装置C中发生反应的化学方程式是___________ 。
(3)上述装置存在一处缺陷,会导致测定的 的纯度偏高,改进的方法是
的纯度偏高,改进的方法是___________ 。
(4)实验装置改进后,向C中加入10.0g样品进行实验,试验结束后后共收集称量得1.6g氧气,则样品中 的纯度为
的纯度为___________ 。【某物质纯度=(该物质质量/样品质量)×100%】
 的纯度。
的纯度。
(1)装置A中a的作用是
(2)装置C中发生反应的化学方程式是
(3)上述装置存在一处缺陷,会导致测定的
 的纯度偏高,改进的方法是
的纯度偏高,改进的方法是(4)实验装置改进后,向C中加入10.0g样品进行实验,试验结束后后共收集称量得1.6g氧气,则样品中
 的纯度为
的纯度为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】氮氧化合物和二氧化硫是引起雾霾的重要物质,工业用多种方法来治理。某种综合处理含 NH4+废水和工业废气(主要含 NO、CO、CO2、SO2、N2)的流程如图:

已知:NO+NO2+2NaOH=2NaNO2+H2O 2NO2+2NaOH=NaNO3+NaNO2+H2O
(1)固体 1 的主要成分有 Ca(OH)2、___________________ 、__________________ (填化学式)。
(2)若实验室需要配制100mL 3.00mol·L-1NaOH溶液进行模拟测试,需用托盘天平称取 NaOH固体质量为______ g。
(3)用 NaNO2溶液处理含NH4+废水反应的离子方程式为_______________________ 。
(4)捕获剂从气体 3 中捕获的气体主要是__________________ (填化学式)。
(5)流程中生成的 NaNO2 因外观和食盐相似,又有咸味,容易使人误食中毒。已知 NaNO2能发生如下反应:2NaNO2+4HI=2NO↑+I2+2NaI+2H2O;I2可以使淀粉变蓝。根据上述反应, 选择生活中常见的物质和有关试剂进行实验,以鉴别 NaNO2和 NaCl。需选用的物质是_____________________ (填序号)。
①水 ②淀粉碘化钾试纸 ③淀粉 ④白酒 ⑤白醋
A.①③⑤ B.①②④ C.①②⑤ D.①②③⑤

已知:NO+NO2+2NaOH=2NaNO2+H2O 2NO2+2NaOH=NaNO3+NaNO2+H2O
(1)固体 1 的主要成分有 Ca(OH)2、
(2)若实验室需要配制100mL 3.00mol·L-1NaOH溶液进行模拟测试,需用托盘天平称取 NaOH固体质量为
(3)用 NaNO2溶液处理含NH4+废水反应的离子方程式为
(4)捕获剂从气体 3 中捕获的气体主要是
(5)流程中生成的 NaNO2 因外观和食盐相似,又有咸味,容易使人误食中毒。已知 NaNO2能发生如下反应:2NaNO2+4HI=2NO↑+I2+2NaI+2H2O;I2可以使淀粉变蓝。根据上述反应, 选择生活中常见的物质和有关试剂进行实验,以鉴别 NaNO2和 NaCl。需选用的物质是
①水 ②淀粉碘化钾试纸 ③淀粉 ④白酒 ⑤白醋
A.①③⑤ B.①②④ C.①②⑤ D.①②③⑤
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】铝的阳极氧化是一种重要的表面处理技术,其原理是用电化学方法处理铝件表面,优化氧化膜结构,增强铝件的抗腐蚀性,同时便于表面着色。取铝片模拟该实验,并测定氧化膜厚度,操作步骤如下:
(1)铝片预处理
铝片表面除去油垢后,用2mol/LNaOH溶液在60~70℃下洗涤,除去铝表面薄氧化膜,离子方程式为:_______ ;再用10%(质量分数)的HNO3溶液对铝片表面进行化学抛光。若取一定体积68%(质量分数)的浓硝酸配制该化学抛光液,需要用到的玻璃仪器有_______ 、_______ 、玻璃棒和胶头滴管。
(2)电解氧化
取预处理过的铝片和铅做电极,控制电流恒定为0.06A,用直流电源在5~6mol/L硫酸中电解。其中铝片接电源_______ 极,产生氧化膜的电极反应式为_______ ,氧化膜的生长过程可大致分为A、B、C三个阶段(如图所示),C阶段多孔层产生孔隙的离子反应方程式为_____ ,A阶段电压逐渐增大的原因是_____ 。
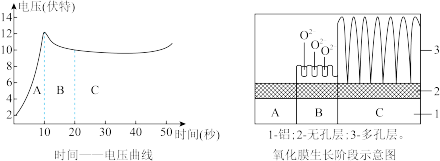
(3)氧化膜质量检验
取出阳极氧化并封闭处理过的铝片,洗净、干燥,在铝片表面滴一滴氧化膜质量检查液(3gK2Cr2O7+75mL水+25mL浓硫酸),用秒表测定表面颜色变为绿色(产生Cr3+)所需时间,可判断氧化膜的耐腐蚀性。写出该变色反应的离子方程式:_______ 。
(4)氧化膜厚度测定
①取氧化完毕的铝片,测得表面积为4.0cm2,洗净吹干,称得质量为0.7654g;
②将铝片浸于60℃的溶膜液中煮沸10分钟进行溶膜处理;
③取出铝片,洗净吹干,称得除膜后铝片质量为0.7442g。
已知氧化膜的密度为2.7g/cm3,可以计算得出氧化膜厚度为_______ μm(1μm=1×10-4cm)。
(1)铝片预处理
铝片表面除去油垢后,用2mol/LNaOH溶液在60~70℃下洗涤,除去铝表面薄氧化膜,离子方程式为:
(2)电解氧化
取预处理过的铝片和铅做电极,控制电流恒定为0.06A,用直流电源在5~6mol/L硫酸中电解。其中铝片接电源

(3)氧化膜质量检验
取出阳极氧化并封闭处理过的铝片,洗净、干燥,在铝片表面滴一滴氧化膜质量检查液(3gK2Cr2O7+75mL水+25mL浓硫酸),用秒表测定表面颜色变为绿色(产生Cr3+)所需时间,可判断氧化膜的耐腐蚀性。写出该变色反应的离子方程式:
(4)氧化膜厚度测定
①取氧化完毕的铝片,测得表面积为4.0cm2,洗净吹干,称得质量为0.7654g;
②将铝片浸于60℃的溶膜液中煮沸10分钟进行溶膜处理;
③取出铝片,洗净吹干,称得除膜后铝片质量为0.7442g。
已知氧化膜的密度为2.7g/cm3,可以计算得出氧化膜厚度为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】硫、氮元素是高中化学学习的两种重要非金属元素,其价类二维图分别如图

(1)列举图中物质“c”的两种常见用途_______ ,图中物质“d”的化学式是_______ 。“Y”代表的物质类别是_______ ,若不加任何其它试剂完成转化过程⑤,则⑤的反应为_______ 反应(填“吸热”或“放热”)。
(2)将一定量的a气体通入下列溶液中,能观察到白色沉淀现象的是_______(填标号)
(3)写出反应③的离子方程式_______
(4) 的结构式为
的结构式为_______ 。a的溶液与 发生反应可观察到的实验现象是
发生反应可观察到的实验现象是_______ 。
(5)若e为钾元素的正盐,能被硫酸酸化的 氧化为
氧化为 ,
, 被还原为
被还原为 ,请配平化学方程式
,请配平化学方程式_______ 。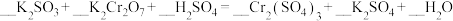
(6)如图为合成氨以及氨氧化制硝酸的流程示意图:
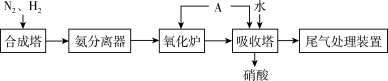
已知:用 溶液进行尾气处理时的化学反应为:
溶液进行尾气处理时的化学反应为: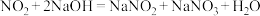 ,
, 。为了防止环境污染,用
。为了防止环境污染,用 溶液进行尾气处理,若尾气能完全被吸收,则尾气中
溶液进行尾气处理,若尾气能完全被吸收,则尾气中 与
与 的体积必须满足的条件是:
的体积必须满足的条件是:
_______ 。

(1)列举图中物质“c”的两种常见用途
(2)将一定量的a气体通入下列溶液中,能观察到白色沉淀现象的是_______(填标号)
A. 溶液 溶液 | B. 溶液 溶液 | C. 溶液 溶液 | D. 溶液 溶液 |
(4)
 的结构式为
的结构式为 发生反应可观察到的实验现象是
发生反应可观察到的实验现象是(5)若e为钾元素的正盐,能被硫酸酸化的
 氧化为
氧化为 ,
, 被还原为
被还原为 ,请配平化学方程式
,请配平化学方程式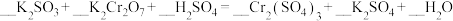
(6)如图为合成氨以及氨氧化制硝酸的流程示意图:

已知:用
 溶液进行尾气处理时的化学反应为:
溶液进行尾气处理时的化学反应为: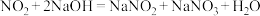 ,
, 。为了防止环境污染,用
。为了防止环境污染,用 溶液进行尾气处理,若尾气能完全被吸收,则尾气中
溶液进行尾气处理,若尾气能完全被吸收,则尾气中 与
与 的体积必须满足的条件是:
的体积必须满足的条件是:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】二氧化氯是一种黄绿色具有刺激性气味的气体,常用于自来水消毒和果蔬保鲜等方面。氯酸钠还原法是目前使用较为广泛的 制备方法,其中是用
制备方法,其中是用 与
与 在催化剂、
在催化剂、 时,发生反应得到
时,发生反应得到 ,下图装置(夹持装置略)对其制备、吸收、释放进行了研究。
,下图装置(夹持装置略)对其制备、吸收、释放进行了研究。
已知:
① 的浓度较大时易分解,实验室用稳定剂吸收
的浓度较大时易分解,实验室用稳定剂吸收 ,生成
,生成 ,使用时加酸只释放出
,使用时加酸只释放出 一种气体
一种气体
② 与KI反应的离子方程式为:
与KI反应的离子方程式为: 。
。
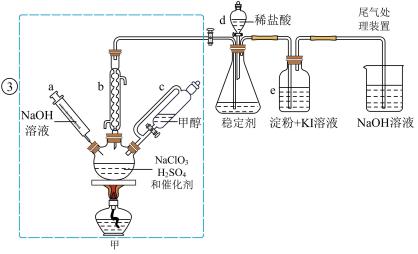
(1)仪器b在装置中的作用是______________ ;比较仪器c和d,实验中c的优点是_____________ 。
(2)制备装置甲中需改进的一项措施是________________ 。
(3)反应中甲醇被氧化为甲酸,写出制备 的化学方程式:
的化学方程式:________________ ;该制备法可选用不同的还原性物质作为还原剂,例如草酸,相比甲醇法,草酸法的优点是________________ 。
(4)下列有关说法正确的是__________ 。
A.仪器a中NaOH溶液主要用于停止反应,并吸收多余的
B.装置e主要用于检验是否有 生成
生成
C.在 释放实验中,发生的离子反应方程式是:
释放实验中,发生的离子反应方程式是: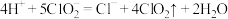
D. 和
和 都为强氧化剂,在相同条件下,等物质的量时
都为强氧化剂,在相同条件下,等物质的量时 的氧化能力是
的氧化能力是 的2.5倍
的2.5倍
(5)自来水厂用碘量法检测水中 的浓度,其实验操作如下:取100.0mL的水样,加入足量的碘化钾,再用氢氧化钠溶液调至中性,并加入淀粉溶液。再用
的浓度,其实验操作如下:取100.0mL的水样,加入足量的碘化钾,再用氢氧化钠溶液调至中性,并加入淀粉溶液。再用 标准溶液滴定碘单质
标准溶液滴定碘单质 ,达到滴定终点时用去15.00mL
,达到滴定终点时用去15.00mL 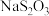 标准溶液,测得该水样中
标准溶液,测得该水样中 的含量为
的含量为__________  。
。
 制备方法,其中是用
制备方法,其中是用 与
与 在催化剂、
在催化剂、 时,发生反应得到
时,发生反应得到 ,下图装置(夹持装置略)对其制备、吸收、释放进行了研究。
,下图装置(夹持装置略)对其制备、吸收、释放进行了研究。已知:
①
 的浓度较大时易分解,实验室用稳定剂吸收
的浓度较大时易分解,实验室用稳定剂吸收 ,生成
,生成 ,使用时加酸只释放出
,使用时加酸只释放出 一种气体
一种气体②
 与KI反应的离子方程式为:
与KI反应的离子方程式为: 。
。| 物质 |  |  |  |
| 沸点 | 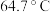 | 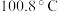 | 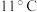 |

(1)仪器b在装置中的作用是
(2)制备装置甲中需改进的一项措施是
(3)反应中甲醇被氧化为甲酸,写出制备
 的化学方程式:
的化学方程式:(4)下列有关说法正确的是
A.仪器a中NaOH溶液主要用于停止反应,并吸收多余的

B.装置e主要用于检验是否有
 生成
生成C.在
 释放实验中,发生的离子反应方程式是:
释放实验中,发生的离子反应方程式是: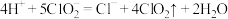
D.
 和
和 都为强氧化剂,在相同条件下,等物质的量时
都为强氧化剂,在相同条件下,等物质的量时 的氧化能力是
的氧化能力是 的2.5倍
的2.5倍(5)自来水厂用碘量法检测水中
 的浓度,其实验操作如下:取100.0mL的水样,加入足量的碘化钾,再用氢氧化钠溶液调至中性,并加入淀粉溶液。再用
的浓度,其实验操作如下:取100.0mL的水样,加入足量的碘化钾,再用氢氧化钠溶液调至中性,并加入淀粉溶液。再用 标准溶液滴定碘单质
标准溶液滴定碘单质 ,达到滴定终点时用去15.00mL
,达到滴定终点时用去15.00mL 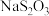 标准溶液,测得该水样中
标准溶液,测得该水样中 的含量为
的含量为 。
。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】理想气体状态方程PV=nRT,是描述理想气体的物质的量与其体积、分压、温度间关系的状态方程。其中,气体常数R可通过如下实验测定。

(1)组装仪器:简易量气装置的量气管用_______ (填常用仪器名称)代替; 组装完成后,须进行_______ (填操作名称)。
(2)装药品:
向反应管内加大足量的稀硫酸_______ (填“能”或“不能”)用稀硝酸代替稀硫酸,理由是_______ ;铝片打磨后称量,再用铜丝缠绕并放在反应管口,用铜丝缠绕铝片的目的是_______ 。
(3)反应:读取量气管的起始读数后,移动反应管,使铝片滑入稀硫酸中。
测量体积:待反应管内溶液无明显气泡产生后,对量气管进行第2次读数。读数时,应注意____ 、____ (回答2点)。
(4)数据计算:实验数据如下表所示。
甲同学用以上数据代入公式进行计算,得到气体常数R =_______ m-3∙Pa∙K-1.mol-1 (用计算式表示)。

(1)组装仪器:简易量气装置的量气管用
(2)装药品:
向反应管内加大足量的稀硫酸
(3)反应:读取量气管的起始读数后,移动反应管,使铝片滑入稀硫酸中。
测量体积:待反应管内溶液无明显气泡产生后,对量气管进行第2次读数。读数时,应注意
(4)数据计算:实验数据如下表所示。
| 铝片质量 | 反应前量气管读数 | 反应后量气管读数 | 室内温度 | 室内压强 |
| 0. 0270 g | 0. 50 mL | 38. 90 mL | 295.4 K | 1.01X105 Pa |
您最近一年使用:0次
【推荐3】利用如图所示装置测定中和热的实验步骤如下:
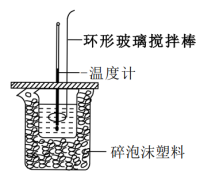
①用量筒量取50mL0.50 mol·L-1盐酸倒入小烧杯中,测出盐酸温度;
②用另一量筒量取50mL0.55 mol·L-1NaOH溶液,并用同一温度计测出其温度;
③将NaOH溶液倒入小烧杯中,设法使之混合均匀,测得混合液最高温度。
回答下列问题:
(1)NaOH溶液要稍过量的原因是___________ 。
(2)倒入NaOH溶液的正确操作是___________ (填字母)。
A.沿玻璃棒缓慢倒入
B.分三次少量倒入
C.一次迅速倒入
(3)使盐酸与NaOH溶液混合均匀的正确操作是___________(填字母)。
(4)现使一定量的稀氢氧化钠溶液、稀氢氧化钙溶液、稀氨水分别与1L1 mol·L-1的稀盐酸恰好完全反应,其反应热分别为△H1、△H2、△H3,则△H1、△H2、△H3的大小关系为___________ 。
(5)假设盐酸和氢氧化钠溶液的密度都是1g∙cm-3,又知中和反应后生成溶液的比热容4.18J·g-1·℃-1。为了计算中和热,某学生记录实验数据如下:
依据该学生的实验数据计算,该实验测得的中和热△H=___________ (结果保留一位小数)。
(6)该同学通过实验测出的中和热有误差,造成这一结果的原因不可能的是___________(填字母)。

①用量筒量取50mL0.50 mol·L-1盐酸倒入小烧杯中,测出盐酸温度;
②用另一量筒量取50mL0.55 mol·L-1NaOH溶液,并用同一温度计测出其温度;
③将NaOH溶液倒入小烧杯中,设法使之混合均匀,测得混合液最高温度。
回答下列问题:
(1)NaOH溶液要稍过量的原因是
(2)倒入NaOH溶液的正确操作是
A.沿玻璃棒缓慢倒入
B.分三次少量倒入
C.一次迅速倒入
(3)使盐酸与NaOH溶液混合均匀的正确操作是___________(填字母)。
| A.用温度计小心搅拌 | B.揭开硬纸片用玻璃棒搅拌 |
| C.轻轻地振荡烧杯 | D.用套在温度计上的环形玻璃搅拌棒轻轻地搅动 |
(5)假设盐酸和氢氧化钠溶液的密度都是1g∙cm-3,又知中和反应后生成溶液的比热容4.18J·g-1·℃-1。为了计算中和热,某学生记录实验数据如下:
| 实验序号 | 起始温度t1/℃ | 终止温度t2/℃ | |
| 盐酸 | 氢氧化钠溶液 | 混合溶液 | |
| 1 | 20.0 | 20.1 | 23.2 |
| 2 | 20.2 | 20.4 | 23.4 |
| 3 | 20.5 | 20.6 | 23.6 |
(6)该同学通过实验测出的中和热有误差,造成这一结果的原因不可能的是___________(填字母)。
| A.实验装置保温,隔热效果差 | B.用量筒量取盐酸时仰视读数 |
| C.分多次将NaOH溶液倒入小烧杯中 | D.用测量盐酸的温度计直接测定NaOH溶液的温度 |
您最近一年使用:0次
【推荐1】草酸存在于自然界的植物中,草酸的钠盐和钾盐易溶于水,而其钙盐难溶于水。草酸晶体(H2C2O4•2H2O)无色,熔点为101℃,易溶于水,受热脱水、升华,170℃以上分解。回答下列问题:

(1)甲组同学按照如图所示的装置,通过实验检验草酸晶体的分解产物。实验开始后,观察到:装置 中有气泡溢出,溶液变浑浊;由此可知草酸晶体分解的产物中一定含有
中有气泡溢出,溶液变浑浊;由此可知草酸晶体分解的产物中一定含有_______ 。
(2)乙组同学认为草酸晶体分解产物中还有CO,并通过实验证明了自己的判断。

乙组同学的实验装置中,依次连接A→B→F→D→G→H→D→I。
①F和G之间连接D的目的是_______ 。
②连接I的目的是_______ 。
③H中反应的化学方程式为_______ 。
④草酸晶体分解的化学方程式为_______ 。
(3)某同学用如图装置证明草酸具有还原性。
①如图安装和连接装置之后,能证明草酸具有还原性的实验现象是_______ 。

②完善反应的离子方程式:_______ 。
2MnO +
+ H2C2O4+
H2C2O4+ H+=2Mn2++
H+=2Mn2++ _______+
_______+ _______
_______

(1)甲组同学按照如图所示的装置,通过实验检验草酸晶体的分解产物。实验开始后,观察到:装置
 中有气泡溢出,溶液变浑浊;由此可知草酸晶体分解的产物中一定含有
中有气泡溢出,溶液变浑浊;由此可知草酸晶体分解的产物中一定含有(2)乙组同学认为草酸晶体分解产物中还有CO,并通过实验证明了自己的判断。

乙组同学的实验装置中,依次连接A→B→F→D→G→H→D→I。
①F和G之间连接D的目的是
②连接I的目的是
③H中反应的化学方程式为
④草酸晶体分解的化学方程式为
(3)某同学用如图装置证明草酸具有还原性。
①如图安装和连接装置之后,能证明草酸具有还原性的实验现象是

②完善反应的离子方程式:
2MnO
 +
+ H2C2O4+
H2C2O4+ H+=2Mn2++
H+=2Mn2++ _______+
_______+ _______
_______
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】有机物M(只含C、H、O三种元素)具有令人愉悦的牛奶香气,主要用于配制奶油、乳品、酸奶和草莓等型香精,是我国批准使用的香料产品,其沸点为148℃。某化学兴趣小组从粗品中分离提纯有机物M,然后借助李比希法、现代科学仪器测定有机物M的分子组成和结构,具体实验过程如下:
步骤一:将粗品用蒸馏法进行纯化。
(1)蒸馏装置如图1所示,图中虚线框内应选用右侧的___________ (填“仪器x”或“仪器y”),该仪器使用时冷水从___________ 口进 (填数字)。
元素分析是有机化合物的表征手段之一、按下图实验装置(部分装置略)对M进行C、H元素分析。___________ (a或者b),进行实验。
(3)c和d中的试剂分别是___________ 、___________ (填标号)。
A.CaCl2 B.NaCl C.碱石灰(CaO+NaOH) D.浓硫酸
(4)Pt坩埚中样品M反应完全后,熄灭燃煤气灯,继续通入氧气至石英管冷却至室温。
①整个过程中氧气的作用除氧化有机物外,还有的作用是___________ 、___________ (答出2点) 。
②取下c和d管称重。若样品M为0.88 g,实验结束后,c管增重0.72 g,d管增重1.76 g。
已知M的密度是同温同压下二氧化碳密度的2倍,则M的分子式为___________ 。
步骤三:确定M的结构简式。
(5)用核磁共振仪测出M的核磁共振氢谱如图2所示,图中峰面积之比为1∶3∶1∶3;利用红外光谱仪测得M的红外光谱如图3所示___________ (填键线式)。
(6)写出一种含有羧基的M的同分异构体G的结构简式:___________ 。
(7)下列方法中不能对鉴别M和G二者进行鉴别的是___________。
步骤一:将粗品用蒸馏法进行纯化。
(1)蒸馏装置如图1所示,图中虚线框内应选用右侧的

元素分析是有机化合物的表征手段之一、按下图实验装置(部分装置略)对M进行C、H元素分析。

(3)c和d中的试剂分别是
A.CaCl2 B.NaCl C.碱石灰(CaO+NaOH) D.浓硫酸
(4)Pt坩埚中样品M反应完全后,熄灭燃煤气灯,继续通入氧气至石英管冷却至室温。
①整个过程中氧气的作用除氧化有机物外,还有的作用是
②取下c和d管称重。若样品M为0.88 g,实验结束后,c管增重0.72 g,d管增重1.76 g。
已知M的密度是同温同压下二氧化碳密度的2倍,则M的分子式为
步骤三:确定M的结构简式。
(5)用核磁共振仪测出M的核磁共振氢谱如图2所示,图中峰面积之比为1∶3∶1∶3;利用红外光谱仪测得M的红外光谱如图3所示

(6)写出一种含有羧基的M的同分异构体G的结构简式:
(7)下列方法中不能对鉴别M和G二者进行鉴别的是___________。
| A.元素分析 | B.核磁共振氢谱 | C.红外光谱法 | D.原子光谱 |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】实验室中制备对氯苯甲酸的反应以及装置如图所示:

常温下,物质的有关数据和性质如表所示:
实验步骤:在规格为250mL的仪器A中加入一定量的催化剂、适量KMnO4、100mL水;安装好装置,在滴液漏斗中加入6.00mL对氯甲苯,在温度为93℃左右时,逐滴滴入对氯甲苯;控制温度在93℃左右,反应2h,过滤,将滤渣用热水洗涤,使洗涤液与滤液合并,加入稀硫酸酸化,加热浓缩,冷却,然后过滤,将滤渣用冷水进行洗涤,干燥后称量其质量。
请回答下列问题:
(1)仪器A的名称为______________________ 。
(2)仪器B是冷凝管,实验过程中,冷却水从a口进入,如此操作的目的是___________ 。
(3)实验过程中两次过滤、洗涤操作,第一次过滤的滤渣成分为___________ (填化学式),洗涤该滤渣用热水,目的是_________________________________ ,第二次过滤后,洗涤滤渣用冷水,目的是______________________ 。
(4)过滤、洗涤操作中能用到的仪器是___________ (填选项字母)。
a.烧杯 b.分液漏斗 c.锥形瓶 d.玻璃棒
(5)第一次过滤后的滤液中加入硫酸,出现的现象是___________ 。
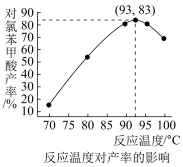
(6)如图是温度对对氯苯甲酸产率的影响关系,最后干燥、称量得到的对氯苯甲酸的质量为___________ (保留小数点后两位)。

常温下,物质的有关数据和性质如表所示:
| 熔点/℃ | 沸点/℃ | 密度/g·cm-3 | 颜色 | 水溶性 | |
| 对氯甲苯 | 7.5 | 162 | 1.07 | 无色 | 难溶 |
| 对氯苯甲酸 | 243 | 275 | 1.54 | 白色 | 微溶 |
| 对氯苯甲酸钾 | 具有盐的通性,属于可溶性盐 | ||||
实验步骤:在规格为250mL的仪器A中加入一定量的催化剂、适量KMnO4、100mL水;安装好装置,在滴液漏斗中加入6.00mL对氯甲苯,在温度为93℃左右时,逐滴滴入对氯甲苯;控制温度在93℃左右,反应2h,过滤,将滤渣用热水洗涤,使洗涤液与滤液合并,加入稀硫酸酸化,加热浓缩,冷却,然后过滤,将滤渣用冷水进行洗涤,干燥后称量其质量。
请回答下列问题:
(1)仪器A的名称为
(2)仪器B是冷凝管,实验过程中,冷却水从a口进入,如此操作的目的是
(3)实验过程中两次过滤、洗涤操作,第一次过滤的滤渣成分为
(4)过滤、洗涤操作中能用到的仪器是
a.烧杯 b.分液漏斗 c.锥形瓶 d.玻璃棒
(5)第一次过滤后的滤液中加入硫酸,出现的现象是
(6)如图是温度对对氯苯甲酸产率的影响关系,最后干燥、称量得到的对氯苯甲酸的质量为

您最近一年使用:0次



