铁是人类较早使用的金属之一、运用铁及其化合物的知识,完成下列问题。
(1)现有铁和铜的混合物,可以通过______把他们分开。
(2)电子工业需要用30%的FeCl3溶液腐蚀敷在绝缘板上的铜,制造印刷电路板。请写出FeCl3溶液与铜反应的离子方程式:_______ 。反应后的废液中含有Fe3+,可以用______ 检验。
(3)现将反应后的废液采用以下流程进行回收再生,根据流程图完成下列填空。
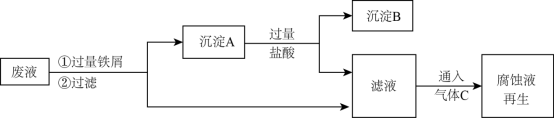
沉淀A中含有的单质:______ ,黄绿色气体C可以把滤液转化成FeCl3腐蚀液,写出反应过程中的离子方程式_______ 。
(4)取“滤液”少许于试管中,然后滴加氢氧化钠溶液,产生白色沉淀,______ (补全实验现象),此过程涉及氧化还原反应的化学方程式是_______ 。
(5)把铁皮插入到的硫酸铜和硫酸的混合溶液中,一段后取出,溶液的质量不变,则参加反应的H+与Cu2+物质的量之比为:______ 。
(1)现有铁和铜的混合物,可以通过______把他们分开。
| A.盐酸 | B.Fe3O4 | C.稀硝酸 | D.Fe2O3 |
(3)现将反应后的废液采用以下流程进行回收再生,根据流程图完成下列填空。

沉淀A中含有的单质:
(4)取“滤液”少许于试管中,然后滴加氢氧化钠溶液,产生白色沉淀,
(5)把铁皮插入到的硫酸铜和硫酸的混合溶液中,一段后取出,溶液的质量不变,则参加反应的H+与Cu2+物质的量之比为:
更新时间:2024-01-24 00:14:13
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
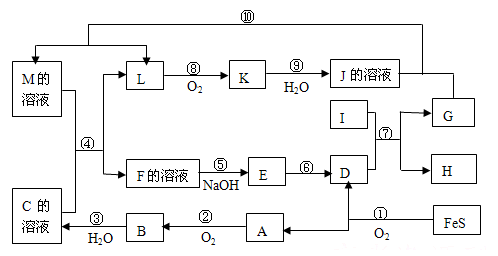
【推荐1】物质A~M在一定条件下的转化关系如图(部分产物及反应条件未列出).其中,I是既能与强酸反应生成氢气又能与强碱反应生成氢气的金属,K是一种红棕色气体,D的俗名叫铁红,A是形成酸雨的主要气体.
请填写下列空白:
(1)推导出下列物质的化学式:C:_____ E:_____
(2)在反应②、③、⑥、⑨中,既属于化合反应又属于非氧化还原反应的是_______________ (填写序号).
(3)反应④的离子方程式是:______________________ .
(4)将化合物D 与KNO3、KOH 共融,可制得一种“绿色”环保高效净水剂K2FeO4 (高铁酸钾),同时还生成KNO2和H2O.该反应的化学方程式是:_______________________ .
请填写下列空白:
(1)推导出下列物质的化学式:C:
(2)在反应②、③、⑥、⑨中,既属于化合反应又属于非氧化还原反应的是
(3)反应④的离子方程式是:
(4)将化合物D 与KNO3、KOH 共融,可制得一种“绿色”环保高效净水剂K2FeO4 (高铁酸钾),同时还生成KNO2和H2O.该反应的化学方程式是:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】某二元化合物X是锂硫电池的电极材料,为探究其组成进行了如下实验:

固体乙是一种单质,固体丙呈红棕色,将气体A通入溶液C中也能生成固体乙。
请回答:
(1)X的化学式是_________________ ,步骤①的化学方程式是_________________________ 。
(2)气体A通入溶液C发生反应的离子方程式是_________________________ 。

固体乙是一种单质,固体丙呈红棕色,将气体A通入溶液C中也能生成固体乙。
请回答:
(1)X的化学式是
(2)气体A通入溶液C发生反应的离子方程式是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】已知A为淡黄色固体,T、R为两种常见的用途很广的金属单质,D是具有磁性的黑色晶体,C是无色无味的气体,H是白色沉淀,W溶液中加入KSCN出现红色。
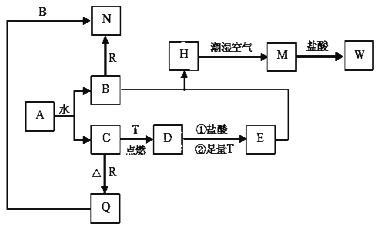
(1)写出下列物质的化学式:A______________ ;D________________ 。
(2)按要求写出下列反应的化学方程式:
H在潮湿空气中变成M的实验现象为___________________ ,
该过程用化学方程式可表示为________________________ 。
(3)B和R反应生成N的离子方程式:________________ 。

(1)写出下列物质的化学式:A
(2)按要求写出下列反应的化学方程式:
H在潮湿空气中变成M的实验现象为
该过程用化学方程式可表示为
(3)B和R反应生成N的离子方程式:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】黄铁矿既是硫矿又是铁矿,因其呈黄色俗称“愚人金”,是重要的工业原料。工业煅烧过程中常产生废渣,废渣成分主要含铁的几种氧化物和二氧化硅等,利用该废渣可以制备高效净水剂聚合硫酸铁,工艺流程如下:

(1)检验“酸溶”后的溶液中含有Fe2+,试剂是___________________ 。
(2)硫铁矿烧渣在“酸溶”前要粉碎的主要目的是_________________ 。
(3)废铁皮使用前要用纯碱溶液浸泡,目的是_____________________ 。
(4)“酸溶”过程中Fe2O3溶解的化学反应方程式为________________ 。
(5)“操作Ⅲ”系统操作名称依次为_________ 、__________ 、过滤和洗涤。洗涤的方法是________ 。
(6)加入适量H2O2的目的是氧化Fe2+,写出H2O2氧化Fe2+为Fe3+的离子方程式:___________ 。

(1)检验“酸溶”后的溶液中含有Fe2+,试剂是
(2)硫铁矿烧渣在“酸溶”前要粉碎的主要目的是
(3)废铁皮使用前要用纯碱溶液浸泡,目的是
(4)“酸溶”过程中Fe2O3溶解的化学反应方程式为
(5)“操作Ⅲ”系统操作名称依次为
(6)加入适量H2O2的目的是氧化Fe2+,写出H2O2氧化Fe2+为Fe3+的离子方程式:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】铁是人体必需的微量元素,铁摄入不足可能引起缺铁性贫血。
Ⅰ:黑木耳中含有比较丰富的铁元素,某研学小组测定其含量。
(1)【铁元素的分离】在坩埚中高温灼烧黑木耳,使之完全灰化。用足量的酸充分溶解,过滤,滤液中铁元素的存在形式是 、
、_______ 。
(2)【铁元素含量测定】研学小组提出如下测量方案。
ⅰ.沉淀法:向(1)滤液中加入足量 溶液,过滤、洗涤沉淀、充分加热至恒重、称量。请评价该测量方案是否可行
溶液,过滤、洗涤沉淀、充分加热至恒重、称量。请评价该测量方案是否可行_______ ,理由是_______ 。
ⅱ.比色法:流程如下。

①溶液 的颜色是
的颜色是_______ 。
②溶液颜色越深,光的透过能力越差,即透光率越小,含铁量越_______ (填“高”或“低”。)
③若不加 ,测出黑木耳中铁元素的含量将
,测出黑木耳中铁元素的含量将_______ (填“偏大”或“偏小”)。
Ⅱ:在肺部,血红蛋白中的亚铁血红素与 结合,把
结合,把 送到各个组织器官。
送到各个组织器官。
(3)已知葡萄糖的分子式是 。铁元素参与人体内的呼吸作用示意图如下图(部分中间产物已略去)。
。铁元素参与人体内的呼吸作用示意图如下图(部分中间产物已略去)。

①反应中起催化作用的物质是_______ 和 。
。
②具有还原性的酶是_______ 。
③该过程总反应的化学方程式是_______ 。
Ⅰ:黑木耳中含有比较丰富的铁元素,某研学小组测定其含量。
(1)【铁元素的分离】在坩埚中高温灼烧黑木耳,使之完全灰化。用足量的酸充分溶解,过滤,滤液中铁元素的存在形式是
 、
、(2)【铁元素含量测定】研学小组提出如下测量方案。
ⅰ.沉淀法:向(1)滤液中加入足量
 溶液,过滤、洗涤沉淀、充分加热至恒重、称量。请评价该测量方案是否可行
溶液,过滤、洗涤沉淀、充分加热至恒重、称量。请评价该测量方案是否可行ⅱ.比色法:流程如下。

①溶液
 的颜色是
的颜色是②溶液颜色越深,光的透过能力越差,即透光率越小,含铁量越
③若不加
 ,测出黑木耳中铁元素的含量将
,测出黑木耳中铁元素的含量将Ⅱ:在肺部,血红蛋白中的亚铁血红素与
 结合,把
结合,把 送到各个组织器官。
送到各个组织器官。(3)已知葡萄糖的分子式是
 。铁元素参与人体内的呼吸作用示意图如下图(部分中间产物已略去)。
。铁元素参与人体内的呼吸作用示意图如下图(部分中间产物已略去)。
①反应中起催化作用的物质是
 。
。②具有还原性的酶是
③该过程总反应的化学方程式是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】实验室以锈蚀程度很大的废铁屑为原料制备 晶体的流程如下:
晶体的流程如下:

已知:在水溶液中 能与
能与 反应生成蓝色沉淀
反应生成蓝色沉淀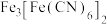 。回答下列问题:
。回答下列问题:
(1)“酸溶”过程中发生的主要反应有:
① ;
;
②
③_______ (用离子方程式表示)
(2)“酸溶”需控制温度在40℃左右,最佳的加热方式为_______ 。
(3)“过滤”需要的玻璃仪器除烧杯外还有_______ 。
(4)“氧化”过程可在下图所示装置中进行。

①装置A中 与浓盐酸反应生成
与浓盐酸反应生成 和
和 ,其反应方程式为
,其反应方程式为_______ 。
②装置C中发生的反应方程式为_______ 。
③B中使用多孔球泡的作用是_______ 。
④证明装置B溶液中 已完全被氧化成
已完全被氧化成 的实验方案是
的实验方案是_______ 。
 晶体的流程如下:
晶体的流程如下:
已知:在水溶液中
 能与
能与 反应生成蓝色沉淀
反应生成蓝色沉淀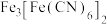 。回答下列问题:
。回答下列问题:(1)“酸溶”过程中发生的主要反应有:
①
 ;
;②

③
(2)“酸溶”需控制温度在40℃左右,最佳的加热方式为
(3)“过滤”需要的玻璃仪器除烧杯外还有
(4)“氧化”过程可在下图所示装置中进行。

①装置A中
 与浓盐酸反应生成
与浓盐酸反应生成 和
和 ,其反应方程式为
,其反应方程式为②装置C中发生的反应方程式为
③B中使用多孔球泡的作用是
④证明装置B溶液中
 已完全被氧化成
已完全被氧化成 的实验方案是
的实验方案是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】某同学利用下图所示的实验装置进行铁跟水蒸气反应的实验,并继续研究铁及其化合物的部分性质。
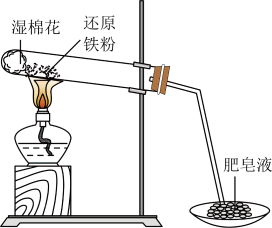
请回答下列问题:
(1)硬质试管中发生反应的化学方程式为___________________________ 。
(2)该同学欲确定反应后硬质试管中固体物质的成分,设计了如下实验方案:
①待硬质试管冷却后,取少许固体物质于试管中,并向试管中加稀硫酸得溶液B;
②取少量溶液B于试管中,滴加几滴KSCN溶液,结果溶液未变红色,说明硬质试管中固体物质的成分有:__________________ 。(填化学式)
(3)该同学马上另取少量溶液B,使其跟NaOH溶液反应。若按下图所示的操作,
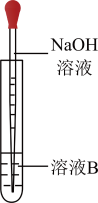
可观察到先生成白色沉淀,迅速变成灰绿色,最后变成红褐色的现象,请按顺序写出与上述现象相关的反应方程式:属于离子反应的只写离子方程式。①_______________________ ②________________________
(4)一段时间后,该同学发现(2)中未变红的溶液变成红色,说明Fe2+ 具有_________ 性。由此可知,实验室中FeSO4溶液在保存时要加入少量铁粉,其原因是_________________ 。(用离子方程式表示)

请回答下列问题:
(1)硬质试管中发生反应的化学方程式为
(2)该同学欲确定反应后硬质试管中固体物质的成分,设计了如下实验方案:
①待硬质试管冷却后,取少许固体物质于试管中,并向试管中加稀硫酸得溶液B;
②取少量溶液B于试管中,滴加几滴KSCN溶液,结果溶液未变红色,说明硬质试管中固体物质的成分有:
(3)该同学马上另取少量溶液B,使其跟NaOH溶液反应。若按下图所示的操作,

可观察到先生成白色沉淀,迅速变成灰绿色,最后变成红褐色的现象,请按顺序写出与上述现象相关的反应方程式:属于离子反应的只写离子方程式。①
(4)一段时间后,该同学发现(2)中未变红的溶液变成红色,说明Fe2+ 具有
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】已知A为淡黄色固体,T为目前使用最广泛的金属单质,D是具有磁性的黑色晶体,C是无色无味的气体,H是白色沉淀。______ 。
(2)H在潮湿空气中变成M的实验现象是______ ,化学方程式为______ 。
(3)A和水反应生成B和C的离子方程式为______ 。
(4)反应①的离子方程式为______ ,②加足量T的目的______ ,反应的离子方程式为______ 。

(2)H在潮湿空气中变成M的实验现象是
(3)A和水反应生成B和C的离子方程式为
(4)反应①的离子方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】实验室用如图所示方法制Fe(OH)2,但一般看不到白色的Fe(OH)2沉淀,原因是Fe(OH)2不稳定,极易被O2氧化生成Fe(OH)3.请回答:

(1)向氯化亚铁溶液中滴加氢氧化钠溶液反应的离子方程式:_______ ,现象是_______
(2)Fe(OH)2被O2 氧化的化学方程式是:_______ 。
(3)实验室保存FeCl2溶液常常加入铁粉,其作用是_______ (用离子方程式表示),检验FeCl2溶液是否变质,可向其中加入_______ (填化学式)溶液,观察现象。

(1)向氯化亚铁溶液中滴加氢氧化钠溶液反应的离子方程式:
(2)Fe(OH)2被O2 氧化的化学方程式是:
(3)实验室保存FeCl2溶液常常加入铁粉,其作用是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】实验室可用草酸(H2C2O4)在浓硫酸的作用下分解得一氧化碳,某研究小组利用如图所示装置探究温度对CO还原Fe2O3的影响(固定装置略):
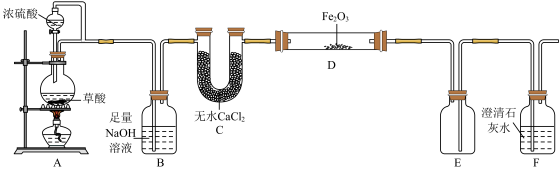
(1)草酸(H2C2O4)在浓硫酸的作用下分解制取一氧化碳的化学方程式为_____________________ 。
(2)装置C的作用是_______________ ,加热D装置之前需进行的操作是___________________ 。
(3)将研究小组分为两组,按上图装置进行对比实验,甲组用酒精灯、乙组用酒精灯对装置D加热,反应产物均为黑色粉末(纯净物),两组分别用产物进行以下实验:
①甲组步骤1中反应的化学方程式为_________________________ 。
②甲组步骤3中,溶液变红的离子方程式为______________________ 。
③乙组得到的黑色粉末是_____________ (填化学式)。
④乙组步骤4中,溶液褪色可能的原因及其验证方法为_______________________ 。
(4)该装置的改进措施除了在E装置后加尾气处理装置外还需_______________________ 。

(1)草酸(H2C2O4)在浓硫酸的作用下分解制取一氧化碳的化学方程式为
(2)装置C的作用是
(3)将研究小组分为两组,按上图装置进行对比实验,甲组用酒精灯、乙组用酒精灯对装置D加热,反应产物均为黑色粉末(纯净物),两组分别用产物进行以下实验:
| 步骤 | 操作 | 甲组现象 | 乙组现象 |
| 1 | 取黑色粉末加入稀硫酸 | 溶解,无气泡 | 溶解,有气泡 |
| 2 | 取步骤1中溶液,滴加K3[Fe(CN)6]溶液 | 蓝色沉淀 | 蓝色沉淀 |
| 3 | 取步骤1中溶液,滴加KSCN溶液 | 变红 | 无现象 |
| 4 | 向步骤3溶液中滴加新制氯水 | 红色褪去 | 先变红,后褪色 |
②甲组步骤3中,溶液变红的离子方程式为
③乙组得到的黑色粉末是
④乙组步骤4中,溶液褪色可能的原因及其验证方法为
(4)该装置的改进措施除了在E装置后加尾气处理装置外还需
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】某实验小组进行Cu和 溶液的实验。实验探究过程如图:
溶液的实验。实验探究过程如图:
实验装置

实验操作与现象:ⅰ.加入Cu粉后充分振荡,静置,溶液变成浅蓝绿色;
ⅱ.取少量ⅰ中清液于试管中,滴加3滴0.1mol/L KSCN溶液,立即出现白色沉淀,溶液局部变为红色,振荡后红色迅速褪去。
查阅资料:
Ⅰ. 可与
可与 反应生成CuSCN(白色沉淀)和
反应生成CuSCN(白色沉淀)和 ,
, 的性质与
的性质与 相似。
相似。
Ⅱ.CuSCN能与稀硝酸反应: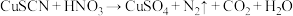 (未配平)。
(未配平)。
回答下列问题:
(1)Cu和 溶液反应的离子方程式为
溶液反应的离子方程式为___________ 。
(2)根据以上给出的实验现象推断白色沉淀为___________ 。为验证该白色沉淀,取少量白色沉淀于试管中,加入___________ ,若___________ 即可证明(补充所加试剂及实验现象)。
(3)用离子方程式解释ⅱ中溶液局部变为红色的原因是___________ 。
(4)根据ⅱ中实验现象可推知 更易与
更易与___________ 结合(填“ ”或“
”或“ ”)
”)
 溶液的实验。实验探究过程如图:
溶液的实验。实验探究过程如图:实验装置

实验操作与现象:ⅰ.加入Cu粉后充分振荡,静置,溶液变成浅蓝绿色;
ⅱ.取少量ⅰ中清液于试管中,滴加3滴0.1mol/L KSCN溶液,立即出现白色沉淀,溶液局部变为红色,振荡后红色迅速褪去。
查阅资料:
Ⅰ.
 可与
可与 反应生成CuSCN(白色沉淀)和
反应生成CuSCN(白色沉淀)和 ,
, 的性质与
的性质与 相似。
相似。Ⅱ.CuSCN能与稀硝酸反应:
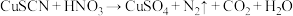 (未配平)。
(未配平)。回答下列问题:
(1)Cu和
 溶液反应的离子方程式为
溶液反应的离子方程式为(2)根据以上给出的实验现象推断白色沉淀为
(3)用离子方程式解释ⅱ中溶液局部变为红色的原因是
(4)根据ⅱ中实验现象可推知
 更易与
更易与 ”或“
”或“ ”)
”)
您最近一年使用:0次
【推荐3】某化学兴趣小组利用下列试剂:铁粉、锌粉、0.1 mol·L-1FeCl3溶液,0.1 mol·L-1FeCl2溶液、KSCN溶液、新制氯水、5%H2O2溶液,探究Fe2+、Fe3+的氧化性、还原性,并利用实验结论解决一些问题。
(1)设计实验方案,完成下列表格。
(2)该兴趣小组为说明“Fe2+具有氧化性”,提出了向FeCl2溶液中加入锌粉,观察实验现象的方案,该反应的离子方程式为____ 。
(3)某反应中反应物与生成物有Fe3+、Mn2+、H+、MnO 、H2O和一种未知离子X,已知MnO
、H2O和一种未知离子X,已知MnO 在反应中得到电子,则X是
在反应中得到电子,则X是____ 。
(1)设计实验方案,完成下列表格。
| 探究内容 | 实验方案 | 实验现象 | 解释 |
| Fe3+具有氧化性 | 取少量0.1 mol/LFeCl3溶液,往溶液中加入足量铁粉,再加入少量KSCN溶液 | ①加入铁粉后,溶液 ②加入KSCN溶液后,溶液 | ③体现Fe3+具有氧化性的离子方程式: |
| Fe2+具有还原性 | ④取少量0.1 mol/LFeCl2溶液,往溶液中加入少量KSCN溶液,再加入 | ⑤加入KSCN溶液后,溶液 ⑥加入你选的试剂后,溶液 | ⑦体现Fe2+具有还原性的离子方程式: |
(3)某反应中反应物与生成物有Fe3+、Mn2+、H+、MnO
 、H2O和一种未知离子X,已知MnO
、H2O和一种未知离子X,已知MnO 在反应中得到电子,则X是
在反应中得到电子,则X是
您最近一年使用:0次



