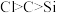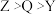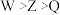物质M可用作牙膏、牙粉的稳定剂,其化学式为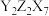 (不溶于水)。已知X、Y、Z为原子序数依次增大的短周期元素,基态Z原子的3p轨道半充满,基态X原子的s能级电子总数与p能级电子总数相等,Y主要用于制造轻金属合金、科学仪器和格氏试剂等。下列说法正确的是
(不溶于水)。已知X、Y、Z为原子序数依次增大的短周期元素,基态Z原子的3p轨道半充满,基态X原子的s能级电子总数与p能级电子总数相等,Y主要用于制造轻金属合金、科学仪器和格氏试剂等。下列说法正确的是
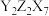 (不溶于水)。已知X、Y、Z为原子序数依次增大的短周期元素,基态Z原子的3p轨道半充满,基态X原子的s能级电子总数与p能级电子总数相等,Y主要用于制造轻金属合金、科学仪器和格氏试剂等。下列说法正确的是
(不溶于水)。已知X、Y、Z为原子序数依次增大的短周期元素,基态Z原子的3p轨道半充满,基态X原子的s能级电子总数与p能级电子总数相等,Y主要用于制造轻金属合金、科学仪器和格氏试剂等。下列说法正确的是| A.Z的最高价含氧酸的酸性强于硫酸 |
| B.电负性:X>Z>Y |
| C.Y和X元素形成的简单二元化合物易溶于水 |
D.M溶液中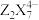 易水解生成 易水解生成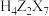 |
更新时间:2024-01-24 06:57:55
|
相似题推荐
【推荐1】某工厂用六水合氯化镁和粗石灰制取的氢氧化镁含有少量氢氧化铁杂质,通过如下流程进行提纯精制,获得阻燃剂氢氧化镁。下列说法不正确的是
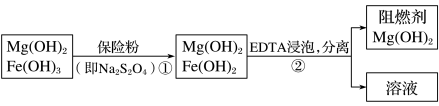

| A.步骤①中保险粉是作还原剂,步骤②中分离操作的名称是过滤 |
B.步骤①中的反应式:3Fe(OH)3+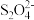 +2OH-=3Fe(OH)2+2 +2OH-=3Fe(OH)2+2 +4H2O +4H2O |
| C.Mg(OH)2可以作阻燃剂是因为它分解需要吸收大量的热 |
| D.从步骤②中可知OH-和EDTA共存时,Fe2+更易和EDTA结合,生成可溶性化合物 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】在给定条件下,下列选项所示的物质间转化均能实现的是
A.MgCO3(s)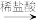 MgCl2(aq) MgCl2(aq) 无水MgCl2 无水MgCl2 |
B.S(s)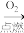 SO2(g) SO2(g)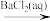 BaSO3(s) BaSO3(s) |
C.N2(g) NH3(g) NH3(g)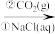 NaHCO3(s) NaHCO3(s) |
D.NaClO(aq) HClO(aq) HClO(aq)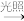 Cl2(g) Cl2(g) |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列离子方程式正确且与对应操作和目的相符的是
| 选项 | 目的 | 操作 | 离子方程式 |
| A | 比较Fe2+和Br−还原性强弱 | 向FeBr2溶液中滴入少量氯水 | 2Br−+Cl2=Br2+2Cl− |
| B | 比较C、Si非金属性强弱 | 向硅酸钠溶液中通入少量二氧化碳 | SiO32-+CO2+H2O=H2SiO3↓+CO32- |
| C | 除去CO2中的SO2 | 将气体通入盛有饱和碳酸氢钠溶液的洗气瓶 | CO32-+SO2= SO32-+CO2 |
| D | 实验室制取氯气 | 向MnO2固体中加入浓盐酸并加热 | MnO2+4HCl(浓) 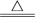 2Mn2+ 2Mn2++2Cl− +Cl2↑+2H2O |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】如图是卤素单质( 、
、 、
、 、
、 )的沸点与相对分子质量的关系图,下列说法错误的是
)的沸点与相对分子质量的关系图,下列说法错误的是

 、
、 、
、 、
、 )的沸点与相对分子质量的关系图,下列说法错误的是
)的沸点与相对分子质量的关系图,下列说法错误的是
A.单质①是最容易与 反应的卤素单质 反应的卤素单质 |
| B.单质②通入淀粉碘化钾溶液,溶液变蓝 |
| C.单质③常温下为液体 |
| D.单质④的氢化物在卤素氢化物中最稳定 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】中学常见的短周期主族元素R、X、Y、Z、M的原子序数依次增大,它们占据三个周期。Y和M位于同主族,Y原子最外层电子数是电子层数的3倍。这五种元素组成一种离子化合物Q。取一定量Q溶于蒸馏水得到溶液,向溶液中滴加稀氢氧化钠溶液,产生沉淀与氢氧化钠溶液体积如图所示。下列说法不正确的是
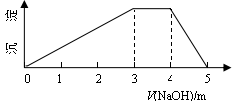

| A.简单的离子半径:M>Y>Z |
| B.气态氢化物的稳定性:Y>X |
| C.最高价氧化物对应水化物的酸性:M>Z |
| D.由R、X、Y、M四种元素可组成至少5种盐 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】W、X、Y、Z 为原子序数依次增大的四种短周期元素,W的简单氢化物可用作制冷剂,Y所在周期数与族序数相同,X与Y为同周期元素,Z原子的最外层电子数与 W 的电子总数相等。下列说法正确的是
| A.简单离子半径: W>X>Y>Z | B.W、X 的氢化物在常温下均为气体 |
| C.X、Y的最高价氧化物的水化物均为强碱 | D.W 与 Z 形成的化合物中只有共价键 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】短周期主族元素X、Y、Z、M、N原子序数依次增大,这五种元素形成的化合物W是一种无色晶体,是厨房中常用的鲜味调味品。下列说法正确的是
| A.原子半径:Y<Z<M<N |
| B.氢化物稳定性:Y<Z<M |
| C.W中的原子均达到8电子稳定结构 |
| D.X与M形成的常见阴、阳离子均可抑制水的电离 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】铝碳酸镁[Mg6Al2(OH)16CO3·4H2O]可以用来治疗胃酸过多。铝碳酸镁受热易分解:Mg6Al2(OH)16CO3·4H2O 6MgO+Al2O3+CO2↑+12H2O,下列说法正确的是
6MgO+Al2O3+CO2↑+12H2O,下列说法正确的是
 6MgO+Al2O3+CO2↑+12H2O,下列说法正确的是
6MgO+Al2O3+CO2↑+12H2O,下列说法正确的是| A.第一电离能大小:I1(Al)>I1(Mg) | B.电负性:O>H>C |
| C.离子半径大小:r(O2−)>r(Mg2+) | D.碱性:Al(OH)3>Mg(OH)2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】短周期主族元素X、Y、Z、Q、W原子序数依次增大,其中X是宇宙中含量最多的元素,其核外电子只有一种自旋取向;在同周期元素中,第一电离能数值比Y大的元素有2种;Z、Q两种原子核外s能级上的电子总数与p能级上电子总数相等,W原子的价电子中,在不同形状的原子轨道中运动的电子数之比为2:1。下列说法正确的是
| A.电负性:Q<Y<X<Z | B.工业上电解熔融化合物QZ制备单质Q |
C.键角: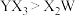 | D.阴离子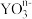 和 和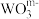 的空间构型相同 的空间构型相同 |
您最近一年使用:0次

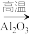 Al
Al H2
H2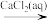 CaSO3
CaSO3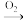 CaSO4
CaSO4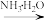 [Ag(NH3)2OH(aq)]
[Ag(NH3)2OH(aq)]  Ag
Ag MgCl2(s)
MgCl2(s)  Mg
Mg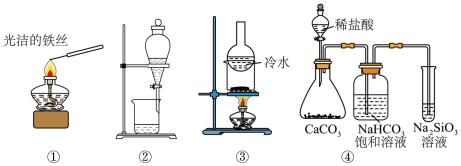
 和
和 固体
固体