Ⅰ.“价类”二维图是学习元素及其化合物的重要工具.如图所示是铁及其化合物的“价类”二维图。__________ 、__________ ;Z在空气中转化为W的化学方程式为__________ 。
(2)含重铬酸根离子 的工业废水有毒,必须经过处理达标后才能排放。工业上常用绿矾
的工业废水有毒,必须经过处理达标后才能排放。工业上常用绿矾 作处理剂,发生反应的离子方程式为
作处理剂,发生反应的离子方程式为 ,则该反应中还原性:
,则该反应中还原性:
______ (填“>”或“<”) 。该反应中,每生成
。该反应中,每生成 ,消耗
,消耗 的质量为
的质量为__________ g。
Ⅱ.硫酸亚铁晶体 在医药上作补血剂。某课外小组取10片补血剂总质量w g,通过一系列反应转变为
在医药上作补血剂。某课外小组取10片补血剂总质量w g,通过一系列反应转变为 来测定该补血剂中铁元素的含量。实验步骤如下:
来测定该补血剂中铁元素的含量。实验步骤如下:
(3)某同学发现部分补血剂药片表面发黄,怀疑该补铁剂已经变质,遂取少量步骤①的滤液,滴加__________ 后,溶液变为红色,证实了怀疑。
(4)步骤②反应的离子方程式为__________ ,下列物质中可以用来代替该步骤中的 是
是__________ (填序号)。
① 溶液 ②氯水 ③稀盐酸 ④碳酸钠
溶液 ②氯水 ③稀盐酸 ④碳酸钠
(5)服用维生素C可使食物中的 转化为
转化为 ,从而实现科学补铁,在这个过程中体现出维生素C的
,从而实现科学补铁,在这个过程中体现出维生素C的__________ 性。假设实验中的损耗忽略不计,则该补血剂含铁元素的质量分数为__________ 。

(2)含重铬酸根离子
 的工业废水有毒,必须经过处理达标后才能排放。工业上常用绿矾
的工业废水有毒,必须经过处理达标后才能排放。工业上常用绿矾 作处理剂,发生反应的离子方程式为
作处理剂,发生反应的离子方程式为 ,则该反应中还原性:
,则该反应中还原性:
 。该反应中,每生成
。该反应中,每生成 ,消耗
,消耗 的质量为
的质量为Ⅱ.硫酸亚铁晶体
 在医药上作补血剂。某课外小组取10片补血剂总质量w g,通过一系列反应转变为
在医药上作补血剂。某课外小组取10片补血剂总质量w g,通过一系列反应转变为 来测定该补血剂中铁元素的含量。实验步骤如下:
来测定该补血剂中铁元素的含量。实验步骤如下:
(3)某同学发现部分补血剂药片表面发黄,怀疑该补铁剂已经变质,遂取少量步骤①的滤液,滴加
(4)步骤②反应的离子方程式为
 是
是①
 溶液 ②氯水 ③稀盐酸 ④碳酸钠
溶液 ②氯水 ③稀盐酸 ④碳酸钠(5)服用维生素C可使食物中的
 转化为
转化为 ,从而实现科学补铁,在这个过程中体现出维生素C的
,从而实现科学补铁,在这个过程中体现出维生素C的
更新时间:2024-01-24 08:53:15
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】已知反应:①SO3+H2O=H2SO4;②Cl2+H2O=HCl+HClO;③2F2+2H2O=4HF+O2;④2Na+2H2O=2NaOH+H2↑;⑤2Na2O2+2H2O=4NaOH+O2↑;⑥SiO2+2NaOH=Na2SiO3+H2O。
(1)上述反应中不属于氧化还原反应的有__ (填序号,下同);H2O被氧化的是___ 。H2O做氧化剂的是__ 。属于氧化还原反应,但其中的H2O既不被氧化,又不被还原的是__ 。
(2)1molNa2O2与水完全反应时转移的电子数目为__ ,产生的气体在标准状况下的体积为__ 。
(3)酸性条件下,K2Cr2O7溶液和FeCl2溶液混合后生成Cr3+,请写出离子方程式__ 。
(1)上述反应中不属于氧化还原反应的有
(2)1molNa2O2与水完全反应时转移的电子数目为
(3)酸性条件下,K2Cr2O7溶液和FeCl2溶液混合后生成Cr3+,请写出离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂,比Cl2、O2、ClO2、KMnO4氧化性更强,无二次污染,工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH至饱和,使高铁酸钾析出。
(1)干法制备高铁酸钠的主要反应为:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑,该反应中还原剂是___ (填化学式),被2molFeSO4还原的过氧化钠为__ mol。
(2)湿法制备高铁酸钾(K2FeO4)的反应体系中有六种微粒:Fe(OH)3、ClO-、OH-、FeO 、Cl-、H2O。写出碱性条件下制高铁酸钾的离子反应方程式:
、Cl-、H2O。写出碱性条件下制高铁酸钾的离子反应方程式:___ 。
(1)干法制备高铁酸钠的主要反应为:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑,该反应中还原剂是
(2)湿法制备高铁酸钾(K2FeO4)的反应体系中有六种微粒:Fe(OH)3、ClO-、OH-、FeO
 、Cl-、H2O。写出碱性条件下制高铁酸钾的离子反应方程式:
、Cl-、H2O。写出碱性条件下制高铁酸钾的离子反应方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】氧化还原反应原理在研究物质性质及物质转化方面具有重要的价值。根据所学知识回答下列问题:
(1) 是一种有毒气体,如果泄漏会造成严重的环境污染,化工厂可用浓氨水来检验
是一种有毒气体,如果泄漏会造成严重的环境污染,化工厂可用浓氨水来检验 是否泄漏,有关反应的化学方程式为
是否泄漏,有关反应的化学方程式为 ,该反应中氧化剂为
,该反应中氧化剂为___________ (填化学式),标准状况下,每生成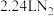 ,反应中转移的电子的物质的量为
,反应中转移的电子的物质的量为___________  。
。
(2)在一定条件下, 可与
可与 发生反应:
发生反应: ,在此过程中
,在此过程中 被
被___________ (填“氧化”或“还原”), 中
中 的化合价是
的化合价是___________ 价。
(3)某一反应体系有反应物和生成物共七种物质: 、
、 、
、 、
、 、
、 、
、 、
、 ,已知该反应中有气体生成。
,已知该反应中有气体生成。
①该反应中的还原剂是___________ (填化学式,下同),被还原的物质为___________ 。
②写出该反应的化学方程式:___________ 。
(1)
 是一种有毒气体,如果泄漏会造成严重的环境污染,化工厂可用浓氨水来检验
是一种有毒气体,如果泄漏会造成严重的环境污染,化工厂可用浓氨水来检验 是否泄漏,有关反应的化学方程式为
是否泄漏,有关反应的化学方程式为 ,该反应中氧化剂为
,该反应中氧化剂为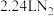 ,反应中转移的电子的物质的量为
,反应中转移的电子的物质的量为 。
。(2)在一定条件下,
 可与
可与 发生反应:
发生反应: ,在此过程中
,在此过程中 被
被 中
中 的化合价是
的化合价是(3)某一反应体系有反应物和生成物共七种物质:
 、
、 、
、 、
、 、
、 、
、 、
、 ,已知该反应中有气体生成。
,已知该反应中有气体生成。①该反应中的还原剂是
②写出该反应的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】有效去除大气中的NOx和水体中的氮是环境保护的重要课题。
(1)磷酸铵镁 沉淀法可去除水体中的氨氮
沉淀法可去除水体中的氨氮  和
和  。实验室中模拟氨氮处理:
。实验室中模拟氨氮处理: 的模拟氨氮废水(主要含
的模拟氨氮废水(主要含  ),置于搅拌器上,设定反应温度为25℃,先后加入
),置于搅拌器上,设定反应温度为25℃,先后加入  溶液,用
溶液,用  调节反应
调节反应  ,投加絮凝剂;开始搅拌,反应
,投加絮凝剂;开始搅拌,反应  后,取液面下
后,取液面下 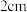 处清液测定氨氮质量浓度。
处清液测定氨氮质量浓度。
①生成磷酸铵镁沉淀的离子反应方程式为___________ 。
②测得反应 对氨氮去除率的影响如图1所示,当反应
对氨氮去除率的影响如图1所示,当反应  为9.0时,该沉淀法对氨氮的去除率达到最高,当
为9.0时,该沉淀法对氨氮的去除率达到最高,当  继续增至10.0时,氨氮的去除率下降,结合离子方程式说明去除率下降的原因是
继续增至10.0时,氨氮的去除率下降,结合离子方程式说明去除率下降的原因是___________ 。

③当 从9.0降低至7.5。的过程中,水中氨氮的去除率明显降低,沉淀减少的原因是
从9.0降低至7.5。的过程中,水中氨氮的去除率明显降低,沉淀减少的原因是___________ 。
(2)纳米零价铁 与
与 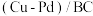 合作用可去除水体中的硝态氮。在
合作用可去除水体中的硝态氮。在  和
和 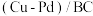 复合材料联合作用的体系中,生物炭
复合材料联合作用的体系中,生物炭 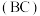 作为
作为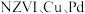 的载体且减少了纳米零价铁的团聚,
的载体且减少了纳米零价铁的团聚, 和
和  作为催化剂且参与吸附活性
作为催化剂且参与吸附活性 
① 和
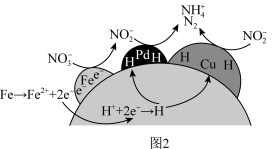
和 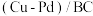 复合材料还原硝酸盐的反应机理如图2所示,
复合材料还原硝酸盐的反应机理如图2所示, 转化为
转化为 或
或  的过程中有两步氧化还原反应,其中第一步的还原剂是
的过程中有两步氧化还原反应,其中第一步的还原剂是___________ ,第二步反应的还原剂是___________ 。
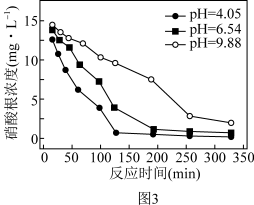
②实验测得体系初始 对
对 去除率的影响如图3,前
去除率的影响如图3,前 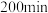 内,
内,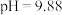 时的去除率远低于
时的去除率远低于  时,其可能的原因是
时,其可能的原因是___________ 。
(1)磷酸铵镁
 沉淀法可去除水体中的氨氮
沉淀法可去除水体中的氨氮  和
和  。实验室中模拟氨氮处理:
。实验室中模拟氨氮处理: 的模拟氨氮废水(主要含
的模拟氨氮废水(主要含  ),置于搅拌器上,设定反应温度为25℃,先后加入
),置于搅拌器上,设定反应温度为25℃,先后加入  溶液,用
溶液,用  调节反应
调节反应  ,投加絮凝剂;开始搅拌,反应
,投加絮凝剂;开始搅拌,反应  后,取液面下
后,取液面下 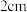 处清液测定氨氮质量浓度。
处清液测定氨氮质量浓度。①生成磷酸铵镁沉淀的离子反应方程式为
②测得反应
 对氨氮去除率的影响如图1所示,当反应
对氨氮去除率的影响如图1所示,当反应  为9.0时,该沉淀法对氨氮的去除率达到最高,当
为9.0时,该沉淀法对氨氮的去除率达到最高,当  继续增至10.0时,氨氮的去除率下降,结合离子方程式说明去除率下降的原因是
继续增至10.0时,氨氮的去除率下降,结合离子方程式说明去除率下降的原因是
③当
 从9.0降低至7.5。的过程中,水中氨氮的去除率明显降低,沉淀减少的原因是
从9.0降低至7.5。的过程中,水中氨氮的去除率明显降低,沉淀减少的原因是(2)纳米零价铁
 与
与 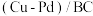 合作用可去除水体中的硝态氮。在
合作用可去除水体中的硝态氮。在  和
和 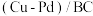 复合材料联合作用的体系中,生物炭
复合材料联合作用的体系中,生物炭 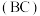 作为
作为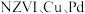 的载体且减少了纳米零价铁的团聚,
的载体且减少了纳米零价铁的团聚, 和
和  作为催化剂且参与吸附活性
作为催化剂且参与吸附活性 
①
 和
和 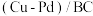 复合材料还原硝酸盐的反应机理如图2所示,
复合材料还原硝酸盐的反应机理如图2所示, 转化为
转化为 或
或  的过程中有两步氧化还原反应,其中第一步的还原剂是
的过程中有两步氧化还原反应,其中第一步的还原剂是
②实验测得体系初始
 对
对 去除率的影响如图3,前
去除率的影响如图3,前 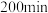 内,
内,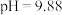 时的去除率远低于
时的去除率远低于  时,其可能的原因是
时,其可能的原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】磷有多种化合物,次磷酸(H3PO2)和次磷酸钠(NaH2PO2)常用作化工生产中的还原剂。
(1)工业上可用白磷(P4)和过量的热NaOH溶液反应生成PH3气体和 NaH2PO2。若反应中转移电子数为3NA,则用去还原剂________ mol,若已知NaH2PO2溶液的pH >7,写出H3PO2电离平衡常数Ka的数学表达式:_________________________ 。
(2)向Ba(H2PO2)2溶液中加入盐酸可制备H3PO2,有人说应该用硫酸代替盐酸,请说明用硫酸代替盐酸的优点:____________ 。
(3)可利用H3PO2把溶液中的Ag+还原为银的反应进行化学镀银,已知该反应中还原剂与氧化剂的物质的量之比为1∶4,则反应的离子方程式为______________________________ 。
(4)利用电解原理制备H3PO2的示意图如图所示(阳离子交换膜、阴离子交换膜分别只允许阳离子、阴离子通过)。已知:阳极反应式为4OH--4e- O2↑+2H2O;阴极反应式为2H++2e-
O2↑+2H2O;阴极反应式为2H++2e- H2↑。试分析在阳极室得到H3PO2的原因:
H2↑。试分析在阳极室得到H3PO2的原因:___________________________ 。

(1)工业上可用白磷(P4)和过量的热NaOH溶液反应生成PH3气体和 NaH2PO2。若反应中转移电子数为3NA,则用去还原剂
(2)向Ba(H2PO2)2溶液中加入盐酸可制备H3PO2,有人说应该用硫酸代替盐酸,请说明用硫酸代替盐酸的优点:
(3)可利用H3PO2把溶液中的Ag+还原为银的反应进行化学镀银,已知该反应中还原剂与氧化剂的物质的量之比为1∶4,则反应的离子方程式为
(4)利用电解原理制备H3PO2的示意图如图所示(阳离子交换膜、阴离子交换膜分别只允许阳离子、阴离子通过)。已知:阳极反应式为4OH--4e-
 O2↑+2H2O;阴极反应式为2H++2e-
O2↑+2H2O;阴极反应式为2H++2e- H2↑。试分析在阳极室得到H3PO2的原因:
H2↑。试分析在阳极室得到H3PO2的原因:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】氮、氧、硫、氯是四种重要的非金属元素,研究它们的性质及用途对生产,生活、科研具有重要意义。
(1)一氯胺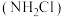 是一种长效缓释水消毒剂,工业上可利用下列反应制备:
是一种长效缓释水消毒剂,工业上可利用下列反应制备: ;一氯胺
;一氯胺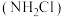 的制备反应中氧化剂是
的制备反应中氧化剂是_______ 氧化产物是_______ 。等质量的 和
和 两种气态产物,同温同体积时的压强比为
两种气态产物,同温同体积时的压强比为_______ 。
(2) 两种气体都能对大气造成污染,需要对其进行吸收处理。用氨水吸收
两种气体都能对大气造成污染,需要对其进行吸收处理。用氨水吸收 能得到含
能得到含 和
和 的吸收液,写出生成
的吸收液,写出生成 的离子方程式:
的离子方程式:_______ 。若向吸收液中通入过量 ,
, 能与
能与 发生反应生成
发生反应生成 和
和 ,此反应中氧化剂与还原剂的物质的量之比为
,此反应中氧化剂与还原剂的物质的量之比为_______ 。
(3) 与
与 溶液反应可制取“84”消毒液。用过量的冷
溶液反应可制取“84”消毒液。用过量的冷 溶液吸收氯气,制得
溶液吸收氯气,制得 溶液(不含
溶液(不含 ),此时
),此时 的浓度为
的浓度为 ;加热时
;加热时 能转化为
能转化为 ,测得t时刻溶液中
,测得t时刻溶液中 的浓度为
的浓度为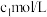 (不考虑加热前后溶液体积的变化)。
(不考虑加热前后溶液体积的变化)。
①写出溶液中 分解生成
分解生成 的化学方程式:
的化学方程式:_______ 。
②t时刻溶液中
_______  (用含
(用含 的代数式表示)。
的代数式表示)。
(1)一氯胺
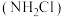 是一种长效缓释水消毒剂,工业上可利用下列反应制备:
是一种长效缓释水消毒剂,工业上可利用下列反应制备: ;一氯胺
;一氯胺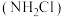 的制备反应中氧化剂是
的制备反应中氧化剂是 和
和 两种气态产物,同温同体积时的压强比为
两种气态产物,同温同体积时的压强比为(2)
 两种气体都能对大气造成污染,需要对其进行吸收处理。用氨水吸收
两种气体都能对大气造成污染,需要对其进行吸收处理。用氨水吸收 能得到含
能得到含 和
和 的吸收液,写出生成
的吸收液,写出生成 的离子方程式:
的离子方程式: ,
, 能与
能与 发生反应生成
发生反应生成 和
和 ,此反应中氧化剂与还原剂的物质的量之比为
,此反应中氧化剂与还原剂的物质的量之比为(3)
 与
与 溶液反应可制取“84”消毒液。用过量的冷
溶液反应可制取“84”消毒液。用过量的冷 溶液吸收氯气,制得
溶液吸收氯气,制得 溶液(不含
溶液(不含 ),此时
),此时 的浓度为
的浓度为 ;加热时
;加热时 能转化为
能转化为 ,测得t时刻溶液中
,测得t时刻溶液中 的浓度为
的浓度为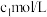 (不考虑加热前后溶液体积的变化)。
(不考虑加热前后溶液体积的变化)。①写出溶液中
 分解生成
分解生成 的化学方程式:
的化学方程式:②t时刻溶液中

 (用含
(用含 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箱,制造印刷电路板。
(1)写出FeCl3溶液与金属铜发生反应的化学方程式:___ 。
(2)某工程师为了从使用过的腐蚀废液中回收铜,并重新获得FeCl3溶液,向废液中先加入过量铁粉,过滤后再向溶液中通入___ (化学式),请写出相关反应的离子方程式___ 、___ 、______ 。
(1)写出FeCl3溶液与金属铜发生反应的化学方程式:
(2)某工程师为了从使用过的腐蚀废液中回收铜,并重新获得FeCl3溶液,向废液中先加入过量铁粉,过滤后再向溶液中通入
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】工业制备氯化铜时,将浓盐酸用蒸气加热到80℃左右,慢慢加入粗CuO粉末(含杂质Fe2O3、FeO)充分搅拌使之溶解,得一强酸性的混合溶液,现欲从该混合溶液中制备纯净的CuCl2溶液[参考数据:pH≥9.6时,Fe2+完全水解成Fe(OH)2;pH≥6.4时,Cu2+完全水解成Cu(OH)2;pH≥3.7时,Fe3+完全水解成Fe(OH)3]。请回答以下问题:
(1)第一步除Fe2+,能否直接调整pH=9.6将Fe2+沉淀除去?_______ ,理由是_______________ 。
有人用强氧化剂NaClO将Fe2+氧化为Fe3+:
①加入NaClO后,溶液的pH变化是_______ (填序号);
A.一定增大 B.一定减小
C.可能增大 D.可能减小
②你认为用NaClO作氧化剂是否妥当?_______ ,理由是___________________ 。
③现有下列几种常用的氧化剂,可用于除去该混合溶液中Fe2+的有_______ (填序号)。
A.浓HNO3 B.Cl2 C.KMnO4 d.H2O2
(2)除去溶液中的Fe3+的方法是调整溶液的pH=3.7,现有下列试剂均可以使强酸性溶液的pH调整到3.7,可选用的有________ (填序号)。
A.NaOH B.氨水 C.Cu2(OH)2CO3 D.Na2CO3
(1)第一步除Fe2+,能否直接调整pH=9.6将Fe2+沉淀除去?
有人用强氧化剂NaClO将Fe2+氧化为Fe3+:
①加入NaClO后,溶液的pH变化是
A.一定增大 B.一定减小
C.可能增大 D.可能减小
②你认为用NaClO作氧化剂是否妥当?
③现有下列几种常用的氧化剂,可用于除去该混合溶液中Fe2+的有
A.浓HNO3 B.Cl2 C.KMnO4 d.H2O2
(2)除去溶液中的Fe3+的方法是调整溶液的pH=3.7,现有下列试剂均可以使强酸性溶液的pH调整到3.7,可选用的有
A.NaOH B.氨水 C.Cu2(OH)2CO3 D.Na2CO3
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】按要求回答下列问题
(1)国家质检部门检出人们端午节包粽子的“返青粽叶”多以胆矾为添加剂,长期食用有害健康。请写出胆矾的化学式___________ 。
(2)次磷酸(H3PO2)是磷的一种含氧酸,与足量NaOH溶液反应生成NaH2PO2,在工业上可做还原剂。
①NaH2PO2属于___________ (选填“正盐”或“酸式盐”)
②请从化合价的角度解释H3PO2可做还原剂的原因___________ 。
(3)钠与水反应的离子方程式是___________ 。
(4)用化学方程式解释新制氯水光照一段时间后,pH减小的原因___________ 。
(5)向FeSO4溶液中滴加NaOH溶液,观察到的现象是___________ 。
(6)打印机使用的墨粉中含有Fe3O4.它的一种制备方法是:将FeSO4溶液、Fe2(SO4)3溶液按一定比例混合,再加入一定量的NaOH溶液,水浴加热。反应如下:
___Fe2++_____Fe3++___OH—=__Fe3O4+____H2O
请配平上述反应___________ 。
(1)国家质检部门检出人们端午节包粽子的“返青粽叶”多以胆矾为添加剂,长期食用有害健康。请写出胆矾的化学式
(2)次磷酸(H3PO2)是磷的一种含氧酸,与足量NaOH溶液反应生成NaH2PO2,在工业上可做还原剂。
①NaH2PO2属于
②请从化合价的角度解释H3PO2可做还原剂的原因
(3)钠与水反应的离子方程式是
(4)用化学方程式解释新制氯水光照一段时间后,pH减小的原因
(5)向FeSO4溶液中滴加NaOH溶液,观察到的现象是
(6)打印机使用的墨粉中含有Fe3O4.它的一种制备方法是:将FeSO4溶液、Fe2(SO4)3溶液按一定比例混合,再加入一定量的NaOH溶液,水浴加热。反应如下:
___Fe2++_____Fe3++___OH—=__Fe3O4+____H2O
请配平上述反应
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】“垃圾是放错了位置的资源”,应该分类回收。某化学兴趣小组拟采用如下处理方法回收废电池中的资源。
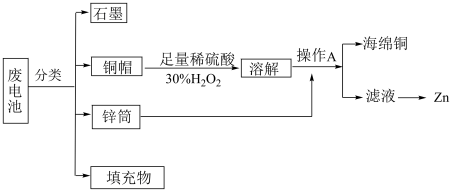
(1)碱性锌锰干电池的电解质为KOH,总反应为Zn+2MnO2+2H2O═2MnOOH+Zn(OH)2, 其正极的电极反应式为_____________________________________________ 。
(2)操作A的名称为____________________ 。
(3)铜帽溶解时加入H2O2的目的是___________________ (用化学方程式表示)。铜帽溶解完全后,可采用________ 方法除去溶液中过量的H2O2。
(4)填充物中可以回收得到氯化铵,写出氯化铵溶液中各离子浓度的大小顺序_________________________________ 。
(5)铜器在潮湿环境中发生的电化学腐蚀如图所示:

①负极反应的电极反应式________________________ 。
②环境中的Cl﹣扩散到孔口,并与正极反应产物和负极产物作用生成多孔粉状锈Cu2(OH)3Cl,其若生成4.29g Cu2(OH)3Cl,则理论上耗氧气体积为________ L(标准状况)。

(1)碱性锌锰干电池的电解质为KOH,总反应为Zn+2MnO2+2H2O═2MnOOH+Zn(OH)2, 其正极的电极反应式为
(2)操作A的名称为
(3)铜帽溶解时加入H2O2的目的是
(4)填充物中可以回收得到氯化铵,写出氯化铵溶液中各离子浓度的大小顺序
(5)铜器在潮湿环境中发生的电化学腐蚀如图所示:

①负极反应的电极反应式
②环境中的Cl﹣扩散到孔口,并与正极反应产物和负极产物作用生成多孔粉状锈Cu2(OH)3Cl,其若生成4.29g Cu2(OH)3Cl,则理论上耗氧气体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】硫酸亚铁晶体(FeSO4·7H2O)在医药上作补血剂。为测定补血剂中铁元素的含量,某化学兴趣小组设计了两套实验方案。
方案一(滴定法):用酸性KMnO4溶液滴定,测定铁元素的含量
(1)写出该滴定反应的离子方程式:___________ 。
(2)实验前,首先要精确配制一定物质的量浓度的KMnO4溶液250mL,配制时需要的仪器除天平、药匙、烧杯、胶头滴管外,还需___________ (填仪器名称)。
在溶液配制过程中,下列操作会导致配制结果偏低的是___________ (填序号)。
A.定容时,俯视容量瓶刻度线
B.容量瓶在使用前内有少量蒸馏水
C.转移溶液后的烧杯、玻璃棒未洗涤
D.定容后摇匀,发现液面降低,又补加少量水,重新达到刻度线
(3)上述实验中KMnO4溶液需要酸化,用于酸化的酸是______(填序号)。
方案二(称量法):操作流程如下:
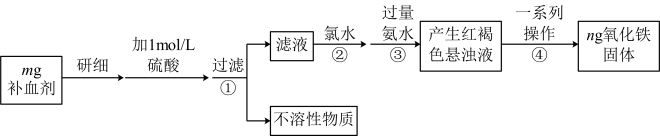
(4)步骤④一系列操作依次是:过滤、洗涤、______ 、冷却、称量。
(5)假设实验无损耗,则该补血剂含铁元素的质量分数为_____ 。(用含m、n的代数式表示)
方案一(滴定法):用酸性KMnO4溶液滴定,测定铁元素的含量
(1)写出该滴定反应的离子方程式:
(2)实验前,首先要精确配制一定物质的量浓度的KMnO4溶液250mL,配制时需要的仪器除天平、药匙、烧杯、胶头滴管外,还需
在溶液配制过程中,下列操作会导致配制结果偏低的是
A.定容时,俯视容量瓶刻度线
B.容量瓶在使用前内有少量蒸馏水
C.转移溶液后的烧杯、玻璃棒未洗涤
D.定容后摇匀,发现液面降低,又补加少量水,重新达到刻度线
(3)上述实验中KMnO4溶液需要酸化,用于酸化的酸是______(填序号)。
| A.浓盐酸 | B.稀硫酸 | C.稀硝酸 | D.浓硫酸 |
方案二(称量法):操作流程如下:

(4)步骤④一系列操作依次是:过滤、洗涤、
(5)假设实验无损耗,则该补血剂含铁元素的质量分数为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】镁铝尖晶石(MgAl2O4)常做耐火材料。共沉淀制备尖晶石的方法是:用AlCl3和MgCl2的混合溶液(用a表示)与过量的氨水(用b表示)反应,再将得到的沉淀高温焙烧。完成下列填空:
(1)为使Mg2+、Al3+同时生成沉淀,应该把_____ (填“a”或“b”)滴入另一溶液中。
(2)将上述制备反应中部分元素的简单离子:Al3+、Cl–、Mg2+、H+、O2–按半径由大到小的顺序排列
______________________ (用离子符号表示)。
(3)AlCl3与氨水反应的反应物和生成物中,属于离子化合物的电子式是_________ ,属于难溶物的电离方程式_____________________________ 。
(4)不能说明氧元素的非金属性比氮元素强的事实是_________ 。
a. H2O比NH3稳定 b. 共用电子对偏向:H-O>H-N
c. 沸点:H2O>NH3 d. NO中氮是+2价,氧是-2价
(1)为使Mg2+、Al3+同时生成沉淀,应该把
(2)将上述制备反应中部分元素的简单离子:Al3+、Cl–、Mg2+、H+、O2–按半径由大到小的顺序排列
(3)AlCl3与氨水反应的反应物和生成物中,属于离子化合物的电子式是
(4)不能说明氧元素的非金属性比氮元素强的事实是
a. H2O比NH3稳定 b. 共用电子对偏向:H-O>H-N
c. 沸点:H2O>NH3 d. NO中氮是+2价,氧是-2价
您最近一年使用:0次



