某化学学习小组为测定草酸晶体的纯度,用托盘天平称取草酸晶体(H2C2O4•2H2O)样品wg;配制成250mL溶液;每次移取25.00mL该溶液于锥形瓶中,用0.10mol/L酸性高锰酸钾溶液滴定;滴定实验重复操作2-3次。已知:①MnO 在酸性环境下的还原产物是Mn2+;②草酸是二元弱酸。
在酸性环境下的还原产物是Mn2+;②草酸是二元弱酸。
(1)上述H2C2O4溶液与酸性KMnO4溶液反应的离子方程式为___________
(2)滴定时,将酸性KMnO4标准液装在如图中的___________ (填“甲”或“乙”)滴定管中;若滴定开始和结束时,滴定管中的液面如图所示,则所用酸性KMnO4标准液的体积为___________ 。


(3)滴定终点的现象为___________
(4)若滴定过程中平均消耗酸性高锰酸钾溶液VmL,则草酸晶体的纯度为___________ (用含w、V的表达式表示)
(5)下列操作中可能使所测草酸晶体纯度偏低的是___________(填字母)。
 在酸性环境下的还原产物是Mn2+;②草酸是二元弱酸。
在酸性环境下的还原产物是Mn2+;②草酸是二元弱酸。(1)上述H2C2O4溶液与酸性KMnO4溶液反应的离子方程式为
(2)滴定时,将酸性KMnO4标准液装在如图中的


(3)滴定终点的现象为
(4)若滴定过程中平均消耗酸性高锰酸钾溶液VmL,则草酸晶体的纯度为
(5)下列操作中可能使所测草酸晶体纯度偏低的是___________(填字母)。
| A.滴定管未用标准液润洗就直接注入KMnO4标准液 |
| B.读取KMnO4标准液时,开始仰视读数,滴定结束时俯视读数 |
| C.滴定管尖嘴部分在滴定前没有气泡,滴定后有气泡 |
| D.滴定前盛放草酸溶液的锥形瓶用蒸馏水洗净后没有干燥 |
更新时间:2024-01-29 14:25:36
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】滴定法测定市售白醋(主要成分是CH3COOH)的总酸量(g·(100 mL)-1)。
Ⅰ.实验步骤:
(1)取10.00 mL食用白醋,在烧杯中用水稀释后转移到100mL_______ (填仪器名称)中定容,摇匀即得待测白醋溶液。
(2)用_______ 取待测白醋溶液20.00 mL于锥形瓶中。
(3)滴加2滴_______ 作指示剂。
(4)滴定,用0.1000mol·L-1 NaOH滴定,当_______ 时,停止滴定,并记录NaOH溶液的终读数。重复滴定3次。
Ⅱ.实验记录
Ⅲ.数据处理与讨论:
(5)据上述数据c(市售白醋)=_______ mol·L-1,市售白醋总酸度_______ g·100mL-1。
(6)在本实验的滴定过程中,下列操作会使实验结果偏小的是_______ (填写序号)。
A.碱式滴定管在滴定时未用标准NaOH溶液润洗
B.碱式滴定管的尖嘴在滴定前有气泡,滴定后气泡消失
C.锥形瓶中加入待测白醋溶液后,再加少量水
D.锥形瓶在滴定时剧烈摇动,有少量液体溅出
E.滴定终点读数时俯视
(7)医学上常用酸性KMnO4溶液和草酸(H2C2O4)溶液反应来测血液中血钙的含量。测定方法是取2mL血液用蒸馏水稀释后,向其中加入足量的(NH4)2C2O4溶液,反应生成CaC2O4沉淀,将沉淀用稀硫酸溶解得到H2C2O4后,再用KMnO4溶液滴定。
①溶解沉淀时_______ (填“能”或“不能”)用稀盐酸,原因是_______
②滴定过程中发生反应的离子方程式为_______
③若上述滴定中消耗了1.0×10-4mol·L-1 KMnO4的溶液20 mL,则200 mL该血液中含钙_______ g。
Ⅰ.实验步骤:
(1)取10.00 mL食用白醋,在烧杯中用水稀释后转移到100mL
(2)用
(3)滴加2滴
(4)滴定,用0.1000mol·L-1 NaOH滴定,当
Ⅱ.实验记录
滴定次数 实验数据(mL) | 1 | 2 | 3 | 4 |
| V(样品) | 20.00 | 20.00 | 20.00 | 20.00 |
| V(NaOH)(消耗) | 15.95 | 15.00 | 15.05 | 14.95 |
(5)据上述数据c(市售白醋)=
(6)在本实验的滴定过程中,下列操作会使实验结果偏小的是
A.碱式滴定管在滴定时未用标准NaOH溶液润洗
B.碱式滴定管的尖嘴在滴定前有气泡,滴定后气泡消失
C.锥形瓶中加入待测白醋溶液后,再加少量水
D.锥形瓶在滴定时剧烈摇动,有少量液体溅出
E.滴定终点读数时俯视
(7)医学上常用酸性KMnO4溶液和草酸(H2C2O4)溶液反应来测血液中血钙的含量。测定方法是取2mL血液用蒸馏水稀释后,向其中加入足量的(NH4)2C2O4溶液,反应生成CaC2O4沉淀,将沉淀用稀硫酸溶解得到H2C2O4后,再用KMnO4溶液滴定。
①溶解沉淀时
②滴定过程中发生反应的离子方程式为
③若上述滴定中消耗了1.0×10-4mol·L-1 KMnO4的溶液20 mL,则200 mL该血液中含钙
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】“84”消毒液是一种以次氯酸( )为有效成分的高效消毒剂,它的灭菌消毒能力用有效氯(
)为有效成分的高效消毒剂,它的灭菌消毒能力用有效氯( 与
与 的总量)来衡量,有效氯含量越高,消毒能力越强。间接碘量法是测定有效氯的经典方法,实验步骤如下:
的总量)来衡量,有效氯含量越高,消毒能力越强。间接碘量法是测定有效氯的经典方法,实验步骤如下:
i.取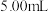 “84”消毒液,置于磨口具塞锥形瓶中,加入
“84”消毒液,置于磨口具塞锥形瓶中,加入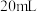 碘化钾溶液(过量,易被空气氧化)和适量稀硫酸,塞上瓶塞;在暗处振荡5分钟。
碘化钾溶液(过量,易被空气氧化)和适量稀硫酸,塞上瓶塞;在暗处振荡5分钟。
ii.加入几滴指示剂,用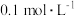 硫代硫酸钠(
硫代硫酸钠( )标准溶液(
)标准溶液(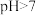 )滴定至终点,记下消耗硫代硫酸钠标准溶液的体积,平行测定四次。
)滴定至终点,记下消耗硫代硫酸钠标准溶液的体积,平行测定四次。
已知:①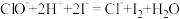 ;
;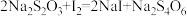 。
。
②实验所得数据如表所示:
回答下列问题:
(1)使用磨口具塞锥形瓶的原因是___________ ;使用硫酸而不使用盐酸酸化的原因是___________ 。
(2)滴定时,盛装标准液的滴定管在使用前需要___________ ,水洗之后需要进行的操作是___________ ,在滴定管中装入标准溶液后,要先赶出滴定管尖嘴处的气泡,其操作正确的图示为___________ (填标号)。
A.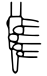 B.
B.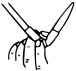 C.
C.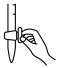 D.
D.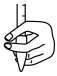
(3)步骤ⅱ选用的指示剂为___________ ,滴定终点的现象为___________ 。
(4)该“84”消毒液中 与
与 的总浓度为
的总浓度为___________  ,测得的结果小于该“84”消毒液标签上的浓度,可能原因为
,测得的结果小于该“84”消毒液标签上的浓度,可能原因为___________ (填标号)。
a.滴定终点读数时仰视刻度线 b.该“84”消毒液在光照下放置时间过长
c.滴定振荡时,有少量待测液溅出 d.滴定前,盛装标准溶液的滴定管下端有气泡未赶出
 )为有效成分的高效消毒剂,它的灭菌消毒能力用有效氯(
)为有效成分的高效消毒剂,它的灭菌消毒能力用有效氯( 与
与 的总量)来衡量,有效氯含量越高,消毒能力越强。间接碘量法是测定有效氯的经典方法,实验步骤如下:
的总量)来衡量,有效氯含量越高,消毒能力越强。间接碘量法是测定有效氯的经典方法,实验步骤如下:i.取
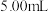 “84”消毒液,置于磨口具塞锥形瓶中,加入
“84”消毒液,置于磨口具塞锥形瓶中,加入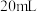 碘化钾溶液(过量,易被空气氧化)和适量稀硫酸,塞上瓶塞;在暗处振荡5分钟。
碘化钾溶液(过量,易被空气氧化)和适量稀硫酸,塞上瓶塞;在暗处振荡5分钟。ii.加入几滴指示剂,用
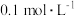 硫代硫酸钠(
硫代硫酸钠( )标准溶液(
)标准溶液(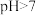 )滴定至终点,记下消耗硫代硫酸钠标准溶液的体积,平行测定四次。
)滴定至终点,记下消耗硫代硫酸钠标准溶液的体积,平行测定四次。已知:①
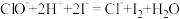 ;
;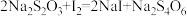 。
。②实验所得数据如表所示:
| 实验次数 | 1 | 2 | 3 | 4 |
标准溶液初始读数/ | 0.00 | 0.10 | 4.40 | 0.50 |
滴定终点时标准溶液读数/ | 31.80 | 31.95 | 31.95 | 32.25 |
(1)使用磨口具塞锥形瓶的原因是
(2)滴定时,盛装标准液的滴定管在使用前需要
A.
 B.
B. C.
C. D.
D.
(3)步骤ⅱ选用的指示剂为
(4)该“84”消毒液中
 与
与 的总浓度为
的总浓度为 ,测得的结果小于该“84”消毒液标签上的浓度,可能原因为
,测得的结果小于该“84”消毒液标签上的浓度,可能原因为a.滴定终点读数时仰视刻度线 b.该“84”消毒液在光照下放置时间过长
c.滴定振荡时,有少量待测液溅出 d.滴定前,盛装标准溶液的滴定管下端有气泡未赶出
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】含氯消毒剂家族庞大、应用广泛, 、
、 、“84”消毒液等都是常见的含氯消毒剂。
、“84”消毒液等都是常见的含氯消毒剂。
(1)① 可用于自来水的消毒、杀菌。
可用于自来水的消毒、杀菌。 与水反应的化学方程式为
与水反应的化学方程式为_______ 。
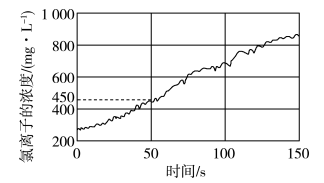
②对新制氯水进行光照并连接氯离子传感器,实验结果如图所示。 浓度变化的原因是
浓度变化的原因是_______ (用离子方程式表示);50s时,氯水中 为
为_______  (保留两位有效数字)。
(保留两位有效数字)。
(2)已知某“84”消毒液瓶体部分标签如图所示,某同学欲使用480mL该消毒液,故用NaClO固体配制该消毒液。
①配制过程中使用的玻璃仪器有烧杯、量筒、玻璃棒、胶头滴管、_______ 。
②需要用托盘天平称量NaClO固体的质量为_______ (保留三位有效数字)。
(3)①一种制备 的反应原理为
的反应原理为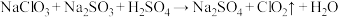 (未配平),配平方程式并用双线桥法标出该反应中电子转移的方向和数目:
(未配平),配平方程式并用双线桥法标出该反应中电子转移的方向和数目:_______ 。
②为测定某 水溶液的浓度,进行以下实验操作:取该待测
水溶液的浓度,进行以下实验操作:取该待测 溶液20.00mL于锥形瓶中,用稀硫酸调节溶液呈酸性,加入足量KI晶体充分反应,再逐滴加入
溶液20.00mL于锥形瓶中,用稀硫酸调节溶液呈酸性,加入足量KI晶体充分反应,再逐滴加入 溶液,恰好完全反应时,消耗
溶液,恰好完全反应时,消耗 溶液10.00mL。
溶液10.00mL。
上述过程中发生反应: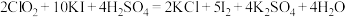 、
、 。
。
该溶液中 的物质的量浓度为
的物质的量浓度为_______ 。若加入KI晶体后在空气中放置时间过长,会导致测得的 浓度
浓度_______ (填“偏高”“偏低”或“无影响”)。
 、
、 、“84”消毒液等都是常见的含氯消毒剂。
、“84”消毒液等都是常见的含氯消毒剂。(1)①
 可用于自来水的消毒、杀菌。
可用于自来水的消毒、杀菌。 与水反应的化学方程式为
与水反应的化学方程式为②对新制氯水进行光照并连接氯离子传感器,实验结果如图所示。
 浓度变化的原因是
浓度变化的原因是 为
为 (保留两位有效数字)。
(保留两位有效数字)。
(2)已知某“84”消毒液瓶体部分标签如图所示,某同学欲使用480mL该消毒液,故用NaClO固体配制该消毒液。
| “84”消毒液 有效成分:NaClO (相对分子质量:74.5) 质量分数:12.5% 密度:  |
②需要用托盘天平称量NaClO固体的质量为
(3)①一种制备
 的反应原理为
的反应原理为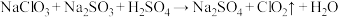 (未配平),配平方程式并用双线桥法标出该反应中电子转移的方向和数目:
(未配平),配平方程式并用双线桥法标出该反应中电子转移的方向和数目:②为测定某
 水溶液的浓度,进行以下实验操作:取该待测
水溶液的浓度,进行以下实验操作:取该待测 溶液20.00mL于锥形瓶中,用稀硫酸调节溶液呈酸性,加入足量KI晶体充分反应,再逐滴加入
溶液20.00mL于锥形瓶中,用稀硫酸调节溶液呈酸性,加入足量KI晶体充分反应,再逐滴加入 溶液,恰好完全反应时,消耗
溶液,恰好完全反应时,消耗 溶液10.00mL。
溶液10.00mL。上述过程中发生反应:
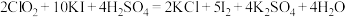 、
、 。
。该溶液中
 的物质的量浓度为
的物质的量浓度为 浓度
浓度
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】硫酸亚铁铵 为浅绿色晶体,实验室中常以废铁屑为原料来制备,其步骤如下:
为浅绿色晶体,实验室中常以废铁屑为原料来制备,其步骤如下:

请回答下列问题:
Ⅰ、(1)在步骤1中,10% 溶液作用是
溶液作用是____________________________ ;
(2)在步骤3中“趁热过滤”的目的是_________________________ ;
(3)当加热浓缩至_______________________ 时,停止加热 ;
(4)抽滤装置如图所示,仪器B的名称是_________________ 。仪器C的作用是______________ 。

(5)过滤晶体后用少量无水乙醇洗涤,目的是__________________________ 。
Ⅱ、称取两份质量均为1.96g的该硫酸亚铁铵,制成溶液。用未知浓度的 酸性溶液进行滴定。
酸性溶液进行滴定。
(1)滴定前排气泡时,应选择图中的_______ 。

(2)已知 被还原为
被还原为 ,试写出该滴定过程中的离子方程式:
,试写出该滴定过程中的离子方程式:___________________ ;
(3)判断该反应到达滴定终点的现象_________________________ ;
(4)假设到达滴定终点时,用去V mL 酸性溶液,则该
酸性溶液,则该 酸性溶液浓度为
酸性溶液浓度为_______  。
。
 为浅绿色晶体,实验室中常以废铁屑为原料来制备,其步骤如下:
为浅绿色晶体,实验室中常以废铁屑为原料来制备,其步骤如下:
请回答下列问题:
Ⅰ、(1)在步骤1中,10%
 溶液作用是
溶液作用是(2)在步骤3中“趁热过滤”的目的是
(3)当加热浓缩至
(4)抽滤装置如图所示,仪器B的名称是

(5)过滤晶体后用少量无水乙醇洗涤,目的是
Ⅱ、称取两份质量均为1.96g的该硫酸亚铁铵,制成溶液。用未知浓度的
 酸性溶液进行滴定。
酸性溶液进行滴定。(1)滴定前排气泡时,应选择图中的

(2)已知
 被还原为
被还原为 ,试写出该滴定过程中的离子方程式:
,试写出该滴定过程中的离子方程式:(3)判断该反应到达滴定终点的现象
(4)假设到达滴定终点时,用去V mL
 酸性溶液,则该
酸性溶液,则该 酸性溶液浓度为
酸性溶液浓度为 。
。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】(一)用碳酸钠粉末配制0.2000 mol·L-1Na2CO3溶液0.5L
(1)需选用的玻璃仪器或用品________________________ (填字母编号)
B、0.5L平底烧瓶 C、0.5L容量瓶 D、0.5L圆底烧瓶 E、烧杯 F、试管 G、胶头滴管 H、量筒 I、托盘天平 J、药匙 M、滤纸 N、玻璃棒
(2)应称取_________ g 碳酸钠粉末来溶于水
(二)用0.2000 mol·L-1Na2CO3溶液标定未知浓度的盐酸
(1)把0.2000 mol·L-1Na2CO3溶液装入_______ (酸式,碱式)滴定管中。从此滴定管中放出20.00mL0.2000 mol·L-1Na2CO3溶液入锥形瓶中,滴2至3滴甲基橙作指示剂,用未知浓度的盐酸来滴定0.2000 mol·L-1Na2CO3溶液,根据________ 判断滴定终点达到。
(2)终点达到时,用去盐酸16.00mL(三次的平均值),则盐酸c(HCl)=_________
(三)中和热的测定
用(二)实验中标定好浓度的盐酸50.0mL与0.55mol·L-1NaOH 50.0mL反应做中和热的测定实验。每次用量均一样,三次实验测得温度升高的平均值为3.41℃,则实验测得中和热△H=____________ (混合后溶液的比热容C = 4.18J·℃-1·g-1),实验测得中和热比理论______ (偏高,相等,偏低)
(1)需选用的玻璃仪器或用品
B、0.5L平底烧瓶 C、0.5L容量瓶 D、0.5L圆底烧瓶 E、烧杯 F、试管 G、胶头滴管 H、量筒 I、托盘天平 J、药匙 M、滤纸 N、玻璃棒
(2)应称取
(二)用0.2000 mol·L-1Na2CO3溶液标定未知浓度的盐酸
(1)把0.2000 mol·L-1Na2CO3溶液装入
(2)终点达到时,用去盐酸16.00mL(三次的平均值),则盐酸c(HCl)=
(三)中和热的测定
用(二)实验中标定好浓度的盐酸50.0mL与0.55mol·L-1NaOH 50.0mL反应做中和热的测定实验。每次用量均一样,三次实验测得温度升高的平均值为3.41℃,则实验测得中和热△H=
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】I.用中和滴定法测定某烧碱的纯度,试根据实验回答:
(1)称取4.1g烧碱样品。将样品配成250mL待测液,需要的主要玻璃仪器除烧杯、玻璃棒外还需____ 。
(2)取10.00mL待测液,用___________ 量取。
(3)用0.2000mol/L标准盐酸滴定待测烧碱溶液,以酚酞为指示剂,滴定终点的现象是___________ 。
(4)根据表中数据,计算样品烧碱的质量分数为___________ (结果保留四位有效数字)。
(5)滴定过程,下列情况会使测定结果偏高的是___________ (填序号)。
① 记录酸式滴定管起始体积时,仰视读数,终点时俯视
② 碱式滴定管水洗后就用来量取待测液
③ 滴定前,酸式滴定管有气泡,滴定后消失
④ 取待测液时滴定过快成细流、将碱液溅到锥形瓶壁而又未摇匀洗下
II. 在常温时,几种酸的电离平衡常数(Ka)如下:
(6)向NaClO溶液中通入少量CO2的离子方程式为 ___________ 。
(7)向10mL0.1 mol·L-1的Na2CO3溶液中滴加5mL0.1mol/LHCl溶液,溶液中离子的浓度由大到小的顺序为___________ 。
(8)室温下pH均为5的CH3COOH、NH4Cl溶液中由水电离产生的c(H+)的比值为___________ 。
(1)称取4.1g烧碱样品。将样品配成250mL待测液,需要的主要玻璃仪器除烧杯、玻璃棒外还需
(2)取10.00mL待测液,用
(3)用0.2000mol/L标准盐酸滴定待测烧碱溶液,以酚酞为指示剂,滴定终点的现象是
(4)根据表中数据,计算样品烧碱的质量分数为
| 滴定次数 | 待测液体积(mL) | 标准盐酸体积(mL) | |
| 滴定前读数(mL) | 滴定后读数(mL) | ||
| 第一次 | 10.00 | 0.50 | 20.40 |
| 第二次 | 10.00 | 4.00 | 24.10 |
| 第三次 | 10.00 | 5.12 | 28.02 |
① 记录酸式滴定管起始体积时,仰视读数,终点时俯视
② 碱式滴定管水洗后就用来量取待测液
③ 滴定前,酸式滴定管有气泡,滴定后消失
④ 取待测液时滴定过快成细流、将碱液溅到锥形瓶壁而又未摇匀洗下
II. 在常温时,几种酸的电离平衡常数(Ka)如下:
| 溶质 | CH3COOH | H2CO3 | HClO |
| Ka | 2×10-5 | Ka1=4.3×10-7 Ka2=5.6×10-11 | 3×10-8 |
(7)向10mL0.1 mol·L-1的Na2CO3溶液中滴加5mL0.1mol/LHCl溶液,溶液中离子的浓度由大到小的顺序为
(8)室温下pH均为5的CH3COOH、NH4Cl溶液中由水电离产生的c(H+)的比值为
您最近一年使用:0次



