一氧化二氯(Cl2O)是一种氯化剂和氧化剂,极易溶于水,与水反应生成HClO,遇有机物易燃烧或爆炸,42℃以上易分解。制备出的Cl2O要冷却成固体才便于操作和保存,制取少量的Cl2O是用干燥的氧化汞和氯气反应:2HgO+2Cl2=Cl2O+HgCl2·HgO(反应放热)。某化学兴趣小组设计如图装置以制备Cl2O(支撑、加热及夹持装置已省略)。
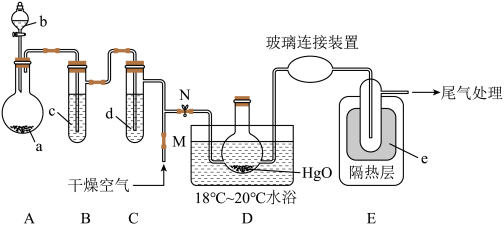
已知:①a中固体试剂是MnO2,b中试剂是浓盐酸。
②有关物质的熔沸点如下表。
请回答:
(1)仪器b的名称___________ ,B中盛有的液体c应是___________ 。
(2)写出装置A中制备氯气的化学方程式___________ 。
(3)待装置A不再产生氯气后,M处通入干燥空气的作用是___________ 。
(4)装置中D的水浴温度应控制在18℃~20℃原因之一是:温度过低反应太慢不利于制备,另一个原因是:___________ 。
(5)E中的保温瓶中盛有液态制冷剂e是___________ (在“干冰”“冰水”“液态空气”“液氨”“液氯”中选择一种)
(6)据文献报道,Cl2O的另一种制备方法是利用Cl2与潮湿的Na2CO3反应来制得,同时生成两种盐,写出该反应的化学方程式___________ 。

已知:①a中固体试剂是MnO2,b中试剂是浓盐酸。
②有关物质的熔沸点如下表。
| Cl2O | N2 | O2 | CO2 | NH3 | Cl2 | |
| 熔点 | -120.6℃ | -209.8℃ | -218.4℃ | -78.5℃(升华) | -77.3℃ | -101℃ |
| 沸点 | 3.8℃ | -195.8℃ | -183℃ | -33.35℃ | -34.6℃ |
(1)仪器b的名称
(2)写出装置A中制备氯气的化学方程式
(3)待装置A不再产生氯气后,M处通入干燥空气的作用是
(4)装置中D的水浴温度应控制在18℃~20℃原因之一是:温度过低反应太慢不利于制备,另一个原因是:
(5)E中的保温瓶中盛有液态制冷剂e是
(6)据文献报道,Cl2O的另一种制备方法是利用Cl2与潮湿的Na2CO3反应来制得,同时生成两种盐,写出该反应的化学方程式
更新时间:2024-02-02 14:06:18
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】海水是巨大的资源宝库,利用海水可以提取镁和溴,提取过程如下:

(1)请写出淡化海水的一种方法___________ ,操作①为___________ 。
(2)写出由 制取Mg的化学方程式
制取Mg的化学方程式___________ 。
(3)吹出塔中通入热空气吹出 ,利用了溴的
,利用了溴的___________ 性。提取溴的过程中,经过2次 转化的目的是
转化的目的是___________ 。
(4)吸收塔中发生反应的离子方程式为________ 。
(5)下列有关海水综合利用的说法不正确的是________ (填字母)。
A.海水提镁流程中, 可循环使用,用于制备盐酸,再溶解
可循环使用,用于制备盐酸,再溶解
B.海水提镁流程中,石灰乳可以通过煅烧贝壳后加水得到
C.电解海水可以制得金属钠
(6)用上述流程进行海水提溴,将 海水浓缩至1L,最终得到
海水浓缩至1L,最终得到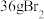 ,若提取率为60%,则原海水中溴的浓度为
,若提取率为60%,则原海水中溴的浓度为___________  。
。

(1)请写出淡化海水的一种方法
(2)写出由
 制取Mg的化学方程式
制取Mg的化学方程式(3)吹出塔中通入热空气吹出
 ,利用了溴的
,利用了溴的 转化的目的是
转化的目的是(4)吸收塔中发生反应的离子方程式为
(5)下列有关海水综合利用的说法不正确的是
A.海水提镁流程中,
 可循环使用,用于制备盐酸,再溶解
可循环使用,用于制备盐酸,再溶解
B.海水提镁流程中,石灰乳可以通过煅烧贝壳后加水得到
C.电解海水可以制得金属钠
(6)用上述流程进行海水提溴,将
 海水浓缩至1L,最终得到
海水浓缩至1L,最终得到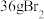 ,若提取率为60%,则原海水中溴的浓度为
,若提取率为60%,则原海水中溴的浓度为 。
。
您最近一年使用:0次
【推荐2】铅的单质、氧化物、盐在现代工业中有着重要用途。
(1)铅能形成多种氧化物,如碱性氧化物PbO、酸性氧化物PbO2、类似Fe3O4的Pb3O4,盛有PbO2的圆底烧瓶中滴加浓盐酸,产生黄绿色气体,其反应的化学方程式为__ 。
(2)以废旧铅酸电池中的含铅废料(Pb、PbO、PbO2、PbSO4及炭黑等)和H2SO4为原料,制备高纯PbO,实现铅的再生利用。其工作流程如图:
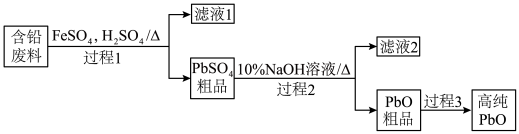
过程1中分离提纯的方法是__ ,滤液2中的溶质主要是_ (填物质的名称)。过程1中,在Fe2+催化下,Pb和PbO2反应生成PbSO4的化学方程式是__ 。
(3)将PbO溶解在HCl和NaCl的混合溶液中,得到含Na2PbCl4的电解液,电解Na2PbCl4溶液生成Pb的装置如图所示。
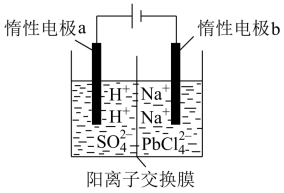
①写出电解时阴极的电极反应式__ 。
②电解过程中,Na2PbCl4电解液浓度不断减小,为了恢复其浓度,应该向__ 极室(填“阴”或者“阳”)加入__ (填化学式)。
(1)铅能形成多种氧化物,如碱性氧化物PbO、酸性氧化物PbO2、类似Fe3O4的Pb3O4,盛有PbO2的圆底烧瓶中滴加浓盐酸,产生黄绿色气体,其反应的化学方程式为
(2)以废旧铅酸电池中的含铅废料(Pb、PbO、PbO2、PbSO4及炭黑等)和H2SO4为原料,制备高纯PbO,实现铅的再生利用。其工作流程如图:

过程1中分离提纯的方法是
(3)将PbO溶解在HCl和NaCl的混合溶液中,得到含Na2PbCl4的电解液,电解Na2PbCl4溶液生成Pb的装置如图所示。

①写出电解时阴极的电极反应式
②电解过程中,Na2PbCl4电解液浓度不断减小,为了恢复其浓度,应该向
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】某科研人员以废镍催化剂(主要成分为 ,另含
,另含 、
、 、
、 、
、 )为原料回收镍,工艺流程如图:
)为原料回收镍,工艺流程如图:
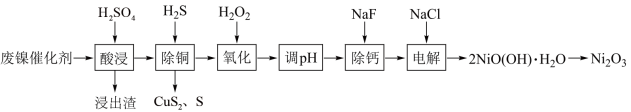
已知:常温下,有关氢氧化物开始沉淀和沉淀完全的 如表:
如表:
回答下列问题:
(1)浸出渣主要成分为___________ (填化学式)。
(2)“氧化”的目的是将溶液中的 氧化为
氧化为 ,温度需控制在
,温度需控制在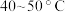 之间,该步骤温度不能太高的原因是
之间,该步骤温度不能太高的原因是___________ 。
(3)“调pH”时,为除去溶液中的铁元素,可向溶液中加入Ni(OH)2试剂来控制pH的范围为___________ 。
(4)“除钙”后,若溶液中 浓度为
浓度为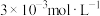 ,则
,则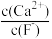 =
=___________ 。[已知常温下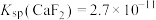 ]
]
(5)高能锂离子电池的总反应为2Li+FeS=Fe+Li2S。用该电池作电源电解含镍酸性废水回收Ni的装置如图(图中X、Y为电极,LiPF6·SO(CH3)2为电解质)。
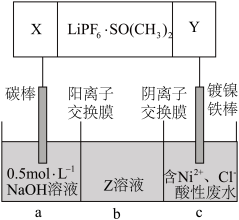
①中间隔室b可以得到的主要物质Z是___________ (填化学式)。
②阳极的电极反应式是___________ 。
 ,另含
,另含 、
、 、
、 、
、 )为原料回收镍,工艺流程如图:
)为原料回收镍,工艺流程如图:
已知:常温下,有关氢氧化物开始沉淀和沉淀完全的
 如表:
如表: |  |  |
| 1.5 | 6.5 | 7.7 |
| 3.7 | 9.7 | 9.2 |
回答下列问题:
(1)浸出渣主要成分为
(2)“氧化”的目的是将溶液中的
 氧化为
氧化为 ,温度需控制在
,温度需控制在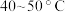 之间,该步骤温度不能太高的原因是
之间,该步骤温度不能太高的原因是(3)“调pH”时,为除去溶液中的铁元素,可向溶液中加入Ni(OH)2试剂来控制pH的范围为
(4)“除钙”后,若溶液中
 浓度为
浓度为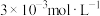 ,则
,则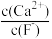 =
=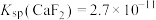 ]
](5)高能锂离子电池的总反应为2Li+FeS=Fe+Li2S。用该电池作电源电解含镍酸性废水回收Ni的装置如图(图中X、Y为电极,LiPF6·SO(CH3)2为电解质)。

①中间隔室b可以得到的主要物质Z是
②阳极的电极反应式是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】氯酸锶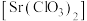 白色结晶粉末,可溶于水,微溶于酒精。它的主要用于制造红色烟火。下图为实验室制取氯酸锶的实验装置图,请回答下列问题:
白色结晶粉末,可溶于水,微溶于酒精。它的主要用于制造红色烟火。下图为实验室制取氯酸锶的实验装置图,请回答下列问题:

(1)仪器b的名称是___________ 。
(2)A中发生反应的离子方程式为___________ 。
(3)装置B中所装试剂名称为:___________ ,其作用是___________ 。
(4)装置C中搅拌的目的是___________ ;发生反应的化学方程式为___________ 。
(5)装置D的作用___________ ;反应一段时间后,可观察到装置D中红色逐渐褪去,某实验小组的同学对红色突然褪去的原因进行猜想:
猜想一:氯水中的酸或氯分子与NaOH发生反应,将NaOH消耗所致
猜想二:氯水中次氯酸的强氧化性,使红色褪去所致。
假如猜想一成立,请设计实验证明该猜想红色褪去的原因:___________ 。
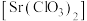 白色结晶粉末,可溶于水,微溶于酒精。它的主要用于制造红色烟火。下图为实验室制取氯酸锶的实验装置图,请回答下列问题:
白色结晶粉末,可溶于水,微溶于酒精。它的主要用于制造红色烟火。下图为实验室制取氯酸锶的实验装置图,请回答下列问题:
(1)仪器b的名称是
(2)A中发生反应的离子方程式为
(3)装置B中所装试剂名称为:
(4)装置C中搅拌的目的是
(5)装置D的作用
猜想一:氯水中的酸或氯分子与NaOH发生反应,将NaOH消耗所致
猜想二:氯水中次氯酸的强氧化性,使红色褪去所致。
假如猜想一成立,请设计实验证明该猜想红色褪去的原因:
您最近一年使用:0次
【推荐2】硫酸镍是一种重要的无机化工产品,广泛用于工业领域。一种以粗制氢氧化镍[主要成分为 ,含有少量
,含有少量 、
、 、
、 等杂质]为原料制备硫酸镍晶体和电积镍的工艺流程如图所示。
等杂质]为原料制备硫酸镍晶体和电积镍的工艺流程如图所示。
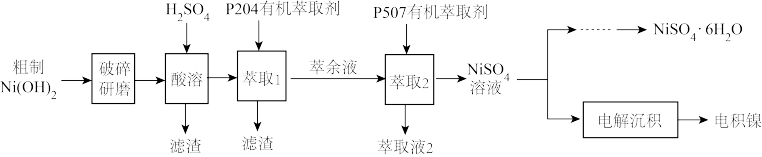
已知:
1.P204萃取剂易萃取 、
、 ;P507萃取剂易萃取
;P507萃取剂易萃取 。
。
2.pH=3.5, 的溶解度随温度升高而增大。
的溶解度随温度升高而增大。
回答下列问题:
(1)“破碎研磨”的目的为_______ 。
(2)“酸溶”时主要成分发生反应的离子方程式为_______ 。
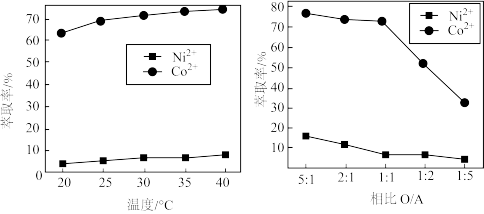
(3)影响P507萃取率的因素有很多,在其他条件相同时,根据下图分析分离镍、钴的最佳条件:温度_______ ;相比(油相O:水相A)_______ 。
(4)由 溶液获得
溶液获得 晶体的操作为
晶体的操作为_______ 。
(5)向“萃取液1、萃取液2”中加入硫酸可进行反萃取是该流程的优点之一,反萃取操作的目的为_______ ;该流程中的优点还有_______ (任写一点)。
(6)电解 溶液的化学方程式为
溶液的化学方程式为_______ 。
 ,含有少量
,含有少量 、
、 、
、 等杂质]为原料制备硫酸镍晶体和电积镍的工艺流程如图所示。
等杂质]为原料制备硫酸镍晶体和电积镍的工艺流程如图所示。
已知:
1.P204萃取剂易萃取
 、
、 ;P507萃取剂易萃取
;P507萃取剂易萃取 。
。2.pH=3.5,
 的溶解度随温度升高而增大。
的溶解度随温度升高而增大。回答下列问题:
(1)“破碎研磨”的目的为
(2)“酸溶”时主要成分发生反应的离子方程式为
(3)影响P507萃取率的因素有很多,在其他条件相同时,根据下图分析分离镍、钴的最佳条件:温度

(4)由
 溶液获得
溶液获得 晶体的操作为
晶体的操作为(5)向“萃取液1、萃取液2”中加入硫酸可进行反萃取是该流程的优点之一,反萃取操作的目的为
(6)电解
 溶液的化学方程式为
溶液的化学方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】高纯锑在光电催化、半导体材料方面有着重要的应用。现以辉锑矿(主要成分为 ,还含有PbS、CuO、
,还含有PbS、CuO、 等)为原料提取锑。
等)为原料提取锑。
①浸出液中主要含过量盐酸和 ,还含有
,还含有 、
、 、
、 等;
等;
②常温下: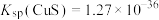 ,
,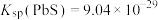 。
。
(1)浸出渣除硫以外,还有___________ 。
(2)“溶浸”时氧化产物是硫, 被氧化的化学方程式为
被氧化的化学方程式为___________ 。
(3)已知:浸出液中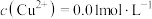 、
、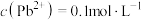 。在沉淀铜、铅过程中,缓慢滴加极稀的硫化钠溶液,先产生的沉淀是
。在沉淀铜、铅过程中,缓慢滴加极稀的硫化钠溶液,先产生的沉淀是___________ (填化学式);所加 不宜过多,其原因为
不宜过多,其原因为___________ 。
(4) 水解的中间产物有难溶于水的SbOCl生成,其对应的化学方程式为
水解的中间产物有难溶于水的SbOCl生成,其对应的化学方程式为___________ ;水解最终产物 的性质与
的性质与 相似,为去除
相似,为去除 中混有的SbOCl,可加入氨水对其“除氯”,不宜用NaOH溶液代替氨水的原因是
中混有的SbOCl,可加入氨水对其“除氯”,不宜用NaOH溶液代替氨水的原因是___________ 。
(5)Hg、Ge、Sb形成的物质X为潜在的拓扑绝缘体材料。X晶胞可视为Y晶胞中部分Ge原子被Hg和Sb取代后形成。X的最简式的相对分子质量为Mr,阿伏加德罗常数的数值为 ,则X晶体的密度为
,则X晶体的密度为___________  (列出计算式)。
(列出计算式)。
 ,还含有PbS、CuO、
,还含有PbS、CuO、 等)为原料提取锑。
等)为原料提取锑。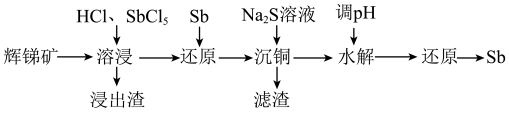
①浸出液中主要含过量盐酸和
 ,还含有
,还含有 、
、 、
、 等;
等;②常温下:
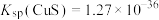 ,
,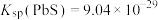 。
。(1)浸出渣除硫以外,还有
(2)“溶浸”时氧化产物是硫,
 被氧化的化学方程式为
被氧化的化学方程式为(3)已知:浸出液中
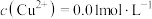 、
、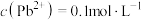 。在沉淀铜、铅过程中,缓慢滴加极稀的硫化钠溶液,先产生的沉淀是
。在沉淀铜、铅过程中,缓慢滴加极稀的硫化钠溶液,先产生的沉淀是 不宜过多,其原因为
不宜过多,其原因为(4)
 水解的中间产物有难溶于水的SbOCl生成,其对应的化学方程式为
水解的中间产物有难溶于水的SbOCl生成,其对应的化学方程式为 的性质与
的性质与 相似,为去除
相似,为去除 中混有的SbOCl,可加入氨水对其“除氯”,不宜用NaOH溶液代替氨水的原因是
中混有的SbOCl,可加入氨水对其“除氯”,不宜用NaOH溶液代替氨水的原因是(5)Hg、Ge、Sb形成的物质X为潜在的拓扑绝缘体材料。X晶胞可视为Y晶胞中部分Ge原子被Hg和Sb取代后形成。X的最简式的相对分子质量为Mr,阿伏加德罗常数的数值为
 ,则X晶体的密度为
,则X晶体的密度为 (列出计算式)。
(列出计算式)。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】某实验小组利用压强传感器采集实验数据,探究外界条件对双氧水分解速率的影响。用如下装置(1图)进行实验,请回答下列问题:
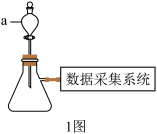
查阅资料:通常情况下, 较稳定,不易分解。
较稳定,不易分解。 对
对 的分解速率无影响。
的分解速率无影响。
(1)仪器a的名称___________ 。
(2)实验原理___________ (用化学方程式表示)。
(3)实验Ⅰ和Ⅱ的目的是___________ 。
(4)实验Ⅱ、Ⅲ探究的是不同催化剂对双氧水分解速率的影响:
①实验Ⅲ中 溶液浓度最好为
溶液浓度最好为_______ (填字母)。
A. B.
B. C.
C. D.
D.
②已知 和
和 都能对
都能对 分解起催化作用,且
分解起催化作用,且 催化效果比
催化效果比 更好。实验结果如图2图所示,请在图2中画出滴加
更好。实验结果如图2图所示,请在图2中画出滴加 溶液的气体压强变化曲线图(t时刻内
溶液的气体压强变化曲线图(t时刻内 未完全分解)
未完全分解)_____ 。
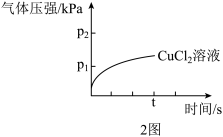
(5)设计实验Ⅳ与实验Ⅰ对比探究温度对双氧水分解速率的影响,填写下面表格:

锥形瓶 实验 | 盛放试剂 | 滴加试剂 | 反应条件 |
| Ⅰ | 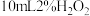 溶液 溶液 | 5滴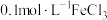 溶液 溶液 | 常温 |
| Ⅱ | 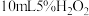 溶液 溶液 | 5滴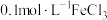 溶液 溶液 | 常温 |
| Ⅲ | 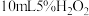 溶液 溶液 | 5滴___________ 溶液 溶液 | 常温 |
 较稳定,不易分解。
较稳定,不易分解。 对
对 的分解速率无影响。
的分解速率无影响。(1)仪器a的名称
(2)实验原理
(3)实验Ⅰ和Ⅱ的目的是
(4)实验Ⅱ、Ⅲ探究的是不同催化剂对双氧水分解速率的影响:
①实验Ⅲ中
 溶液浓度最好为
溶液浓度最好为A.
 B.
B. C.
C. D.
D.
②已知
 和
和 都能对
都能对 分解起催化作用,且
分解起催化作用,且 催化效果比
催化效果比 更好。实验结果如图2图所示,请在图2中画出滴加
更好。实验结果如图2图所示,请在图2中画出滴加 溶液的气体压强变化曲线图(t时刻内
溶液的气体压强变化曲线图(t时刻内 未完全分解)
未完全分解)
(5)设计实验Ⅳ与实验Ⅰ对比探究温度对双氧水分解速率的影响,填写下面表格:
锥形瓶 实验 | 盛放试剂 | 滴加试剂 | 反应条件 |
| Ⅳ | ① | ② | ③ |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】乙二酸俗称草酸,其钠盐和钾盐易溶于水,钙盐难溶于水。草酸晶体(H2C2O4·2H2O)无色、熔点为101℃。易溶于水,150℃-160℃大量升华,170℃以上分解。回答下列问题:
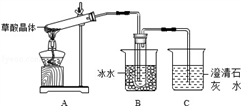
(1)甲组同学按照如图所示的装置,通过实验检验草酸晶体的分解产物,装置C中可观察到的现象是__________________________ ,由此可知草酸晶体分解的产物中有______________ ,装置B的主要作用是_____________________________________ 。
(2)乙组同学认为草酸晶体分解的产物中含有H2O和CO,为进行验证,选用下图中的装置进行实验。

实验装置连接的合理顺序为a→___________________ →k(填小写字母),能证明草酸晶体分解产物中有CO的现象是______________________________________________________________ ,草酸晶体受热分解的化学方程式为_______________________________________________________________ 。
(3)用酸性KMnO4溶液滴定反应结束后的F溶液,测定Na2C2O4的浓度
实验步骤:取20.00mLF中的溶液于锥形瓶中,再向锥形瓶中加入足量稀H2SO4,用0.1600mol/L酸性高锰酸钾溶液滴定,滴定至终点时消耗高锰酸钾溶液25.00mL。
①高锰酸钾溶液应装在_________ (填“酸式”或“碱式”)滴定管中。
②滴定终点的现象是_______________________________________________________ 。
③计算F溶液中Na2C2O4的物质的量浓度为_________ 。

(1)甲组同学按照如图所示的装置,通过实验检验草酸晶体的分解产物,装置C中可观察到的现象是
(2)乙组同学认为草酸晶体分解的产物中含有H2O和CO,为进行验证,选用下图中的装置进行实验。

实验装置连接的合理顺序为a→
(3)用酸性KMnO4溶液滴定反应结束后的F溶液,测定Na2C2O4的浓度
实验步骤:取20.00mLF中的溶液于锥形瓶中,再向锥形瓶中加入足量稀H2SO4,用0.1600mol/L酸性高锰酸钾溶液滴定,滴定至终点时消耗高锰酸钾溶液25.00mL。
①高锰酸钾溶液应装在
②滴定终点的现象是
③计算F溶液中Na2C2O4的物质的量浓度为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】Ⅰ.某小组利用数字化实验模拟制备Fe(OH)2并探究其相关性质。
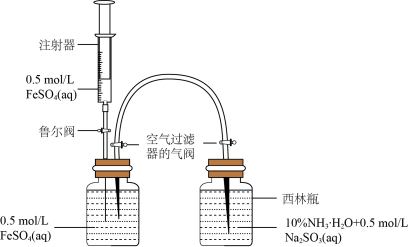
(1)模拟制备Fe(OH)2装置如图:打开右瓶上方空气过滤器的气阀(平衡压强,便于FeSO4溶液能够进入右瓶);然后,依次打开鲁尔阀、推动注射器,将注射器中的FeSO4溶液加入左瓶的溶液中,促使左瓶中的FeSO4溶液流入右瓶;当右瓶中明显有白色沉淀生成时,停止加液,依次关闭鲁尔阀、关闭右瓶上方的空气过滤器的气阀、打开左瓶上方的空气过滤器的气阀。实验证明制备Fe(OH)2最佳pH是6~8,氨水代替NaOH溶液效果更好的原因是_____ ,Na2SO3的作用是_____ 。
(2)探究原材料FeSO4的相关性质。向50mL蒸馏水中加入FeSO4·7H2O晶体搅拌以加快溶解,用溶解氧传感器测定液体中溶解氧浓度随时间的变化, 点时加入NaOH溶液所得曲线如图。
点时加入NaOH溶液所得曲线如图。

对比ab、bc段溶解氧的消耗速率,可以得出什么结论_____ 。
(3)已知:在 时溶液中,
时溶液中, 被氧化成
被氧化成 的过程中会产生
的过程中会产生 ,且
,且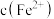 降低量大于
降低量大于 增加量,
增加量, 几乎不变,用总离子方程式说明原因
几乎不变,用总离子方程式说明原因_____ ,检验反应后的溶液中是否存在 ,可以选择的试剂是
,可以选择的试剂是_____ 。
A.NaOH溶液 B.K3[Fe(CN)6] C.KSCN D.KMnO4
Ⅱ.
(4)用氢氧化钠固体配制实验所需的NaOH溶液,下列图示对应的操作规范的是_____
(5)用NaOH固体配制实验所需的NaOH溶液时,下列操作会导致所配溶液浓度偏高的是_____ 。
A.未冷却至室温就定容
B.容量瓶用蒸馏水洗净后未干燥
C.定容时俯视读取刻度
D.定容时液面超过了刻度线,并将多余溶液吸出
E.称量NaOH时用了生锈的砝码
(1)模拟制备Fe(OH)2装置如图:打开右瓶上方空气过滤器的气阀(平衡压强,便于FeSO4溶液能够进入右瓶);然后,依次打开鲁尔阀、推动注射器,将注射器中的FeSO4溶液加入左瓶的溶液中,促使左瓶中的FeSO4溶液流入右瓶;当右瓶中明显有白色沉淀生成时,停止加液,依次关闭鲁尔阀、关闭右瓶上方的空气过滤器的气阀、打开左瓶上方的空气过滤器的气阀。实验证明制备Fe(OH)2最佳pH是6~8,氨水代替NaOH溶液效果更好的原因是

(2)探究原材料FeSO4的相关性质。向50mL蒸馏水中加入FeSO4·7H2O晶体搅拌以加快溶解,用溶解氧传感器测定液体中溶解氧浓度随时间的变化,
 点时加入NaOH溶液所得曲线如图。
点时加入NaOH溶液所得曲线如图。
对比ab、bc段溶解氧的消耗速率,可以得出什么结论
(3)已知:在
 时溶液中,
时溶液中, 被氧化成
被氧化成 的过程中会产生
的过程中会产生 ,且
,且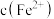 降低量大于
降低量大于 增加量,
增加量, 几乎不变,用总离子方程式说明原因
几乎不变,用总离子方程式说明原因 ,可以选择的试剂是
,可以选择的试剂是A.NaOH溶液 B.K3[Fe(CN)6] C.KSCN D.KMnO4
Ⅱ.
(4)用氢氧化钠固体配制实验所需的NaOH溶液,下列图示对应的操作规范的是_____
 |  | 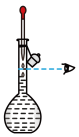 |  |
| A.称量 | B.转移 | C、定容 | D、摇匀 |
| A.A | B.B | C.C | D.D |
(5)用NaOH固体配制实验所需的NaOH溶液时,下列操作会导致所配溶液浓度偏高的是
A.未冷却至室温就定容
B.容量瓶用蒸馏水洗净后未干燥
C.定容时俯视读取刻度
D.定容时液面超过了刻度线,并将多余溶液吸出
E.称量NaOH时用了生锈的砝码
您最近一年使用:0次



