某铝土矿的主要成分为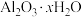 ,还含有
,还含有 和
和 杂质。称取
杂质。称取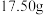 铝土矿样品,加入
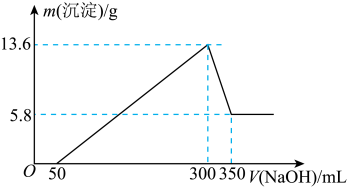
铝土矿样品,加入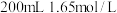 的稀硫酸,恰好完全反应,过滤得沉淀
的稀硫酸,恰好完全反应,过滤得沉淀 ,然后在滤液中加入足量的
,然后在滤液中加入足量的 溶液,得到沉淀
溶液,得到沉淀 。
。
(1)该试样中 的物质的量为
的物质的量为___________ mol。
(2)样品中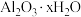 的x=
的x=___________ 。
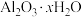 ,还含有
,还含有 和
和 杂质。称取
杂质。称取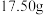 铝土矿样品,加入
铝土矿样品,加入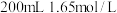 的稀硫酸,恰好完全反应,过滤得沉淀
的稀硫酸,恰好完全反应,过滤得沉淀 ,然后在滤液中加入足量的
,然后在滤液中加入足量的 溶液,得到沉淀
溶液,得到沉淀 。
。(1)该试样中
 的物质的量为
的物质的量为(2)样品中
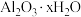 的x=
的x=
2024高三·全国·专题练习 查看更多[1]
(已下线)题型17 化学实验综合-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)
更新时间:2024-02-01 12:27:29
|
相似题推荐
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】计算填空:
(1)同温同压下,同体积的甲烷(CH4)和二氧化碳物质的量之比为___ ,原子总数之比为___ ,密度之比为____ 。
(2)标准状况下,在4gH2、11.2LO2、NA个H2O中,所含分子数最多的是___ ,含原子数最多的是___ ,质量最大的是___ ,体积最小的是____ 。
(3)在14.2gNa2SO4中:含有的Na+的数目是___ ;含有的SO 的质量是
的质量是____ ;含氧原子的物质的量是___ 。
(1)同温同压下,同体积的甲烷(CH4)和二氧化碳物质的量之比为
(2)标准状况下,在4gH2、11.2LO2、NA个H2O中,所含分子数最多的是
(3)在14.2gNa2SO4中:含有的Na+的数目是
 的质量是
的质量是
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】室温下,某容积固定的密闭容器由可移动的活塞隔成A、B两室,分别向A、B两室充入H2、O2的混合气体和1 mol空气,此时活塞的位置如图所示。
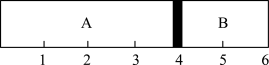
(1)A室混合气体的物质的量为________ ,标况下体积为________ 。
(2)实验测得A室混合气体的质量为34 g,则该混合气体的密度是同温同压条件下氦气密度的________ 倍。若将A室H2、O2的混合气体点燃引爆,恢复原温度后,最终活塞停留的位置在________ 刻度,容器内气体压强与反应前气体压强之比为________ 。

(1)A室混合气体的物质的量为
(2)实验测得A室混合气体的质量为34 g,则该混合气体的密度是同温同压条件下氦气密度的
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐3】化学计量在化学中占有重要地位,请回答下列问题:
(1)0.3 mol NH3分子中所含原子数与______ 个H2O分子中所含原子数相等。
(2)含0.4 mol Al3+的Al2(SO4)3中所含的 的质量是
的质量是_______ 。
(3)已知16 g A和20 g B恰好完全反应生成0.04 mol C和31.76 g D,则C的相对分子质量为______ 。
(4)在一定的温度和压强下,1体积气体X2跟3体积气体Y2化合生成2体积化合物,则该化合物的化学式是_____ 。
(5)某盐混合溶液中含有离子:Na+、Mg2+ 、Cl-、 ,测得Na+、Mg2+ 和Cl-的物质的量浓度依次为: 0.2 mol·L-1、0.25 mol·L-1、0.4 mol·L-1,则c(
,测得Na+、Mg2+ 和Cl-的物质的量浓度依次为: 0.2 mol·L-1、0.25 mol·L-1、0.4 mol·L-1,则c( )=
)=______ 。
(1)0.3 mol NH3分子中所含原子数与
(2)含0.4 mol Al3+的Al2(SO4)3中所含的
 的质量是
的质量是(3)已知16 g A和20 g B恰好完全反应生成0.04 mol C和31.76 g D,则C的相对分子质量为
(4)在一定的温度和压强下,1体积气体X2跟3体积气体Y2化合生成2体积化合物,则该化合物的化学式是
(5)某盐混合溶液中含有离子:Na+、Mg2+ 、Cl-、
 ,测得Na+、Mg2+ 和Cl-的物质的量浓度依次为: 0.2 mol·L-1、0.25 mol·L-1、0.4 mol·L-1,则c(
,测得Na+、Mg2+ 和Cl-的物质的量浓度依次为: 0.2 mol·L-1、0.25 mol·L-1、0.4 mol·L-1,则c( )=
)=
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】将一定质量的Mg和Al的混合物投入100mL的稀硫酸中,固体全部溶解并产生气体.待反应完全后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入NaOH溶液体积的关系如图所示:

(1)当加入氢氧化钠溶液的体积为20mL时,溶液中的溶质有_________________ 。
(2)固体溶解时生成的气体在标准状况下的体积为____________ L。
(3)稀硫酸的物质的量浓度为____________  (结果保留一位小数)。
(结果保留一位小数)。

(1)当加入氢氧化钠溶液的体积为20mL时,溶液中的溶质有
(2)固体溶解时生成的气体在标准状况下的体积为
(3)稀硫酸的物质的量浓度为
 (结果保留一位小数)。
(结果保留一位小数)。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】(1)在质量分数为28%的KOH水溶液中,OH-与H2O数目之比是________ 。
(2)由硫酸钾、硫酸铁和硫酸组成的混合溶液,其中c(H+)=0.1 mol/L,c(Fe3+)=0.3 mol/L,c(SO42-)=0.6 mol/L,则c(K+)为________ 。
(3)相同物质的量浓度的氯化钠、氯化镁、氯化铝溶液,分别与硝酸银溶液反应,当生成沉淀的质量之比为3∶2∶1时,消耗三种盐溶液的体积比为________ 。
(4)A物质按下式分解:2A=B↑+ 2C↑ + 2D↑,测得生成的混合气体在相同条件下的密度是O2密度的m倍,则A的摩尔质量为______________ 。
(5)某状况下a L氨气(此时气体摩尔体积为Vm)溶解在一定量的水中形成b mL氨水溶液,所得溶液的密度为ρ g/mL,则该氨水的物质的量浓度可表示为________ mol/L;氨水的质量分数为________ 。
(2)由硫酸钾、硫酸铁和硫酸组成的混合溶液,其中c(H+)=0.1 mol/L,c(Fe3+)=0.3 mol/L,c(SO42-)=0.6 mol/L,则c(K+)为
(3)相同物质的量浓度的氯化钠、氯化镁、氯化铝溶液,分别与硝酸银溶液反应,当生成沉淀的质量之比为3∶2∶1时,消耗三种盐溶液的体积比为
(4)A物质按下式分解:2A=B↑+ 2C↑ + 2D↑,测得生成的混合气体在相同条件下的密度是O2密度的m倍,则A的摩尔质量为
(5)某状况下a L氨气(此时气体摩尔体积为Vm)溶解在一定量的水中形成b mL氨水溶液,所得溶液的密度为ρ g/mL,则该氨水的物质的量浓度可表示为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】称取一定质量镁铝合金放入500mL稀硫酸中,固体全部溶解并产生气体。待反应完全后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积关系如图(生成沉淀阶段的图象斜率视为恒定)。
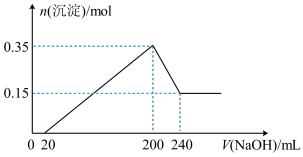
计算:
(1)合金中Al的质量为多少____ ?
(2)所加NaOH溶液的物质的量浓度为多少____ ?

计算:
(1)合金中Al的质量为多少
(2)所加NaOH溶液的物质的量浓度为多少
您最近一年使用:0次
【推荐2】I.有200 mL氯化镁和氯化铝的混合溶液,其中c(Mg2+)为0.2mol·L-1,c(Cl-)为1.3mol·L-1。要使Mg2+全部转化为沉淀分离出来,至少需加4mol·L-1NaOH溶液的体积为___________________ mL
II.焊接铜件时常用的焊药为氯化铵,其作用是消除焊接处的氧化铜。其反应式为 NH4C1+ CuO→Cu+CuCl2+ N2↑+ H2O
(1)配平,并用双线桥法标出电子转移情况。:____________
(2)该反应中,氧化剂和还原剂的物质的量之比为:___________ 。
(3)若反应中电子转移了0.3mol,则产生的气体在标准状况下的体积为_______ L。
II.焊接铜件时常用的焊药为氯化铵,其作用是消除焊接处的氧化铜。其反应式为 NH4C1+ CuO→Cu+CuCl2+ N2↑+ H2O
(1)配平,并用双线桥法标出电子转移情况。:
(2)该反应中,氧化剂和还原剂的物质的量之比为:
(3)若反应中电子转移了0.3mol,则产生的气体在标准状况下的体积为
您最近一年使用:0次