I.有200 mL氯化镁和氯化铝的混合溶液,其中c(Mg2+)为0.2mol·L-1,c(Cl-)为1.3mol·L-1。要使Mg2+全部转化为沉淀分离出来,至少需加4mol·L-1NaOH溶液的体积为___________________ mL
II.焊接铜件时常用的焊药为氯化铵,其作用是消除焊接处的氧化铜。其反应式为 NH4C1+ CuO→Cu+CuCl2+ N2↑+ H2O
(1)配平,并用双线桥法标出电子转移情况。:____________
(2)该反应中,氧化剂和还原剂的物质的量之比为:___________ 。
(3)若反应中电子转移了0.3mol,则产生的气体在标准状况下的体积为_______ L。
II.焊接铜件时常用的焊药为氯化铵,其作用是消除焊接处的氧化铜。其反应式为 NH4C1+ CuO→Cu+CuCl2+ N2↑+ H2O
(1)配平,并用双线桥法标出电子转移情况。:
(2)该反应中,氧化剂和还原剂的物质的量之比为:
(3)若反应中电子转移了0.3mol,则产生的气体在标准状况下的体积为
更新时间:2020-04-30 16:48:54
|
相似题推荐
【推荐1】过量的铁粉与稀硝酸反应的方程式为:3Fe +8HNO3 =3Fe(NO3)2+ 2NO↑+4H2O
(1)标出电子转移的方向和数目______ 。
(2)在标准状况下,当生成22.4LNO气体时,有_______ gFe参加反应,转移电子的物质的量为_______ 。
(1)标出电子转移的方向和数目
(2)在标准状况下,当生成22.4LNO气体时,有
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】根据反应8NH3+3Cl2=6NH4Cl+N2回答下列问题。
(1)氧化剂______________ ,还原剂____________
(2)用双线桥法标出反应中电子转移情况_________________________
(3)氧化剂与氧化产物的质量比__________
(4)当生成28gN2时,被氧化的物质的质量是__________ g。
(1)氧化剂
(2)用双线桥法标出反应中电子转移情况
(3)氧化剂与氧化产物的质量比
(4)当生成28gN2时,被氧化的物质的质量是
您最近一年使用:0次
【推荐1】氯化亚铜(CuCl)广泛应用于化工、印染、电镀等行业。CuCl难溶于醇和水,可溶于氯离子浓度较大的体系,在潮湿空气中易水解氧化。
准确称取氯化亚铜样品mg,将其置于过量的FeCl3溶液中,待样品完全溶解后,加入适量稀硫酸,用amol/L的K2Cr2O7溶液滴定到终点,消耗K2Cr2O7溶液bmL,反应中Cr2O72-被还原为Cr3+,样品中CuCl的质量分数为__________ 。
准确称取氯化亚铜样品mg,将其置于过量的FeCl3溶液中,待样品完全溶解后,加入适量稀硫酸,用amol/L的K2Cr2O7溶液滴定到终点,消耗K2Cr2O7溶液bmL,反应中Cr2O72-被还原为Cr3+,样品中CuCl的质量分数为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】氯及其化合物有广泛用途。二氧化氯是一种新型的消毒剂。
①NaClO2中Cl的化合价为____________ 。
②实验室用氯酸钾与浓盐酸反应制备ClO2,产物除ClO2外,还有Cl2,KCl等,写出该反应的化学方程式__________ 。若生成11.2L氯气(标准状况),转移电子数为_________ 。
③ClO2和Cl2在消毒时自身均被还原为Cl-,则常温常压下,等体积的ClO2的消毒能力是Cl2的_________ 倍。
④自来水厂用ClO2处理后的水中,要求ClO2的浓度在0.1﹣0.8 mg•L-1之间。碘量法可以检测水中ClO2的浓度(不同pH环境中粒子种类如图所示),步骤如下:
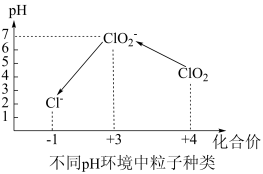
Ⅰ.取一定体积的水样,加入一定量的碘化钾,再将反应后溶液调至中性,并加入淀粉溶液,溶液变蓝。
Ⅱ.加入一定量的Na2S2O3溶液。(已知:2S2O32-+I2═S4O62-+2I-)
Ⅲ.加硫酸调节水样pH至1﹣3。
请问答:
若水样的体积为1.0L,在操作II时消耗了1.0×10-3mol•L-1的Na2S2O3溶液10mL.则水样中ClO2的浓度是_____ mg•L-1。
①NaClO2中Cl的化合价为
②实验室用氯酸钾与浓盐酸反应制备ClO2,产物除ClO2外,还有Cl2,KCl等,写出该反应的化学方程式
③ClO2和Cl2在消毒时自身均被还原为Cl-,则常温常压下,等体积的ClO2的消毒能力是Cl2的
④自来水厂用ClO2处理后的水中,要求ClO2的浓度在0.1﹣0.8 mg•L-1之间。碘量法可以检测水中ClO2的浓度(不同pH环境中粒子种类如图所示),步骤如下:

Ⅰ.取一定体积的水样,加入一定量的碘化钾,再将反应后溶液调至中性,并加入淀粉溶液,溶液变蓝。
Ⅱ.加入一定量的Na2S2O3溶液。(已知:2S2O32-+I2═S4O62-+2I-)
Ⅲ.加硫酸调节水样pH至1﹣3。
请问答:
若水样的体积为1.0L,在操作II时消耗了1.0×10-3mol•L-1的Na2S2O3溶液10mL.则水样中ClO2的浓度是
您最近一年使用:0次
【推荐1】请回答以下问题:
(1)氢化钠(NaH)为白色晶体,其中 有很强的还原性,因此常用氢化钠在高温下将TiCl4还原为Ti,自身被氧化为+1价。写出其化学反应方程式,并用单线桥标出电子的转移的方向与数目
有很强的还原性,因此常用氢化钠在高温下将TiCl4还原为Ti,自身被氧化为+1价。写出其化学反应方程式,并用单线桥标出电子的转移的方向与数目___________ ;NaH能与水剧烈反应NaH+H2O=NaOH+H2↑,NaH与液氨也有类似反应,写出反应的化学方程式___________ 。
(2)在3BrF3+5H2O=HBrO3+Br2+9HF+O2↑的反应中,3mol的BrF3参加反应时,被H2O所还原的BrF3的物质的量是___________ 。
(3)已知砒霜As2O3与Zn可以发生如下反应:As2O3+6Zn+6H2SO4=2AsH3↑+6ZnSO4+3H2O
①请用双线桥法标出电子转移的方向和数目___________ 。
②若生成0.2molAsH3,则转移的电子数为___________ 。
(4)氧化氯(ClO2)是一种在水处理等方面有广泛应用的高效安全消毒剂,制备ClO2有下列两种方法:
方法一:2NaClO3+4HCl=2ClO2↑+Cl2↑+2NaCl+2H2O
方法二:2NaClO3+H2O2+H2SO4=2ClO2↑+O2↑+Na2SO4+2H2O
①方法一中氧化剂与还原剂的物质的量之比为___________ ;
②若两种方法制备得到相同条件下相同体积的ClO2气体,则两方法中消耗的还原剂质量之比为___________ ;
③Cl2与ClO2均用作水处理剂,若它们中的氯元素均被还原为 ,则相同质量的ClO2是Cl2消毒效率的
,则相同质量的ClO2是Cl2消毒效率的___________ 倍。
(5)配平反应方程式(答题卡上写出完整的化学方程式)___________________ 。
______Al+_______NaNO3+_____H2O=____Al(OH)3+____N2↑+____NaAlO2
(1)氢化钠(NaH)为白色晶体,其中
 有很强的还原性,因此常用氢化钠在高温下将TiCl4还原为Ti,自身被氧化为+1价。写出其化学反应方程式,并用单线桥标出电子的转移的方向与数目
有很强的还原性,因此常用氢化钠在高温下将TiCl4还原为Ti,自身被氧化为+1价。写出其化学反应方程式,并用单线桥标出电子的转移的方向与数目(2)在3BrF3+5H2O=HBrO3+Br2+9HF+O2↑的反应中,3mol的BrF3参加反应时,被H2O所还原的BrF3的物质的量是
(3)已知砒霜As2O3与Zn可以发生如下反应:As2O3+6Zn+6H2SO4=2AsH3↑+6ZnSO4+3H2O
①请用双线桥法标出电子转移的方向和数目
②若生成0.2molAsH3,则转移的电子数为
(4)氧化氯(ClO2)是一种在水处理等方面有广泛应用的高效安全消毒剂,制备ClO2有下列两种方法:
方法一:2NaClO3+4HCl=2ClO2↑+Cl2↑+2NaCl+2H2O
方法二:2NaClO3+H2O2+H2SO4=2ClO2↑+O2↑+Na2SO4+2H2O
①方法一中氧化剂与还原剂的物质的量之比为
②若两种方法制备得到相同条件下相同体积的ClO2气体,则两方法中消耗的还原剂质量之比为
③Cl2与ClO2均用作水处理剂,若它们中的氯元素均被还原为
 ,则相同质量的ClO2是Cl2消毒效率的
,则相同质量的ClO2是Cl2消毒效率的(5)配平反应方程式(答题卡上写出完整的化学方程式)
______Al+_______NaNO3+_____H2O=____Al(OH)3+____N2↑+____NaAlO2
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】2g Cu2S和CuS的混合物在酸性溶液中用400mL 0.075mol/L KMnO4溶液处理,发生反应如下:
8MnO4-+5Cu2S+44H+=10Cu2++5SO2+8Mn2++22H2O
6MnO4-+5CuS+28H+=5Cu2++5SO2+6Mn2++14H2O
反应后煮沸溶液,赶尽SO2,剩余的KMnO4恰好与350mL 0.1mol/L(NH4)2Fe(SO4)2溶液完全反应。
(1)配平KMnO4与(NH4)2Fe(SO4)2反应的离子方程式:
___ MnO4-+ Fe2++ H+= Mn2++ Fe3++H2O
(2)KMnO4溶液与混合物反应后,剩余KMnO4的物质的量为_____ mol。
(3)欲配制500mL 0.1mol/L Fe2+溶液,需称取(NH4)2Fe(SO4)2·6H2O(M=392g/mol)的质量为_________ g。
(4)混合物中Cu2S的质量分数为________________ 。
8MnO4-+5Cu2S+44H+=10Cu2++5SO2+8Mn2++22H2O
6MnO4-+5CuS+28H+=5Cu2++5SO2+6Mn2++14H2O
反应后煮沸溶液,赶尽SO2,剩余的KMnO4恰好与350mL 0.1mol/L(NH4)2Fe(SO4)2溶液完全反应。
(1)配平KMnO4与(NH4)2Fe(SO4)2反应的离子方程式:
(2)KMnO4溶液与混合物反应后,剩余KMnO4的物质的量为
(3)欲配制500mL 0.1mol/L Fe2+溶液,需称取(NH4)2Fe(SO4)2·6H2O(M=392g/mol)的质量为
(4)混合物中Cu2S的质量分数为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】饮用水质量是关系人类健康的重要问题。
(1)Cl2是最早用于饮用水消毒的物质,写出Cl2溶于水发生反应的离子方程式:___ 。
(2)ClO2是一种高效、低毒的消毒剂,逐渐取代Cl2成为生产自来水的消毒剂,工业上用KClO3与Na2SO3在H2SO4存在下制得ClO2,该反应中氧化剂与还原剂物质的量之比为____ 。
(3)高铁酸钾(K2FeO4)是一种新型、高效、多功能水处理剂,比Cl2、ClO2氧化性更强,是无二次污染的绿色水处理剂。工业上先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH至饱和就可析出高铁酸钾。由以上信息可知,相同条件下,高铁酸钠溶解度比高铁酸钾溶解度__ (填“大”或“小”)。高铁酸钾溶于水放出氧气,能杀菌消毒,生成能吸附水中悬浮物的氢氧化铁胶体。用一个离子方程式表示高铁酸钾处理水的过程____ 。干法制备高铁酸钠的主要反应为2FeSO4+6Na2O2===2Na2FeO4+2Na2O+2Na2SO4+O2↑,该反应的还原剂是___ ,每生成1molNa2FeO4转移__ mol电子。
(1)Cl2是最早用于饮用水消毒的物质,写出Cl2溶于水发生反应的离子方程式:
(2)ClO2是一种高效、低毒的消毒剂,逐渐取代Cl2成为生产自来水的消毒剂,工业上用KClO3与Na2SO3在H2SO4存在下制得ClO2,该反应中氧化剂与还原剂物质的量之比为
(3)高铁酸钾(K2FeO4)是一种新型、高效、多功能水处理剂,比Cl2、ClO2氧化性更强,是无二次污染的绿色水处理剂。工业上先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH至饱和就可析出高铁酸钾。由以上信息可知,相同条件下,高铁酸钠溶解度比高铁酸钾溶解度
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】某种治疗胃病药物的化学成分是AlxMgy(OH)z(CO3)w·nH2O。
(1)取该碱式盐3.40g,研磨、加水、搅拌使之充分分散,滴加2.00mol·L-1盐酸,先后与OH-和CO 反应,当加入盐酸35.0mL时,开始产生CO2,加入盐酸45.0mL时恰好完全反应,该碱式盐中氢氧根与碳酸根的物质的量之比为
反应,当加入盐酸35.0mL时,开始产生CO2,加入盐酸45.0mL时恰好完全反应,该碱式盐中氢氧根与碳酸根的物质的量之比为_____ 。
(2)在上述反应后所得溶液中加入过量氢氧化钠溶液,过滤、洗涤、干燥后沉淀物重1.74g,该碱式盐中铝离子与镁离子的物质的量之比为_____ 。
(3)若3.40g该碱式盐完全受热分解产生0.81g水,该碱式盐的化学式为_____ 。
(1)取该碱式盐3.40g,研磨、加水、搅拌使之充分分散,滴加2.00mol·L-1盐酸,先后与OH-和CO
 反应,当加入盐酸35.0mL时,开始产生CO2,加入盐酸45.0mL时恰好完全反应,该碱式盐中氢氧根与碳酸根的物质的量之比为
反应,当加入盐酸35.0mL时,开始产生CO2,加入盐酸45.0mL时恰好完全反应,该碱式盐中氢氧根与碳酸根的物质的量之比为(2)在上述反应后所得溶液中加入过量氢氧化钠溶液,过滤、洗涤、干燥后沉淀物重1.74g,该碱式盐中铝离子与镁离子的物质的量之比为
(3)若3.40g该碱式盐完全受热分解产生0.81g水,该碱式盐的化学式为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】将1.05 g由铝和过氧化钠的混合物放入一量的水中,充分反应后固体无剩余。再向其中慢慢滴加50 mL 1 mol/L的盐酸,可恰好使反应过程中产生的沉淀溶解。
(1)要使混合物溶于水无剩余,则n(Al)与n(Na2O2)的关系须满足_________ ;
(2)写出沉淀溶解的离子方程式:___________________ ;
(3)求原混合物中铝、过氧化钠的质量___________________ ;
(4)求滴加盐酸过程中开始出现沉淀时盐酸的体积___________________ 。
(1)要使混合物溶于水无剩余,则n(Al)与n(Na2O2)的关系须满足
(2)写出沉淀溶解的离子方程式:
(3)求原混合物中铝、过氧化钠的质量
(4)求滴加盐酸过程中开始出现沉淀时盐酸的体积
您最近一年使用:0次

 、
、 、
、 三种固体组成的混合物溶于足量水中,有
三种固体组成的混合物溶于足量水中,有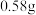 白色沉淀生成,向所得混合液中,逐滴加入
白色沉淀生成,向所得混合液中,逐滴加入 的盐酸,加入盐酸的体积和生成沉淀的质量如图所示[图中的Y表示沉淀质量
的盐酸,加入盐酸的体积和生成沉淀的质量如图所示[图中的Y表示沉淀质量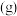 ,X表示加入盐酸体积
,X表示加入盐酸体积 ]
]
 ,
, 和
和 的物质的量之比是
的物质的量之比是 。
。


