请回答以下问题:
(1)氢化钠(NaH)为白色晶体,其中 有很强的还原性,因此常用氢化钠在高温下将TiCl4还原为Ti,自身被氧化为+1价。写出其化学反应方程式,并用单线桥标出电子的转移的方向与数目
有很强的还原性,因此常用氢化钠在高温下将TiCl4还原为Ti,自身被氧化为+1价。写出其化学反应方程式,并用单线桥标出电子的转移的方向与数目___________ ;NaH能与水剧烈反应NaH+H2O=NaOH+H2↑,NaH与液氨也有类似反应,写出反应的化学方程式___________ 。
(2)在3BrF3+5H2O=HBrO3+Br2+9HF+O2↑的反应中,3mol的BrF3参加反应时,被H2O所还原的BrF3的物质的量是___________ 。
(3)已知砒霜As2O3与Zn可以发生如下反应:As2O3+6Zn+6H2SO4=2AsH3↑+6ZnSO4+3H2O
①请用双线桥法标出电子转移的方向和数目___________ 。
②若生成0.2molAsH3,则转移的电子数为___________ 。
(4)氧化氯(ClO2)是一种在水处理等方面有广泛应用的高效安全消毒剂,制备ClO2有下列两种方法:
方法一:2NaClO3+4HCl=2ClO2↑+Cl2↑+2NaCl+2H2O
方法二:2NaClO3+H2O2+H2SO4=2ClO2↑+O2↑+Na2SO4+2H2O
①方法一中氧化剂与还原剂的物质的量之比为___________ ;
②若两种方法制备得到相同条件下相同体积的ClO2气体,则两方法中消耗的还原剂质量之比为___________ ;
③Cl2与ClO2均用作水处理剂,若它们中的氯元素均被还原为 ,则相同质量的ClO2是Cl2消毒效率的
,则相同质量的ClO2是Cl2消毒效率的___________ 倍。
(5)配平反应方程式(答题卡上写出完整的化学方程式)___________________ 。
______Al+_______NaNO3+_____H2O=____Al(OH)3+____N2↑+____NaAlO2
(1)氢化钠(NaH)为白色晶体,其中
 有很强的还原性,因此常用氢化钠在高温下将TiCl4还原为Ti,自身被氧化为+1价。写出其化学反应方程式,并用单线桥标出电子的转移的方向与数目
有很强的还原性,因此常用氢化钠在高温下将TiCl4还原为Ti,自身被氧化为+1价。写出其化学反应方程式,并用单线桥标出电子的转移的方向与数目(2)在3BrF3+5H2O=HBrO3+Br2+9HF+O2↑的反应中,3mol的BrF3参加反应时,被H2O所还原的BrF3的物质的量是
(3)已知砒霜As2O3与Zn可以发生如下反应:As2O3+6Zn+6H2SO4=2AsH3↑+6ZnSO4+3H2O
①请用双线桥法标出电子转移的方向和数目
②若生成0.2molAsH3,则转移的电子数为
(4)氧化氯(ClO2)是一种在水处理等方面有广泛应用的高效安全消毒剂,制备ClO2有下列两种方法:
方法一:2NaClO3+4HCl=2ClO2↑+Cl2↑+2NaCl+2H2O
方法二:2NaClO3+H2O2+H2SO4=2ClO2↑+O2↑+Na2SO4+2H2O
①方法一中氧化剂与还原剂的物质的量之比为
②若两种方法制备得到相同条件下相同体积的ClO2气体,则两方法中消耗的还原剂质量之比为
③Cl2与ClO2均用作水处理剂,若它们中的氯元素均被还原为
 ,则相同质量的ClO2是Cl2消毒效率的
,则相同质量的ClO2是Cl2消毒效率的(5)配平反应方程式(答题卡上写出完整的化学方程式)
______Al+_______NaNO3+_____H2O=____Al(OH)3+____N2↑+____NaAlO2
更新时间:2021-03-17 15:00:56
|
相似题推荐
【推荐1】ClO2是一种杀菌效率高、二次污染小的水处理剂。实验室可以通过以下反应制得ClO2:2KClO3+H2C2O4+H2SO4=2ClO2+K2SO4+2CO2+2H2O,
(1)双线桥表示氧化还原,线桥上标明得失电子、发生的反应。_______
(2)若1mo KClO3参加反应时有_______ mol电子转移。
(3)若生成标准状况下的CO2的体积是44.8L,则参加反应的还原剂的物质的量是多少mol?(要求有规范的过程)_______ 。
(1)双线桥表示氧化还原,线桥上标明得失电子、发生的反应。
(2)若1mo KClO3参加反应时有
(3)若生成标准状况下的CO2的体积是44.8L,则参加反应的还原剂的物质的量是多少mol?(要求有规范的过程)
您最近一年使用:0次
【推荐2】把Cl2通入浓氨水中,发生如下反应:3Cl2+8NH3=6NH4Cl+N2
(1)用单线桥表示反应的电子转移方向和数目:_______ 。
(2)反应中发生电子转移的NH3与Cl2的分子数之比为:_______ 。
(3)若反应中有3.4克氨发生氧化反应,则反应中有生成氮气的质量为_______ 。
(4)高铁酸钠(Na2FeO4)(铁为+6 价)是一种新型的净水剂,可以通过下述反应制取:Fe(OH)3+ NaOH+NaClO—Na2FeO4+NaCl+H2O
①该反应中 (用化学式表示, 下同),还原产物为_______ ,_______ 元素被氧化。
②配平该反应的方程式并用双线桥在方程式中标出电子转移的情况:_______ 。
(1)用单线桥表示反应的电子转移方向和数目:
(2)反应中发生电子转移的NH3与Cl2的分子数之比为:
(3)若反应中有3.4克氨发生氧化反应,则反应中有生成氮气的质量为
(4)高铁酸钠(Na2FeO4)(铁为+6 价)是一种新型的净水剂,可以通过下述反应制取:Fe(OH)3+ NaOH+NaClO—Na2FeO4+NaCl+H2O
①该反应中 (用化学式表示, 下同),还原产物为
②配平该反应的方程式并用双线桥在方程式中标出电子转移的情况:
您最近一年使用:0次
【推荐3】I.有200 mL氯化镁和氯化铝的混合溶液,其中c(Mg2+)为0.2mol·L-1,c(Cl-)为1.3mol·L-1。要使Mg2+全部转化为沉淀分离出来,至少需加4mol·L-1NaOH溶液的体积为___________________ mL
II.焊接铜件时常用的焊药为氯化铵,其作用是消除焊接处的氧化铜。其反应式为 NH4C1+ CuO→Cu+CuCl2+ N2↑+ H2O
(1)配平,并用双线桥法标出电子转移情况。:____________
(2)该反应中,氧化剂和还原剂的物质的量之比为:___________ 。
(3)若反应中电子转移了0.3mol,则产生的气体在标准状况下的体积为_______ L。
II.焊接铜件时常用的焊药为氯化铵,其作用是消除焊接处的氧化铜。其反应式为 NH4C1+ CuO→Cu+CuCl2+ N2↑+ H2O
(1)配平,并用双线桥法标出电子转移情况。:
(2)该反应中,氧化剂和还原剂的物质的量之比为:
(3)若反应中电子转移了0.3mol,则产生的气体在标准状况下的体积为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】纳米级Cu2O可以作为太阳光分解水的催化剂,有这重要的应用前景。在加热的条件下用液态肼(N2H4)还原新制Cu(OH)2可制备纳米级Cu2O,同时生成N2,写出该反应的化学方程式_______ 。当收集的N2体积为3.36L(标准状况),计算制得纳米Cu2O的质量_______ 和转移电子数_______ 。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】写出298K时,下列反应的热化学方程式
(1)28 g CO还原Fe2O3生成单质铁,放出8.3 kJ热量;_________________________
(2)N2和O2化合生成184 g NO2气体,吸收热量135.4 kJ;__________________________
(1)28 g CO还原Fe2O3生成单质铁,放出8.3 kJ热量;
(2)N2和O2化合生成184 g NO2气体,吸收热量135.4 kJ;
您最近一年使用:0次
【推荐3】(1)反应2NaClO3+4HCl=2ClO2↑+Cl2↑+2H2O+2NaCl中,氧化产物是___________ ,氧化剂和还原剂的物质的量之比为___________ ,依据氧化还原反应规律判断,氧化性强弱为NaClO3___________ Cl2(填>、<或=)。
(2)根据下图中的能量关系,可求得C-H键的键能___________ kJ/mol。
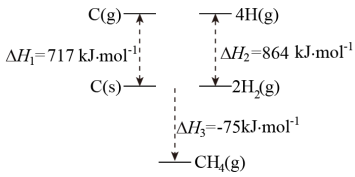
(3)已知:
I. CO(g) + 2H2(g) =CH 3OH(l) △H= −128.6 kJ/mol
II.2CO(g) + O2(g) =2 CO2(g) △H=−566.0 kJ/mol
III.2H2(g) + O2(g) =2 H2O(l) △H=−571.6 kJ/mol
写出 CH3OH燃烧热的热化学方程式:___________ 。
(2)根据下图中的能量关系,可求得C-H键的键能

(3)已知:
I. CO(g) + 2H2(g) =CH 3OH(l) △H= −128.6 kJ/mol
II.2CO(g) + O2(g) =2 CO2(g) △H=−566.0 kJ/mol
III.2H2(g) + O2(g) =2 H2O(l) △H=−571.6 kJ/mol
写出 CH3OH燃烧热的热化学方程式:
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】计算
(1)已知酸性条件下, 可将
可将 还原为
还原为 。将标准状况下
。将标准状况下 的
的 气体通入足量酸性
气体通入足量酸性 溶液中,
溶液中,
①写出该反应的离子方程式______ 。
②被还原的 的质量为
的质量为______ 。
(2)为了检验某含有 杂质的
杂质的 样品的纯度,现将
样品的纯度,现将 样品充分加热,当固体质量不再变化时,再次称量固体质量为
样品充分加热,当固体质量不再变化时,再次称量固体质量为 ,则该样品的纯度(质量分数)为
,则该样品的纯度(质量分数)为______ (用含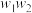 的代数式来表示)。
的代数式来表示)。
(3)有一块表面氧化成氧化钠的金属钠,总质量为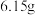 ,投入到足量水中,待充分反应后收集到氢气
,投入到足量水中,待充分反应后收集到氢气 (标准状况下),求未被氧化前金属钠质量是多少?写出计算过程
(标准状况下),求未被氧化前金属钠质量是多少?写出计算过程_____ 。
(1)已知酸性条件下,
 可将
可将 还原为
还原为 。将标准状况下
。将标准状况下 的
的 气体通入足量酸性
气体通入足量酸性 溶液中,
溶液中,①写出该反应的离子方程式
②被还原的
 的质量为
的质量为(2)为了检验某含有
 杂质的
杂质的 样品的纯度,现将
样品的纯度,现将 样品充分加热,当固体质量不再变化时,再次称量固体质量为
样品充分加热,当固体质量不再变化时,再次称量固体质量为 ,则该样品的纯度(质量分数)为
,则该样品的纯度(质量分数)为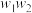 的代数式来表示)。
的代数式来表示)。(3)有一块表面氧化成氧化钠的金属钠,总质量为
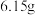 ,投入到足量水中,待充分反应后收集到氢气
,投入到足量水中,待充分反应后收集到氢气 (标准状况下),求未被氧化前金属钠质量是多少?写出计算过程
(标准状况下),求未被氧化前金属钠质量是多少?写出计算过程
您最近一年使用:0次
【推荐2】汽车尾气中CO、 以及燃煤废气中的
以及燃煤废气中的 都是大气污染物,对它们的治理具有重要意义。
都是大气污染物,对它们的治理具有重要意义。
 氧化还原法消除
氧化还原法消除 的转化如下所示:
的转化如下所示: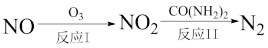
 反应Ⅰ为
反应Ⅰ为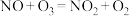 ,生成标准状况下
,生成标准状况下 L
L  时,转移电子的物质的量是
时,转移电子的物质的量是______
mol。
 反应Ⅱ中,当
反应Ⅱ中,当 :
: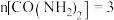 :2时,氧化产物与还原产物的质量比为
:2时,氧化产物与还原产物的质量比为______ 。
 使用“催化转化器”可以减少尾气中的CO和
使用“催化转化器”可以减少尾气中的CO和 ,转化过程中发生反应的化学方程式为
,转化过程中发生反应的化学方程式为 未配平
未配平 ,若
,若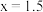 ,则方程式中
,则方程式中 和
和 的化学计量数之比为
的化学计量数之比为______ 。
 吸收
吸收 和NO,获得
和NO,获得 和
和 产品的流程图如图所示
产品的流程图如图所示 为铈元素
为铈元素 。
。

装置Ⅱ中,酸性条件下NO被 氧化的产物主要是
氧化的产物主要是 和
和 ,请写出生成等物质的量的
,请写出生成等物质的量的 和
和 时的离子方程式:
时的离子方程式:______ 。
 已知进入装置Ⅳ的溶液中
已知进入装置Ⅳ的溶液中 的浓度为a
的浓度为a  ,要使1
,要使1  该溶液中的
该溶液中的 完全转化为
完全转化为 ,至少需向装置Ⅳ中通入标准状况下的氧气
,至少需向装置Ⅳ中通入标准状况下的氧气______ 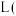 用含a代数式表示,结果保留整数
用含a代数式表示,结果保留整数 。
。
 以及燃煤废气中的
以及燃煤废气中的 都是大气污染物,对它们的治理具有重要意义。
都是大气污染物,对它们的治理具有重要意义。 氧化还原法消除
氧化还原法消除 的转化如下所示:
的转化如下所示: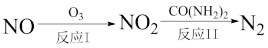
 反应Ⅰ为
反应Ⅰ为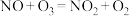 ,生成标准状况下
,生成标准状况下 L
L  时,转移电子的物质的量是
时,转移电子的物质的量是mol。
 反应Ⅱ中,当
反应Ⅱ中,当 :
: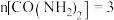 :2时,氧化产物与还原产物的质量比为
:2时,氧化产物与还原产物的质量比为 使用“催化转化器”可以减少尾气中的CO和
使用“催化转化器”可以减少尾气中的CO和 ,转化过程中发生反应的化学方程式为
,转化过程中发生反应的化学方程式为 未配平
未配平 ,若
,若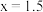 ,则方程式中
,则方程式中 和
和 的化学计量数之比为
的化学计量数之比为 吸收
吸收 和NO,获得
和NO,获得 和
和 产品的流程图如图所示
产品的流程图如图所示 为铈元素
为铈元素 。
。
装置Ⅱ中,酸性条件下NO被
 氧化的产物主要是
氧化的产物主要是 和
和 ,请写出生成等物质的量的
,请写出生成等物质的量的 和
和 时的离子方程式:
时的离子方程式: 已知进入装置Ⅳ的溶液中
已知进入装置Ⅳ的溶液中 的浓度为a
的浓度为a  ,要使1
,要使1  该溶液中的
该溶液中的 完全转化为
完全转化为 ,至少需向装置Ⅳ中通入标准状况下的氧气
,至少需向装置Ⅳ中通入标准状况下的氧气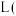 用含a代数式表示,结果保留整数
用含a代数式表示,结果保留整数 。
。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】某一反应体系有反应物和生成物共七种物质:O2,KMnO4,MnSO4,H2SO4,H2O,H2O2,K2SO4,已知H2O2只发生反应H2O2→O2,回答下列问题:
(1)该反应的氧化剂是________ 。
(2)氧化剂与还原剂的物质的量之比______________ 。
(3)若反应转移了0.3mol电子,则在标况下生成气体体积___________ 。
(1)该反应的氧化剂是
(2)氧化剂与还原剂的物质的量之比
(3)若反应转移了0.3mol电子,则在标况下生成气体体积
您最近一年使用:0次
【推荐2】氯酸钾和浓盐酸之间有下列反应:2KClO3+4HCl(浓)=2KCl+Cl2↑+2ClO2+2H2O。
(1)该反应中发生还原反应的物质是__________ ,氧化产物是___________ 。
(2)用双线桥标出方程式中的电子得失_______________________________ 。
(3)当有0.2mol电子发生转移时,生成的氯气的体积为____ L(标准状况)。被氧化的HCl的物质的量为____ mol。
(4)若分别用:
①2KMnO4+16HCl(浓)=2KCl+2MnCl2+8H2O+5Cl2↑
②MnO2+4HCl(浓)=MnCl2 +Cl2↑+2H2O
③Ca(ClO)2+4HCl(浓)=CaCl2+2Cl2↑+2H2O
用上述三种方法氧化浓盐酸制备氯气,当浓盐酸足量且这三种氧化剂的物质的量相同时,生成氯气的物质的量最少的是________ 。(填①或②或③)
(5)ClO2具有很强的氧化性。因此,常被用作消毒剂(还原产物为Cl-)其消毒的效率(以单位质量得到的电子数表示)是Cl2(消毒后还原产物也为Cl-)的__________ 倍(结果保留两位小数)。
(1)该反应中发生还原反应的物质是
(2)用双线桥标出方程式中的电子得失
(3)当有0.2mol电子发生转移时,生成的氯气的体积为
(4)若分别用:
①2KMnO4+16HCl(浓)=2KCl+2MnCl2+8H2O+5Cl2↑
②MnO2+4HCl(浓)=MnCl2 +Cl2↑+2H2O
③Ca(ClO)2+4HCl(浓)=CaCl2+2Cl2↑+2H2O
用上述三种方法氧化浓盐酸制备氯气,当浓盐酸足量且这三种氧化剂的物质的量相同时,生成氯气的物质的量最少的是
(5)ClO2具有很强的氧化性。因此,常被用作消毒剂(还原产物为Cl-)其消毒的效率(以单位质量得到的电子数表示)是Cl2(消毒后还原产物也为Cl-)的
您最近一年使用:0次
【推荐3】(1)在 2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O的反应中,_____________ 是氧化剂,________ 元素被氧化,氧化产物是________________ ,还原产物是_______________ 。
(2)在 P+CuSO4+H2O→Cu3P+H3PO4+H2SO4(未配平)的反应中,7.5 mol CuSO4可氧化P的物质的量为______ mol。 生成1 mol Cu3P时,参加反应的P的物质的量为_________ mol。
(2)在 P+CuSO4+H2O→Cu3P+H3PO4+H2SO4(未配平)的反应中,7.5 mol CuSO4可氧化P的物质的量为
您最近一年使用:0次



