写出298K时,下列反应的热化学方程式
(1)28 g CO还原Fe2O3生成单质铁,放出8.3 kJ热量;_________________________
(2)N2和O2化合生成184 g NO2气体,吸收热量135.4 kJ;__________________________
(1)28 g CO还原Fe2O3生成单质铁,放出8.3 kJ热量;
(2)N2和O2化合生成184 g NO2气体,吸收热量135.4 kJ;
11-12高二上·河南许昌·阶段练习 查看更多[1]
(已下线)2011-2012年河南省长葛市第三实验高中高二上学期第一次月考化学试卷
更新时间:2011-11-10 21:58:51
|
相似题推荐
计算题
|
适中
(0.65)
【推荐1】铜与浓硝酸反应的方程式为:
(1)在该反应中,被还原的元素是_______ ,氧化产物是_______ 。
(2)在方程式标出电子转移的方向和数目_______ 。
(3)若有32g铜参与反应,被还原的硝酸有_______ mol。

(1)在该反应中,被还原的元素是
(2)在方程式标出电子转移的方向和数目
(3)若有32g铜参与反应,被还原的硝酸有
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】取48.0gFe2O3,一定温度下加热,残留固体47.36g。将该剩余固体溶于足量盐酸,此过程没有气体产生;所得溶液中再加入足量KI溶液。请计算:
(1)生成I2的物质的量_____ 。
(2)若分解产物为Fe3O4,求Fe2O3的分解率_____ 。
(1)生成I2的物质的量
(2)若分解产物为Fe3O4,求Fe2O3的分解率
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】0.3mol的气态高能燃料乙硼烷(B2H6)在氧气中燃烧,生成固态三化二硼和液态水,放出649.5kJ热量, 又已知:H2O(l)=H2O(g) ΔH=+44kJ/mol,则0.5mol乙硼烷完全燃烧生成气态水时放出的热量是_____ 。
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】(1)已知下列反应的焓变
①CH3COOH(l)+2O2(g)=2CO2(g)+2H2O(l) △H1=-870.3kJ/mol
②C(s)+O2(g) =CO2(g) △H2=-393.5kJ/mol
③2H2(g)+O2(g) =2H2O(l) △H3=-285.8kJ/mol
试计算反应CH3COOH(l) = 2C(s)+2H2(g)+O2(g)的焓变ΔH=_____________ 。
(2)实验测得,5g液态甲醇(CH3OH)在氧气中充分燃烧生成二氧化碳气体和液态水时释放出113.5kJ的热量,试写出表示甲醇燃烧热的热化学方程式:_________________________________________ 。
(3)火箭推进器常以气态联氨(N2H4)为燃料、液态过氧化氢为助燃剂进行热能提供.反应过程中生成的气体可参与大气循环。测得当反应过程中有1mol水蒸气生成时放出161kJ的热量.试写出反应过程中的热化学方程式:___________________________ 。
①CH3COOH(l)+2O2(g)=2CO2(g)+2H2O(l) △H1=-870.3kJ/mol
②C(s)+O2(g) =CO2(g) △H2=-393.5kJ/mol
③2H2(g)+O2(g) =2H2O(l) △H3=-285.8kJ/mol
试计算反应CH3COOH(l) = 2C(s)+2H2(g)+O2(g)的焓变ΔH=
(2)实验测得,5g液态甲醇(CH3OH)在氧气中充分燃烧生成二氧化碳气体和液态水时释放出113.5kJ的热量,试写出表示甲醇燃烧热的热化学方程式:
(3)火箭推进器常以气态联氨(N2H4)为燃料、液态过氧化氢为助燃剂进行热能提供.反应过程中生成的气体可参与大气循环。测得当反应过程中有1mol水蒸气生成时放出161kJ的热量.试写出反应过程中的热化学方程式:
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】根据要求写出下列反应的热化学方程式
(1)一定量氢气与氯气反应生成氯化氢气体,当生成1mol氢氯键时放出91.5kJ的热量______________________ .
(2)某化学反应的能量变化如图所示,该反应的热化学方程式是(反应热用abc表示)_____________________ .

(3)某反应的平衡常数 如果有1molN2完全反应,要吸收热量68kJ.写出该反应的热化学方程式
如果有1molN2完全反应,要吸收热量68kJ.写出该反应的热化学方程式_______________ .
(4)实验中不能直接测出石墨和氢气生成甲烷反应的反应热,但可测出甲烷、石墨、氢气燃烧的反应热:
CH4(g)+2O2(g)=CO2(g)+2H2O(l);△H1=-890.3kJ/mol
C(石墨,s)+O2(g)=CO2(g) ;ΔH2=-393.5 kJ/mol
H2(g)+1/2O2(g)=H2O(l) ;△H3=-285.8 kJ/moL
则由石墨与氢气反应生成甲烷的热化学反应方程式为____________________ .
(1)一定量氢气与氯气反应生成氯化氢气体,当生成1mol氢氯键时放出91.5kJ的热量
(2)某化学反应的能量变化如图所示,该反应的热化学方程式是(反应热用abc表示)

(3)某反应的平衡常数
 如果有1molN2完全反应,要吸收热量68kJ.写出该反应的热化学方程式
如果有1molN2完全反应,要吸收热量68kJ.写出该反应的热化学方程式(4)实验中不能直接测出石墨和氢气生成甲烷反应的反应热,但可测出甲烷、石墨、氢气燃烧的反应热:
CH4(g)+2O2(g)=CO2(g)+2H2O(l);△H1=-890.3kJ/mol
C(石墨,s)+O2(g)=CO2(g) ;ΔH2=-393.5 kJ/mol
H2(g)+1/2O2(g)=H2O(l) ;△H3=-285.8 kJ/moL
则由石墨与氢气反应生成甲烷的热化学反应方程式为
您最近一年使用:0次
【推荐1】氢气作为一种清洁能源,一直是能源研究的热点,工业上制取氢气有多种方法:
①C(s)+H2O(g)=CO(g)+H2(g) △H1=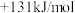
②CH4 (g)+CO2(g)=2CO(g)+2H2 (g) △H2=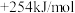
③CH4 (g)+H2O(g)=CO(g)+3H2 (g) △H3=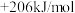
④CH3OH(1)=CO(g)+2H2 (g) △H4=
(1)根据以上数据,请写出CH4(g)分解生成C(s)和H2(g)的热化学方程式______ 。
(2)几种化学键的键能如下表所示:
根据以上有关反应的△H,计算 x=______ 。
(3)我国科学家通过计算机模拟,研究了在某催化剂表面上发生反应④的反应历程(吸附在催化剂表面的物质,用"*"标注)。甲醇(CH3OH)脱氢反应的第一步历程,有两种可能方式:
方式Ⅰ: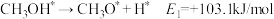
方式Ⅱ:
活化能E值推测,甲醇脱氢过程中主要历程的方式为______ (填"Ⅰ"或"Ⅱ")。计算机模拟的各步反应的能量变化示意图如下。

该历程中最大能垒(活化能)E正=______ kJ/mol,写出该步骤的化学方程式______ 。
①C(s)+H2O(g)=CO(g)+H2(g) △H1=
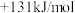
②CH4 (g)+CO2(g)=2CO(g)+2H2 (g) △H2=
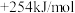
③CH4 (g)+H2O(g)=CO(g)+3H2 (g) △H3=
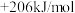
④CH3OH(1)=CO(g)+2H2 (g) △H4=

(1)根据以上数据,请写出CH4(g)分解生成C(s)和H2(g)的热化学方程式
(2)几种化学键的键能如下表所示:
| 化学键 | C=O | H—H | 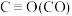 | C—H | O—H |
| 键能/kJ·mol-1 | 803 | 436 | x | 414 | 463 |
根据以上有关反应的△H,计算 x=
(3)我国科学家通过计算机模拟,研究了在某催化剂表面上发生反应④的反应历程(吸附在催化剂表面的物质,用"*"标注)。甲醇(CH3OH)脱氢反应的第一步历程,有两种可能方式:
方式Ⅰ:
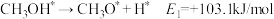
方式Ⅱ:

活化能E值推测,甲醇脱氢过程中主要历程的方式为

该历程中最大能垒(活化能)E正=
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】Ⅰ.已知下列热化学方程式:
①2C(s)+O2(g)=2CO(g) ΔH=-220.0 kJ•mol-1;
②C(s)+O2(g)=CO2(g) ΔH =-393.5 kJ•mol-1;
③2CO(g)+O2(g)=2CO2(g) ΔH =-566.0 kJ•mol-1;
④CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH =-890.0 kJ•mol-1。
请回答下列问题:
(1)CO的燃烧热为________________ 。
(2)炽热的木炭与二氧化碳反应生成一氧化碳的反应为___ (填“放热”或“吸热”)反应,理由是____________ 。
(3)写出甲烷与氧气反应生成CO的热化学方程式:_________________________ 。
Ⅱ.常温常压下,一定质量的无水乙醇(C2H5OH)完全燃烧时放出热量Q kJ,其燃烧生成的CO2用过量饱和石灰水吸收可得100 g CaCO3沉淀,请写出乙醇燃烧的热化学方程式__________________________ 。
①2C(s)+O2(g)=2CO(g) ΔH=-220.0 kJ•mol-1;
②C(s)+O2(g)=CO2(g) ΔH =-393.5 kJ•mol-1;
③2CO(g)+O2(g)=2CO2(g) ΔH =-566.0 kJ•mol-1;
④CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH =-890.0 kJ•mol-1。
请回答下列问题:
(1)CO的燃烧热为
(2)炽热的木炭与二氧化碳反应生成一氧化碳的反应为
(3)写出甲烷与氧气反应生成CO的热化学方程式:
Ⅱ.常温常压下,一定质量的无水乙醇(C2H5OH)完全燃烧时放出热量Q kJ,其燃烧生成的CO2用过量饱和石灰水吸收可得100 g CaCO3沉淀,请写出乙醇燃烧的热化学方程式
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐3】研究化学反应中的能量变化有重要意义。请根据学过的知识回答下列问题:
(1)已知一氧化碳与水蒸气反应过程的能量变化如图所示:

反应的热化学方程式为____________________________ 。
(2)化学反应可视为旧键断裂和新键形成的过程。化学键的键能是形成(或拆开)1 mol化学键时释放(或吸收)的能量。已知:N≡N键的键能是948.9 kJ•mol−1,H—H键的键能是436.0 kJ•mol−1,N—H键的键能是391.55 kJ•mol−1,则1/2N2(g)+3/2H2(g) NH3(g) ΔH=
NH3(g) ΔH=_____________________ 。
(3)依据盖斯定律可以对某些难以通过实验直接测定的化学反应的焓变进行推算。
已知:①C(s,石墨)+O2(g) CO2(g) ΔH1=−393.5 kJ•mol−1
CO2(g) ΔH1=−393.5 kJ•mol−1
②2H2(g)+O2(g) 2H2O(l) ΔH2=−571.6 kJ•mol−1
2H2O(l) ΔH2=−571.6 kJ•mol−1
③2C2H2(g)+5O2(g) 4CO2(g)+2H2O(l)ΔH3=−2599 kJ•mol−1
4CO2(g)+2H2O(l)ΔH3=−2599 kJ•mol−1
298 K时反应2C(s,石墨)+H2(g)=C2H2(g)的焓变:ΔH=_____________________ 。
(4)已知:铝热反应是放热反应,又知,常温下: 4Al(s)+3O2(g) 2Al2O3(s) ΔH1
2Al2O3(s) ΔH1
4Fe(s)+3O2(g) 2Fe2O3(s) ΔH2
2Fe2O3(s) ΔH2
下面关于ΔH1、ΔH2的比较正确的是________
A.ΔH1>ΔH2 B.ΔH1<ΔH2 C.ΔH1=ΔH2 D.无法计算
(1)已知一氧化碳与水蒸气反应过程的能量变化如图所示:

反应的热化学方程式为
(2)化学反应可视为旧键断裂和新键形成的过程。化学键的键能是形成(或拆开)1 mol化学键时释放(或吸收)的能量。已知:N≡N键的键能是948.9 kJ•mol−1,H—H键的键能是436.0 kJ•mol−1,N—H键的键能是391.55 kJ•mol−1,则1/2N2(g)+3/2H2(g)
 NH3(g) ΔH=
NH3(g) ΔH=(3)依据盖斯定律可以对某些难以通过实验直接测定的化学反应的焓变进行推算。
已知:①C(s,石墨)+O2(g)
 CO2(g) ΔH1=−393.5 kJ•mol−1
CO2(g) ΔH1=−393.5 kJ•mol−1②2H2(g)+O2(g)
 2H2O(l) ΔH2=−571.6 kJ•mol−1
2H2O(l) ΔH2=−571.6 kJ•mol−1③2C2H2(g)+5O2(g)
 4CO2(g)+2H2O(l)ΔH3=−2599 kJ•mol−1
4CO2(g)+2H2O(l)ΔH3=−2599 kJ•mol−1298 K时反应2C(s,石墨)+H2(g)=C2H2(g)的焓变:ΔH=
(4)已知:铝热反应是放热反应,又知,常温下: 4Al(s)+3O2(g)
 2Al2O3(s) ΔH1
2Al2O3(s) ΔH14Fe(s)+3O2(g)
 2Fe2O3(s) ΔH2
2Fe2O3(s) ΔH2下面关于ΔH1、ΔH2的比较正确的是
A.ΔH1>ΔH2 B.ΔH1<ΔH2 C.ΔH1=ΔH2 D.无法计算
您最近一年使用:0次



