氯及其化合物有广泛用途。二氧化氯是一种新型的消毒剂。
①NaClO2中Cl的化合价为____________ 。
②实验室用氯酸钾与浓盐酸反应制备ClO2,产物除ClO2外,还有Cl2,KCl等,写出该反应的化学方程式__________ 。若生成11.2L氯气(标准状况),转移电子数为_________ 。
③ClO2和Cl2在消毒时自身均被还原为Cl-,则常温常压下,等体积的ClO2的消毒能力是Cl2的_________ 倍。
④自来水厂用ClO2处理后的水中,要求ClO2的浓度在0.1﹣0.8 mg•L-1之间。碘量法可以检测水中ClO2的浓度(不同pH环境中粒子种类如图所示),步骤如下:
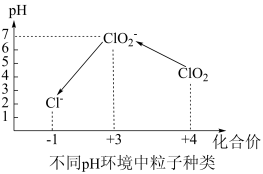
Ⅰ.取一定体积的水样,加入一定量的碘化钾,再将反应后溶液调至中性,并加入淀粉溶液,溶液变蓝。
Ⅱ.加入一定量的Na2S2O3溶液。(已知:2S2O32-+I2═S4O62-+2I-)
Ⅲ.加硫酸调节水样pH至1﹣3。
请问答:
若水样的体积为1.0L,在操作II时消耗了1.0×10-3mol•L-1的Na2S2O3溶液10mL.则水样中ClO2的浓度是_____ mg•L-1。
①NaClO2中Cl的化合价为
②实验室用氯酸钾与浓盐酸反应制备ClO2,产物除ClO2外,还有Cl2,KCl等,写出该反应的化学方程式
③ClO2和Cl2在消毒时自身均被还原为Cl-,则常温常压下,等体积的ClO2的消毒能力是Cl2的
④自来水厂用ClO2处理后的水中,要求ClO2的浓度在0.1﹣0.8 mg•L-1之间。碘量法可以检测水中ClO2的浓度(不同pH环境中粒子种类如图所示),步骤如下:

Ⅰ.取一定体积的水样,加入一定量的碘化钾,再将反应后溶液调至中性,并加入淀粉溶液,溶液变蓝。
Ⅱ.加入一定量的Na2S2O3溶液。(已知:2S2O32-+I2═S4O62-+2I-)
Ⅲ.加硫酸调节水样pH至1﹣3。
请问答:
若水样的体积为1.0L,在操作II时消耗了1.0×10-3mol•L-1的Na2S2O3溶液10mL.则水样中ClO2的浓度是
更新时间:2020-01-23 20:39:32
|
相似题推荐
计算题
|
适中
(0.65)
解题方法
【推荐1】将某质量的镁铝合金溶解在500 mL盐酸中,向反应后的溶液中逐滴加入2 mol/L NaOH溶液,产生沉淀质量与碱溶液体积的关系如图所示。请填写下列空白:
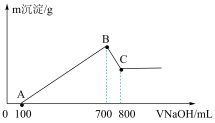
(1)写出BC段发生反应的化学方程式:_______ 。
(2)合金中铝的质量为_______ 。
(3)盐酸的物质的量浓度(假设反应后溶液体积不变)是_______ 。

(1)写出BC段发生反应的化学方程式:
(2)合金中铝的质量为
(3)盐酸的物质的量浓度(假设反应后溶液体积不变)是
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】(1)在一定条件下,将NH4HCO3受热分解生成NH3、CO2、H2O(g),得到的混合气体的平均摩尔质量为_______ g/mol(保留小数点后一位)。
(2)在10.0 mL0.1 mol/LNa2CO3溶液中逐滴加入0.1 mol/L的稀盐酸,边加边振荡,若使反应不产生CO2气体,加入的稀盐酸的体积最多不超过_______ mL。
(3)将不纯的NaOH样品1 g (样品含少量Na2CO3和水),放入50 mL 2 mol/L的盐酸中,充分反应后,溶液呈酸性,中和多余的酸又用去40 mL1 mol/L的NaOH溶液,蒸发中和后的溶液,最终得到_______  的固体。
的固体。
(2)在10.0 mL0.1 mol/LNa2CO3溶液中逐滴加入0.1 mol/L的稀盐酸,边加边振荡,若使反应不产生CO2气体,加入的稀盐酸的体积最多不超过
(3)将不纯的NaOH样品1 g (样品含少量Na2CO3和水),放入50 mL 2 mol/L的盐酸中,充分反应后,溶液呈酸性,中和多余的酸又用去40 mL1 mol/L的NaOH溶液,蒸发中和后的溶液,最终得到
 的固体。
的固体。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】(1)等质量的①H2②O2③N2④CO2所含分子数最多的是___ 。
(2)要使NH3与CH4含有相同数目的H原子,则NH3与CH4的物质的量之比为___ 。
(3)在一定的条件下,56.0gM单质与1.50molCl2恰好完全反应,生成1.00molMClx,则x=___ ,M的摩尔质量为___ 。
(4)已知铵盐与碱混合加热时可生成NH3,如:NH4Cl+NaOH NaCl+NH3↑+H2O。将100mL(NH4)2SO4与NH4Cl的混合液分两等份,一份需要用0.5mol烧碱恰好把NH3赶出,另一份与0.2molBaCl2恰好反应,则原溶液中Cl-的物质的量浓度为
NaCl+NH3↑+H2O。将100mL(NH4)2SO4与NH4Cl的混合液分两等份,一份需要用0.5mol烧碱恰好把NH3赶出,另一份与0.2molBaCl2恰好反应,则原溶液中Cl-的物质的量浓度为___ 。
(2)要使NH3与CH4含有相同数目的H原子,则NH3与CH4的物质的量之比为
(3)在一定的条件下,56.0gM单质与1.50molCl2恰好完全反应,生成1.00molMClx,则x=
(4)已知铵盐与碱混合加热时可生成NH3,如:NH4Cl+NaOH
 NaCl+NH3↑+H2O。将100mL(NH4)2SO4与NH4Cl的混合液分两等份,一份需要用0.5mol烧碱恰好把NH3赶出,另一份与0.2molBaCl2恰好反应,则原溶液中Cl-的物质的量浓度为
NaCl+NH3↑+H2O。将100mL(NH4)2SO4与NH4Cl的混合液分两等份,一份需要用0.5mol烧碱恰好把NH3赶出,另一份与0.2molBaCl2恰好反应,则原溶液中Cl-的物质的量浓度为
您最近一年使用:0次
【推荐1】①已知白磷和氯酸溶液可发生如下反应,将该反应进行配平:
______ P4+_______ HClO3+_______ ______ =______ HCl+____ H3PO4
②白磷有毒,有实验室可采用CuSO4溶液进行处理,其反应为:11P4+60CuSO4+96H2O=20Cu3P+24H3PO4+60H2SO4
在该反应中30 mol CuSO4可氧化P4的物质的量是______ mol.
②白磷有毒,有实验室可采用CuSO4溶液进行处理,其反应为:11P4+60CuSO4+96H2O=20Cu3P+24H3PO4+60H2SO4
在该反应中30 mol CuSO4可氧化P4的物质的量是
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】(1)实验室由Al盐制备Al(OH)3最佳选择NH3·H2O,其离子反应方程式:____________________________
(2)12.4g Na2X含有0.4mol Na+, Na2X的摩尔质量为________ 。
(3)由氨气和氢气组成的混合气体的平均相对分子质量为12,则氨气和氢气的物质的量之比为_________
(4)已知 离子可与R2-离子反应,R2-被氧化为R单质,
离子可与R2-离子反应,R2-被氧化为R单质, 的还原产物中M为+3价;又已知100mL c(
的还原产物中M为+3价;又已知100mL c( )=0.2 mol·L-1的溶液可与100mL c(R2- )=0.6 mol·L-1的溶液恰好完全反应,则n值为
)=0.2 mol·L-1的溶液可与100mL c(R2- )=0.6 mol·L-1的溶液恰好完全反应,则n值为__________
A.4 B.5 C.6 D.7
(2)12.4g Na2X含有0.4mol Na+, Na2X的摩尔质量为
(3)由氨气和氢气组成的混合气体的平均相对分子质量为12,则氨气和氢气的物质的量之比为
(4)已知
 离子可与R2-离子反应,R2-被氧化为R单质,
离子可与R2-离子反应,R2-被氧化为R单质, 的还原产物中M为+3价;又已知100mL c(
的还原产物中M为+3价;又已知100mL c( )=0.2 mol·L-1的溶液可与100mL c(R2- )=0.6 mol·L-1的溶液恰好完全反应,则n值为
)=0.2 mol·L-1的溶液可与100mL c(R2- )=0.6 mol·L-1的溶液恰好完全反应,则n值为A.4 B.5 C.6 D.7
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】一个体重50 kg的健康人身体中含铁2 g。铁在人体中不是以游离态的形式存在,而是以Fe2+和Fe3+形式存在。Fe2+易被吸收,给贫血者补充铁时,应给予含Fe2+的盐,如硫酸亚铁(FeSO4)。人体中经常进行Fe2+和Fe3+的转化,服用维生素C,可使食物中的Fe3+转化为Fe2+”,说明维生素C具有__________ 性。
(2)羟胺(NH2OH)是一种还原剂,用25.00 mL 0.049 mol/L羟胺的酸性溶液跟足量的硫酸铁溶液在煮沸条件下反应,生成的Fe2+离子恰好与24.5 mL 0.020 mol/L的KMnO4酸性溶液反应。则在上述反应中,羟胺的氧化产物是_________________ 。
(2)羟胺(NH2OH)是一种还原剂,用25.00 mL 0.049 mol/L羟胺的酸性溶液跟足量的硫酸铁溶液在煮沸条件下反应,生成的Fe2+离子恰好与24.5 mL 0.020 mol/L的KMnO4酸性溶液反应。则在上述反应中,羟胺的氧化产物是
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐1】为了测定铁铜合金的组成,将15.2 g铁铜合金加入200 mL某浓度的稀硝酸中,待合金完全溶解,共生成NO气体4.48 L(标准状况下),并测得溶液中H+的物质的量浓度为0.5 mol·L-1,若反应前后溶液的体积变化忽略不计
(1)n(Fe)=_________ n(Cu)=_________
(2)硝酸的物质的量浓度为______________
(1)n(Fe)=
(2)硝酸的物质的量浓度为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】向铁和氧化铁的混合物中加入500mL0.20mol·L-1稀盐酸后恰好完全反应,得到只含一种金属离子的浅绿色溶液,并收集到448mL氢气(标准状况下测定)。回答下列问题;
(1)反应后溶液中的溶质为_______ (填写化学式)。
(2)反应后溶液中的溶质为_______ mol。
(3)原混合物中单质铁的质量为_______ g。
(1)反应后溶液中的溶质为
(2)反应后溶液中的溶质为
(3)原混合物中单质铁的质量为
您最近一年使用:0次

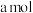 ,其中
,其中 的物质的量分数为b,将其全部投入
的物质的量分数为b,将其全部投入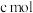 的稀硝酸中,加热使其充分反应(假设
的稀硝酸中,加热使其充分反应(假设 是唯一的还原产物)。
是唯一的还原产物)。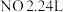 ,则反应转移电子的物质的量为
,则反应转移电子的物质的量为
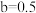 ,溶液中的
,溶液中的 与
与 的物质的量之比
的物质的量之比 ,标准状况下产生
,标准状况下产生 ,
,


