向铁和氧化铁的混合物中加入500mL0.20mol·L-1稀盐酸后恰好完全反应,得到只含一种金属离子的浅绿色溶液,并收集到448mL氢气(标准状况下测定)。回答下列问题;
(1)反应后溶液中的溶质为_______ (填写化学式)。
(2)反应后溶液中的溶质为_______ mol。
(3)原混合物中单质铁的质量为_______ g。
(1)反应后溶液中的溶质为
(2)反应后溶液中的溶质为
(3)原混合物中单质铁的质量为
20-21高一下·浙江·期中 查看更多[3]
浙江省北斗联盟2020-2021学年高一下学期期中联考化学试题(已下线)新人教必修1第3章第二节第2课时物质的量在化学方程式金属中的应用(课后)(已下线)专题02 化学计算中常用的几种方法-2022年高考化学毕业班二轮热点题型归纳与变式演练(全国通用)
更新时间:2021-05-28 19:32:55
|
相似题推荐
计算题
|
适中
(0.65)
【推荐1】铜既能与稀硝酸反应,也能与浓硝酸反应,现将32 g Cu投入50 mL 12 mol/L的浓硝酸中,充分反应后,收集到4.48 L(标准状态)NO和NO2的混合气体。(Cu的相对原子质量为64)
(1)被还原硝酸的物质的量是_______ mol。
(2)反应后溶液中有_______ mol NO ,所以,剩余
,所以,剩余_______ (填反应物的化学式),其物质的量是_______ mol。
(3)如果往反应后的体系内再加入100 mL0.4 mol/L的稀硫酸,又会有气体逸出,离子反应方程式为_______ ,产生的气体在标准状况下的体积为_______ mL。
(1)被还原硝酸的物质的量是
(2)反应后溶液中有
 ,所以,剩余
,所以,剩余(3)如果往反应后的体系内再加入100 mL0.4 mol/L的稀硫酸,又会有气体逸出,离子反应方程式为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】(1)2molO3和3molO2的质量之比_______ ,分子数之比______ ,同温同压下密度之比________ ,含氧原子数之比______ ,体积之比______ 。
(2)O3与Cl2具有相似的性质,均可用于自来水的消毒。已知二者在消毒时均被还原为最低价态,则相同状况下10LO3与______ LCl2的消毒能力相当。
(3)气体化合物A分子式可表示为OxFy,已知同温同压下10mLA受热分解生成15mLO2和10mLF2,则A的化学式为_________ 。
(2)O3与Cl2具有相似的性质,均可用于自来水的消毒。已知二者在消毒时均被还原为最低价态,则相同状况下10LO3与
(3)气体化合物A分子式可表示为OxFy,已知同温同压下10mLA受热分解生成15mLO2和10mLF2,则A的化学式为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐3】取部分被氧化的铁粉若干克,将其溶于 200mL 某浓度的硝酸溶液中,恰好完全反应,并释放出448mL NO(标准状况下)。将所得溶液平均分为两份,向第一份溶液中加入足量氢氧化钠溶液,过滤、 洗涤、灼烧,得到 8.00g 红棕色固体;向第二份溶液中通入 672mL Cl2(标准状况下),恰好完全反应(不考虑氯气的溶解)。试计算:
(1)样品和硝酸反应后的溶液中,n(Fe2+) : n(Fe3+) =_______ 。
(2)原硝酸溶液的浓度 c =_______ mol/L。
(1)样品和硝酸反应后的溶液中,n(Fe2+) : n(Fe3+) =
(2)原硝酸溶液的浓度 c =
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】ag铁粉和铜粉的混合物加入到100mLbmol•L-1FeCl3溶液中,固体全部溶解,再向此溶液中不断加入铁粉,当铁粉质量加至0.1ag后开始有固体析出,当铁粉加至ag时,剩余固体质量为ag。
(1)a与b的关系为___
(2)ag铁粉和铜粉的混合物中铁粉的质量为___ g(用含a的式子表示)。
(1)a与b的关系为
(2)ag铁粉和铜粉的混合物中铁粉的质量为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】有一稀硫酸和硝酸铁的混合溶液,向其中加入铁粉,溶液中的Fe2+浓度如图所示(不考虑溶液体积的变化):
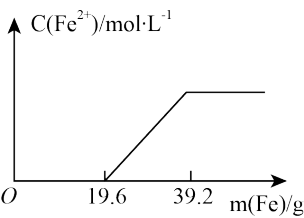
溶液中H2SO4与Fe(NO3)3的物质的量之比为_______

溶液中H2SO4与Fe(NO3)3的物质的量之比为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐3】电子工业常用一定浓度的FeCl3溶液腐蚀敷有铜箔的绝缘板,制成印刷线路板。现将一块敷有铜箔的绝缘板没入500mL某浓度FeCl3溶液中,一段时间后,将该线路板取出,向所得溶液中加入一定量的铁粉,充分反应后有固体剩余;将固体滤出并从滤液中取出20.00mL,向其中滴入2.00mol/LAgNO3溶液60.00 mL时,溶液中的Cl-恰好完全沉淀。请回答下列有关问题(忽略反应前后溶液体积的变化):
(1)原FeCl3溶液的物质的量浓度为_____________________ 。
(2)假若剩余固体中有铁粉,则向溶液中加入的铁粉质量至少应当大于_______________________ 。
(1)原FeCl3溶液的物质的量浓度为
(2)假若剩余固体中有铁粉,则向溶液中加入的铁粉质量至少应当大于
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】取Al2O3和Fe2O3混合物10.0 g,加入200 mL过量稀硫酸将固体完全溶解,加水稀释形成250 mL溶液,取25.0 mL逐滴滴加2.0 mol·L-1的NaOH溶液,得到如图所示的变化关系。
已知Al(OH)3能被过量NaOH溶解:Al(OH)3+NaOH===NaAlO2+2H2O
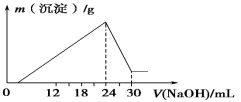
求原稀硫酸物质的量浓度。___________________
已知Al(OH)3能被过量NaOH溶解:Al(OH)3+NaOH===NaAlO2+2H2O

求原稀硫酸物质的量浓度。
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】某红色固体粉末可能是 、
、 或二者混合物,为探究其组成,称取
或二者混合物,为探究其组成,称取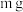 该固体粉末样品,用足量的稀
该固体粉末样品,用足量的稀 充分反应,反应后得到的固体质量为
充分反应,反应后得到的固体质量为 。
。
已知:
(1)若红色固体粉末为纯净物,则
___________ (用含m的最简式表示)。
(2)若 ,计算溶液中
,计算溶液中 与
与 的物质的量之比
的物质的量之比___________ (写出计算过程)。
 、
、 或二者混合物,为探究其组成,称取
或二者混合物,为探究其组成,称取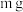 该固体粉末样品,用足量的稀
该固体粉末样品,用足量的稀 充分反应,反应后得到的固体质量为
充分反应,反应后得到的固体质量为 。
。已知:

(1)若红色固体粉末为纯净物,则

(2)若
 ,计算溶液中
,计算溶液中 与
与 的物质的量之比
的物质的量之比
您最近一年使用:0次
【推荐1】合成氨工业生产中所用的α—Fe催化剂的主要成分为FeO、Fe2O3。
(1)某FeO、Fe2O3混合物中,铁、氧的物质的量之比为4:5,其中Fe2+与Fe3+物质的量之比为
(2)当催化剂中Fe2+与Fe3+的物质的量之比为1:2时,其催化剂活性最高,此时混合物中铁的质量分数为
(3)写出由C(炭粉)与Fe2O3在高温下反应制备α—Fe催化剂的化学方程式(另一种产物可溶于水):
(4)为制得这种活性最高的催化剂,理论上应向480gFe2O3粉末加入炭粉的质量是
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】铁粉和氧化铁粉末的混合物共13.6g,加入到200mL的稀硫酸中,固体完全溶解,得到标准状况下1.12L 氢气。经测定,反应后的溶液中c (H+) 为0.200mol·L-1,且无Fe3+(忽略反应前后溶液体积变化)。请计算:
(1)原混合物中铁和氧化铁的物质的量之比为_____________ 。
(2)原稀硫酸的物质的量浓度为______________ mol·L-1。
(1)原混合物中铁和氧化铁的物质的量之比为
(2)原稀硫酸的物质的量浓度为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】向一定量的Fe、FeO、Fe2O3的混合物中,加入100mL l.0mol·L−1的盐酸,恰好使混合物完全溶解并放出约224mL(标准状况)气体,溶液体积仍为100mL,所得溶液中加入KSCN溶液无血红色出现。
请回答下列问题:
(1)生成的气体为__________ (填化学式),物质的量为__________ mol。
(2)所得溶液中溶质为__________ (填化学式),物质的量浓度为__________ mol·L−1。
(3)若用足量的CO在高温下还原相同质量的该混合物,最多能得到单质铁的质量为__________ g。
(4)该混合物中铁原子与氧原子的个数比N(Fe)∶N(O)=__________ 。
请回答下列问题:
(1)生成的气体为
(2)所得溶液中溶质为
(3)若用足量的CO在高温下还原相同质量的该混合物,最多能得到单质铁的质量为
(4)该混合物中铁原子与氧原子的个数比N(Fe)∶N(O)=
您最近一年使用:0次



