短周期主族元素W、X、Y、Z原子序数依次增大,Z的最外层最高能级上只有1个未成对的电子,Y的最高价氧化物能与X、Z的最高价氧化物对应的水化物反应,W的简单氢化物与其含氧酸反应能生成盐。下列说法正确的是
| A.W的简单氢化物及其最高价含氧酸根中W原子的杂化方式相同 |
| B.电解X、Y与Z生成的二元化合物可生成X、Y的单质 |
C.W、X、Z的简单氢化物的沸点: |
| D.W与X形成的化合物中可能含有非极性键 |
更新时间:2024-02-05 19:04:06
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列图中的实验方案,能达到实验目的是
| A | B | C | D | |
| 实验 方案 | 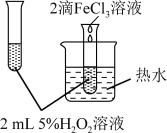 | 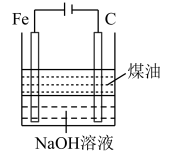 | 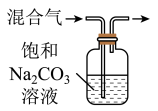 |  |
| 实验 目的 | 验证FeCl3对H2O2分解反应有催化作用 | 制备Fe(OH)2并能较长时间观察其颜色 | 除去CO2气体中混有的SO2 | 比较HCl、H2CO3和H2SiO3的酸性强弱 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】短周期主族元素X、Y、Z、W的原子序数依次增大。X原子的最外层电子数是其内层电子数的2倍,Y是地壳中含量最高的元素,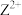 与
与 具有相同的电子层结构,W与Y同主族。下列说法不正确的是
具有相同的电子层结构,W与Y同主族。下列说法不正确的是
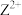 与
与 具有相同的电子层结构,W与Y同主族。下列说法不正确的是
具有相同的电子层结构,W与Y同主族。下列说法不正确的是A.原子半径的大小顺序: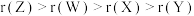 |
| B.Y与Z形成的化合物能与碱反应 |
| C.X的最高价氧化物对应的水化物的酸性比W的弱 |
| D.Y的简单氢化物的沸点比W的高 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】X、Y、Z、W是原子序数依次增大的前四周期元素,X的价层电子排布式为nsnnpn,基态Y原子的未成对电子数为2,基态Z原子的M能层电子只有1种自旋状态,W3+的3d轨道处于半充满状态,下列说法错误的是
| A.Y与X、Z元素均能形成常见的两种化合物 |
| B.由X、Y、Z三种元素形成的化合物,其水溶液可能呈酸性 |
| C.基态W原子的未成对电子数为4 |
D. 中的各原子均满足8电子稳定结构 中的各原子均满足8电子稳定结构 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中T所处的周期序数与主族序数相等,下列叙述错误的是


| A.Q和W元素形成化合物QW2分子中,各原子的最外层均满足8电子的稳定结构 |
| B.T的氧化物能与NaOH溶液反应 |
| C.R元素的气态氢化物能与其最高价氧化物对应的水化物反应 |
| D.元素的非金属性:Q强于W |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】用图示的方法能够直观形象地将化学知识传授给学生。下列说法正确的是
A.溴原子的结构示意图为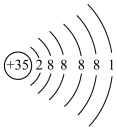 |
B.轨道表示式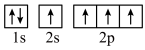 表示的碳原子处于基态 表示的碳原子处于基态 |
C.NH 的电子式为 的电子式为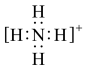 ,形状为平面正方形 ,形状为平面正方形 |
D.SO 的VSEPR模型为 的VSEPR模型为 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列说法正确的是
A.基态Cu的核外电子排布式为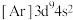 |
B. 中B的杂化方式为 中B的杂化方式为 杂化 杂化 |
C. 分子为非极性分子 分子为非极性分子 |
D. 的稳定性强于 的稳定性强于 的原因为 的原因为 存在分子间氢键 存在分子间氢键 |
您最近半年使用:0次


 、
、 均为分子晶体
均为分子晶体




