回答下列问题:
I.高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂,比 Cl2、O2、ClO2、KMnO4 氧化性更强,无二次污染,工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH 至饱和,使高铁酸钾析出。
(1)干法制备高铁酸钠的主要反应为2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑,该反应中还原剂是_____ 。(填化学式)
(2)湿法制备高铁酸钾(K2FeO4)是在碱性环境中进行,反应体系中有六种反应微粒:Fe(OH)3、ClO-、OH-、FeO 、Cl-、H2O。
、Cl-、H2O。
①请依据上述信息,写出并配平湿法制高铁酸钾的离子反应方程式_____ 。
②每生成1molFeO 转移
转移_____ 个电子。
(3) 是一种有毒气体,如果泄漏会造成严重的危害。已知
是一种有毒气体,如果泄漏会造成严重的危害。已知 ,化工厂可用浓氨水来检验
,化工厂可用浓氨水来检验 是否泄漏。反应中被氧化和未被氧化的
是否泄漏。反应中被氧化和未被氧化的 分子个数比为
分子个数比为_____ 。
Ⅱ.用电弧法合成碳纳米管,常伴有大量杂质—碳纳米颗粒,这种碳纳米颗粒可用氧化气化法提纯,其反应方程式为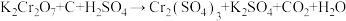 。
。
(4)配平该反应方程式:_____ 。
(5)此反应的氧化产物为_____ 。
(6)KMnO4在加热的条件下与硫酸酸化的Na2C2O4溶液反应,生成Mn2+和CO2,该反应的离子方程式为:_____ 。
(7)某条件下, 氧气所占的体积为
氧气所占的体积为 ,则在该条件下的气体摩尔体积为
,则在该条件下的气体摩尔体积为_____ 。
I.高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂,比 Cl2、O2、ClO2、KMnO4 氧化性更强,无二次污染,工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH 至饱和,使高铁酸钾析出。
(1)干法制备高铁酸钠的主要反应为2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑,该反应中还原剂是
(2)湿法制备高铁酸钾(K2FeO4)是在碱性环境中进行,反应体系中有六种反应微粒:Fe(OH)3、ClO-、OH-、FeO
 、Cl-、H2O。
、Cl-、H2O。①请依据上述信息,写出并配平湿法制高铁酸钾的离子反应方程式
②每生成1molFeO
 转移
转移(3)
 是一种有毒气体,如果泄漏会造成严重的危害。已知
是一种有毒气体,如果泄漏会造成严重的危害。已知 ,化工厂可用浓氨水来检验
,化工厂可用浓氨水来检验 是否泄漏。反应中被氧化和未被氧化的
是否泄漏。反应中被氧化和未被氧化的 分子个数比为
分子个数比为Ⅱ.用电弧法合成碳纳米管,常伴有大量杂质—碳纳米颗粒,这种碳纳米颗粒可用氧化气化法提纯,其反应方程式为
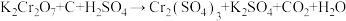 。
。(4)配平该反应方程式:
(5)此反应的氧化产物为
(6)KMnO4在加热的条件下与硫酸酸化的Na2C2O4溶液反应,生成Mn2+和CO2,该反应的离子方程式为:
(7)某条件下,
 氧气所占的体积为
氧气所占的体积为 ,则在该条件下的气体摩尔体积为
,则在该条件下的气体摩尔体积为
更新时间:2024/01/31 21:55:14
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】以下是与绿色化学、环境保护和人类健康息息相关的三个主题,请根据已知信息回答下列问题:
(1)下列制备氯乙烷的反应中原子经济性最高的是_____ (填字母)。
A.CH2=CH2+HCl→CH3CH2Cl
B.CH3CH2OH+HCl CH3CH2Cl+H2O
CH3CH2Cl+H2O
C.CH3CH3+Cl2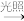 CH3CH2Cl+HCl
CH3CH2Cl+HCl
D.CH2=CHCl+H2 CH3CH2Cl
CH3CH2Cl
由上述四个反应可归纳出,原子经济性最高的是______ (填反应类型)。
(2)有毒物质的无害化处理也是绿色化学研究的内容之一。ClO2是一种性能优良的消毒剂,它可将废水中少量的CN-等有毒的酸根离子氧化而除去。请写出用ClO2将废水中的CN-氧化成无毒气体的离子方程式:______ ,该方法的优点是_______ 。
(3)某饮用水厂由天然水制备纯净水(去离子水)的工艺流程示意图如图:
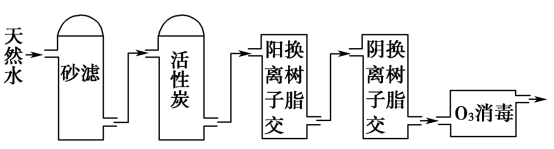
活性炭的作用是_______ ;O3消毒的优点是_______ 。
(1)下列制备氯乙烷的反应中原子经济性最高的是
A.CH2=CH2+HCl→CH3CH2Cl
B.CH3CH2OH+HCl
 CH3CH2Cl+H2O
CH3CH2Cl+H2OC.CH3CH3+Cl2
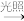 CH3CH2Cl+HCl
CH3CH2Cl+HClD.CH2=CHCl+H2
 CH3CH2Cl
CH3CH2Cl由上述四个反应可归纳出,原子经济性最高的是
(2)有毒物质的无害化处理也是绿色化学研究的内容之一。ClO2是一种性能优良的消毒剂,它可将废水中少量的CN-等有毒的酸根离子氧化而除去。请写出用ClO2将废水中的CN-氧化成无毒气体的离子方程式:
(3)某饮用水厂由天然水制备纯净水(去离子水)的工艺流程示意图如图:

活性炭的作用是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】磷是重要的元素,能形成多种含氧酸和含氧酸盐。回答下列问题:
Ⅰ. 亚磷酸(H3PO3)是二元酸,H3PO3溶液存在电离平衡:H3PO3 H+ + H2PO
H+ + H2PO 。亚磷酸与足量NaOH溶液反应,生成水和Na2HPO3。
。亚磷酸与足量NaOH溶液反应,生成水和Na2HPO3。
(1)写出亚磷酸钠(Na2HPO3)中磷的化合价_______ 。
(2)当亚磷酸与少量NaOH溶液反应的离子方程式为_______ 。
(3)亚磷酸具有强还原性,可使碘水褪色,该反应的化学方程式_______ 。
Ⅱ.已知:①次磷酸(H3PO2)是一种一元弱酸;
②常温下,电离平衡常数Ka(H3PO2)=5.9×10-2,Ka(CH3COOH)=1.8×10-5;
(4)下列说法正确的是_______。
Ⅰ. 亚磷酸(H3PO3)是二元酸,H3PO3溶液存在电离平衡:H3PO3
 H+ + H2PO
H+ + H2PO 。亚磷酸与足量NaOH溶液反应,生成水和Na2HPO3。
。亚磷酸与足量NaOH溶液反应,生成水和Na2HPO3。(1)写出亚磷酸钠(Na2HPO3)中磷的化合价
(2)当亚磷酸与少量NaOH溶液反应的离子方程式为
(3)亚磷酸具有强还原性,可使碘水褪色,该反应的化学方程式
Ⅱ.已知:①次磷酸(H3PO2)是一种一元弱酸;
②常温下,电离平衡常数Ka(H3PO2)=5.9×10-2,Ka(CH3COOH)=1.8×10-5;
(4)下列说法正确的是_______。
A.次磷酸的电离方程式为:H3PO2⇌H++H2PO |
| B.NaH2PO2属于酸式盐 |
| C.浓度均为0.1mol•L-1的次磷酸(H3PO2)与盐酸相比前者导电能力强 |
| D.0.1mol•L-1NaH2PO2溶液的pH比0.1mol•L-1CH3COONa溶液的pH小 |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】HNO3是极其重要的化工原料,在工业、农业、医药、军事等领域有着广泛的应用,现代工业上常用氨催化氧化制硝酸的流程示意图如下:________________________ 。
(2)工业上常用碱液来吸收NOx,有关的化学反应为:
①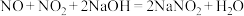 ;
;
② 。
。
现有一定条件下0.2molNO2和0.1molNO的混合气体恰好被200mLNaOH溶液完全吸收,则NaOH溶液的物质的量浓度为____________ mol/L。
(3)已知氨氮废水中氮元素多以 和NH3•H2O的形式存在,加入NaClO可将废水中的NH3•H2O转化为无污染气体,该反应的化学方程式为
和NH3•H2O的形式存在,加入NaClO可将废水中的NH3•H2O转化为无污染气体,该反应的化学方程式为_______________________________________________ 。
(4)《本草纲目拾遗》记载“强水性最烈,能蚀五金”,请写出稀强水与铜反应的离子方程式:__________________________ 。
(5)长期存放的浓硝酸呈黄色是因为其分解生成的_____________ 溶于硝酸中,实验室常将浓硝酸保存在
__________ 试剂瓶中,并放在__________ 处。
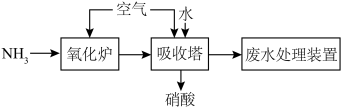
(2)工业上常用碱液来吸收NOx,有关的化学反应为:
①
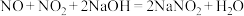 ;
;②
 。
。现有一定条件下0.2molNO2和0.1molNO的混合气体恰好被200mLNaOH溶液完全吸收,则NaOH溶液的物质的量浓度为
(3)已知氨氮废水中氮元素多以
 和NH3•H2O的形式存在,加入NaClO可将废水中的NH3•H2O转化为无污染气体,该反应的化学方程式为
和NH3•H2O的形式存在,加入NaClO可将废水中的NH3•H2O转化为无污染气体,该反应的化学方程式为(4)《本草纲目拾遗》记载“强水性最烈,能蚀五金”,请写出稀强水与铜反应的离子方程式:
(5)长期存放的浓硝酸呈黄色是因为其分解生成的
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】I:我国古代四大发明之一的黑火药是由硫黄粉、硝酸钾和木炭粉按一定比例混合而成,爆炸时发生的反应为:S+2KNO3+3C=K2S+N2↑+3X↑请回答:
(1)X的化学式是___________ ,按照物质的组成和性质分类,属于___________ (填字母)。
A.单质 B.酸性氧化物 C.化合物 D.盐
(2)在上述反应中,氧化剂是(填化学式)___________ 。
II:如图是一块用FeCl3溶液与Cu反应制作的印刷电路板,其制作原理可用方程式2FeCl3 +Cu = CuCl2 + 2X表示。___________ 。
(4)在上述反应中,氧化剂为___________ ,氧化产物为___________ ,将两者的氧化性相比较,___________ 的氧化性更强。
(5)写出该反应的离子方程式,并用双线桥表示电子转移的方向和数目___________ 。
(1)X的化学式是
A.单质 B.酸性氧化物 C.化合物 D.盐
(2)在上述反应中,氧化剂是(填化学式)
II:如图是一块用FeCl3溶液与Cu反应制作的印刷电路板,其制作原理可用方程式2FeCl3 +Cu = CuCl2 + 2X表示。

(4)在上述反应中,氧化剂为
(5)写出该反应的离子方程式,并用双线桥表示电子转移的方向和数目
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】氧化还原反应在生产生活中应用十分广泛。
Ⅰ.人体正常的血红蛋白含有 ,若误食亚硝酸盐(如
,若误食亚硝酸盐(如 ),则导致血红蛋白中的
),则导致血红蛋白中的 转化为
转化为 而中毒,服用维生素C可解毒。
而中毒,服用维生素C可解毒。
(1)关于上述过程,下列叙述正确的是___________(填字母)。
(2)金属加工后的废切削液中含2%~3%的 ,它是环境污染物,人们用
,它是环境污染物,人们用 溶液来处理,使
溶液来处理,使 转化为无毒物质,该反应分两步进行:
转化为无毒物质,该反应分两步进行:
第一步: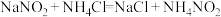
第二步: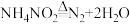
下列对第二步反应说法正确的是___________ 。
①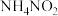 只是氧化剂 ②
只是氧化剂 ②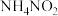 只是还原剂 ③
只是还原剂 ③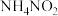 发生了分解反应
发生了分解反应
④只有氮元素的化合价发生了变化 ⑤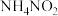 既是氧化剂又是还原剂
既是氧化剂又是还原剂
Ⅱ.高铁酸钾是一种非氯高效消毒剂,主要用于饮用水处理。高铁酸钾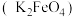 在强碱性条件下能够稳定存在。工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入饱和的KOH溶液,使高铁酸钾析出。
在强碱性条件下能够稳定存在。工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入饱和的KOH溶液,使高铁酸钾析出。
(3)方法一: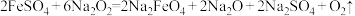 ,该反应中的氧化剂是
,该反应中的氧化剂是___________ ,氧化产物是___________ 。
(4)方法二: (未配平)
(未配平)
①配平离子反应方程式:_____ ____ _____
_____ _____
_____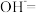 ______
______ _____
_____ ___
___
②若反应过程中转移了1.5mol电子,则还原产物的物质的量为______ mol。
(5)向 溶液中加入适量饱和的KOH溶液,有
溶液中加入适量饱和的KOH溶液,有 析出,请写出该反应的离子方程式:
析出,请写出该反应的离子方程式:___________ 。
Ⅰ.人体正常的血红蛋白含有
 ,若误食亚硝酸盐(如
,若误食亚硝酸盐(如 ),则导致血红蛋白中的
),则导致血红蛋白中的 转化为
转化为 而中毒,服用维生素C可解毒。
而中毒,服用维生素C可解毒。(1)关于上述过程,下列叙述正确的是___________(填字母)。
| A.亚硝酸盐被还原 | B.维生素C是还原剂 |
C.维生素C还原性比 强 强 | D.亚硝酸盐是还原剂 |
 ,它是环境污染物,人们用
,它是环境污染物,人们用 溶液来处理,使
溶液来处理,使 转化为无毒物质,该反应分两步进行:
转化为无毒物质,该反应分两步进行:第一步:
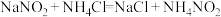
第二步:
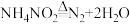
下列对第二步反应说法正确的是
①
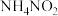 只是氧化剂 ②
只是氧化剂 ②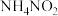 只是还原剂 ③
只是还原剂 ③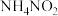 发生了分解反应
发生了分解反应④只有氮元素的化合价发生了变化 ⑤
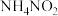 既是氧化剂又是还原剂
既是氧化剂又是还原剂Ⅱ.高铁酸钾是一种非氯高效消毒剂,主要用于饮用水处理。高铁酸钾
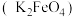 在强碱性条件下能够稳定存在。工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入饱和的KOH溶液,使高铁酸钾析出。
在强碱性条件下能够稳定存在。工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入饱和的KOH溶液,使高铁酸钾析出。(3)方法一:
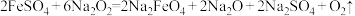 ,该反应中的氧化剂是
,该反应中的氧化剂是(4)方法二:
 (未配平)
(未配平)①配平离子反应方程式:
 _____
_____ _____
_____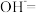 ______
______ _____
_____ ___
___
②若反应过程中转移了1.5mol电子,则还原产物的物质的量为
(5)向
 溶液中加入适量饱和的KOH溶液,有
溶液中加入适量饱和的KOH溶液,有 析出,请写出该反应的离子方程式:
析出,请写出该反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】(1)氮元素在元素周期表中的位置为_______ 。
(2)氮元素原子核外电子排布式为_______ ,有_______ 种形状的电子云。
(3)氮元素气态氢化物的电子式为_______ 。
与氮元素同主族的磷元素化合物有如下反应,其中反应物有:PH3、H2SO4、KClO3;生成物有:K2SO4、H3PO4、H2O 和一种未知物质 X。
(4)已知 KClO3 在反应中得到电子,则该反应的还原剂是_______ 。
(5)已知 0.2mol KClO3 在反应中得到 1mol 电子生成 X,则 X 的化学式为_______ 。
(6)完成并配平上述反应的化学方程式,标出电子转移方向和数目:_______ 。
(7)根据上述反应可推知_______ 。(填序号)
A.氧化性:KClO3 > H3PO4 B.氧化性:KClO3 > H2O
C.还原性:PH3 > X D.还原性:PH3 > K2SO4
(8)在该反应中转移电子 2mol 时,生成H3PO4_______ mol。
(2)氮元素原子核外电子排布式为
(3)氮元素气态氢化物的电子式为
与氮元素同主族的磷元素化合物有如下反应,其中反应物有:PH3、H2SO4、KClO3;生成物有:K2SO4、H3PO4、H2O 和一种未知物质 X。
(4)已知 KClO3 在反应中得到电子,则该反应的还原剂是
(5)已知 0.2mol KClO3 在反应中得到 1mol 电子生成 X,则 X 的化学式为
(6)完成并配平上述反应的化学方程式,标出电子转移方向和数目:
(7)根据上述反应可推知
A.氧化性:KClO3 > H3PO4 B.氧化性:KClO3 > H2O
C.还原性:PH3 > X D.还原性:PH3 > K2SO4
(8)在该反应中转移电子 2mol 时,生成H3PO4
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】现有中学化学中常见的几种物质:①HNO3 ②Zn ③CO ④CO2 ⑤Fe(NO3)3 ⑥Cl2。请回答下列问题:
(1)①②③④四种物质中常用作还原剂的有__________ (填序号)。
(2)①②在一定条件下发生反应:4Zn+10HNO3=4Zn(NO3)2+N2O↑+5H2O,反应中硝酸体现的性质是__________ 和__________ ,被还原的HNO3与未被还原的HNO3的质量比为__________ 。
(3)工业上可用⑤⑥制备净水剂高铁酸钠,其反应为:Fe(NO3)3+NaOH+Cl2 →Na2FeO4+NaNO3+NaCl+H2O。
①配平该反应的化学方程式,并用单线桥法标出电子转移方向和数目:____________________ 。
②氧化剂与还原剂物质的量之比为__________ 。
(1)①②③④四种物质中常用作还原剂的有
(2)①②在一定条件下发生反应:4Zn+10HNO3=4Zn(NO3)2+N2O↑+5H2O,反应中硝酸体现的性质是
(3)工业上可用⑤⑥制备净水剂高铁酸钠,其反应为:Fe(NO3)3+NaOH+Cl2 →Na2FeO4+NaNO3+NaCl+H2O。
①配平该反应的化学方程式,并用单线桥法标出电子转移方向和数目:
②氧化剂与还原剂物质的量之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】无机化合物可根据其组成和性质进行分类,分类比较是研究物质性质常用的一类方法。
(1)下图所示的物质分类方法名称是___________ 。

(2)根据氧化物与酸碱反应的性质,可以对氧化物再分类:能与碱反应生成盐和水的氧化物是酸性氧化物,如CO2、SO3;能与酸反应生成盐和水的氧化物是碱性氧化物,如Na2O、CuO。下列有关说法正确的是___________ 。(填序号)
A.在化合物中,只要含有氧元素就属于氧化物
B.SO2既是非金属氧化物,又是酸性氧化物
C.不能与酸反应的氧化物一定能与碱反应
(3)砷有多种化合物,其中As2O5溶于水缓慢化合生成一种三元酸(H3AsO4)。某工业废渣中含有As2O5、Fe2O3和MgO三种物质。现要分离提取 出砷元素,有同学建议用NaOH溶液,理由是___________ ,写出反应的化学方程式___________ 。
(4)As2O3俗称砒霜,是宫廷剧中“鹤顶红”的有效成分,可以用马氏试砷法来检测砒霜。具体方法是:用Zn、盐酸和试样混在一起,将生成的气体导入热玻璃管,若试样中有砒霜,就会在热玻璃管中产生As,As积集而成亮黑色的“砷镜”。生成“砷镜”过程中共发生两个反应,①___________ ;②2AsH3=2As+3H2
(1)下图所示的物质分类方法名称是

(2)根据氧化物与酸碱反应的性质,可以对氧化物再分类:能与碱反应生成盐和水的氧化物是酸性氧化物,如CO2、SO3;能与酸反应生成盐和水的氧化物是碱性氧化物,如Na2O、CuO。下列有关说法正确的是
A.在化合物中,只要含有氧元素就属于氧化物
B.SO2既是非金属氧化物,又是酸性氧化物
C.不能与酸反应的氧化物一定能与碱反应
(3)砷有多种化合物,其中As2O5溶于水缓慢化合生成一种三元酸(H3AsO4)。某工业废渣中含有As2O5、Fe2O3和MgO三种物质。现要
(4)As2O3俗称砒霜,是宫廷剧中“鹤顶红”的有效成分,可以用马氏试砷法来检测砒霜。具体方法是:用Zn、盐酸和试样混在一起,将生成的气体导入热玻璃管,若试样中有砒霜,就会在热玻璃管中产生As,As积集而成亮黑色的“砷镜”。生成“砷镜”过程中共发生两个反应,①
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】自然界中的氮循环部分过程如图所示,回答下列问题:___________ (任写一种)。
②在哈伯等科学家的努力下,路径Ⅱ已实现工业大规模合成氨,反应方程式为___________ 。
(2)实验室的硝酸一般储存在棕色瓶中,涉及的化学方程式为___________ 。
(3)除反硝化作用外,铵态氮( )与亚硝态氮(
)与亚硝态氮( )也可以在细菌的作用下转化为氮气。请写出所涉及的离子反应方程式
)也可以在细菌的作用下转化为氮气。请写出所涉及的离子反应方程式___________ 。该反应中,当产生0.02mol氮气时,转移电子的物质的量为___________ 。
为探究氨的还原性,某同学设计了如图所示实验装置(其中夹持装置略去),在实验室中进行实验探究。回答下列问题
A中氧化铜全部转化成光亮的红色固体
B中U形管内物质变蓝;
(4)C中集气瓶内收集到一种无色气态单质,该气体用排水法收集的理由是___________ 。
(5)氧化铜和氨气发生反应,化学方程式是___________ 。

②在哈伯等科学家的努力下,路径Ⅱ已实现工业大规模合成氨,反应方程式为
(2)实验室的硝酸一般储存在棕色瓶中,涉及的化学方程式为
(3)除反硝化作用外,铵态氮(
 )与亚硝态氮(
)与亚硝态氮( )也可以在细菌的作用下转化为氮气。请写出所涉及的离子反应方程式
)也可以在细菌的作用下转化为氮气。请写出所涉及的离子反应方程式为探究氨的还原性,某同学设计了如图所示实验装置(其中夹持装置略去),在实验室中进行实验探究。回答下列问题

A中氧化铜全部转化成光亮的红色固体
B中U形管内物质变蓝;
(4)C中集气瓶内收集到一种无色气态单质,该气体用排水法收集的理由是
(5)氧化铜和氨气发生反应,化学方程式是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】氧化还原反应在生产生活中有广泛的应用,中国传统文化中有广泛记载。
(1)“春蚕到死丝方尽,蜡炬成灰泪始干”中涉及到蜡烛与 的燃烧反应,反应生成
的燃烧反应,反应生成 和
和 ,该反应一定是___________。
,该反应一定是___________。
(2)“熬胆矾铁釜,久之亦化为铜”涉及到的化学反应为: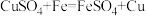 。该反应中被氧化的元素是
。该反应中被氧化的元素是___________ (填元素符号,下同),化合价降低的元素是___________ 。
(3)宋代《洗冤集录》中记载有“银针探毒”,其原理是: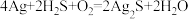 。该反应的还原剂是
。该反应的还原剂是___________ (填化学式,下同),还原产物是___________ 。用双线桥法表示该反应中转移电子数及氧化反应和还原反应:___________ 。
(4)我国古代四大发明之一的黑火药是由硫磺粉、硝酸钾和木炭按一定比例混合而成的,爆炸时发生的反应为: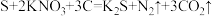 。该反应中,氧化剂是
。该反应中,氧化剂是___________ (填化学式,下同),氧化产物是___________ 。在上述反应中若有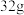 硫单质完全反应,被硫单质氧化的单质C的质量是
硫单质完全反应,被硫单质氧化的单质C的质量是___________ g。
(1)“春蚕到死丝方尽,蜡炬成灰泪始干”中涉及到蜡烛与
 的燃烧反应,反应生成
的燃烧反应,反应生成 和
和 ,该反应一定是___________。
,该反应一定是___________。| A.化合反应 | B.分解反应 | C.氧化还原反应 | D.置换反应 |
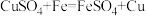 。该反应中被氧化的元素是
。该反应中被氧化的元素是(3)宋代《洗冤集录》中记载有“银针探毒”,其原理是:
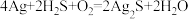 。该反应的还原剂是
。该反应的还原剂是(4)我国古代四大发明之一的黑火药是由硫磺粉、硝酸钾和木炭按一定比例混合而成的,爆炸时发生的反应为:
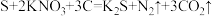 。该反应中,氧化剂是
。该反应中,氧化剂是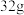 硫单质完全反应,被硫单质氧化的单质C的质量是
硫单质完全反应,被硫单质氧化的单质C的质量是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】氧化还原反应在工农业生产、日常生活中具有广泛的用途。
(1)在焊接铜器时,可先用 除去其表面的氧化铜再进行焊接。
除去其表面的氧化铜再进行焊接。
①请配平上述过程中发生的氧化还原反应的化学方程式:___________ 。
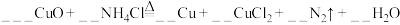 。(1也要写出)
。(1也要写出)
②该反应中,氧化剂是___________ (填化学式),被氧化的元素是___________ (填元素名称)。
(2)二氧化氯是一种高效消毒剂。工业上制备 的反应为
的反应为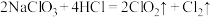
 。
。
①该反应中的还原产物是___________ (填化学式)。
②该反应中每生成1个 分子,转移
分子,转移___________ 个电子。
③ 在杀菌消毒的过程中会生成副产物亚氯酸盐(
在杀菌消毒的过程中会生成副产物亚氯酸盐( ),需要将其转化为
),需要将其转化为 除去,为实现其转化过程可加入的试剂是
除去,为实现其转化过程可加入的试剂是___________ (填字母)。
A. B.
B. C.KI D.
C.KI D.
(3)双氧水是公认的绿色氧化剂。请写出向 溶液中加入足量硫酸酸化的双氧水时发生氧化还原反应的离子方程式:
溶液中加入足量硫酸酸化的双氧水时发生氧化还原反应的离子方程式:___________ 。(已知: 是可溶性盐)
是可溶性盐)
(1)在焊接铜器时,可先用
 除去其表面的氧化铜再进行焊接。
除去其表面的氧化铜再进行焊接。①请配平上述过程中发生的氧化还原反应的化学方程式:
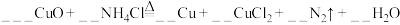 。(1也要写出)
。(1也要写出)②该反应中,氧化剂是
(2)二氧化氯是一种高效消毒剂。工业上制备
 的反应为
的反应为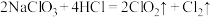
 。
。①该反应中的还原产物是
②该反应中每生成1个
 分子,转移
分子,转移③
 在杀菌消毒的过程中会生成副产物亚氯酸盐(
在杀菌消毒的过程中会生成副产物亚氯酸盐( ),需要将其转化为
),需要将其转化为 除去,为实现其转化过程可加入的试剂是
除去,为实现其转化过程可加入的试剂是A.
 B.
B. C.KI D.
C.KI D.
(3)双氧水是公认的绿色氧化剂。请写出向
 溶液中加入足量硫酸酸化的双氧水时发生氧化还原反应的离子方程式:
溶液中加入足量硫酸酸化的双氧水时发生氧化还原反应的离子方程式: 是可溶性盐)
是可溶性盐)
您最近一年使用:0次

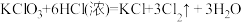 ,
, ,
,

