利用化学原理可以对工厂排放的废水、废渣等进行有效检测与合理处理。某工厂对制革工业污泥Cr(Ⅲ)的处理工艺流程如图:
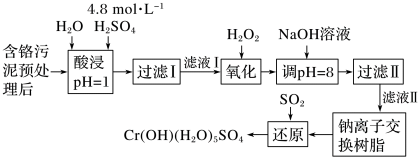
已知硫酸浸取液中的金属离子主要是Cr3+,其次是Fe3+、Al3+、Ca2+和Mg2+。
(1)酸浸时,为了提高浸取率可采取的措施有_______ 、_______ 。(答出两点)
(2)H2O2的作用是将滤液Ⅰ中的Cr3+转化为Cr2O ,则此反应中氧化剂和还原剂物质的量之比为
,则此反应中氧化剂和还原剂物质的量之比为_______ 。
(3)上述流程中,加入NaOH溶液后,溶液呈碱性,Cr2O 转化为CrO
转化为CrO ,写出上述流程中用SO2进行还原时发生反应的离子方程式:
,写出上述流程中用SO2进行还原时发生反应的离子方程式:_______ 。

已知硫酸浸取液中的金属离子主要是Cr3+,其次是Fe3+、Al3+、Ca2+和Mg2+。
(1)酸浸时,为了提高浸取率可采取的措施有
(2)H2O2的作用是将滤液Ⅰ中的Cr3+转化为Cr2O
 ,则此反应中氧化剂和还原剂物质的量之比为
,则此反应中氧化剂和还原剂物质的量之比为(3)上述流程中,加入NaOH溶液后,溶液呈碱性,Cr2O
 转化为CrO
转化为CrO ,写出上述流程中用SO2进行还原时发生反应的离子方程式:
,写出上述流程中用SO2进行还原时发生反应的离子方程式:
更新时间:2024-02-14 09:40:58
|
相似题推荐
解答题-无机推断题
|
较易
(0.85)
名校
【推荐1】A~G为中学化学中常见的物质,转化关系如图所示,反应①为常温下的反应,A、C、D中均含有氯元素,且A中氯元素的化合价介于C和D中氯元素的化合价之间,C是常用的调味剂。E在常温下为无色无味的液体,F是淡黄色固体,G为常见的无色气体。请据图回答下列问题:
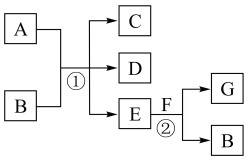
(1)B的化学式___________ ,它的摩尔质量为___________ 。
(2)标况下,等质量的A和G,其分子数之比为:___________ 。
(3)D在水溶液中的电离方程式为___________ 。
(4)F中阴阳离子个数比为:___________ , F可用于呼吸面具和潜水艇中,作为供氧剂,请分析原因___________ 。
(5)请写出反应①的离子反应方程式___________ 。
(6)将B的溶液滴入FeCl2溶液中,先产生白色絮状沉淀,沉淀迅速变为灰绿色,最终变为红褐色,该过程中发生的氧化还原反应的化学方程式为___________ 。

(1)B的化学式
(2)标况下,等质量的A和G,其分子数之比为:
(3)D在水溶液中的电离方程式为
(4)F中阴阳离子个数比为:
(5)请写出反应①的离子反应方程式
(6)将B的溶液滴入FeCl2溶液中,先产生白色絮状沉淀,沉淀迅速变为灰绿色,最终变为红褐色,该过程中发生的氧化还原反应的化学方程式为
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐2】硼砂的化学式为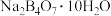 。利用硼镁矿(主要成分为
。利用硼镁矿(主要成分为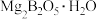 )制取金属镁及粗硼的工艺流程为:
)制取金属镁及粗硼的工艺流程为:
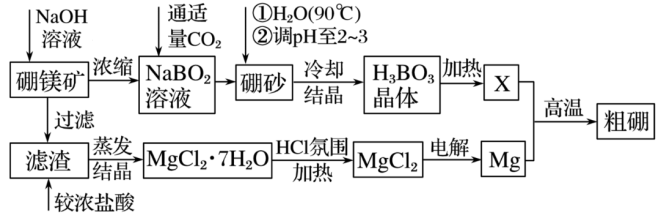
回答下列有关问题:
(1)硼镁矿加入NaOH溶液后过滤得到的滤渣的主要成分为___________ 。
(2)硼砂中B的化合价为___________ ,溶于热水后,常用稀H2SO4调pH=2~3得到H3BO3,该反应的离子方程式为___________ 。
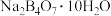 。利用硼镁矿(主要成分为
。利用硼镁矿(主要成分为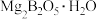 )制取金属镁及粗硼的工艺流程为:
)制取金属镁及粗硼的工艺流程为:
回答下列有关问题:
(1)硼镁矿加入NaOH溶液后过滤得到的滤渣的主要成分为
(2)硼砂中B的化合价为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐3】为了除去粗盐中含有的可溶性杂质CaCl2、MgCl2和Na2SO4,需进行下列实验操作,请在( )中填写所使用和除杂试剂的化学式,在 中填写实验操作名称。写出符合下列条件的离子方程式
中填写实验操作名称。写出符合下列条件的离子方程式
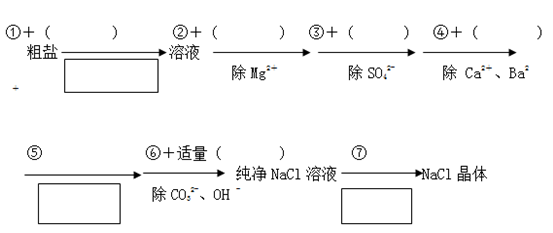
(1)①___________ 、 ____________ ;②_______________________ ;③____________ ;④____________ ;⑤____________ ;⑥____________ ;⑦____________ 。
(2)除去Mg2+的离子方程式_______________________________________________
(3)除去SO42-的离子方程式______________________________________________
 中填写实验操作名称。写出符合下列条件的离子方程式
中填写实验操作名称。写出符合下列条件的离子方程式
(1)①
(2)除去Mg2+的离子方程式
(3)除去SO42-的离子方程式
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐1】铁、铝的混合物进行如图实验:

(1)操作X的名称是___________ ;
(2)气体A是___________ (填化学式);
(3)A与 混合光照可能发生爆炸,生成
混合光照可能发生爆炸,生成___________ (填化学式),A在该反应中作为___________ (填“氧化剂”或“还原剂”);
(4)溶液B中阴离子除 外还有
外还有___________ (填离子符号),溶液D中存在的金属离子为___________ ;
(5)加入稀盐酸发生反应的离子方程式为:___________ ;
(6)铝表面会生成一层致密的氧化膜,用烧碱除去铝制品表面氧化膜的化学方程式为:_____ 。

(1)操作X的名称是
(2)气体A是
(3)A与
 混合光照可能发生爆炸,生成
混合光照可能发生爆炸,生成(4)溶液B中阴离子除
 外还有
外还有(5)加入稀盐酸发生反应的离子方程式为:
(6)铝表面会生成一层致密的氧化膜,用烧碱除去铝制品表面氧化膜的化学方程式为:
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐2】海洋是巨大的资源宝库,从海洋中获取部分资源的流程图如下:

回答下列问题:
Ⅰ.海水提溴
溴被称为“海洋元素”,空气吹出法从海水中提取溴单质的流程如下图所示:

(1)过程③中 所起的作用为
所起的作用为___________ (用离子方程式表示)
(2)上图过程①②③④中含Br元素的物质发生的变化依次为___________ ,___________ ,___________ ,___________ 。(选填字母标号并排序,选项可重复使用,也可不选用)
A.被氧化 B.被还原 C.未参与氧化还原反应
(3)步骤①已经获得 ,步骤②③④的目的是
,步骤②③④的目的是___________
Ⅱ.海水提镁
(4)该工业生产过程中,为了使 转化为
转化为 ,应加入的试剂为
,应加入的试剂为___________ (填化学式)。
(5)写出冶炼金属Mg的化学方程式___________ 。
Ⅲ.产品应用
(6)以下属于纯碱在日常生活或工业生产中的用途的有___________(填标号)。

回答下列问题:
Ⅰ.海水提溴
溴被称为“海洋元素”,空气吹出法从海水中提取溴单质的流程如下图所示:

(1)过程③中
 所起的作用为
所起的作用为(2)上图过程①②③④中含Br元素的物质发生的变化依次为
A.被氧化 B.被还原 C.未参与氧化还原反应
(3)步骤①已经获得
 ,步骤②③④的目的是
,步骤②③④的目的是Ⅱ.海水提镁
(4)该工业生产过程中,为了使
 转化为
转化为 ,应加入的试剂为
,应加入的试剂为(5)写出冶炼金属Mg的化学方程式
Ⅲ.产品应用
(6)以下属于纯碱在日常生活或工业生产中的用途的有___________(填标号)。
| A.抗酸药 | B.制玻璃 | C.去油污 | D.抗氧化剂 |
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐3】物质世界的多姿多彩源自元素及其化合物的多种多样。
Ⅰ.补铁剂中的铁--检验其中铁元素的价态
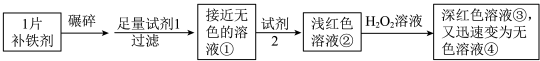
【查阅资料】该补铁剂不溶于水,但能溶于人体中的胃液(含盐酸)。
1.试剂1是___________ 。
2.写出上述条件下 与
与 发生反应的离子方程式
发生反应的离子方程式___________ 。
3.能证明溶液①中含有 的实验现象是
的实验现象是___________ 。
Ⅱ.硫元素是动植物生长不可缺少的元素。
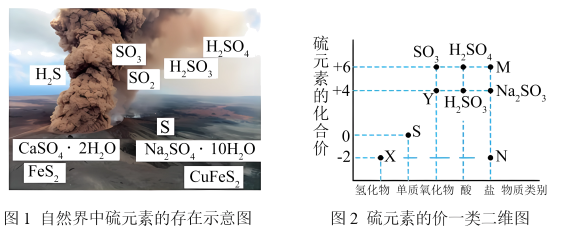
4.X与Y反应中氧化剂与还原剂的物质的量之比为___________ 。
5. 水溶液易变质,实验室检验
水溶液易变质,实验室检验 水溶液是否变质的基本操作是
水溶液是否变质的基本操作是________ 。
6.已知 通入酸性
通入酸性 ,可以生成
,可以生成 和
和 ,则
,则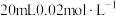 的
的 溶液最多可以吸收
溶液最多可以吸收___________ 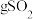 。
。
Ⅰ.补铁剂中的铁--检验其中铁元素的价态

【查阅资料】该补铁剂不溶于水,但能溶于人体中的胃液(含盐酸)。
1.试剂1是
2.写出上述条件下
 与
与 发生反应的离子方程式
发生反应的离子方程式3.能证明溶液①中含有
 的实验现象是
的实验现象是Ⅱ.硫元素是动植物生长不可缺少的元素。

4.X与Y反应中氧化剂与还原剂的物质的量之比为
5.
 水溶液易变质,实验室检验
水溶液易变质,实验室检验 水溶液是否变质的基本操作是
水溶液是否变质的基本操作是6.已知
 通入酸性
通入酸性 ,可以生成
,可以生成 和
和 ,则
,则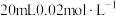 的
的 溶液最多可以吸收
溶液最多可以吸收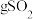 。
。
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐1】根据下表回答问题:

(1)元素⑦在周期表中的位置是_______ 。
(2)元素①和⑤的原子序数相差_______ 。
(3)写出元素⑤形成的常见化合物与元素⑧形成的单质反应的化学方程式_______ 。
(4)写出元素③形成的不同化合价的化合物的化学式(写出四个)_______ ,其中能与元素⑥形成的单质反应的化学方程式为_______ 。

(1)元素⑦在周期表中的位置是
(2)元素①和⑤的原子序数相差
(3)写出元素⑤形成的常见化合物与元素⑧形成的单质反应的化学方程式
(4)写出元素③形成的不同化合价的化合物的化学式(写出四个)
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
解题方法
【推荐2】常温下,浓度均为0.1 mol·L-1的5种溶液pH如表:
请由表中数据回答:
(1)NaClO溶液显碱性的原因是___________ (用离子方程式表示)。
(2)侯氏制碱中,使NH4Cl从母液中析出的措施不包括___________ (选填编号)。
A.冷却 B.加入食盐细颗粒 C.通入CO2 D.通入NH3
(3)0.1 mol·L-1的 NaHSO3溶液中离子浓度:c(SO )
)___________ c(HSO )(填 “>”、“<”或“=”);
)(填 “>”、“<”或“=”);
要使其中的c(SO )减小,下列方法不可行的是
)减小,下列方法不可行的是___________ (选填编号)。
A.加入过量CaO(s) B.加入少量NaOH(s) C.通入过量HCl(g) D.加入少量的H2O2(aq)
(4)5种溶液中,水的电离程度最小的是(填化学式)___________ ;向氯水中加入NaHCO3可增强其漂白性,用化学平衡移动原理解释原因:___________ 。
(5)NaHSO3溶液在不同温度下均可被过量KIO3酸性溶液氧化,当NaHSO3完全消耗时有I2析出,写出该反应的离子方程式并用单线桥法标出电子转移的方向和数目:___________ ;若有25.4g I2生成,则转移电子数是___________ 个。
| 溶质 | Na2CO3 | NaHCO3 | Na2SO3 | NaHSO3 | NaClO |
| pH | 11.6 | 9.7 | 10.0 | 4.0 | 10.3 |
请由表中数据回答:
(1)NaClO溶液显碱性的原因是
(2)侯氏制碱中,使NH4Cl从母液中析出的措施不包括
A.冷却 B.加入食盐细颗粒 C.通入CO2 D.通入NH3
(3)0.1 mol·L-1的 NaHSO3溶液中离子浓度:c(SO
 )
) )(填 “>”、“<”或“=”);
)(填 “>”、“<”或“=”);要使其中的c(SO
 )减小,下列方法不可行的是
)减小,下列方法不可行的是A.加入过量CaO(s) B.加入少量NaOH(s) C.通入过量HCl(g) D.加入少量的H2O2(aq)
(4)5种溶液中,水的电离程度最小的是(填化学式)
(5)NaHSO3溶液在不同温度下均可被过量KIO3酸性溶液氧化,当NaHSO3完全消耗时有I2析出,写出该反应的离子方程式并用单线桥法标出电子转移的方向和数目:
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
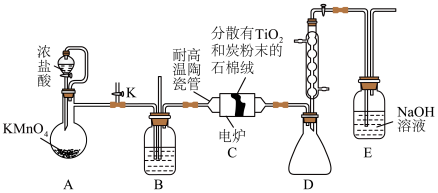
【推荐3】钛在医疗领域的应用非常广泛,如:制人造关节、主动心瓣等。实验室利用含杂质的二氧化钛做原料制取高纯度的二氧化钛,装置如图(夹持装置已略去)。
已知:① ;
;
② 为无色或淡黄色液体,熔点为-30℃,沸点为136.4℃,极易与水反应,能溶于有机溶剂,易挥发,与HCl不发生反应;
为无色或淡黄色液体,熔点为-30℃,沸点为136.4℃,极易与水反应,能溶于有机溶剂,易挥发,与HCl不发生反应;
③ 的盐酸溶液可吸收CO而生成黑色颗粒Pd;
的盐酸溶液可吸收CO而生成黑色颗粒Pd;
④ 在盐酸溶液中的存在形式为
在盐酸溶液中的存在形式为 。
。
a.制备
_______ (填序号)。
①先给陶瓷管通电加热,一段时间后,再打开分液漏斗活塞
②先打开分液漏斗活塞,一段时间后,再给陶瓷管通电加热
③先将陶瓷管断电停止加热,一段时间后,再关闭分液漏斗活塞
④先关闭分液漏斗活塞,一段时间后,再将陶瓷管断电停止加热
(2)装置B中盛放的试剂是_______ (填名称)。
(3)该实验设计存在的缺陷是_______ 、_______
(4)用 的盐酸溶液吸收CO的离子方程式为
的盐酸溶液吸收CO的离子方程式为_______ 。
(5)所得的 可用Mg制Ti,该过程可在
可用Mg制Ti,该过程可在_______ (填序号)氛围保护下进行。
①氮气 ②氩气 ③水蒸气 ④氧气
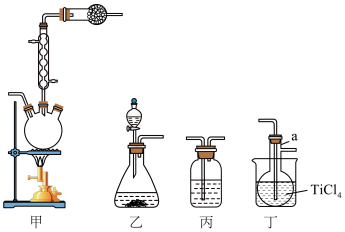
b. 气相氧化法制备
气相氧化法制备
_______ 。
(7)实验装置按从左到右的连接顺序为_______ 。
(8)写出装置甲三颈烧瓶内发生反应的化学方程式_______ 。
已知:①
 ;
;②
 为无色或淡黄色液体,熔点为-30℃,沸点为136.4℃,极易与水反应,能溶于有机溶剂,易挥发,与HCl不发生反应;
为无色或淡黄色液体,熔点为-30℃,沸点为136.4℃,极易与水反应,能溶于有机溶剂,易挥发,与HCl不发生反应;③
 的盐酸溶液可吸收CO而生成黑色颗粒Pd;
的盐酸溶液可吸收CO而生成黑色颗粒Pd;④
 在盐酸溶液中的存在形式为
在盐酸溶液中的存在形式为 。
。a.制备

①先给陶瓷管通电加热,一段时间后,再打开分液漏斗活塞
②先打开分液漏斗活塞,一段时间后,再给陶瓷管通电加热
③先将陶瓷管断电停止加热,一段时间后,再关闭分液漏斗活塞
④先关闭分液漏斗活塞,一段时间后,再将陶瓷管断电停止加热
(2)装置B中盛放的试剂是
(3)该实验设计存在的缺陷是
(4)用
 的盐酸溶液吸收CO的离子方程式为
的盐酸溶液吸收CO的离子方程式为(5)所得的
 可用Mg制Ti,该过程可在
可用Mg制Ti,该过程可在①氮气 ②氩气 ③水蒸气 ④氧气
b.
 气相氧化法制备
气相氧化法制备
(7)实验装置按从左到右的连接顺序为
(8)写出装置甲三颈烧瓶内发生反应的化学方程式
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
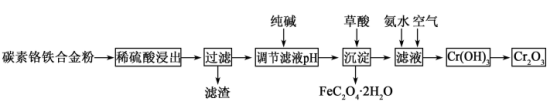
【推荐1】 常用作建筑材料的着色剂。由碳素铬铁合金粉制取
常用作建筑材料的着色剂。由碳素铬铁合金粉制取 的流程如下所示:
的流程如下所示:
已知:金属 与稀硫酸反应生成
与稀硫酸反应生成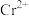 。
。
回答下列问题:
(1)滤渣的主要成分为___________ (填化学式)。
(2)在稀硫酸浸出时铁发生反应的离子方程式为___________ 。
浸出过程中会有少量的 等还原性气体生成,可用高锰酸钾溶液吸收,已知
等还原性气体生成,可用高锰酸钾溶液吸收,已知 与高锰酸钾溶液反应生成
与高锰酸钾溶液反应生成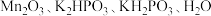 ,参加反应的
,参加反应的 与
与 的物质的量之比为
的物质的量之比为___________ (最简单整数比)。
(3)加草酸的目的是除去 ,写出反应的离子方程式:
,写出反应的离子方程式:___________ 。
(4)生成 后的溶液中存在两种主要副产物,其化学式为
后的溶液中存在两种主要副产物,其化学式为___________ 。
(5) 与
与 的性质相似。写出
的性质相似。写出 与氢氧化钠溶液反应的化学方程式:
与氢氧化钠溶液反应的化学方程式:___________ 。
 常用作建筑材料的着色剂。由碳素铬铁合金粉制取
常用作建筑材料的着色剂。由碳素铬铁合金粉制取 的流程如下所示:
的流程如下所示:
已知:金属
 与稀硫酸反应生成
与稀硫酸反应生成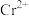 。
。回答下列问题:
(1)滤渣的主要成分为
(2)在稀硫酸浸出时铁发生反应的离子方程式为
浸出过程中会有少量的
 等还原性气体生成,可用高锰酸钾溶液吸收,已知
等还原性气体生成,可用高锰酸钾溶液吸收,已知 与高锰酸钾溶液反应生成
与高锰酸钾溶液反应生成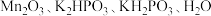 ,参加反应的
,参加反应的 与
与 的物质的量之比为
的物质的量之比为(3)加草酸的目的是除去
 ,写出反应的离子方程式:
,写出反应的离子方程式:(4)生成
 后的溶液中存在两种主要副产物,其化学式为
后的溶液中存在两种主要副产物,其化学式为(5)
 与
与 的性质相似。写出
的性质相似。写出 与氢氧化钠溶液反应的化学方程式:
与氢氧化钠溶液反应的化学方程式:
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐2】醋酸亚铬水合物([Cr(CH3COO)2)]2·2H2O,深红色晶体)是一种氧气吸收剂,通常以二聚体分子存在。实验室以Zn、盐酸、CrCl3溶液、CH3COONa溶液为原料,制备醋酸亚铬水合物的装置如图所示:
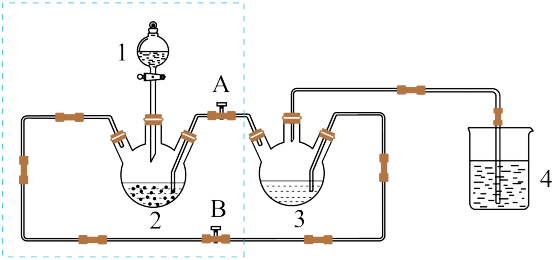
已知:醋酸亚铬水合物不溶于冷水和醚,易溶于盐酸。
Zn(s) + 2HCl(aq) = ZnCl2(aq) + H2(g)
2CrCl3(aq) + Zn(s)= 2CrCl2 (aq) + ZnCl2(aq)
2Cr2+(aq) + 4CH3COO-(aq) + 2H2O(l) = [Cr(CH3COO)2]2·2H2O (s)
请回答:
(1)检查虚线框内装置气密性的方法是_______ 。
(2)醋酸钠溶液应放在装置_______ 中(填写装置编号,下同);盐酸应放在装置_______ 中。
(3)将生成的CrCl2溶液与CH3COONa溶液混合时的操作是_______ 阀门A、_______ 阀门B (填“打开”或“关闭”)。
(4)本实验中锌粒须过量,其原因是_______ 。
(5)为洗涤[Cr(CH3COO)2)]2·2H2O产品,下列方法中最适合的是_______。

已知:醋酸亚铬水合物不溶于冷水和醚,易溶于盐酸。
Zn(s) + 2HCl(aq) = ZnCl2(aq) + H2(g)
2CrCl3(aq) + Zn(s)= 2CrCl2 (aq) + ZnCl2(aq)
2Cr2+(aq) + 4CH3COO-(aq) + 2H2O(l) = [Cr(CH3COO)2]2·2H2O (s)
请回答:
(1)检查虚线框内装置气密性的方法是
(2)醋酸钠溶液应放在装置
(3)将生成的CrCl2溶液与CH3COONa溶液混合时的操作是
(4)本实验中锌粒须过量,其原因是
(5)为洗涤[Cr(CH3COO)2)]2·2H2O产品,下列方法中最适合的是_______。
| A.先用盐酸洗,后用冷水洗 | B.先用冷水洗,后用盐酸洗 |
| C.先用冷水洗,后用乙醚洗 | D.先用盐酸洗涤,后用乙醚洗 |
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐3】重铬酸钾是一种重要的化工原料,一般由铬铁矿制备,铬铁矿的主要成分为 ,还含有硅、铝等杂质。制备流程如图所示:
,还含有硅、铝等杂质。制备流程如图所示:
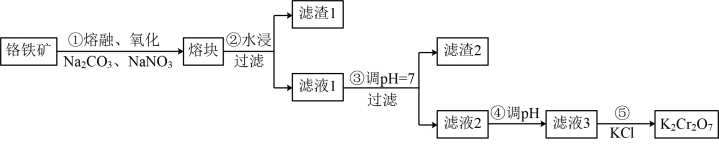
回答下列问题:
(1)步骤①的主要反应为: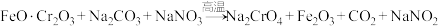
上述反应配平后 与
与 的系数比为
的系数比为___________ 。
(2)滤渣1中含量最多的金属元素是___________ ,滤渣2的主要成分是___________ 及含硅杂质。
(3)步骤④调滤液2的 使之变
使之变___________ (填“大”或“小”),原因是___________ (用离子方程式表示)。
(4)有关物质的溶解度如图所示。

向“滤液3”中加入适量 ,蒸发浓缩,冷却结晶,过滤得到
,蒸发浓缩,冷却结晶,过滤得到 固体。冷却到
固体。冷却到___________ (填标号)得到的 固体产品最多。
固体产品最多。
a. 80℃ b. 60℃ c. 40℃ d. 10℃
 ,还含有硅、铝等杂质。制备流程如图所示:
,还含有硅、铝等杂质。制备流程如图所示:
回答下列问题:
(1)步骤①的主要反应为:
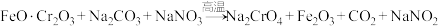
上述反应配平后
 与
与 的系数比为
的系数比为(2)滤渣1中含量最多的金属元素是
(3)步骤④调滤液2的
 使之变
使之变(4)有关物质的溶解度如图所示。

向“滤液3”中加入适量
 ,蒸发浓缩,冷却结晶,过滤得到
,蒸发浓缩,冷却结晶,过滤得到 固体。冷却到
固体。冷却到 固体产品最多。
固体产品最多。a. 80℃ b. 60℃ c. 40℃ d. 10℃
您最近一年使用:0次



