完成下列问题
(1)已知下列反应:①HPO3+H2O=H3PO4;②2Na2O2+2H2O=4NaOH+O2↑;③ 2F2+2H2O=4HF+O2;④2K+2H2O=2KOH+H2↑;⑤Cl2+H2O=HCl+HClO,其中,H2O做氧化剂的是___________ ,H2O做还原剂的是___________ ,H2O既不是氧化剂又不是还原剂的是___________ ,其中不属于氧化还原反应的是___________ (用序号表示);
(2)标准状况下有四种气体①6.72LCH4;②3.01×1023个HCl;③13.6gH2S;④0.2molNH3质量从小到大的顺序为:___________ 氢原子数从小到大的顺序为:___________ (用序号表示)。
(1)已知下列反应:①HPO3+H2O=H3PO4;②2Na2O2+2H2O=4NaOH+O2↑;③ 2F2+2H2O=4HF+O2;④2K+2H2O=2KOH+H2↑;⑤Cl2+H2O=HCl+HClO,其中,H2O做氧化剂的是
(2)标准状况下有四种气体①6.72LCH4;②3.01×1023个HCl;③13.6gH2S;④0.2molNH3质量从小到大的顺序为:
更新时间:2024-02-25 10:46:03
|
相似题推荐
填空题
|
较易
(0.85)
名校
【推荐1】物质的量是高中化学常用的物理量,请完成以下问题:
(1)某气体氧化物的化学式为 ,在标准状况下,
,在标准状况下, 该氧化物的体积为
该氧化物的体积为 ,则该氧化物的摩尔质量为
,则该氧化物的摩尔质量为__________ ,R的相对原子质量为__________ 。
(2)相同物质的量的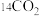 与
与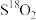 的质量之比为
的质量之比为__________ ;所含中子数之比为__________ ;所含电子数之比为__________ 。
(3)在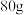 密度为
密度为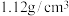 的硫酸铁溶液中,含有
的硫酸铁溶液中,含有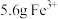 离子,则此溶液中
离子,则此溶液中 的物质的量浓度为
的物质的量浓度为__________ 。
(4)某溶液中含有离子: 、
、 、
、 、
、 ,测得
,测得 、
、 和
和 的物质的量浓度依次为:
的物质的量浓度依次为: 、
、 、
、 ,则
,则
__________
(5)有等体积的 、
、 、
、 三种溶液,分别与足量的
三种溶液,分别与足量的 溶液反应,若生成沉淀的质量相等,则三种溶液中所含溶质的物质的量浓度之比为
溶液反应,若生成沉淀的质量相等,则三种溶液中所含溶质的物质的量浓度之比为__________ 。
(1)某气体氧化物的化学式为
 ,在标准状况下,
,在标准状况下, 该氧化物的体积为
该氧化物的体积为 ,则该氧化物的摩尔质量为
,则该氧化物的摩尔质量为(2)相同物质的量的
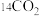 与
与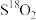 的质量之比为
的质量之比为(3)在
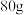 密度为
密度为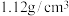 的硫酸铁溶液中,含有
的硫酸铁溶液中,含有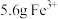 离子,则此溶液中
离子,则此溶液中 的物质的量浓度为
的物质的量浓度为(4)某溶液中含有离子:
 、
、 、
、 、
、 ,测得
,测得 、
、 和
和 的物质的量浓度依次为:
的物质的量浓度依次为: 、
、 、
、 ,则
,则
(5)有等体积的
 、
、 、
、 三种溶液,分别与足量的
三种溶液,分别与足量的 溶液反应,若生成沉淀的质量相等,则三种溶液中所含溶质的物质的量浓度之比为
溶液反应,若生成沉淀的质量相等,则三种溶液中所含溶质的物质的量浓度之比为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】在标准状况下,体积为8.96L的CO和CO2的混合气体共14.4g。请计算:
(1)CO的质量_______ ;
(2)CO2的体积_______ ;
(3)混合气体的平均摩尔质量______ ;
(4)混合气体的密度(小数点后保留1位)_________ 。
(1)CO的质量
(2)CO2的体积
(3)混合气体的平均摩尔质量
(4)混合气体的密度(小数点后保留1位)
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】20世纪80年代,物理学家们发现了一种新的陶瓷材料,其可以在零下200摄氏度左右的环境下实现超导性,也因此被称作“高温超导体”。这些陶瓷材料其中有一种是钇钡铜氧化合物(YBa2Cu3O7),未来或可应用于超导电缆、马达以及发电机等设备。
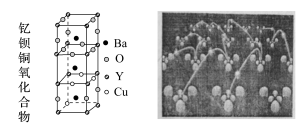
(1)66.7g该超导陶瓷的物质的量是_______ (相对原子质量为Y:89,Ba:137,Cu:64)。
(2)0.6mol该晶体中含有的氧原子数目是_______ 。

(1)66.7g该超导陶瓷的物质的量是
(2)0.6mol该晶体中含有的氧原子数目是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】(1)在同温同压下,11.5g气体A所占的体积和8gO2所占的体积相同,气体A的摩尔质量为____________________
(2)6.72L氯气(Cl2) ( 标准状况下 ) 和元素R完全反应, 生成0.2molRCln, 则n值为___________
(3)0.3mol的氧气和0.2mol的臭氧(O3),它们的质量之比_____________ ,它们所含分子数之比________ ,所含氧原子数之比________ 。
(2)6.72L氯气(Cl2) ( 标准状况下 ) 和元素R完全反应, 生成0.2molRCln, 则n值为
(3)0.3mol的氧气和0.2mol的臭氧(O3),它们的质量之比
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】回答下列问题:
(1)56g氮气在标准状况下的体积为____ 。
(2)3.9gNa2O2中Na+的数目为____ 。
(3)现有标准状况下CO和CO2混合气体6.72L,其质量为11.6g,则此混合气体中,CO和CO2的物质的量之比是____ 。
(1)56g氮气在标准状况下的体积为
(2)3.9gNa2O2中Na+的数目为
(3)现有标准状况下CO和CO2混合气体6.72L,其质量为11.6g,则此混合气体中,CO和CO2的物质的量之比是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】I.根据物质的组成、结构、性质等进行分类,可预剥物质的性质及变化:
现有下列九种物质:①HCl气体②固体Cu③乙醇④三氧化硫⑤熔融NaCl⑥Al2O3固体⑦硫酸溶液⑧NaHCO3固体⑨硫酸钡固体。按照不同的依据对其进行分类:
(1)所给状态能导电的是________ ,属于电解质的是_______ ;属于非电解质的是________ (均填序号)。
(2)属于酸式盐的物质为___________ (填序号),其电离方程式为___________ 。
(3)属于两性氧化物的是___________ (填序号),请从9种物质中选出一种物质与其反应,对应的化学反应方程式为___________ 。
Ⅱ.物质的量是联系宏观和微观的桥梁:
(4)40.5g某金属氧化物MCl2中含0.6molCl-,则该氯化物的摩尔质量为___________ 。
(5)标准状况下,与34g的H2S气体含相同H原子数的CH4的体积为___________ 。
(6)在同温同压下,等质量的CO和CO2.其体积之比为___________ ,密度之比为___________ ,质子数之比为___________ 。
现有下列九种物质:①HCl气体②固体Cu③乙醇④三氧化硫⑤熔融NaCl⑥Al2O3固体⑦硫酸溶液⑧NaHCO3固体⑨硫酸钡固体。按照不同的依据对其进行分类:
(1)所给状态能导电的是
(2)属于酸式盐的物质为
(3)属于两性氧化物的是
Ⅱ.物质的量是联系宏观和微观的桥梁:
(4)40.5g某金属氧化物MCl2中含0.6molCl-,则该氯化物的摩尔质量为
(5)标准状况下,与34g的H2S气体含相同H原子数的CH4的体积为
(6)在同温同压下,等质量的CO和CO2.其体积之比为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】现有① ②
② ③
③ ④
④ ⑤CO ⑥Al六种物质,从氧化性、还原性的角度分类,若将常用的氧化剂放入甲中,常用的还原剂放入乙中,则:
⑤CO ⑥Al六种物质,从氧化性、还原性的角度分类,若将常用的氧化剂放入甲中,常用的还原剂放入乙中,则:
(1)甲中有________ ;乙中有________ 。(填序号)
(2)由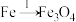 ,
,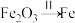 可知,欲实现I反应过程应从
可知,欲实现I反应过程应从________ (填“甲”或“乙”,下同)中找物质,欲实现Ⅱ反应过程应从________ 中找物质。
(3)请将下列6种物质: 、
、 、
、 、
、 、
、 、
、 (提示:能按
(提示:能按 ________+________→________+________+
________+________→________+________+ 形式反生化学反应)写出该反应对应的离子方式
形式反生化学反应)写出该反应对应的离子方式_______ ;并在离子方程式上标出电子转移的方向和数目______ 。
(4)一氧化氮是工业制硝酸的中间产物,生成一氧化氮的化学方程式为: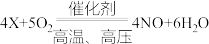 ,请推出X的化学式为
,请推出X的化学式为_____ 。
 ②
② ③
③ ④
④ ⑤CO ⑥Al六种物质,从氧化性、还原性的角度分类,若将常用的氧化剂放入甲中,常用的还原剂放入乙中,则:
⑤CO ⑥Al六种物质,从氧化性、还原性的角度分类,若将常用的氧化剂放入甲中,常用的还原剂放入乙中,则:(1)甲中有
(2)由
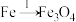 ,
,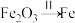 可知,欲实现I反应过程应从
可知,欲实现I反应过程应从(3)请将下列6种物质:
 、
、 、
、 、
、 、
、 、
、 (提示:能按
(提示:能按 ________+________→________+________+
________+________→________+________+ 形式反生化学反应)写出该反应对应的离子方式
形式反生化学反应)写出该反应对应的离子方式(4)一氧化氮是工业制硝酸的中间产物,生成一氧化氮的化学方程式为:
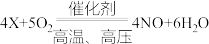 ,请推出X的化学式为
,请推出X的化学式为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】按要求回答下列问题:
(1)下列几种物质:①铜丝 ②石墨 ③ ④
④ 溶液 ⑤氨水 ⑥液氧 ⑦
溶液 ⑤氨水 ⑥液氧 ⑦ 胶体 ⑧熔融
胶体 ⑧熔融 ⑨蔗糖 ⑩
⑨蔗糖 ⑩ 晶体。
晶体。
以上物质中能导电的是______ (填序号,下同);属于电解质的是______ 。
(2)黑火药是我国古代的四大发明之一、黑火药着火时,发生如下氧化还原反应:
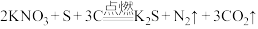 。在此反应中,被还原的元素为
。在此反应中,被还原的元素为______ (填元素符号),氧化产物是______ (填化学式),当该反应转移3mol电子时,产生气体的体积为______ L(标况下)。
(3)已知CO、 混合气体的质量共10.0g,在标准状况下的体积为6.72L,则混合气体中CO的质量为
混合气体的质量共10.0g,在标准状况下的体积为6.72L,则混合气体中CO的质量为______ g; 在相同状况下的体积为
在相同状况下的体积为______ L。
(1)下列几种物质:①铜丝 ②石墨 ③
 ④
④ 溶液 ⑤氨水 ⑥液氧 ⑦
溶液 ⑤氨水 ⑥液氧 ⑦ 胶体 ⑧熔融
胶体 ⑧熔融 ⑨蔗糖 ⑩
⑨蔗糖 ⑩ 晶体。
晶体。以上物质中能导电的是
(2)黑火药是我国古代的四大发明之一、黑火药着火时,发生如下氧化还原反应:
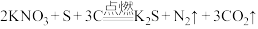 。在此反应中,被还原的元素为
。在此反应中,被还原的元素为(3)已知CO、
 混合气体的质量共10.0g,在标准状况下的体积为6.72L,则混合气体中CO的质量为
混合气体的质量共10.0g,在标准状况下的体积为6.72L,则混合气体中CO的质量为 在相同状况下的体积为
在相同状况下的体积为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】“纳米零价铁—H2O2”体系可将烟气中难溶的NO氧化为可溶的NO 。回答下列问题:
。回答下列问题:
(1)制备纳米零价铁:将FeSO4溶液与碱性NaBH4溶液混合可生成纳米零价铁,反应的化学方程式为FeSO4+NaBH4+NaOH→Fe(纳米零价铁)+NaBO2+Na2SO4+H2↑+H2O(未配平,NaBH4、NaBO2中B元素均为+3价)。该反应中,还原剂和氧化剂的物质的量之比为n(还原剂):n(氧化剂)=____ 。
(2)NO的氧化:在一定温度下,将H2O2溶液和HCl溶液雾化后与烟气按一定比例混合,以一定流速通过装有纳米零价铁的反应装置,可将烟气中的NO氧化。
①Fe2+催化H2O2分解产生HO•,HO•将NO氧化为NO 的机理如图1所示,Y与H2O2反应的离子方程式为
的机理如图1所示,Y与H2O2反应的离子方程式为____ 。

②NO与H2O2反应生成HNO3的化学方程式为____ 。
③纳米零价铁的作用是____ (用离子方程式表示)。
④NO脱除率随温度的变化如图2所示。温度高于120℃时,NO脱除率随温度升高逐渐降低,主要原因是____ 。

(3)氧化产物的吸收:氧化后的产物在烟气的携带下被Ca(OH)2溶液吸收,反应的化学方程式为____ 。
 。回答下列问题:
。回答下列问题:(1)制备纳米零价铁:将FeSO4溶液与碱性NaBH4溶液混合可生成纳米零价铁,反应的化学方程式为FeSO4+NaBH4+NaOH→Fe(纳米零价铁)+NaBO2+Na2SO4+H2↑+H2O(未配平,NaBH4、NaBO2中B元素均为+3价)。该反应中,还原剂和氧化剂的物质的量之比为n(还原剂):n(氧化剂)=
(2)NO的氧化:在一定温度下,将H2O2溶液和HCl溶液雾化后与烟气按一定比例混合,以一定流速通过装有纳米零价铁的反应装置,可将烟气中的NO氧化。
①Fe2+催化H2O2分解产生HO•,HO•将NO氧化为NO
 的机理如图1所示,Y与H2O2反应的离子方程式为
的机理如图1所示,Y与H2O2反应的离子方程式为
②NO与H2O2反应生成HNO3的化学方程式为
③纳米零价铁的作用是
④NO脱除率随温度的变化如图2所示。温度高于120℃时,NO脱除率随温度升高逐渐降低,主要原因是

(3)氧化产物的吸收:氧化后的产物在烟气的携带下被Ca(OH)2溶液吸收,反应的化学方程式为
您最近一年使用:0次
【推荐1】阅读下面科普信息,回答问题:一个体重50kg的健康人含铁2g,这2g铁在入体中以Fe2+和Fe3+的形式存在。亚铁离子易被吸收,给贫血者补充铁时,应给予含亚铁离子的亚铁盐,如硫酸亚铁。服用维生素C,可使食物中的铁离子还原成亚铁离子,有利于铁的吸收。
(1)工业盐的主要成分是NaNO2,曾多次发生过因误食NaNO2而中毒的事件,其原因是NaNO2把人体内的Fe2+转化为Fe3+而失去与O2结合的能力,这说明NaNO2具有____ 性。下列不能实现上述转化的物质是____ (填字母)。
A.Cl2 B.O2 C.FeCl3 D.KMnO4(H+)
(2)工业盐中毒后,可服用维生素C来缓解中毒状况,这说明维生素C具有___ 性。
(3)在Fe+4HNO3(稀)=Fe(NO3)3+NO↑+2H2O的反应中,则56gFe参加反应时,被还原的HNO3为____ g。
(4)请用双线桥法标出下列已知化学方程式电子转移的方向和数目:____ 。
KClO3+6HCl(浓)=KCl+3H2O+3Cl2↑
(1)工业盐的主要成分是NaNO2,曾多次发生过因误食NaNO2而中毒的事件,其原因是NaNO2把人体内的Fe2+转化为Fe3+而失去与O2结合的能力,这说明NaNO2具有
A.Cl2 B.O2 C.FeCl3 D.KMnO4(H+)
(2)工业盐中毒后,可服用维生素C来缓解中毒状况,这说明维生素C具有
(3)在Fe+4HNO3(稀)=Fe(NO3)3+NO↑+2H2O的反应中,则56gFe参加反应时,被还原的HNO3为
(4)请用双线桥法标出下列已知化学方程式电子转移的方向和数目:
KClO3+6HCl(浓)=KCl+3H2O+3Cl2↑
您最近一年使用:0次
【推荐2】工业上可用氨与 反应检验输送氯气的管道是否漏气:
反应检验输送氯气的管道是否漏气:  。
。
(1)作氧化剂的物质是_______ ,氯元素的化合价_______ (填“升高”或“降低”)。
(2)反应中每消耗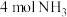 ,生成
,生成 的物质的量是
的物质的量是_______  ,转移电子的物质的量是
,转移电子的物质的量是_______  。
。
 反应检验输送氯气的管道是否漏气:
反应检验输送氯气的管道是否漏气:  。
。(1)作氧化剂的物质是
(2)反应中每消耗
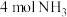 ,生成
,生成 的物质的量是
的物质的量是 ,转移电子的物质的量是
,转移电子的物质的量是 。
。
您最近一年使用:0次
【推荐3】碘酸钾和碘化钾是两种常见的食盐补碘剂。 易溶于水,在水中电离为
易溶于水,在水中电离为 和
和 。回答下列问题:
。回答下列问题:
(1)用铂丝蘸取添加有碘化钾补碘剂的食盐于酒精灯火焰上灼烧,通过观察火焰颜色可证明其中含有钾元素,该实验方法称为_______ ,观察火焰颜色时应采用的操作方法是_______ 。
(2)有如下反应:①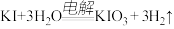 ,②
,②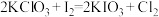 ,③
,③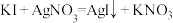 。其中属于氧化还原反应的是反应①和
。其中属于氧化还原反应的是反应①和_______ ,属于置换反应的是_______ ,反应①中被还原的物质是_______ 。
(3)碘酸钾与碘化钾在酸性条件下可发生如下反应: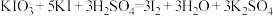 ,写出该反应的离子方程式,并用单线桥标出电子转移的方向和数目:
,写出该反应的离子方程式,并用单线桥标出电子转移的方向和数目:_______ 。
 易溶于水,在水中电离为
易溶于水,在水中电离为 和
和 。回答下列问题:
。回答下列问题:(1)用铂丝蘸取添加有碘化钾补碘剂的食盐于酒精灯火焰上灼烧,通过观察火焰颜色可证明其中含有钾元素,该实验方法称为
(2)有如下反应:①
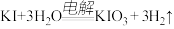 ,②
,②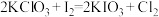 ,③
,③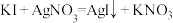 。其中属于氧化还原反应的是反应①和
。其中属于氧化还原反应的是反应①和(3)碘酸钾与碘化钾在酸性条件下可发生如下反应:
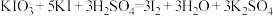 ,写出该反应的离子方程式,并用单线桥标出电子转移的方向和数目:
,写出该反应的离子方程式,并用单线桥标出电子转移的方向和数目:
您最近一年使用:0次



