下列依据热化学方程式得出的结论正确的是
A.已知 (石墨, (石墨, )= )= (金刚石, (金刚石, ) ) ;则金刚石比石墨稳定 ;则金刚石比石墨稳定 |
B.已知: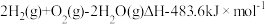 ;则氢气的燃烧热为 ;则氢气的燃烧热为 |
C.已知 ;则 ;则 |
D.已知 ;则含 ;则含 的稀溶液与稀醋酸完全中和,放出 的稀溶液与稀醋酸完全中和,放出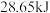 的热量 的热量 |
更新时间:2024-03-12 07:11:20
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列有关叙述正确的是
| A.增大反应物浓度,可提高活化分子百分数,使有效碰撞增多,化学反应速率加快 |
| B.升高温度,可提高活化分子百分数,使有效碰撞增多,化学反应速率加快 |
C.已知 ; ; ,则白磷比红磷稳定 ,则白磷比红磷稳定 |
| D.升温,放热反应的反应速率增大,吸热反应的反应速率减小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列叙述不正确的是
| A.物质发生化学变化一定会伴有能量的变化 |
| B.可逆反应的ΔH表示完全反应时的热量变化,与反应是否可逆无关 |
| C.同温同压下,反应H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件下的ΔH相同 |
| D.水蒸气变为液态水时放出的能量就是该变化的反应热 |
您最近一年使用:0次
【推荐3】化学反应过程中总是伴随着能量的变化。反应中能量变化说法正确的是
| A.相同条件下,2mol氢原子所具有的能量小于1mol氢分子所具有的能量 |
| B.常温下,反应Fe+S=FeS不能自发进行,则该反应的为吸热反应 |
| C.常温常压下,将0.5mol N2和1.5molH2置于某密闭容器中充分反应生成NH3(g),放热QkJ,其热化学方程式为:N2(g)+3H2(g)⇌2NH3(g)+2QkJ |
| D.旧键断裂所吸收的总能量与新键形成所放出的总能量之差,是化学反应的热效应。 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】已知辛烷的燃烧热为5518kJ·mol-1,强酸与强碱在稀溶液中发生反应时的中和热为57.3kJ·mol-1,则下列热化学方程式书写正确的是
①C8H18(l)+25/2O2(g)=8CO2(g)+9H2O(g);△H=-5518kJ·mol-1
②2C8H18(l)+25O2(g)=16CO2(g)+18H2O(l);△H=-11036kJ·mol-1
③H+(aq) + OH-(aq) =H2O(l); △H= +57.3kJ·mol-1
④2NaOH(aq) +H2SO4(aq)=Na2SO4(aq) + 2H2O(l);△H=-57.3kJ·mol-1
①C8H18(l)+25/2O2(g)=8CO2(g)+9H2O(g);△H=-5518kJ·mol-1
②2C8H18(l)+25O2(g)=16CO2(g)+18H2O(l);△H=-11036kJ·mol-1
③H+(aq) + OH-(aq) =H2O(l); △H= +57.3kJ·mol-1
④2NaOH(aq) +H2SO4(aq)=Na2SO4(aq) + 2H2O(l);△H=-57.3kJ·mol-1
| A.①③ | B.②③ | C.②④ | D.只有② |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列说法正确的是
| A.在25°C、101 kPa时,1 mol S(s)和2 mol S(s)分别充分燃烧,S(s)的燃烧热相等 |
| B.含1molH2SO4的稀溶液与含1molBa(OH)2的稀溶液完全中和时所放出的热量为中和热 |
| C.1 mol H2(g)燃烧生成1 mol H2O(g)时放出的热量为H2(g)的燃烧热 |
| D.中和热指的是酸与碱发生中和反应时放出的热量 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列事实与对应的方程式相符的是
A.自然界正常雨水 是因为: 是因为: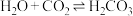 , ,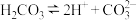 |
B.用 溶液处理水垢中的 溶液处理水垢中的 : :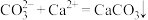 |
C.硫代硫酸钠溶液与稀硫酸混合出现浑浊: |
D.甲烷的燃烧热为890.3 kJ·mol ,则甲烷燃烧的热化学方程式可表示为: ,则甲烷燃烧的热化学方程式可表示为:  kJ/mol kJ/mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列热化学方程式正确的是
A. ;则处于相同条件的石墨更加稳定 ;则处于相同条件的石墨更加稳定 |
B. 混合反应后,放出热量 混合反应后,放出热量 ,则 ,则 |
C. ,则 ,则 |
D. 的燃烧热为 的燃烧热为 ,则 ,则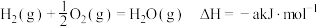 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】下列有关热化学方程式及其叙述正确的是
| A.H2的燃烧热为285.8 kJ/mol,则H2O电解的热化学方程式为2H2O(l)=2H2(g)+O2(g) ΔH=+285.8 kJ/mol |
| B.3.2克 CH4完全燃烧生成CO2(g)和H2O(l)时放出178 kJ的热量,其热化学方程式为CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH=-890kJ/mol |
| C.已知2C(s)+O2(g)=2CO(g) ΔH=-221 kJ/mol,则C的燃烧热为110.5 kJ/mol |
| D.含有1 mol的HF与NaOH溶液反应放热57.3 kJ:H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3 kJ/mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列各组反应中关于能量的比较正确的是( )
①H2(g)+Cl2(g)=2HCl(g)△H1; H2(g)+
H2(g)+ Cl2(g)=HCl (g)△H2;△H1>△H2
Cl2(g)=HCl (g)△H2;△H1>△H2
②2H2O(l)=2H2(g)+O2(g)△H1; 2Na(s)+2H2O(l)=2NaOH(aq)+H2(g)△H2;△H1>△H2
③CH3OH(g)+ O2(g)=CO2(g)+2H2O(l)△H1;CH3OH(l)+
O2(g)=CO2(g)+2H2O(l)△H1;CH3OH(l)+ O2(g)=CO2(g)+2H2O(g)△H2;△H1<△H2
O2(g)=CO2(g)+2H2O(g)△H2;△H1<△H2
④t℃时,在一定条件下,将 1mol N2和 3mol H2 分别置于恒容和恒压的两个密闭容器中,达到平衡状态时放出的热量分别为 Q1、Q2; Q1<Q2.
①H2(g)+Cl2(g)=2HCl(g)△H1;
 H2(g)+
H2(g)+ Cl2(g)=HCl (g)△H2;△H1>△H2
Cl2(g)=HCl (g)△H2;△H1>△H2②2H2O(l)=2H2(g)+O2(g)△H1; 2Na(s)+2H2O(l)=2NaOH(aq)+H2(g)△H2;△H1>△H2
③CH3OH(g)+
 O2(g)=CO2(g)+2H2O(l)△H1;CH3OH(l)+
O2(g)=CO2(g)+2H2O(l)△H1;CH3OH(l)+ O2(g)=CO2(g)+2H2O(g)△H2;△H1<△H2
O2(g)=CO2(g)+2H2O(g)△H2;△H1<△H2④t℃时,在一定条件下,将 1mol N2和 3mol H2 分别置于恒容和恒压的两个密闭容器中,达到平衡状态时放出的热量分别为 Q1、Q2; Q1<Q2.
| A.①③④ | B.①②④ | C.②③④ | D.①③ |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】根据以下热化学方程式中, 的是
的是
 的是
的是A.  ; ;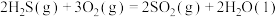  |
B.  ; ;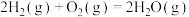  |
C.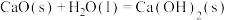  : :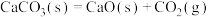  |
D.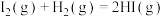  ; ;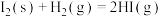  |
您最近一年使用:0次

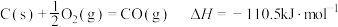 ,则
,则 的燃烧热为
的燃烧热为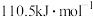
 和
和 在一定条件下反应放出热量86kJ,热化学反应方程式为:
在一定条件下反应放出热量86kJ,热化学反应方程式为: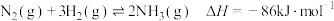
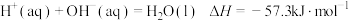 ,则稀硫酸与稀氢氧化钠溶液反应生成
,则稀硫酸与稀氢氧化钠溶液反应生成 水时,放热
水时,放热
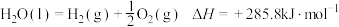 ,则
,则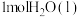 的总能量比
的总能量比 小
小