某研究性学习小组学生根据氧化还原反应规律,探究 、
、 与
与 反应的情况,提出假设并进行相关实验。
反应的情况,提出假设并进行相关实验。
Ⅰ.从理论上分析 和
和 都既有氧化性又有还原性,于是提出如下假设:
都既有氧化性又有还原性,于是提出如下假设:
假设1: 氧化
氧化 ;
;
假设2: 氧化
氧化 。
。
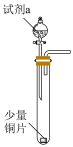
(1)甲同学设计如图装置进行实验:___________ 。
②待试管B中充满红棕色气体,关闭旋塞a和b;取下试管B,向其中加入适量 粉末,塞上塞子,轻轻振荡试管内粉末,观察到红棕色气体迅速消失;再将带火星的木条迅速伸进试管内,木条复燃。
粉末,塞上塞子,轻轻振荡试管内粉末,观察到红棕色气体迅速消失;再将带火星的木条迅速伸进试管内,木条复燃。
结论:甲同学认为假设2正确。
(2)乙同学认为甲同学设计的实验存在缺陷,为达到实验目的,在A、B之间应增加一个装置,该装置的作用是___________ 。乙同学用改进后的装置,重复了甲同学的实验操作,观察到红棕色气体迅速消失;带火星的木条未复燃,得出结论:假设Ⅰ正确。则 和
和 反应的化学方程式是
反应的化学方程式是___________ 。
Ⅱ.该研究性学习小组同学还认为易与 发生反应,应该更易被氧化。查阅资料:
发生反应,应该更易被氧化。查阅资料: ;
;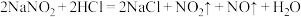 ;酸性条件下,能与
;酸性条件下,能与 反应生成
反应生成 和
和 。
。
(3)丙同学用下图所示装置(部分夹持装置略)探究 与
与 的反应。
的反应。 ,目的是
,目的是___________ 。
②B中观察到的主要现象的是___________ (填字母编号)。
a.铜片逐渐溶解,溶液变为蓝色
b.有红棕色气泡产生
c.有无色气泡产生
③C、E中所盛装的试剂不能是___________ (填字母编号)。
a.无水硫酸铜 b.无水氯化钙 c.碱石灰 d.生石灰
④充分反应后,检验D装置中产物的方法是:取D装置中产物少许,___________ ,则产物是 。
。
 、
、 与
与 反应的情况,提出假设并进行相关实验。
反应的情况,提出假设并进行相关实验。Ⅰ.从理论上分析
 和
和 都既有氧化性又有还原性,于是提出如下假设:
都既有氧化性又有还原性,于是提出如下假设:假设1:
 氧化
氧化 ;
;假设2:
 氧化
氧化 。
。(1)甲同学设计如图装置进行实验:

②待试管B中充满红棕色气体,关闭旋塞a和b;取下试管B,向其中加入适量
 粉末,塞上塞子,轻轻振荡试管内粉末,观察到红棕色气体迅速消失;再将带火星的木条迅速伸进试管内,木条复燃。
粉末,塞上塞子,轻轻振荡试管内粉末,观察到红棕色气体迅速消失;再将带火星的木条迅速伸进试管内,木条复燃。结论:甲同学认为假设2正确。
(2)乙同学认为甲同学设计的实验存在缺陷,为达到实验目的,在A、B之间应增加一个装置,该装置的作用是
 和
和 反应的化学方程式是
反应的化学方程式是Ⅱ.该研究性学习小组同学还认为易与
 发生反应,应该更易被氧化。查阅资料:
发生反应,应该更易被氧化。查阅资料: ;
;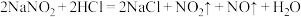 ;酸性条件下,能与
;酸性条件下,能与 反应生成
反应生成 和
和 。
。(3)丙同学用下图所示装置(部分夹持装置略)探究
 与
与 的反应。
的反应。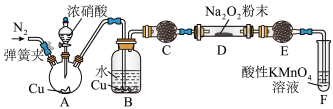
 ,目的是
,目的是②B中观察到的主要现象的是
a.铜片逐渐溶解,溶液变为蓝色
b.有红棕色气泡产生
c.有无色气泡产生
③C、E中所盛装的试剂不能是
a.无水硫酸铜 b.无水氯化钙 c.碱石灰 d.生石灰
④充分反应后,检验D装置中产物的方法是:取D装置中产物少许,
 。
。
更新时间:2024-04-08 16:49:47
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】工业上由含铜废料(含有Cu、CuS、CuSO4等)制备硝酸铜晶体的流程如图:
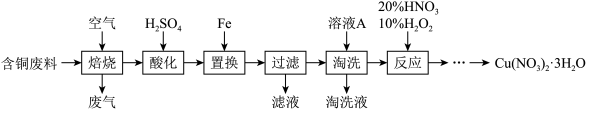
(1)“焙烧”时CuS转化为CuO和SO2,反应的化学方程式为___ 。
(2)“酸化”步骤反应的离子方程式为___ 。
(3)“过滤”所得滤液中溶质的主要成分为___ 。
(4)“淘洗”所用的溶液A应选用___ (填序号)。
a.稀硫酸 b.浓硫酸 c.稀硝酸 d.浓硝酸
(5)“反应”一步的过程中无红棕色气体生成。
①理论上消耗HNO3和H2O2的物质的量之比为___ 。
②若不加10% H2O2,只用浓HNO3,随着反应的进行,容器内持续出现大量红棕色气体,写出该反应的离子方程式____ 。
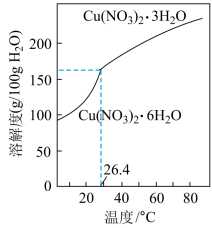
(6)由“反应”所得溶液中尽可能多地析出Cu(NO3)2·3H2O晶体的方法是___ 。(相关物质的溶解度曲线如图所示)

(1)“焙烧”时CuS转化为CuO和SO2,反应的化学方程式为
(2)“酸化”步骤反应的离子方程式为
(3)“过滤”所得滤液中溶质的主要成分为
(4)“淘洗”所用的溶液A应选用
a.稀硫酸 b.浓硫酸 c.稀硝酸 d.浓硝酸
(5)“反应”一步的过程中无红棕色气体生成。
①理论上消耗HNO3和H2O2的物质的量之比为
②若不加10% H2O2,只用浓HNO3,随着反应的进行,容器内持续出现大量红棕色气体,写出该反应的离子方程式
(6)由“反应”所得溶液中尽可能多地析出Cu(NO3)2·3H2O晶体的方法是

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】实验小组研究铜与过量硝酸的反应,实验如下(加持装置和尾气处理装置略)。
(1)氮在元素周期表中的位置为___________ 。
(2)实验Ⅰ、Ⅱ中的红棕色气体均是NO2.实验Ⅰ产生NO2的化学方程式是___________ 。
(3)对实验Ⅰ产生NO2,实验Ⅱ产生NO的原因提出解释。
①硝酸浓度越稀,溶液中单位体积内的NO 数目越少。被还原时,每个NO
数目越少。被还原时,每个NO 从铜片处获得较多电子的机会越
从铜片处获得较多电子的机会越___________ (填“大”或“小”),因此越易被还原为较低价态的含氮物质。
②浓硝酸具有较强的___________ 性,可将NO转化为NO2。
(4)有同学针对I中溶液呈绿色的原因,提出假设:
假设1:Cu2+的浓度较大所致;假设2:溶解了生成的NO2。
探究如下:取I中绿色溶液,分为两等份。
①取一份于如图所示装置中,向上拉动活塞a,___________ (填现象),证实I中溶解了NO2。___________ (填化学试剂),溶液变为蓝色。证实假设1不成立,假设2成立。
(5)硝酸与金属反应会产生氮氧化物。
①下列环境问题与氮的氧化物排放无关的是___________ 。
A.酸雨B.光化学烟雾C温室效应 D.白色污染
②在含有agHNO3的稀硝酸中,加入bg铁粉充分反应,铁全部溶解并生成NO,有0.25agHNO3被还原,则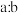 可能为
可能为___________ 。
A.2:1 B.3:1 C.4:1 D.9:2
③为避免氮氧化物污染环境,人们开发了溶液吸收法。比如用碱性的Na2CO3溶液吸收NO2,请写出相关的化学反应方程式:___________ 。
| 装置 | 编号 | 试剂a | 现象 |
| Ⅰ | 4mL浓硝酸(过量) | 铜片完全溶解,溶液变绿,出现大量红棕色气体 |
| Ⅱ | 4mL稀硝酸(过量) | 铜片完全溶解,溶液变蓝,液面上方气体呈浅红棕色 |
(1)氮在元素周期表中的位置为
(2)实验Ⅰ、Ⅱ中的红棕色气体均是NO2.实验Ⅰ产生NO2的化学方程式是
(3)对实验Ⅰ产生NO2,实验Ⅱ产生NO的原因提出解释。
①硝酸浓度越稀,溶液中单位体积内的NO
 数目越少。被还原时,每个NO
数目越少。被还原时,每个NO 从铜片处获得较多电子的机会越
从铜片处获得较多电子的机会越②浓硝酸具有较强的
(4)有同学针对I中溶液呈绿色的原因,提出假设:
假设1:Cu2+的浓度较大所致;假设2:溶解了生成的NO2。
探究如下:取I中绿色溶液,分为两等份。
①取一份于如图所示装置中,向上拉动活塞a,

(5)硝酸与金属反应会产生氮氧化物。
①下列环境问题与氮的氧化物排放无关的是
A.酸雨B.光化学烟雾C温室效应 D.白色污染
②在含有agHNO3的稀硝酸中,加入bg铁粉充分反应,铁全部溶解并生成NO,有0.25agHNO3被还原,则
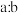 可能为
可能为A.2:1 B.3:1 C.4:1 D.9:2
③为避免氮氧化物污染环境,人们开发了溶液吸收法。比如用碱性的Na2CO3溶液吸收NO2,请写出相关的化学反应方程式:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】某化学自主实验小组利用如图所示装置探究 能否被
能否被 还原(
还原( 、
、 为止水夹,部分夹持固定装置略去)。
为止水夹,部分夹持固定装置略去)。
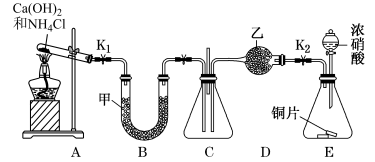
(1)A装置中制取 的化学方程式是
的化学方程式是___________ 。
(2)甲、乙分别是___________(填字母)。
(3)若 能够被
能够被 还原,预期C装置中能观察到的现象是
还原,预期C装置中能观察到的现象是___________ 。
(4)此实验装置存在一个明显的缺陷是___________ 。
(5)工业上常用碱液来吸收 ,有关的化学反应:
,有关的化学反应:
①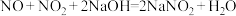
②
现有一定条件下amol 和bmol NO的混合气体恰好被200mL NaOH溶液完全吸收,则a、b应满足的关系为
和bmol NO的混合气体恰好被200mL NaOH溶液完全吸收,则a、b应满足的关系为___________ ,NaOH溶液的物质的量浓度为___________  (用含a、b的式子表示)。
(用含a、b的式子表示)。
 能否被
能否被 还原(
还原( 、
、 为止水夹,部分夹持固定装置略去)。
为止水夹,部分夹持固定装置略去)。
(1)A装置中制取
 的化学方程式是
的化学方程式是(2)甲、乙分别是___________(填字母)。
| A.硫酸、碱石灰 | B.碱石灰、碱石灰 |
| C.碱石灰、无水氯化钙 | D.五氧化二磷、五氧化二磷 |
 能够被
能够被 还原,预期C装置中能观察到的现象是
还原,预期C装置中能观察到的现象是(4)此实验装置存在一个明显的缺陷是
(5)工业上常用碱液来吸收
 ,有关的化学反应:
,有关的化学反应:①
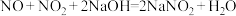
②

现有一定条件下amol
 和bmol NO的混合气体恰好被200mL NaOH溶液完全吸收,则a、b应满足的关系为
和bmol NO的混合气体恰好被200mL NaOH溶液完全吸收,则a、b应满足的关系为 (用含a、b的式子表示)。
(用含a、b的式子表示)。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】某实验小组研究Na2O2与水的反应,实验如图所示:
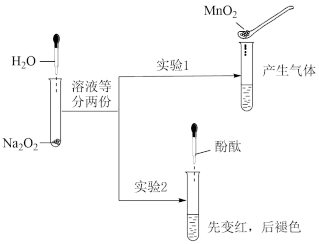
(1)结合实验1和实验2的现象,推测出Na2O2与水的反应经历2个反应过程,写出第一个反应的化学方程式:___ 。
Ⅱ.实验小组对实验2现象中“后褪色”做了进一步的探究。
(2)甲同学猜测:H2O2氧化了酚酞,导致溶液褪色,并向实验2褪色后的溶液中滴加酚酞,若溶液中的现象是:___ ,则猜测正确。
(3)甲同学查阅资料,H2O2溶液中主要存在H2O2 H++HO
H++HO ,K=2×10-12。实验小组进行实验。
,K=2×10-12。实验小组进行实验。
实验3:配制20mL3%H2O2与NaOH的混合溶液,调节pH分别为10~14。再滴入3滴酚酞试液,搅拌后静置,记录酚酞完全褪色的时间,实验结果如图所示:
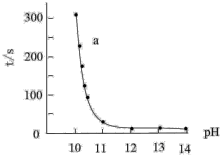
结论:溶液褪色起氧化作用的微粒为____ (填“H2O2”或“HO ”),解释原因:
”),解释原因:_____ 。
(4)乙同学查阅资料发现酚酞(以H2In表示)存在多种结构,其颜色及转化关系为:H2In(无色) HIn-(红色)
HIn-(红色)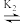 In2-(红色)
In2-(红色)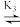 In(OH)3-(无色)。在不同pH下粒子分布曲线如图所示。
In(OH)3-(无色)。在不同pH下粒子分布曲线如图所示。
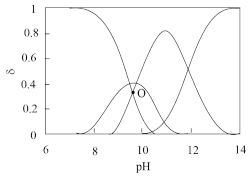
①O点的pH=_____ (用K1、K2表示)
②乙同学猜测溶液褪色的另一原因是:____ 。
(5)针对甲、乙同学的猜测,该实验小组设计了如图实验:
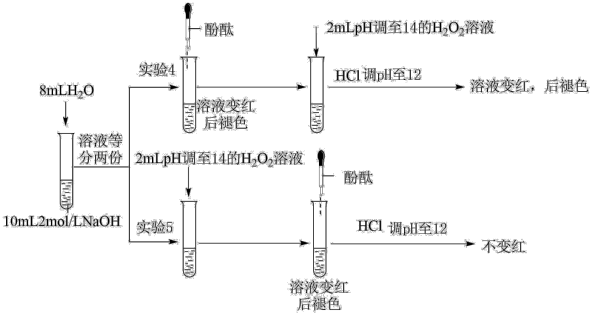
①In(OH)3-比In2-更____ 被氧化(填“难”或“易”)。
②根据实验得出结论:甲、乙两同学的推测均合理,与不同环境下存在微粒的种类及其性质有关。请解释甲同学实验3中pH˃13时红色褪去的主要原因是____ 猜测(填“甲”或“乙”)

(1)结合实验1和实验2的现象,推测出Na2O2与水的反应经历2个反应过程,写出第一个反应的化学方程式:
Ⅱ.实验小组对实验2现象中“后褪色”做了进一步的探究。
(2)甲同学猜测:H2O2氧化了酚酞,导致溶液褪色,并向实验2褪色后的溶液中滴加酚酞,若溶液中的现象是:
(3)甲同学查阅资料,H2O2溶液中主要存在H2O2
 H++HO
H++HO ,K=2×10-12。实验小组进行实验。
,K=2×10-12。实验小组进行实验。实验3:配制20mL3%H2O2与NaOH的混合溶液,调节pH分别为10~14。再滴入3滴酚酞试液,搅拌后静置,记录酚酞完全褪色的时间,实验结果如图所示:

结论:溶液褪色起氧化作用的微粒为
 ”),解释原因:
”),解释原因:(4)乙同学查阅资料发现酚酞(以H2In表示)存在多种结构,其颜色及转化关系为:H2In(无色)
 HIn-(红色)
HIn-(红色)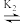 In2-(红色)
In2-(红色)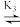 In(OH)3-(无色)。在不同pH下粒子分布曲线如图所示。
In(OH)3-(无色)。在不同pH下粒子分布曲线如图所示。
①O点的pH=
②乙同学猜测溶液褪色的另一原因是:
(5)针对甲、乙同学的猜测,该实验小组设计了如图实验:

①In(OH)3-比In2-更
②根据实验得出结论:甲、乙两同学的推测均合理,与不同环境下存在微粒的种类及其性质有关。请解释甲同学实验3中pH˃13时红色褪去的主要原因是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】有A、B两种常见化合物,其焰色反应均呈黄色,C是一种单质气体,相互转化关系如图所示(其他物质均已略去)。回答下列问题:
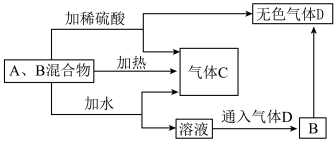
(1)写出A的化学式____________________________________________________ 。
(2)①B加热产生D的化学方程式:____________________________________________________ 。
②B加稀硫酸产生D的离子方程式:_____________________________________________________ 。
(3)请用化学方程式表示A在潜水艇中的一种重要用途___________________ 。
(4)A、B在密闭装置中加热,充分反应后,若只得到一种固体化合物E,其化学式为___________ 。

(1)写出A的化学式
(2)①B加热产生D的化学方程式:
②B加稀硫酸产生D的离子方程式:
(3)请用化学方程式表示A在潜水艇中的一种重要用途
(4)A、B在密闭装置中加热,充分反应后,若只得到一种固体化合物E,其化学式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】现有中学化学常见的A、B、C、D、E、F、G、H、M九种物质,其中A为淡黄色粉末,B为日常生活中最常见的无色无味液体,E为无色气体单质。F的水溶液与石灰水混合可得D的溶液,G为黄绿色气体单质,H是“84”消毒液的有效成分,它们之间的相互转化关系如图所示,其他与题无关的生成物均已略去。

回答下列问题:
(1)写出F的化学式:_______ ,M的化学式:_______ 。
(2)化合物A中非金属元素的化合价是_______ ,物质H的名称是_______ 。
(3)写出反应D→H的化学方程式_______ ,写出反应①的离子方程式:_______ 。
(4)“84”消毒液的有效成分是_______ (填化学式)。
(5)“84”消毒液久置于空气而失效。用化学方程式表示“84”消毒液在空气中易失效的原因:_______ 。
(6)已知浓盐酸和次氯酸钙能发生如下反应:Ca(ClO)2+4HCl(浓)=CaCl2+2Cl2↑+2H2O用贮存很久的漂白粉与浓盐酸制得的氯气中,可能含有的杂质气体是_______ (填字母)。
①CO2 ②HCl ③H2O ④O2
A.①②③ B.②③④ C.②③

回答下列问题:
(1)写出F的化学式:
(2)化合物A中非金属元素的化合价是
(3)写出反应D→H的化学方程式
(4)“84”消毒液的有效成分是
(5)“84”消毒液久置于空气而失效。用化学方程式表示“84”消毒液在空气中易失效的原因:
(6)已知浓盐酸和次氯酸钙能发生如下反应:Ca(ClO)2+4HCl(浓)=CaCl2+2Cl2↑+2H2O用贮存很久的漂白粉与浓盐酸制得的氯气中,可能含有的杂质气体是
①CO2 ②HCl ③H2O ④O2
A.①②③ B.②③④ C.②③
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】在初中化学“金属的性质”中有如下实验:将无锈铁钉没入 溶液,观察到铁钉表面出现红色物质。研究性学习小组对其展开了进一步探究。
溶液,观察到铁钉表面出现红色物质。研究性学习小组对其展开了进一步探究。
【提出问题】Al和 溶液也能发生化学反应吗?
溶液也能发生化学反应吗?
(1)预测Al能和
 溶液反应,理由是
溶液反应,理由是___________ 。
【进行实验】将一端缠绕的铝丝浸入 溶液(如图),观察现象。
溶液(如图),观察现象。
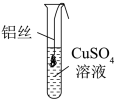
(2)铝丝表面未出现红色物质,原因是___________ (用化学方程式解释)。
【实验改进】用砂纸将铝丝表面打磨光亮,将其浸入 溶液,观察现象。
溶液,观察现象。
(3)填写实验报告单:
【深入探究】为研究上述异常现象,同学们查阅了相关资料,继续开展探究。
资料:① 呈蓝绿色,不溶于水;②
呈蓝绿色,不溶于水;② 可加快铝丝和其他物质的反应速率。
可加快铝丝和其他物质的反应速率。
(4)取出铝丝,将试管中的混合物分离得到蓝绿色固体。加入稀硫酸,固体溶解形成蓝色溶液,该反应的化学方程式为___________ 。
(5)欲加快Al和
 溶液的反应,可加入的物质是
溶液的反应,可加入的物质是___________ (填一种即可)。
【拓展应用】通过探究,同学们提出了铝制品使用的注意事项。
(6)下列食品不能长时间用铝制炊具盛放的是___________(填序号)。
 溶液,观察到铁钉表面出现红色物质。研究性学习小组对其展开了进一步探究。
溶液,观察到铁钉表面出现红色物质。研究性学习小组对其展开了进一步探究。【提出问题】Al和
 溶液也能发生化学反应吗?
溶液也能发生化学反应吗?(1)预测Al能和
 溶液反应,理由是
溶液反应,理由是【进行实验】将一端缠绕的铝丝浸入
 溶液(如图),观察现象。
溶液(如图),观察现象。
(2)铝丝表面未出现红色物质,原因是
【实验改进】用砂纸将铝丝表面打磨光亮,将其浸入
 溶液,观察现象。
溶液,观察现象。(3)填写实验报告单:
| 序号 | 实验现象 | 结论与解释 |
| ① | 铝丝表面有少量气泡;铝丝周围出现蓝绿色物质 |  溶液呈弱酸性,与Al反应产生的气体是 溶液呈弱酸性,与Al反应产生的气体是 |
| ② |  后,铝丝仍光亮; 后,铝丝仍光亮;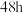 后,铝丝表面出现少量红色物质 后,铝丝表面出现少量红色物质 | 红色物质是 溶液反应,但反应较慢 溶液反应,但反应较慢 |
| ③ | 铝丝周围溶液逐渐变成无色,铝丝以下溶液仍为蓝色;两层溶液界面清晰 | 反应生成的 为无色; 为无色; 溶液的密度小于 溶液的密度小于 溶液 溶液 |
【深入探究】为研究上述异常现象,同学们查阅了相关资料,继续开展探究。
资料:①
 呈蓝绿色,不溶于水;②
呈蓝绿色,不溶于水;② 可加快铝丝和其他物质的反应速率。
可加快铝丝和其他物质的反应速率。(4)取出铝丝,将试管中的混合物分离得到蓝绿色固体。加入稀硫酸,固体溶解形成蓝色溶液,该反应的化学方程式为
(5)欲加快Al和
 溶液的反应,可加入的物质是
溶液的反应,可加入的物质是【拓展应用】通过探究,同学们提出了铝制品使用的注意事项。
(6)下列食品不能长时间用铝制炊具盛放的是___________(填序号)。
| A.食醋 | B.食用油 | C.面粉 | D.咸菜 |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】实验室用下图所示装置制备氯气并进行性质实验(必要时可加热,夹持装置已省略)。
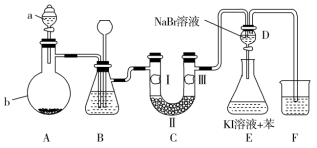
(1)仪器a的名称是_______ ;蒸馏烧瓶b中发生反应的化学方程式为_______ 。
(2)洗气装置B中试剂是饱和食盐水,其作用是_______ ,分液漏斗D中发生反应的离子方程式为_______ 。
(3)装置C中I、II、III依次放入湿润的有色布条、无水氯化钙、干燥的有色布条,设计C装置的目的是_______ 。
(4)E瓶中实验现象_______ 。

(1)仪器a的名称是
(2)洗气装置B中试剂是饱和食盐水,其作用是
(3)装置C中I、II、III依次放入湿润的有色布条、无水氯化钙、干燥的有色布条,设计C装置的目的是
(4)E瓶中实验现象
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】为了探究实验室制氯气过程中反应物与生成氯气之间量的关系,设计了如下图所示的装置。
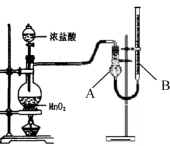
(1)装置A的名称是_____________________ 。
(2)该实验装置检查气密性的方法是________________________________ 。
(3)如果将过量二氧化锰与20mL 12mol/L的盐酸混合加热,充分反应后收集到的氯气少于0.06mol,其可能原因有__________
a.加热使浓盐酸挥发出大量HCl b.盐酸变稀后不发生该反应
c.烧瓶中残留有氯气 d.装置B中液面高于A

(1)装置A的名称是
(2)该实验装置检查气密性的方法是
(3)如果将过量二氧化锰与20mL 12mol/L的盐酸混合加热,充分反应后收集到的氯气少于0.06mol,其可能原因有
a.加热使浓盐酸挥发出大量HCl b.盐酸变稀后不发生该反应
c.烧瓶中残留有氯气 d.装置B中液面高于A
您最近一年使用:0次