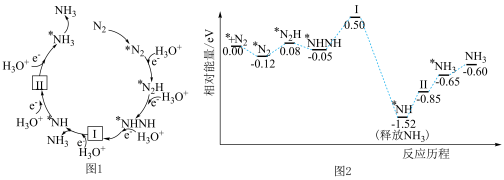
科研人员利用高压 气流将水微滴喷射到涂覆催化剂的石墨网上,研究常温制氨,其反应历程中微粒转化关系如图1,相对能量变化关系如图2,图中“*”表示催化剂表面吸附位。下列说法错误的是
气流将水微滴喷射到涂覆催化剂的石墨网上,研究常温制氨,其反应历程中微粒转化关系如图1,相对能量变化关系如图2,图中“*”表示催化剂表面吸附位。下列说法错误的是
 气流将水微滴喷射到涂覆催化剂的石墨网上,研究常温制氨,其反应历程中微粒转化关系如图1,相对能量变化关系如图2,图中“*”表示催化剂表面吸附位。下列说法错误的是
气流将水微滴喷射到涂覆催化剂的石墨网上,研究常温制氨,其反应历程中微粒转化关系如图1,相对能量变化关系如图2,图中“*”表示催化剂表面吸附位。下列说法错误的是
A.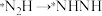 过程中,未发生非极性键的形成 过程中,未发生非极性键的形成 |
B.I、Ⅱ表示的微粒符号分别是 |
C.反应历程中放热最多的反应是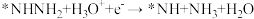 |
D. 的能高于 的能高于 |
更新时间:2024-03-26 22:43:56
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】某种含二价铜的催化剂[CuⅡ(OH)(NH3)]+可用于汽车尾气脱硝。催化机理如图1所示,反应过程中不同态物质体系所具有的能量如图2所示。下列说法不正确的是


| A.该脱硝过程总反应的焓变△H<0 |
| B.状态①到状态②所发生的反应不是氧化还原反应 |
| C.状态③到状态④的变化过程中有O-H键的形成 |
| D.NH3的键角小于H2O的键角,其主要原因是中心原子的杂化轨道类型不同 |
您最近一年使用:0次
【推荐2】下列有关图中所示实验装置的说法合理的是


| A.用图甲装置进行中和反应反应热的测定 |
| B.向图乙的试管A中加入某固体,若注射器的活塞右移,说明A中发生了放热反应 |
C.用图丙探究温度对可逆反应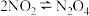 的影响 的影响 |
| D.用图丁装置蒸发饱和食盐水获得氯化钠晶体 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】NH3、NH4Cl、NO、NO2、HNO3等是氮的重要化合物,工业合成氨的反应为N2(g)+3H2(g) 2NH3(g) ΔH=-92.4kJ•mol-1。NH3可与酸反应制得铵盐,也可通过催化氧化生成NO,用于生产HNO3。浓氨水加到生石灰中,放出大量热量,促进NH3·H2O分解,可用于实验室制取NH3。对于工业合成氨的反应:N2(g)+3H2(g)
2NH3(g) ΔH=-92.4kJ•mol-1。NH3可与酸反应制得铵盐,也可通过催化氧化生成NO,用于生产HNO3。浓氨水加到生石灰中,放出大量热量,促进NH3·H2O分解,可用于实验室制取NH3。对于工业合成氨的反应:N2(g)+3H2(g) 2NH3(g) ΔH=-92.4kJ•mol-1。下列说法正确的是
2NH3(g) ΔH=-92.4kJ•mol-1。下列说法正确的是
 2NH3(g) ΔH=-92.4kJ•mol-1。NH3可与酸反应制得铵盐,也可通过催化氧化生成NO,用于生产HNO3。浓氨水加到生石灰中,放出大量热量,促进NH3·H2O分解,可用于实验室制取NH3。对于工业合成氨的反应:N2(g)+3H2(g)
2NH3(g) ΔH=-92.4kJ•mol-1。NH3可与酸反应制得铵盐,也可通过催化氧化生成NO,用于生产HNO3。浓氨水加到生石灰中,放出大量热量,促进NH3·H2O分解,可用于实验室制取NH3。对于工业合成氨的反应:N2(g)+3H2(g) 2NH3(g) ΔH=-92.4kJ•mol-1。下列说法正确的是
2NH3(g) ΔH=-92.4kJ•mol-1。下列说法正确的是| A.该反应为吸热反应 |
| B.升高温度能加快反应速率 |
| C.0.1molN2与0.3molH2充分反应可释放9.24kJ的能量 |
| D.若3v(N2)=v(H2),该反应处于平衡状态 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列说法正确的有几项
①活化分子间的碰撞一定能发生化学反应
②普通分子不会发生碰撞
③升高温度会加快反应速率,原因是增加了活化分子的有效碰撞次数
④增大反应物浓度会加快反应速率的原因是单位体积内有效碰撞的次数增多
⑤使用催化剂能加快反应速率,原因是提高了分子的能量,使有效碰撞频率增大
⑥化学反应的实质是活化分子有合适取向时的有效碰撞
①活化分子间的碰撞一定能发生化学反应
②普通分子不会发生碰撞
③升高温度会加快反应速率,原因是增加了活化分子的有效碰撞次数
④增大反应物浓度会加快反应速率的原因是单位体积内有效碰撞的次数增多
⑤使用催化剂能加快反应速率,原因是提高了分子的能量,使有效碰撞频率增大
⑥化学反应的实质是活化分子有合适取向时的有效碰撞
| A.1项 | B.2项 | C.3项 | D.4项 |
您最近一年使用:0次
【推荐2】自由基是化学键断裂时产生的含未成对电子的中间体,活泼自由基与氧气的反应一直是科研人员的关注点,HNO自由基与O2反应过程的能量变化如图所示,下列说法不正确是


| A.三种中间产物中稳定顺序为:X<Y<Z |
| B.该历程中正反应最大的能垒为186.19kJ/mol |
| C.相同条件下Z转化为产物的速率:v(P1)>v(P2) |
| D.每生成1mol产物P2,反应吸收热量320.40kJ |
您最近一年使用:0次

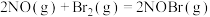
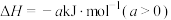 ,其反应机理如下:
,其反应机理如下: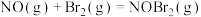
 快反应;
快反应;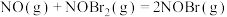
 慢反应。
慢反应。