科学家想要用组成相似的钴氧化物(Co3O4/CoO)代替铁氧化物进行循环制氢。查阅资料发现,使用钴氧化物后反应Ⅰ和反应Ⅱ的ΔH-TΔS值随温度T变化如图所示。
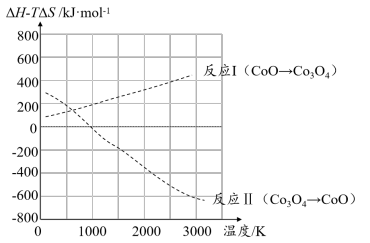
(1)结合图像判断能否用钴氧化物代替铁氧化物进行热化学循环制氢?若可行,举出采用钴氧化物的一个优势;若不可行,说明理由。
(2)除了上述“直接热分解”、“光催化分解”和“热化学循环”外,请再设计一种利用太阳能从水中获取氢气的方法:
更新时间:2024-03-27 09:07:56
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】汽车尾气中含有CO、NOx等有毒气体,对汽车加装尾气净化装置,可使有毒气体相互反应转化为无毒气体。
I.已知4CO(g)+2NO2(g) 4CO2(g)+N2(g)∆H=﹣1200kJ•mol﹣1
4CO2(g)+N2(g)∆H=﹣1200kJ•mol﹣1
(1)该反应在___ (填“高温、低温或任何温度”)下能自发进行。
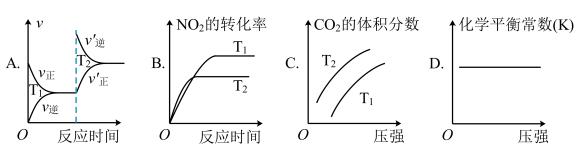
(2)对于该反应,改变某一反应条件(温度T1>T2),下列图象正确的是___ (填标号)。
经过一段时间后达到平衡状态。
①N2的平衡体积分数:甲___ 乙(填“>、=、<或不确定”,下同)。
②NO2的平衡浓度:甲___ 乙。
③甲中CO的转化率为50%,该反应的平衡常数为___ 。
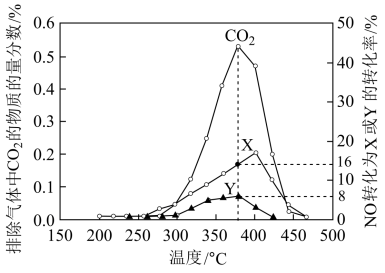
II.柴油汽车尾气中的碳烟(C)和NOx可通过某含钴催化剂催化消除。不同温度下,将模拟尾气(成分如表所示)以相同的流速通过该催化剂测得所有产物(CO2、N2、N2O)与NO的相关数据结果如图所示。
(4)375℃时,测得排出的气体中含amol O2和0.0525 mol CO2,已知X为N2,Y为N2O,则a=___ 。
(5)实验过程中采用NO模拟NOx,而不采用NO2的原因是___ 。
I.已知4CO(g)+2NO2(g)
 4CO2(g)+N2(g)∆H=﹣1200kJ•mol﹣1
4CO2(g)+N2(g)∆H=﹣1200kJ•mol﹣1(1)该反应在
(2)对于该反应,改变某一反应条件(温度T1>T2),下列图象正确的是
经过一段时间后达到平衡状态。
①N2的平衡体积分数:甲
②NO2的平衡浓度:甲
③甲中CO的转化率为50%,该反应的平衡常数为
II.柴油汽车尾气中的碳烟(C)和NOx可通过某含钴催化剂催化消除。不同温度下,将模拟尾气(成分如表所示)以相同的流速通过该催化剂测得所有产物(CO2、N2、N2O)与NO的相关数据结果如图所示。
| 模拟尾气 | 气体(10mol) | 碳烟 | ||
| NO | O2 | He | ||
| 物质的量(mol) | 0.025 | 0.5 | 9.475 | 一定量 |
(5)实验过程中采用NO模拟NOx,而不采用NO2的原因是
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】含铁化合物是重要的基础材料。
请问答:
(1)已知: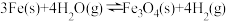
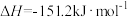 ,
,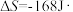
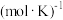 。
。 。当
。当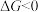 时,正反应是自发的,此时的逆转温度为
时,正反应是自发的,此时的逆转温度为___________ K。
(2)高炉炼铁中发生的基本反应之一为:

①在1100℃时,K=0.263,若此时测得高炉中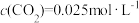 ,
,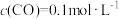 ,判断反应速率
,判断反应速率 (正)
(正)___________  (逆),理由是
(逆),理由是___________ 。
②下列说法不正确的是___________ 。
A.须采用高温高压的反应条件使FeO还原为
B.粉碎FeO能增大接触面积从而提高反应速率
C.平衡时提高CO气体的分压有利于提高Fe的产量
D.加入CaCO3(s)后因分解产生CO2必使平衡逆向移动
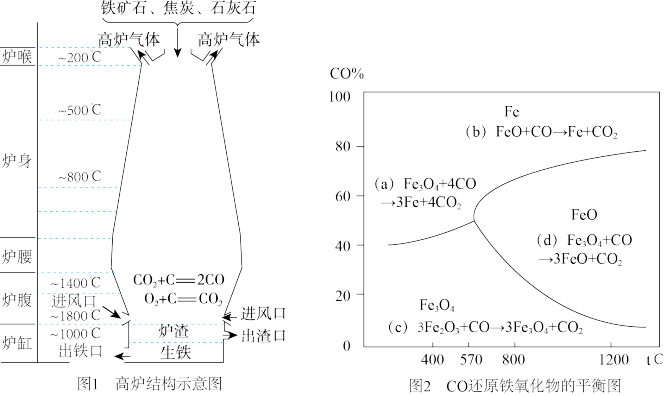
③高炉炉体结构如图1所示,以铁矿石、焦炭、石灰石和空气为原料,由图2推测炉腹中发生的主要反应是___________ (选填:a、b、c、d)。
④若将体积比为1:1的CO和H2混合煤气通入进风口,测得不同温度下FeO还原到 后,还原剂剩余的物质的量n值如下:
后,还原剂剩余的物质的量n值如下:
请结合表格中的数据说明CO和H2分别还原FeO的倾向性大小是___________ 。
(3)一定条件下,FeCl2或FeCl3都可以催化分解H2O2。总反应都是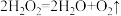 。请写出用FeCl3催化的离子方程式。①
。请写出用FeCl3催化的离子方程式。①___________ ;②___________ 。
请问答:
(1)已知:
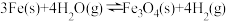
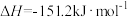 ,
,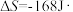
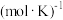 。
。 。当
。当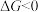 时,正反应是自发的,此时的逆转温度为
时,正反应是自发的,此时的逆转温度为(2)高炉炼铁中发生的基本反应之一为:


①在1100℃时,K=0.263,若此时测得高炉中
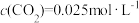 ,
,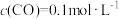 ,判断反应速率
,判断反应速率 (正)
(正) (逆),理由是
(逆),理由是②下列说法不正确的是
A.须采用高温高压的反应条件使FeO还原为

B.粉碎FeO能增大接触面积从而提高反应速率
C.平衡时提高CO气体的分压有利于提高Fe的产量
D.加入CaCO3(s)后因分解产生CO2必使平衡逆向移动
③高炉炉体结构如图1所示,以铁矿石、焦炭、石灰石和空气为原料,由图2推测炉腹中发生的主要反应是

④若将体积比为1:1的CO和H2混合煤气通入进风口,测得不同温度下FeO还原到
 后,还原剂剩余的物质的量n值如下:
后,还原剂剩余的物质的量n值如下:| 还原剂 | 600℃ | 700℃ | 800℃ | 900℃ | 1000℃ | 1100℃ | 1200℃ |
| H2 | 4.18 | 3.34 | 2.94 | 2.60 | 2.32 | 2.30 | 2.25 |
| CO | 1.66 | 2.50 | 2.90 | 3.24 | 3.52 | 3.54 | 3.59 |
请结合表格中的数据说明CO和H2分别还原FeO的倾向性大小是
(3)一定条件下,FeCl2或FeCl3都可以催化分解H2O2。总反应都是
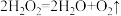 。请写出用FeCl3催化的离子方程式。①
。请写出用FeCl3催化的离子方程式。①
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】PCl3与PCl5均是有机合成的重要中间体,两者存在以下相互转化关系:PCl5(g) PCl3(g)+Cl2(g)△H=a kJ•mol-1。在210℃时,将4 mol PCl5气体充入2 L真空密闭容器中发生上述反应,得到如下数据:
PCl3(g)+Cl2(g)△H=a kJ•mol-1。在210℃时,将4 mol PCl5气体充入2 L真空密闭容器中发生上述反应,得到如下数据:
(1)已知上述反应在温度较高时才能自发进行,则a______ 0(填>、﹦、<)。
(2)计算从20 s至40 s共20 s的时间内,用PCl3表示的平均反应速率为______ 。
(3)反应进行至60 s后,将混合物的温度降低,重新达到平衡后氯气浓度将______ (填“增大”、“减少”或“不变”)。
(4)欲增大该反应的K值,可采取的措施有(填序号)______ 。
A.降低温度 B.向混合气体中通入Cl2
C.使用高效催化剂 D.升高温度
(5)如图是210℃时容器中PCl5物质的量的变化曲线,请在该图中补画出该反应在160℃时PCl5物质的量的变化曲线_______________ 。

 PCl3(g)+Cl2(g)△H=a kJ•mol-1。在210℃时,将4 mol PCl5气体充入2 L真空密闭容器中发生上述反应,得到如下数据:
PCl3(g)+Cl2(g)△H=a kJ•mol-1。在210℃时,将4 mol PCl5气体充入2 L真空密闭容器中发生上述反应,得到如下数据:| 时间(s) | 0 | 20 | 40 | 60 |
| n(PCl5) | 4 | 2.8 | 2 | 2 |
(2)计算从20 s至40 s共20 s的时间内,用PCl3表示的平均反应速率为
(3)反应进行至60 s后,将混合物的温度降低,重新达到平衡后氯气浓度将
(4)欲增大该反应的K值,可采取的措施有(填序号)
A.降低温度 B.向混合气体中通入Cl2
C.使用高效催化剂 D.升高温度
(5)如图是210℃时容器中PCl5物质的量的变化曲线,请在该图中补画出该反应在160℃时PCl5物质的量的变化曲线

您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐1】城市使用的燃料,现大多用煤气、液化石油气。煤气的主要成分是CO和H2的混合气体,它由煤炭和水蒸气反应制得,故又称水煤气。
(1)试写出制取水煤气的主要化学方程式____________________________ .
(2)液化石油气的主要成分是丙烷,丙烷燃烧的热化学方程式为C3H8(g) +5O2(g) == 3CO2(g) + 4H2O(l);△H=–2220.0 kJ·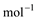 ,又知CO气体燃烧的热化学方程式为:CO(g) +1/2O2(g) == CO2(g) ;△H=–282.57kJ·
,又知CO气体燃烧的热化学方程式为:CO(g) +1/2O2(g) == CO2(g) ;△H=–282.57kJ·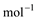 ,试比较同质量的C3H8和CO燃烧,产生的热量比值约为
,试比较同质量的C3H8和CO燃烧,产生的热量比值约为_________ :1。
(3)已知氢气燃烧的热化学方程式为2H2(g) + O2(g) == 2H2O(l);△H=–571.6 kJ·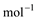 ,试比较同质量的H2和C3H8燃烧,产生的热量比值约为
,试比较同质量的H2和C3H8燃烧,产生的热量比值约为____________ :1。
(4)氢气是未来的能源,除来源丰富之外,还具有的优点是____________________
(1)试写出制取水煤气的主要化学方程式
(2)液化石油气的主要成分是丙烷,丙烷燃烧的热化学方程式为C3H8(g) +5O2(g) == 3CO2(g) + 4H2O(l);△H=–2220.0 kJ·
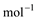 ,又知CO气体燃烧的热化学方程式为:CO(g) +1/2O2(g) == CO2(g) ;△H=–282.57kJ·
,又知CO气体燃烧的热化学方程式为:CO(g) +1/2O2(g) == CO2(g) ;△H=–282.57kJ·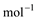 ,试比较同质量的C3H8和CO燃烧,产生的热量比值约为
,试比较同质量的C3H8和CO燃烧,产生的热量比值约为(3)已知氢气燃烧的热化学方程式为2H2(g) + O2(g) == 2H2O(l);△H=–571.6 kJ·
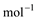 ,试比较同质量的H2和C3H8燃烧,产生的热量比值约为
,试比较同质量的H2和C3H8燃烧,产生的热量比值约为(4)氢气是未来的能源,除来源丰富之外,还具有的优点是
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】化学反应总是伴随着能量的转化,给世界带来了生机和光明。
(1)冷敷袋在日常生活中有降温、保鲜和镇痛等多种作用。
①制作冷敷袋可以利用___________ 。(填字母)
a.放热的化学变化 b.吸热的化学变化 c.放热的物理变化 d.吸热的物理变化
②某品牌冷敷袋是利用十水合碳酸钠( )与硝酸铵在一定条件下反应起作用的,该反应过程中有两种气体产生。反应的化学方程式为
)与硝酸铵在一定条件下反应起作用的,该反应过程中有两种气体产生。反应的化学方程式为___________ 。该冷敷袋的缺点是___________ 。
(2)市场出现的“暖贴”中主要成分是铁粉、炭粉、少量氯化钠和水等,“暖贴”用塑料袋密封,使用时从塑料袋中取出轻轻揉搓就会释放热量,用完后袋内有大量铁锈生成。
①“暖贴”中炭粉的作用是___________ 。
②产生大量铁锈的主要原因是___________ 。
(3)氢能是发展中的新能源,与汽油相比, 作为燃料的优点是
作为燃料的优点是___________ 。 直接燃烧的能量转换率
直接燃烧的能量转换率___________ (填写“高于”或“等于”或“低于”)燃料电池。
(1)冷敷袋在日常生活中有降温、保鲜和镇痛等多种作用。
①制作冷敷袋可以利用
a.放热的化学变化 b.吸热的化学变化 c.放热的物理变化 d.吸热的物理变化
②某品牌冷敷袋是利用十水合碳酸钠(
 )与硝酸铵在一定条件下反应起作用的,该反应过程中有两种气体产生。反应的化学方程式为
)与硝酸铵在一定条件下反应起作用的,该反应过程中有两种气体产生。反应的化学方程式为(2)市场出现的“暖贴”中主要成分是铁粉、炭粉、少量氯化钠和水等,“暖贴”用塑料袋密封,使用时从塑料袋中取出轻轻揉搓就会释放热量,用完后袋内有大量铁锈生成。
①“暖贴”中炭粉的作用是
②产生大量铁锈的主要原因是
(3)氢能是发展中的新能源,与汽油相比,
 作为燃料的优点是
作为燃料的优点是 直接燃烧的能量转换率
直接燃烧的能量转换率
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】科学家认为,氢气是一种高效而无污染的理想能源,近20年来,对以氢气作为未来的动力燃料氢能源的研究获得了迅速发展。
(1)为了有效发展民用氢能源,首先必须制得廉价的氢气,下列可供开发又较经济且资源可持续利用的制氢气的方法是_________ 。(选填字母)
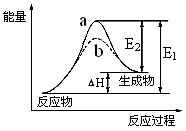
(2)用水分解获得氢气的能量变化如右图所示,表示使用催化剂是曲线_________ 。该反应为_________ (放热还是吸热)反应
(3)1g的氢气完全燃烧生成液态水释放出142.9kJ的热量写出其完全燃烧的热化学方程式:_______________________________ 。
(4)利用氢气和CO合成二甲醚的三步反应如下:
① 2H2(g) + CO(g) CH3OH(g);ΔH =-90.8 kJ·mol-1
CH3OH(g);ΔH =-90.8 kJ·mol-1
② 2CH3OH(g) CH3OCH3(g) + H2O(g);ΔH=-23.5 kJ·mol-1
CH3OCH3(g) + H2O(g);ΔH=-23.5 kJ·mol-1
③ CO(g) + H2O(g) CO2(g) + H2(g);ΔH=-41.3 kJ·mol-1
CO2(g) + H2(g);ΔH=-41.3 kJ·mol-1
总反应:3H2(g) + 3CO(g) CH3OCH3(g) + CO2(g)的ΔH=
CH3OCH3(g) + CO2(g)的ΔH=_________
(5)氢氧燃料电池能量转化率高,具有广阔的发展前景。现用氢氧燃料电池进行下图所示实验:
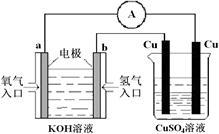
①氢氧燃料电池中,正极的电极反应式为_________________ 。
②上图装置中,某一铜电极的质量减轻3.2g,则 a 极上消耗的O2在标准状况下的体积为
_________ L。
(6)有人设想寻求合适的催化剂和电极材料,以N2、H2为电极反应物,以HCl-NH4Cl为电解质溶液制取新型燃料电池。则正极电极方程式_________ 。
(1)为了有效发展民用氢能源,首先必须制得廉价的氢气,下列可供开发又较经济且资源可持续利用的制氢气的方法是
| A.电解水 | B.锌和稀硫酸反应 |
| C.光解海水 | D.分解天然气 |
(2)用水分解获得氢气的能量变化如右图所示,表示使用催化剂是曲线

(3)1g的氢气完全燃烧生成液态水释放出142.9kJ的热量写出其完全燃烧的热化学方程式:
(4)利用氢气和CO合成二甲醚的三步反应如下:
① 2H2(g) + CO(g)
 CH3OH(g);ΔH =-90.8 kJ·mol-1
CH3OH(g);ΔH =-90.8 kJ·mol-1② 2CH3OH(g)
 CH3OCH3(g) + H2O(g);ΔH=-23.5 kJ·mol-1
CH3OCH3(g) + H2O(g);ΔH=-23.5 kJ·mol-1③ CO(g) + H2O(g)
 CO2(g) + H2(g);ΔH=-41.3 kJ·mol-1
CO2(g) + H2(g);ΔH=-41.3 kJ·mol-1总反应:3H2(g) + 3CO(g)
 CH3OCH3(g) + CO2(g)的ΔH=
CH3OCH3(g) + CO2(g)的ΔH=(5)氢氧燃料电池能量转化率高,具有广阔的发展前景。现用氢氧燃料电池进行下图所示实验:

①氢氧燃料电池中,正极的电极反应式为
②上图装置中,某一铜电极的质量减轻3.2g,则 a 极上消耗的O2在标准状况下的体积为
(6)有人设想寻求合适的催化剂和电极材料,以N2、H2为电极反应物,以HCl-NH4Cl为电解质溶液制取新型燃料电池。则正极电极方程式
您最近半年使用:0次



